 Oggi, 28 febbraio, si celebra la Giornata mondiale delle malattie rare (in inglese “Rare Disease Day“). La giornata si celebra ogni anno il 28 febbraio (o il 29 febbraio negli anni bisestili, il giorno più Continua a leggere
Oggi, 28 febbraio, si celebra la Giornata mondiale delle malattie rare (in inglese “Rare Disease Day“). La giornata si celebra ogni anno il 28 febbraio (o il 29 febbraio negli anni bisestili, il giorno più Continua a leggere
Archivi tag: malattie rare
Si taglia in spiaggia e muore dopo pochi giorni per una fascite necrotizzante
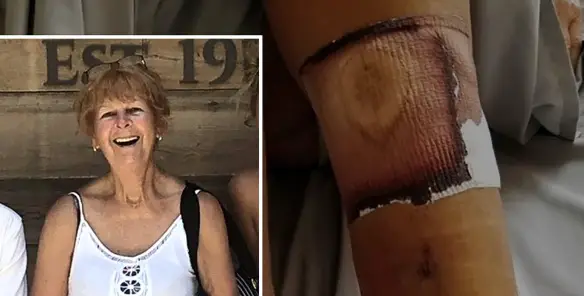 Lynn Fleming, una donna statunitense, è stata uccisa da un’infezione provocata da un batterio “carnivoro” che l’ha Continua a leggere
Lynn Fleming, una donna statunitense, è stata uccisa da un’infezione provocata da un batterio “carnivoro” che l’ha Continua a leggere
Acondrogenesi: un rara forma di nanismo letale
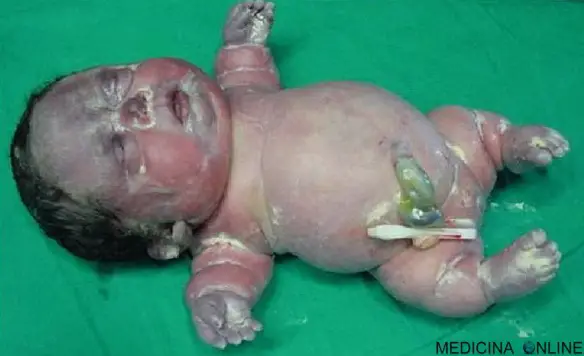 Con “acondrogenesi” (in inglese “achondrogenesis”) si indica un gruppo di patologie che corrispondono alle forme più gravi di “condrodisplasia congenita” (caratterizzata da malformazione Continua a leggere
Con “acondrogenesi” (in inglese “achondrogenesis”) si indica un gruppo di patologie che corrispondono alle forme più gravi di “condrodisplasia congenita” (caratterizzata da malformazione Continua a leggere
Sindrome di Hughes-Stovin: cause, sintomi, diagnosi e terapia
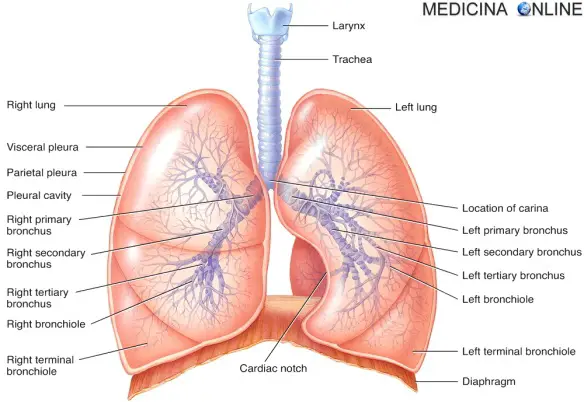 Con “sindrome di Hughes-Stovin” in medicina si indica un rarissimo disordine autoimmune. Ricordiamo che alla base di una patologia autoimmune vi è Continua a leggere
Con “sindrome di Hughes-Stovin” in medicina si indica un rarissimo disordine autoimmune. Ricordiamo che alla base di una patologia autoimmune vi è Continua a leggere
Insensibilità congenita al dolore: la strana malattia che non ti fa sentire nessun dolore
 Immaginate di soffrire il mal di denti ma di non provare alcun dolore. Oppure di ricevere un pugno sul naso e continuare senza problemi a fare quel che stavate facendo.
Immaginate di soffrire il mal di denti ma di non provare alcun dolore. Oppure di ricevere un pugno sul naso e continuare senza problemi a fare quel che stavate facendo.
Quante volte, durante una malattia o dopo una caduta, ci siamo detti “quanto sarebbe bella una vita senza dolore”. Dopo aver letto questo articolo non la penserete allo stesso modo!
L’importanza del dolore
A parità di stimolo la percezione dell’intensità del dolore varia da persona a persona. La soglia del dolore è soggettiva, tuttavia il nostro comportamento di fronte ad un forte dolore è quasi sempre lo stesso: molte volte quando qualcosa “ci fa male” noi ricorriamo subito ai farmaci per alleviare il dolore, come ad esempio gli antinfiammatori. Tuttavia spesso ci dimentichiamo che il dolore è un sentimento necessario, un allarme che il nostro corpo ci invia per avvertirci che qualcosa nel nostro corpo funziona male o ha dei danni. Il dolore è il modo che ha il nostro corpo per spingerci a prendere delle contromisure al danno per evitarci ulteriori danni e curarci adeguatamente e tempestivamente.
Leggi anche: Perché si piange? Per quale motivo si piange di gioia, di dolore e dal ridere?
Il caso di Isaac Brown
Qualche tempo fa dal Regno Unito, era diventato famoso il piccolo Isaac Brown, 5 anni, affetto da insensibilità congenita al dolore. Il bambino, a causa di questa patologia, di fatto non è consapevole dei pericoli che affronta anche nei più semplici atti quotidiani. Può succedere ad esempio che il piccolo, pur avendo una frattura al piede, continui a giocare a calcio non curandosi del trauma: mentre un bambino sano smetterebbe di giocare e verrebbe curato adeguatamente, Isaac continuerebbe a giocare provocando danni molto più elevati! La frattura al piede è un caso “ottimistico”, pensate ad esempio ad un trauma che provochi una emorragia interna: il piccolo continuerebbe tranquillamente a giocare, per poi morire dissanguato pochi minuti dopo.
Per risolvere il problema la famiglia Brown educa il figlioletto a riconoscere i potenziali rischi per la propria incolumità, dato che il bambino non saprebbe riconoscere i rischi cui si sottopone, ancor più rispetto a qualsiasi bambino della stessa età.
Leggi anche: La morte per mancanza di sonno è davvero possibile? Per quanto tempo si può restare svegli?
Cos’è l’insensibilità congenita al dolore?
I problemi che scaturiscono dalla totale mancanza del dolore, si manifestano nella insensibilità congenita al dolore (anche detta CIPA che è l’acronimo di Congenital Insensitivity to Pain with Anhidrosis che in italiano significa “insensibilità congenita al dolore con anidrosi“). La CIPA è una malattia molto rara – forse causata da una mutazione genetica a carico del gene SCN9A – caratterizzata fondamentalmente da assenza tattile e anidrosi (assenza della sudorazione) e quindi impossibilità di avvertire il dolore, il calore e il freddo. La mancata sudorazione porta poi a frequenti episodi di ipertermia, pericolosa specie per i bambini. Dietro l’insensibilità congenita al dolore vi sarebbe la disfunzione del sistema nervoso periferico: le terminazioni nervose non sarebbero in grado di rispondere adeguatamente alle stimolazioni, specie quelle nocive recepite come dolore.
Leggi anche: Mark Sloan e il recupero fittizio: il mistero del cervello pochi attimi prima di morire
Epidemiologia
La CIPA è una patologia rarissima, che colpisce circa 1000 persone nel mondo. Attualmente vi sono 84 casi viventi documentati negli Stati Uniti e circa 300 in Giappone. Solo un caso è documentato in Nuova Zelanda, mentre due casi sono stati individuati in Marocco. Sessanta casi sono stati riportati a livello mondiale nel 1983, quando la CIPA è stata classificata come malattia.
Prognosi
La maggior parte dei bambini affetti da questo disturbo non vive oltre i 3 anni di età e raramente superano i 25 anni. La ragione di questa aspettativa di vita così ridotta è spesso legata all’incapacità del malato di sudare, e ciò porta a ipertermia, alla quale specie i bambini sono particolarmente sensibili.
Leggi anche: Mal di schiena: cibi consigliati, farmaci, rimedi naturali e prevenzione del dolore
Quali sono le cause dell’insensibilità congenita al dolore?
Come detto qualche riga prima, dietro questa patologia ci sarebbe una mutazione a carico del gene SCN9A. Il gene SCN9A codificherebbe per la costruzione di una parte della proteina detta subunità Nav 1.7. La proteina in questione è un canale per il passaggio dello ione Sodio (Na+), importante regolatore della propagazione dei segnali nervosi lungo le fibre nervose dirette al sistema nervoso centrale dalla periferia e viceversa. Detto in parole semplici la mutazione del gene in questione interferirebbe sulla struttura di una proteina presente nella membrana delle cellule nervose periferiche, che rappresentano le porte di accesso per le informazioni al cervello. L’impossibilità di tale accesso rende impossibile provare l’impulso doloroso. Nuovi studi sembrano confermare l’interessamento del gene che codifica il recettore tirosin chinasico neurotrofico (gene NTRK1). Tale recettore è specifico per il nerve growth factor (NGF o fattore di crescita nervosa) che induce la formazione di assoni e dendriti e promuove la sopravvivenza dei neuroni embrionali sensoriali e simpatici. La mutazione dell’NTRK1 non consente di legare NGF correttamente e può causare difetti nello sviluppo. La ricerca in tale direzione è agli inizi e solo l’informazione e la dedizione riescono a garantire una vita quasi “normale” alle persone affette da insensibilità congenita al dolore.
Come si cura l’insensibilità congenita al dolore?
Ad oggi non esiste una cura risolutiva per una patologia che rende le persone insensibili al dolore fisico e, di fatto, a rischio di non sapere riconoscere le fonti di pericolo. Oggi, nonostante la medicina non trovi ancora cure efficaci per la malattia rara, un aiuto giunge dai mondi della comunicazione e dei social network, dalla buona informazione. La famiglia di Isaac, ad esempio, ha trovato aiuto in vari forum sul web dove si incontrano pazienti e familiari di pazienti che vivono il dramma dell’insensibilità congenita al dolore: in questi gruppi possono trovare uno spazio per confronti e suggerimenti.
Leggi anche:
- Dolore: come si misura? La scala visiva e numerica verbale
- Dolore: quando chiamare il medico e cosa riferirgli
- Dolore: esistono esami specifici per rilevarlo?
- Quali sono i dolori più diffusi?
- Paralisi del sonno e allucinazioni ipnagogiche: cause, pericoli, rimedi
- Perché sentiamo dolore? Il meccanismo di trasmissione del dolore
- Differenza tra sintomo e segno con esempi
- Differenza tra malattia, sindrome e disturbo con esempi
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Dolore muscolare il giorno dopo l’allenamento: cause, cure e prevenzione
- Differenza tra malattia acuta e cronica con esempi
- Che significa malattia cronica? Esempi di malattia cronica
- Differenza tra dolore acuto, cronico, persistente ed episodico con esempi
- Differenza tra dolore somatico e psicosomatico
- Differenza dolore al seno da gravidanza e da ciclo mestruale
- Che significa “effetto placebo” e perché un placebo funziona?
- Differenze tra Efferalgan e Co-Efferalgan
- Posso assumere Tachipirina in gravidanza e allattamento? Quante compresse?
- Che significa somministrazione di un farmaco PER OS o PO?
- Via di somministrazione orale, per os: vantaggi e svantaggi
- Supposta rettale: vantaggi e svantaggi rispetto ad altre vie di somministrazione
- Ollie, il “bambino Pinocchio” nato con il cervello nel naso
- Dolore: cos’è, da cosa è causato, quanti tipi di dolore esistono?
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Sindrome di Cornelia de Lange: avere l’aspetto di un bambino per tutta la vita
 La sindrome di Cornelia de Lange (CDLS) è una sindrome malformativa riconosciuta per la prima volta nel 1933 da una pediatra che diede ad essa il nome, la cui incidenza è stimata pari ad 1 nuovo caso ogni 10-20.000 nati (circa 50 nuovi nati all’anno in Italia). Una sindrome malformativa è una malattia congenita (cioè presente sin dalla nascita) caratterizzata dalla possibile presenza contemporanea di malformazioni maggiori (alterazione della struttura di cuore, reni, palato, sistema nervoso centrale, arti, genitali esterni ecc.), di problemi di crescita in peso e altezza (in eccesso o in difetto), di anomalo sviluppo psicomotorio e intellettivo e di tratti somatici spesso molto particolari.
La sindrome di Cornelia de Lange (CDLS) è una sindrome malformativa riconosciuta per la prima volta nel 1933 da una pediatra che diede ad essa il nome, la cui incidenza è stimata pari ad 1 nuovo caso ogni 10-20.000 nati (circa 50 nuovi nati all’anno in Italia). Una sindrome malformativa è una malattia congenita (cioè presente sin dalla nascita) caratterizzata dalla possibile presenza contemporanea di malformazioni maggiori (alterazione della struttura di cuore, reni, palato, sistema nervoso centrale, arti, genitali esterni ecc.), di problemi di crescita in peso e altezza (in eccesso o in difetto), di anomalo sviluppo psicomotorio e intellettivo e di tratti somatici spesso molto particolari.
Segni e sintomi in generali
Le caratteristiche principali di un soggetto affetto sono costituite da basso peso alla nascita (inferiore a due chili e mezzo), scarsa crescita postnatale in peso e altezza, ridotte dimensioni della testa (microcefalia), eccessiva peluria sul corpo (avambraccio e regione lombare in particolare), mani e piedi piccoli o gravi alterazioni malformative a carico delle mani stesse. I pazienti si assomigliano molto tra di loro: le ciglia sono lunghe, il naso è piccolo con narici all’insù, le labbra sono sottili con angoli rivolti in basso. Le sopracciglia sono sottili, arcuate e unite frequentemente sulla linea mediana e danno l’impressione di essere state disegnate con la matita. L’acquisizione delle comuni tappe di sviluppo di ogni bambino (stare seduto, gattonare, camminare, dire le prime parole) è ritardata, così come ritardato in modo variabile è lo sviluppo intellettivo. Per quanto riguarda infine l’area della comunicazione verbale (linguaggio), si tratta della sfera più compromessa ed è ormai chiaro che le capacità di comprensione dei soggetti affetti superano notevolmente le loro possibilità di espressione verbale.
Leggi anche: Cos’è un cromosoma ed a che serve?
Crescita e alimentazione
Altezza, peso e circonferenza cranica durante l’infanzia di solito sono al di sotto del terzo percentile. Individui con la forma lieve della sindrome hanno un ritardo di crescita meno severo. Lo scatto di crescita puberale si ha in tempi normali (una media di 15 anni per i maschi e di 13 anni per le femmine), ma l’ampiezza dello scatto di crescita e inferiore a quella della popolazione generale. L’altezza media, da adulti, e di 155.78 cm per i maschi e di 131.13 per le femmine. Fin dalla nascita, la capacita di nutrirsi e scarsa, e non di rado i bambini affetti necessitano di alimentazione per via nasogastrica. In qualche e necessaria l’inserzione un tubo per gastrostomia. E comune il reflusso gastroesofageo, che contribuisce alle difficolta di alimentazione e alla scarsa crescita. La prognosi per una crescita normale e buona se il sottostante reflusso gastroesofageo e diagnosticato e trattato precocemente.
Sviluppo e comportamento
Numerosi studi e case report hanno documentato il QI dei soggetti affetti, e i risultati variavano da 30 a 60 per gli individui con la forma classica, fino a 102 in quelli con la forma lieve. Barney et al. Nel 1999, condussero uno studio dettagliato sul comportamento di 49 individui con i fenotipi classico e lieve. L’età dei pazienti dello studio variava della prima infanzia all’età adulta. Essi evidenziarono una grande varietà di sintomi, che includevano l’iperattività (40%), l’autolesionismo (44%), aggressioni quotidiane (49%) e disturbi del sonno (55%). I disturbi del comportamento correlavano strettamente con la presenza di una sindrome simil-autistica e con il grado di ritardo mentale. Questi autori descrissero come questi disturbi del comportamento continuassero anche in età adulta. Kline e colleghi misero a punto una valutazione dello sviluppo in 122 individui con sindrome di Cornelia de Lange, usando una varietà di metodi, e furono in grado di costruire tavole con le tappe di sviluppo, prendendo in considerazione la motricità grossolana, la motricità fine, le abilita sociali e lo sviluppo del linguaggio. Vi sono molte descrizioni, in letteratura, di assenza di linguaggio negli individui con la sindrome di Cornelia de Lange. All’altro estremo dello spettro, vi e la descrizione di una ragazza con la forma lieve della sindrome che a 14 anni era in grado di parlare con frasi articolate. In uno studio sugli indicatori prognostici per lo sviluppo del linguaggio, i fattori che predicevano una prognosi scarsa erano: un peso alla nascita al di sotto 2.270 kg, deficit uditivo da moderato a grave, malformazioni a carico degli arti superiori, scarse interazioni sociali e un grave ritardo motorio. Molti lavori hanno descritto un pianto simile ad un ringhio sommesso come caratteristico della sindrome in infanzia. Non e stato possibile valutare gli effetti della sordità combinata sensitiva e conduttiva, che si osserva nella sindrome, sul deficit di linguaggio, perché nessuno degli studi sulla sindrome ha incluso una valutazione dell’udito. Poiché adesso gli individui affetti dalla sindrome di Cornelia de Lange sono trattati con dispositivi di ausilio all’udito e con l’inserzione di tube di ventilazione, sembra che lo sviluppo del linguaggio andrà via via migliorando negli anni avvenire. Praticamente tutti i bambini con la sindrome alla fine impareranno a camminare. Quelli con il fenotipo lieve staranno seduti intorno all’anno e cammineranno intorno ai due anni, mentre la maggior parte dei pazienti con fenotipo classico staranno seduti prima dei due anni e cammineranno prima dei tre anni. Una minoranza dei bambini con la forma classica pronuncerà qualche parola, mentre la maggioranza di quelli con la forma lieve sarà in grado di parlare a frasi. I disturbi del comportamento sono comuni nella sindrome di Cornelia de Lange e sono più frequenti nei pazienti con grave ritardo mentale. E importante il ruolo delle cause mediche, come il reflusso gastroesofageo, quando si ha un peggioramento del comportamento: drammatici miglioramenti del comportamento non sono rari dopo terapia antireflusso. La prognosi, per quanto riguarda la gestione dei problemi di comportamento, e buona se viene individuato e trattato un problema clinico sottostante o se il problema di base era una difficolta di comunicazione che viene risolta con l’aiuto del linguaggio dei segni. In assenza di problemi di questo tipo, il comportamento rimane comunque un aspetto di difficile gestione da parte dei familiari e dei terapeuti.
Orecchie e udito
Un certo grado di deficit dell’udito e presente nel 90% degli individui con la sindrome di Cornelia de Lange. Ora si e visto che e di origine neurosensoriale e che di solito e bilaterale. Otiti medie e malattie croniche dell’orecchio medio (‘glue ear’) che si sovrappongono sono comuni e possono essere difficili da diagnosticare perché il canale uditivo esterno, in questa sindrome, tende ad essere molto stretto. Gli ausili auricolari vengono meglio tollerati quando sono impiantati precocemente.
Anomalie degli arti
Le anomalie degli arti che si possono vedere nella sindrome di Cornelia de Lange variano dalla presenza di mani piccole con dita corte a riduzioni bilaterali con assenza di mani e avambracci. Anomalie minori della mani includono impianto prossimale dei pollici, solco palmare singolo e clinodattilia del quinto dito. Più di rado, si possono vedere fusione di due dita o polidattilia e vi e una descrizione di un dito con due unghie. A livello dell’arto superiore, omero, ulna e radio sono di lunghezza ridotta, e occasionalmente il radio o l’ulna sono aplastici. E comune la brevità dei metacarpi, in particolare del primo. Sono comuni contratture in flessione dei gomiti, secondarie alla deformazione della metafisi prossimale del radio, che solitamente e sublussato.
Leggi anche: Cos’è un gene ed a che serve?
Problemi gastrointestinali
Il reflusso gastroesofageo rappresenta il più comune problema gastrointestinale, nella sindrome di Cornelia de Lange, e colpisce sia la forma classica sia quella lieve. Se non trattato, il reflusso può condurre a morbilità e mortalità significative. E comune che si sviluppi esofago di Barrett e stenosi esofagea, e si può sviluppare anche adenocarcinoma dell’esofago. La condizione si può presentare in individui con deficit di crescita, ridotta velocita di accrescimento, anemia, polmoniti ricorrenti, apnea o disturbi del comportamento. Poiché l’associazione tra reflusso e sindrome di Cornelia de Lange e emersa solo in tempi relativamente recenti, spesso al momento della diagnosi il danno esofageo e già grave. Malformazioni del tratto gastrointestinale che si presentino subito dopo la nascita includono stenosi pilorica in circa l’1% dei pazienti effetti o, molto raramente, un pancreas anulare che si manifesta con ostruzione duodenale.
Problemi cardiovascolari
Nel 20-25% dei pazienti con la forma classica della sindrome di Cornelia de Lange sono presenti difetti cardiaci congeniti, che sono invece rari nella forma lieve. L’anomalia più comune e la stenosi della valvola polmonare, sia isolata, sia in combinazione con un difetto del setto interventricolare. Una grande varietà di altri difetti e stata descritta in questa sindrome, compresa la tetralogia di Fallot, la coartazione aortica, il difetto del setto interatriale, il cuore sinistro ipoplasico, il ventricolo unico e il difetto del canale atrioventricolare. Nel 2% dei pazienti con la forma lieve si può osservare una modesta stenosi del ramo polmonare, che raramente richiede trattamento. I difetti cardiaci più gravi spesso si vedono nei pazienti con ernia diaframmatica e grave accorciamento degli arti. I bambini con difetti cardiaci più complessi di solito stentano a crescere e muoiono prima o durante l’intervento di chirurgia correttiva. Quelli con difetti più semplice, invece, hanno una buona prognosi.
Anomalie craniofacciali
Gli individui con la sindrome di Cornelia de Lange di frequente hanno il palato arcuato e alto. L’incidenza della palatoschisi varia tra il 18 e il 59% a seconda delle descrizioni. Al contrario di tante altre anomalie, la palatoschisi si può osservare anche nei pazienti con la forma lieve della sindrome. La palatoschisi non e mai associata a labioschisi. La prognosi di solito e buona, anche se i bambini con la forma lieve della sindrome di Cornelia de Lange e palatoschisi hanno meno probabilità di imparare a parlare rispetto a quelli senza.
Problemi oculistici
La ptosi della palpebra superiore e un reperto frequente specialmente nella forma classica, in cui può variare da un semplice problema estetico ad una interruzione dell’asse visivo. Anche la miopia e molto comune, ed e stata descritta nel 60% dei pazienti con la forma classica della sindrome di Cornelia de Lange. Sono molto comuni anche sintomi suggestivi di ostruzione del canale nasolacrimale, come gli occhi bagnati e le congiuntiviti ricorrenti. Questi sintomi, comunque, si risolvono quasi sempre spontaneamente col tempo, e sono rari dopo i sei anni.
Problemi al tratto genitourinario
La più frequente anomalia del tratto renale, in questa sindrome, e il rene a ferro di cavallo. Nei maschi, reperto estremamente comune e il criptorchidismo, che puo presentarsi in associazione con ipospadia e scroto ipoplasico. Nelle femmine, l’anomalia piu comune e l’utero bicorne.
Problemi neurologici
Sono state descritte molte anomalie del sistema nervoso centrale, ma nella maggior parte dei casi si tratta di pubblicazioni di singoli casi. Le convulsioni sono infrequenti, e si controllano bene con i farmaci.
CAUSE DELLA SINDROME DI CORNELIA DE LANGE
La sindrome di Cornelia de Lange è una malattia genetica, causata cioè da un’alterazione molto piccola nel patrimonio genetico della persona affetta. Nel maggio del 2004 è stato dimostrato che un’anomalia di una singola informazione genetica (gene NIPBL) è responsabile di tutte le manifestazioni cliniche nel 50% circa dei soggetti con questa condizione. La ricerca è ora impegnata a capire quale sia il difetto genetico di base nella restante parte delle persone con CDLS. L’alterazione genetica che causa la sindrome insorge solitamente in modo casuale nel patrimonio genetico del soggetto affetto; questo fa sì, quindi, che il rischio di ripetizione della malattia in altri figli dopo la nascita di un figlio affetto sia, di regola, molto basso. Esistono però rarissimi casi (una decina circa al mondo) in cui si è verificata una ripetizione della malattia; è per altro importante che ogni coppia che ha avuto un bambino affetto esegua un’appropriata consulenza genetica.
DIAGNOSI DELLA SINDROME DI CORNELIA DE LANGE
La diagnosi di CDLS è ancora prevalentemente basata sul riconoscimento delle caratteristiche cliniche da parte di un medico esperto (pediatra, genetista, ecc). Essa può essere fatta già alla nascita o nei mesi o negli anni successivi. Le recenti scoperte fanno sì che entro breve sarà possibile confermare la diagnosi clinica con l’esecuzione di un esame di laboratorio specifico (test genetico). Recentemente si è dimostrato anche che esistono pazienti con un quadro clinico meno marcato (forme mild = lievi) per i quali la diagnosi frequentemente è fatta più tardi e la prognosi è migliore.
Diagnosi prenatale e prevenzione
Poiché non vi sono test diagnostici per la sindrome, le gravidanze successive alla nascita di un bambino affetto vanno seguite con ecografie accurate, cercando anomalie strutturali come un igroma cistico, difetti a carico degli arti nel senso di una riduzione, un’ernia diaframmatica, anomalie cardiache o il caratteristico profilo della faccia. Il profilo del volto presenta una grave micrognatia con filtro lungo e sporgente, e naso piccolo. Il ritardo di crescita intrauterino, presente alla nascita nella maggior parte dei casi, raramente si vede prima del terzo trimestre. Nel 1983, Westergaard e colleghi descrissero la completa assenza della proteina-A plasmatica associata alla gravidanza (PAPP-A) in una serie di campioni di siero di donne gravide che che successivamente ebbero un bambino con la sindrome di Cornelia de Lange. In uno studio recente questo autore trovo che la PAPP-A era presente nei 19 campioni di siero materni analizzati, al secondo trimestre di gravidanza, ma che i suoi livelli erano significativamente ridotti. Sebbene non sia un test diagnostico, la PAPP-A può dimostrarsi un prezioso marcatore aggiuntivo per le gravidanze a rischio di ricorrenza o per quelle in cui siano state riscontrate delle anomalie compatibili con la sindrome di Cornelia de Lange.
Sospetti e conferme
La diagnosi prenatale della sindrome di Cornelia de Lange può essere sospettata dopo il precoce riscontro di un ritardo di crescita simmetrico, che diventa particolarmente evidente dopo la 25 settimana di gravidanza. La diagnosi può essere ulteriormente confermata quando si ricerchino segni ecografici aggiuntivi, come la facies tipica, difetti agli arti superiori, che di solito sono unilaterali, e varie anomalie viscerali tra cui l’ernia diaframmatica, la stenosi pilorica, il reflusso ureterale e lesioni cardiache di vario tipo (difetti del setto interatriale e interventricolare, stenosi dell’arteria polmonare o aortica, tetralogia di Fallot, finestra aorto-polmonare, canale atrioventricolare e ventricolo unico).
Il cariotipo fetale rappresenta il primo passo nella diagnosi differenziale in epoca prenatale, per escludere la trisomia 18 e la tetrasomia 12p, ed e essenziale, vista la somiglianza della sindrome di Cornelia de Lange con la duplicazione 3q. Nella maggior parte dei casi, la sindrome di Cornelia de Lange mostra un grave ritardo di crescita, oligodattilia, pollici in posizione prossimale e un filtro sporgente, mentre la duplicazione 3q e più spesso associata a craniosinostosi, palatoschisi e anomalie del tratto urinario.
PROBLEMI DEI PAZIENTI CON SINDROME DI CORNELIA DE LANGE
I problemi principali per i pazienti affetti da sindrome di Cornelia de Lange riguardano la scarsa crescita (esistono in proposito curve di crescita specifiche) e il ritardo psicomotorio e intellettivo. A questo proposito è importante che vengano intrapresi programmi di stimolazione precoci soprattutto per quanto riguarda l’area della comunicazione. Tra i problemi pediatrici più frequentemente associati vi sono il reflusso gastroesofageo e le sue complicanze (70-80% dei casi), le convulsioni (20% circa dei casi), difficoltà d’udito, otiti e sinusiti frequenti, blefariti e miopia. Possono poi insorgere problemi comportamentali (irritabilità, iperattività ecc.), a volte legati al mancato riconoscimento e trattamento di problemi medici in grado di causare dolore. La sopravvivenza di una persona affetta, che non presenti malformazioni maggiori gravi, non è particolarmente ridotta: oggi, infatti, sono ampiamente noti soggetti che hanno raggiunto l’età adulta.
TERAPIA NEI PAZIENTI CON SINDROME DI CORNELIA DE LANGE
Crescita e alimentazione
Se il bambino non è in grado di succhiare dal biberon, un introito calorico adeguato dovrebbe essere garantito per mezzo di nutrizione per via nasogastrica. Nei casi con grave reflusso gastroesofageo e difficolta di alimentazione, può essere necessario il posizionamento di un tubo per gastrostomia nel momento della funduplicatio.
Sviluppo e comportamento
Nei pazienti con la forma lieve della sindrome dovrebbe essere intrapresa terapia del linguaggio. Come aiuto alla comunicazione, dovrebbero essere introdotti il linguaggio dei segni o altre tecniche. Le patologie dell’orecchio medio dovrebbero essere trattate con antibiotici e, se necessario, con cannule di ventilazione. Ogni problema medico sottostante che deteriori il comportamento dovrebbe essere trattato. I problemi comportamentali di lunga data sono difficili da modificare, ma si possono migliorare con la modificazione comportamentale, guidata da uno psicologo del comportamento o da un pediatra dello sviluppo.
Anomalie degli arti
Non vi sono pubblicazioni che documentino che un approccio chirurgico alle anomalie degli arti possa dare dei benefici; anche i pazienti con grave ritardo mentale spesso hanno un controllo della motricità fine straordinariamente buono.
Problemi gastrointestinali
Nella pratica, sono molto pochi i pazienti che rispondono ad un trattamento conservativo del reflusso gastroesofageo, e la maggior parte necessita di un approccio chirurgico. Il trattamento iniziale del reflusso dovrebbe consistere nel suggerimento di assumere pasti piccoli e solidi e di rimanere in posizione eretta il più possibile. Va tentata la terapia con antiacidi, anti-H2 e inibitori della pompa protonica. Di solito si rende necessaria la funduplicatio, talvolta con inserzione di un tubo da gastrostomia.
Leggi anche:
- Le malattie genetiche più diffuse al mondo
- Differenza tra allele dominante e recessivo
- Differenza tra omozigote ed eterozigote
- Differenza tra gene e allele
- Differenza tra genotipo e fenotipo
- Cosa sono gli alleli ed a che servono?
- Differenza tra cellule eucariote e procariote
- Virus e virioni: cosa sono, come sono fatti, come funzionano e come si riproducono
- Quanti cromosomi hanno esseri umani, scimmie, cani, gatti e topi?
- Quanti cromosomi ha chi è affetto da Sindrome di Down?
- Sindrome di Turner: cariotipo, cause, sintomi e segni caratteristici
- Sindrome di Klinefelter: cariotipo, cause, sintomi e cura
- Sindrome di Down: cause, sintomi in gravidanza e nei neonati
- Fibrosi cistica polmonare: cos’è, sintomi in neonati e bambini, cure
- Malattia di Huntington: cos’è, ereditarietà, come si trasmette, età di insorgenza
- Anemia falciforme: cosa significa, cause, sintomi e cure
- Differenze tra la distrofia muscolare di Duchenne e di Becker
- Talassemia: cos’è, sintomi, cure, differenti tipi ed alimentazione
- Celiachia: cos’è il glutine, in quali alimenti è contenuto ed in quali no?
- Sindrome di Bloom: cause, sintomi, diagnosi e terapia
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Uomo nel DNA, donna all’esterno: la Sindrome da insensibilità agli androgeni (Sindrome di Morris)
 La Sindrome da insensibilità agli androgeni, in inglese androgen insensitivity syndrome, anche conosciuta col nome di Sindrome di Morris o Femminilizzazione testicolare, è una patologia appartenente ai “Disordini della Differenziazione Sessuale” (DSD): i soggetti affetti sono persone con corredo cromosomico 46,XY (a cui corrisponde un fenotipo maschile) sviluppano caratteri sessuali femminili. Per farvi capire meglio: il soggetto ha “cromosomi da uomo” tuttavia esternamente appare una donna a tutti gli effetti. E’ una malattia rara, l’incidenza è stimata tra 1/20.000 e 1.99.000 maschi nati vivi; essendo rara consente l’esenzione dal ticket. Le persone affette da questa sindrome sono dal punto di vista anatomico, psicologico e legale delle donne.
La Sindrome da insensibilità agli androgeni, in inglese androgen insensitivity syndrome, anche conosciuta col nome di Sindrome di Morris o Femminilizzazione testicolare, è una patologia appartenente ai “Disordini della Differenziazione Sessuale” (DSD): i soggetti affetti sono persone con corredo cromosomico 46,XY (a cui corrisponde un fenotipo maschile) sviluppano caratteri sessuali femminili. Per farvi capire meglio: il soggetto ha “cromosomi da uomo” tuttavia esternamente appare una donna a tutti gli effetti. E’ una malattia rara, l’incidenza è stimata tra 1/20.000 e 1.99.000 maschi nati vivi; essendo rara consente l’esenzione dal ticket. Le persone affette da questa sindrome sono dal punto di vista anatomico, psicologico e legale delle donne.
CAUSE
L’insensibilità dei tessuti agli androgeni è causata da un allele recessivo che si trova nel cromosoma X (X-linked): è pertanto la madre che trasmette tale condizione alla prole.
Leggi anche: La vagina è uguale in tutte le donne?
TRASMISSIONE AI FIGLI
Una madre portatrice di un gene difettoso ha una possibilità su due che suo figlio XY sia affetto da AIS e una possibilità su due che una figlia XX sia lei stessa portatrice di un gene difettoso. Le donne XX possono sottoporsi a test specifici per verificare se sono portatrici. Alle famiglie affette deve essere offerta la consulenza genetica per informarle sul rischio di ricorrenza e per identificare eventuali portatrici nella famiglia. È consigliata di rado la diagnosi prenatale.
FISIOPATOLOGIA
Nei soggetti affetti da questa sindrome vi è un’insensibilità dei tessuti bersaglio fetali all’azione degli ormoni androgeni. La conseguenza è: sviluppo di gonadi maschili ritenute in addome, sviluppo caratteri sessuali femminili secondari (mammelle, ma non utero né ovaie), ipoplasia vaginale.
L’insensibilità agli androgeni può essere di vari gradi, da 1 (leggera) a 7 (totale o completa).
Se l’insensibilità agli androgeni è completa (grado 7) si parla di CAIS.
Se invece l’insensibilità è parziale (gradi da 1 a 6) si parla di PAIS.
Nel PAIS sono quindi comprese situazioni diverse: dal grado 1 in cui l’insensibilità è lieve e i genitali esterni sono maschili, al grado 6 in cui l’insensibilità è elevata e l’aspetto dei genitali è femminile, passando per varie forme (gradi 2, 3, 4 e 5) in cui c’è una presenza di caratteri sia maschili sia femminili.
Nella forma completa (CAIS) così come in quella parziale (PAIS) non ci sono ovaie, né utero, né tube di Falloppio; la vagina è a fondo cieco e talvolta è corta o quasi inesistente. Alla pubertà avviene lo sviluppo femminile del corpo, però non compaiono le mestruazioni e non è possibile la gravidanza. Alcune ragazze con AIS possono avere una certa quantità di peluria (AIS grado 6), ma normalmente essa è assente (Grado 7) perché la sua crescita dipende dagli androgeni. I capezzoli sono poco sviluppati e di colore chiaro. Può essere necessario ampliare la vagina per permettere i rapporti sessuali.
SINTOMI
I sintomi e segni includono:
- Amenorrea primaria.
- Assenza di peli pubici.
- Individui longilinei, bacino stretto, riduzione dei peli pubici e ascellari.
- Capezzoli di colore più chiaro.
- Sterilità.
- Soggetti psicologicamente e socialmente femminili.
- Ernia inguinale, rigonfiamenti e dolore in addome a causa dei testicoli ritenuti nel canale inguinale.
Leggi anche: Intersessualità: cause, tipi, sintomi, terapia
DIAGNOSI
La diagnosi si effettua tramite esame obiettivo della vagina fatto spesso in pubertà quando sorge il sospetto per via della mancata comparsa del menarca. Oltre alla clinica, sono importanti i dati di laboratorio. Il profilo ormonale caratteristico comprende l’aumento basale dell’ormone luteinizzante (LH) e dei livelli del testosterone negli adulti e dei livelli di testosterone nei neonati dopo stimolazione con gonadotropina corionica umana (HCG). I livelli sierici dell’ormone anti-Mülleriano (AMH) sono normali o aumentati. L’ecografia o la risonanza pelvica mostrano l’assenza delle strutture Mülleriane (utero, tube di Falloppio e porzione superiore della vagina), in conseguenza dell’azione dell’ormone anti-Mülleriano (AMH) testicolare. A causa della resistenza agli androgeni, sono assenti le strutture che derivano dai dotti di Wolff (dotti deferenti, epididimo, vescichette seminali). La diagnosi viene confermata dall’analisi genetica.
DIAGNOSI DIFFERENZIALE
La diagnosi differenziale si pone con il deficit di 17-beta-idrossisteroido deidrogenasi, l’ipoplasia delle cellule di Leydig, la disgenesia gonadica completa XY (sindrome di Swyer), il deficit di 5-alfa-reduttasi tipo 2 e le varianti dell’iperplasia congenita del surrene
TERAPIA E FOLLOW UP
La terapia ha come obbiettivo l’asportazione chirurgica delle gonadi ritenute in addome(gonadectomia), che può essere eseguita dopo la pubertà – quando la femminilizzazione è completa – o prima della pubertà, quando deve essere seguita una terapia estrogenica sostitutiva. L’asportazione dei testicoli elimina il rischio – seppur basso – di una degenerazione neoplastica. Secondo alcuni colleghi il pericolo di degenerazione tumorale è talmente basso che si tende ad aspettare ad effettuare la gonadectomia o addirittura ad evitarla. La dilatazione della vagina può rendersi necessaria per evitare la dispareunia. Nei pazienti adulti è necessario misurare la densità minerale ossea ogni cinque anni. È necessario un sostegno psicologico. I pazienti adulti hanno una normale identità femminile, sono sterili e sono a rischio di osteoporosi, se la terapia sostitutiva ormonale è inadeguata. Il rischio di carcinoma in situ e di gonadoblastoma è inferiore al 5%.
Leggi anche:
- Ermafrodita, ermafroditismo, pseudoermafroditismo maschile e femminile, cosa significa?
- Androgino e androginia: etimologia, sessualità, genitali, mito di Platone
- Differenza tra ermafrodita e androgino
- Sindrome di Reifenstein (parziale insensibilità agli androgeni): cause, sintomi, diagnosi, terapia, complicanze
- Sindrome di Swyer (disgenesia gonadica pura) e gonadi a striscia
- Sindrome di Perrault: cause, sintomi, diagnosi, terapia, prognosi
- Sindrome dell’ovaio resistente (sindrome di Savage)
- La ragazza con due vagine che ha dovuto perdere la verginità due volte
- Punto G femminile: trovarlo e stimolarlo [VIDEO] Attenzione: immagini sessualmente esplicite
- Donne nate senza vagina: è la sindrome di Rokitansky-Kuster-Hauser
- Quando le donne odiano ed invidiano le altre donne: è la Sindrome dell’ape regina
- Né donna, né uomo: io sono una transessuale
- Norrie May Welby è la prima persona al mondo dichiarata ufficialmente né uomo né donna: non ha sesso
- Donna rimane incinta dopo sesso anale, ecco la spiegazione scientifica
- L’incredibile storia delle fotografie ritrovate di Vivian Maier
- La “donna vampiro” e la sua trasformazione [FOTO]
- Come capire se una donna ha avuto davvero un orgasmo? Ecco i segnali del piacere femminile
- Non ho mai raggiunto l’orgasmo: è un problema? Quali soluzioni?
- Il sesso è davvero importante in una coppia?
- Amore senza sesso o sesso senza amore?
- Come distinguere un vero orgasmo femminile da uno “finto”
- L’orgasmo femminile è tutta questione di ritmo
- Lui ha il pene piccolo? I 6 trucchi per raggiungere lo stesso l’orgasmo
- Le 6 cose che gli uomini con il pene piccolo vogliono che la donna sappia
- Micropene: intervista a due uomini che hanno il pene piccolo
- Le donne rivelano le 16 piccole cose che rendono un uomo irresistibile
- Orgasmo femminile: dieci consigli per raggiungerlo più facilmente
- Differenza tra orgasmo maschile e femminile
- L’orgasmo e le altre fasi del ciclo di risposta sessuale
- Orgasmo maschile e femminile: nuovo studio sulle differenze fisiologiche
- Qual è la lunghezza media del pene?
- Come raggiungere un orgasmo femminile lungo ed intenso
- Orgasmo femminile: una donna su 5 non lo ha mai provato in vita sua
- Dare un nome al proprio pene ed altre cose che fanno gli uomini di nascosto
- Come avere un orgasmo vaginale
- Orgasmo femminile: le posizioni migliori per raggiungerlo
- Sintomi di eccitazione sessuale femminile e maschile
- Cos’è il liquido emesso da una donna durante l’orgasmo?
- Differenza tra ovaio microcistico, policistico e cisti ovariche
- Differenza tra ovaio policistico, micropolicistico e microfollicolare
- Differenza tra ovaio policistico e multifollicolare
- Ovaio: anatomia, funzioni e patologie in sintesi
- Vagina: anatomia, funzioni e patologie in sintesi
- Differenza tra vagina e vulva
- Utero: anatomia, funzioni, patologie e sintomi in sintesi
- Apparato genitale femminile: anatomia, funzioni e patologie in sintesi
- Quanto è profonda una vagina?
- Carcinoma dell’ovaio: quali sono i sintomi da non sottovalutare?
- In quale giorno e settimana del ciclo è più probabile rimanere incinta?
- Come e quando fare il test di gravidanza
- Che possibilità ho di rimanere incinta?
- Ho dimenticato di prendere la pillola contraccettiva, cosa faccio? Rischio di rimanere incinta?
- Perché l’uomo può avere figli per tutta la vita e la donna no?
- Quali sono le differenze tra orgasmo vaginale e clitorideo?
- Il liquido pre-eiaculatorio può indurre gravidanza e trasmettere l’HIV?
- Rimanere incinta: i 30 migliori consigli alla coppia per aumentare le possibilità di gravidanza
- Capire se sono incinta: i primi sintomi di gravidanza
- Perché ho un ritardo del ciclo? Quanti giorni devono passare prima di preoccuparmi? Come mi devo comportare?
- Il punto G femminile: come trovarlo e stimolarlo e quali sono le posizioni sessuali che più lo eccitano
- Restare incinta vergine senza penetrazione è possibile?
- Problemi di infertilità? E’ utile effettuare il Post-coital test
- E’ possibile essere vergini anche dopo essere state penetrate?
- E’ possibile non essere più vergini anche senza essere state penetrate?
- A che velocità viaggiano sperma e spermatozoi? Quanto è lungo il loro viaggio?
- Per quanto vivono gli spermatozoi dopo un’eiaculazione in vagina e nell’ambiente?
- Come fa uno spermatozoo a fecondare un ovulo femminile?
- Com’è fatto uno spermatozoo e quanto è piccolo rispetto al gamete femminile?
- Astenospermia: spermiogramma, spermatozoi deboli e fattori che influenzano la loro motilità
- Ipoposia: quando lo sperma è troppo poco. Cause e terapie per aumentare la quantità di eiaculato
- Masturbazione maschile: 10 cose che le donne non sanno
- Dieci ragazze raccontano le loro tecniche di masturbazione
- Tecniche di masturbazione femminile: 5 errori da non fare
- “Se ti tocchi diventi cieco”: tutti i falsi miti sulla masturbazione
- Maggio è il mese della masturbazione: tutto sull’orgasmo
- Masturbazione: ecco i 10 effetti sulla salute della donna
- Come bloccare sul nascere il desiderio di masturbarti in 10 passi
- Masturbazione maschile: suggerimenti per raggiungere orgasmi incredibili
- La masturbazione secondo la Bibbia è un peccato?
- USA: in arrivo la prima legge contro la masturbazione
- 13 ragioni per cui ogni donna dovrebbe masturbarsi regolarmente
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Sindrome X: è morta a 20 anni Brooke Greenberg, la “bambina” che non invecchiava mai
Ha trascorso la sua vita in braccio a mamma e papà. Aveva vent’anni ma il suo aspetto e la sua mente era quello di una bambina un anno o poco più. Brooke Greenberg è morta qualche giorno fa per cause non ancora note, nel Maryland (Stati Uniti). Era fra le pochissime persone al mondo (le stime parlano di meno di dieci malati) affette da una sindrome misteriosa denominata «X», che non permette a chi ne soffre di invecchiare, nè di crescere sin dall’infanzia. Brooke aveva tre sorelle cresciute normalmente e, secondo i medici, è vissuta inspiegabilmente a lungo. Ora il suo Dna potrebbe rivelare i segreti dell’eterna giovinezza.
LE ANOMALIE
Brooke viveva in un seggiolone e non è mai cresciuta. Le uniche parti del corpo che crescevano erano le unghie e i capelli e per anni le sono stati inutilmente somministrati speciali ormoni per la crescita, ma ogni terapia è risultata vana e nessun medico è mai riuscito a effettuare una diagnosi e a individuare con precisione il male di cui era affetta nonostante sia stata visitata dai più prestigiosi medici degli Stati Uniti. Test medici hanno dimostrato che Brooke potrebbe aver subito una mutazione del gene che spegne la capacità di crescere, ma nulla è mai stato chiarito davvero perché la piccola aveva anomalie apparenti nel sistema endocrino, ma non nei cromosomi. Il suo Dna, insieme a quello di casi simili, è ora sotto la lente della scienza perché potrebbe nascondere i segreti dell’eterna giovinezza e fornire importanti informazioni sul processo di invecchiamento che porta allo sviluppo di malattie come il morbo di Parkinson. «Anche dopo la sua morte Brooke potrà aiutarci a capire i meccanismi dell’invecchiamento» ha commentato Eric Schadt, direttore dell’Icahn Institute for Genomics and Multiscale Biology al Mount Sinai Medical Center di New York.
LA VITA DI BROOKE
Il blocco totale della crescita per Brooke è arrivato intorno ai 4 anni. Da allora in poi non è più cresciuta, non ha mai parlato e ha sempre mantenuto i denti da latte. «La crescita di Brooke è sempre stata strana sin da quando ero incinta – ha raccontato la madre Melanie ai media americani – un mese cresceva, poi si fermava, poi recuperava. È nata pretermine di un mese, pesava 1,8 chili, ma era nella norma». Negli anni successivi la bambina è stata colpita da una serie di emergenze mediche: ebbe sette ulcere gastriche perforate e attacchi di convulsioni. A cinque anni le fu diagnosticata una massa cerebrale che la portò in coma per due settimane, ma al risveglio della piccola la massa, che si sospettava fosse un tumore cerebrale scomparve. L’anno successivo superò un ictus. Quando è morta era alta 76 centimetri e pesava poco più di sette chili.
Leggi anche:
- Le malattie genetiche più diffuse al mondo
- Sindrome di Turner: cariotipo, cause, sintomi e segni caratteristici
- Sindrome di Klinefelter: cariotipo, cause, sintomi e cura
- Fibrosi cistica polmonare: cos’è, sintomi in neonati e bambini, cure
- Malattia di Huntington: cos’è, ereditarietà, come si trasmette, età di insorgenza
- Anemia falciforme: cosa significa, cause, sintomi e cure
- Differenze tra la distrofia muscolare di Duchenne e di Becker
- Talassemia: cos’è, sintomi, cure, differenti tipi ed alimentazione
- Celiachia: cos’è il glutine, in quali alimenti è contenuto ed in quali no?
- Sindrome di Noonan: cause, sintomi nel neonato, aspettative di vita
- Sindrome di Bloom: cause, sintomi, diagnosi e terapia
- Fetus in fetu: gemelli evanescenti e Sindrome del gemello parassita
- La donna che convive da 40 anni con un feto pietrificato nella panciaLa donna che convive da 40 anni con un feto pietrificato nella pancia
- Operata a Pechino la bambina cinese con un gemello parassita sulla schiena
- Lina Medina è la mamma più giovane al mondo: ha partorito il suo primo figlio a 5 anni
- Bambini scoprono per prima volta la loro ombra
- Arinia: la mancanza congenita del naso
- Il cardiochirurgo stremato dopo un trapianto cardiaco durato 23 ore
- Emette gas intestinali durante l’intervento chirurgico: i risultati sono disastrosi
- Trapianto di faccia: i casi più famosi al mondo
- Ipertimesia: la donna che ricorda tutto da quando è nata
- Ollie, il “bambino Pinocchio” nato con il cervello nel naso
- Sindrome del bambino scosso: i gravissimi danni della violenza sul neonato
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

