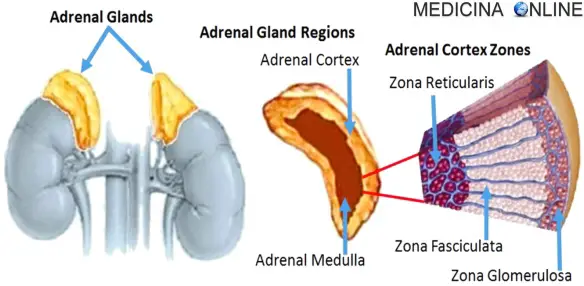
 La sindrome di Conn, o iperaldosteronismo primario, è una malattia dovuta ad un eccesso di produzione di aldosterone da parte della corticale del surrene con conseguente basso livello di renina. L’aldosterone è un ormone steroideo prodotto dalla zona glomerulare della corticale (la parte più esterna) del surrene. È il capostipite degli ormoni mineralcorticoidi che, come i glucocorticoidi, vengono prodotti nella corteccia del surrene (entrambi appartengono quindi al gruppo dei corticosteroidi) ma attraverso due vie biosintetiche distinte.
La sindrome di Conn, o iperaldosteronismo primario, è una malattia dovuta ad un eccesso di produzione di aldosterone da parte della corticale del surrene con conseguente basso livello di renina. L’aldosterone è un ormone steroideo prodotto dalla zona glomerulare della corticale (la parte più esterna) del surrene. È il capostipite degli ormoni mineralcorticoidi che, come i glucocorticoidi, vengono prodotti nella corteccia del surrene (entrambi appartengono quindi al gruppo dei corticosteroidi) ma attraverso due vie biosintetiche distinte.
La sindrome di Conn spesso produce pochi sintomi. La maggior parte delle persone presenta alta pressione sanguigna che può causare danni alla vista (retinopatia ipertensiva ) e/o emicranie. Occasionalmente può esserci debolezza muscolare, spasmi muscolari, sensazioni di formicolio o urinazione eccessiva. Le complicanze includono malattie cardiovascolari come ictus, infarto miocardico, insufficienza renale e aritmie. L’aldosteronemia primaria è presente in circa il 10% delle persone con pressione alta. Si verifica più spesso nelle donne tra i 30 ed i 50 anni di età. Può portare a ipopotassemia e alcalosi, l’aumentata produzione di aldosterone determina, infatti, una perdita di potassio nelle urine con conseguente ipopotassiemia; è la causa più comune di ipertensione secondaria.
Cause
L’iperaldosteronismo primario ha una serie di cause. Circa il 66% dei casi è dovuto all’iperplasia surrenale congenita, il 33% dei casi è dovuto ad un adenoma surrenale che produce l’aldosterone . Altre cause non comuni includono un cancro surrenale e un disturbo ereditario chiamato iperaldosteronismo familiare. Alcuni consigliano di fare screening nella popolazione ipertesa con maggiore rischio maggiore mentre altri raccomandano di screenare tutte le persone con alta pressione sanguigna per la Sindrome di Conn. Lo screening è di solito effettuato misurando il rapporto aldosterone-renina nel sangue con ulteriori test utilizzati per confermare i risultati positivi. Mentre il basso livello di potassio nel sangue, che è descritto classicamente in letteratura, è presente solo in circa un quarto di persone. Per determinare la causa sottostante si effettua l’imaging medico. La condizione è causata da:
- iperplasia surrenale congenita bilaterale (micronodulare) (66% dei casi);
- adenoma surrenale (sindrome di Conn) (33%);
- iperplasia surrenale primaria (unilaterale) (2%);
- carcinoma adrenocorticale che produce aldosterone (<1%);
- iperaldosteronismo famigliare;
- aldosteronismo (FH tipo I) (<1%);
- FH tipo II (APA o IHA) (2%);
- adenoma o carcinoma produttivo di aldosterone ectopico (<0,1%).
Leggi anche:
- Iperaldosteronismo primario e secondario: tipi e sintomi
- Iperaldosteronismo secondario: cause, sintomi e terapia
Genetica
Il 40% delle persone affette da un adenoma surrenale che produce aldosterone presenta mutazioni somatiche di gain of function in un singolo gene (KCNJ5). Questo gene è mutato nei casi ereditari, anche se meno frequentemente. Queste mutazioni tendono ad avvenire in giovani donne con un adenoma nella zona fascicolatasecernente cortisolo. Gli adenomi senza questa mutazione tendono a colpire uomini anziani con un’ipertensione resistente.
Fisiopatologia
L’aldosterone ha effetti sulla maggior parte o su tutte le cellule del corpo, ma, clinicamente, le azioni più importanti sono sul rene, sulle cellule del tubulo distale e nel condotto di raccolta. Nelle cellule principali, l’aldosterone aumenta l’attività della sodio-potassio ATPasi nella membrana basalaterale e dei canali sodio apicali, ENaC, così come i canali di potassio, ROMK. Queste azioni aumentano il riassorbimento del sodio e la secrezione di potassio. Poiché l’aumento del riassorbimento del sodio, rispetto al potassio secreto, rende anche il lume del tubulo più elettricamente negativo, permettendo al cloruro di seguire il sodio. L’acqua segue quindi il sodio e il cloruro per osmosi. Nella sindrome di Conn, queste azioni causano un aumento del volume di sodio e di liquido extracellulare e una riduzione del potassio extracellulare. L’aldosterone agisce anche sulle cellule intercalate per stimolare l’ATPasi apicale, causando la secrezione di protoni che acidifica l’urina e alcalizza il fluido extracellulare. In sintesi, l’iperaldosteronismo provoca l’ipernatremia, l’ipokalemia e l’alcalosi metabolica. Inoltre l’aldosterone permette la stimolazione dell’ATPasi sodio-potassio nelle cellule muscolari, aumentando il potassio intracellulare e aumenta anche il riassorbimento di sodio lungo l’intestino e il nefrone. Infine, le cellule epiteliali dei condotti del sudore e della superficie distale del colon rispondono esattamente come le cellule principali del nefrone. Queste risposte sono importanti nell’adattamento al clima e come causa di costipazione nei quadri clinici con elevato aldosterone. La ritenzione di sodio porta ad espansione del volume plasmatico e all’aumento di pressione arteriosa. Quest’ultima porterà ad un aumento della velocità di filtrazione glomerulare e causerà una diminuzione della rilascio di renina dalle cellule granulari dell’apparato iuxtaglomerulare nel rene, diminuendo il riassorbimento di sodio e restituendo l’escrezione renale di sodio a livelli prossimi ai normali consentendo al sodio di “sfuggire” all’effetto dei Mineralcorticoidi (noto anche come meccanismo di fuga dall’Aldosterone nel iperaldosteronismo primario che contribuisce anche all’aumento del livello di peptide natriuretico atriale. In caso di iperaldosteronismo primario, la diminuzione della renina (e successiva riduzione dell’angiotensina II) non comporterà una riduzione dei livelli di aldosterone . Questo è uno strumento clinico molto utile nella diagnosi di iperaldosteronismo primario.
Sintomi
Tra i sintomi oltre all’ipertensione vi possono essere stanchezza, debolezza muscolare ed aumentata emissione di urine (poliuria), specie di notte (nicturia). L’alta pressione sanguigna, le manifestazioni di crampi muscolari (a causa dell’ipereccitabilità dei neuroni per il basso livello di calcio nel sangue), la debolezza muscolare (dovuta all’ipoeccitabilità dei muscoli scheletrici secondaria all’ipocalemia) ed emicrania (a causa di bassi valori di potassio o di alta pressione sanguigna) possono essere osservate. L’iperaldosteronismo secondario è spesso correlato a una diminuzione della gittata cardiaca associata a livelli di renina elevati.
Diagnosi
La diagnosi inizia con lo screening dell’aldosterone e del rapporto di valori dell’aldosterone plasmatico (ALDO) e dell’attività della renina plasmatica (PRA), detto “rapporto ALDO/PRA”. Se questi due test restituissero valori alti, si può procedere a:
- test di inibizione, con il Test di carico salino (infusione di soluzione fisiologica) od il Test con Captopril;
- test di stimolo, con il Test di deplezione sodica (dieta iposodica e furosemide) od il Test dell’ortostatismo;
- prova di normalizzazione della pressione arteriosa, attraverso il Test con Spironolattone.
Per individuare la sede della malattia, si possono usare i seguenti esami:
- TC addome;
- Adrenal Venous Sampling (cateterismo selettivo delle vene surrenali);
- scintigrafia.
Trattamento
Alcuni casi possono essere curati rimuovendo l’adenoma con un intervento chirurgico. Può anche essere rimossa una singola ghiandola surrenale nei casi in cui solo una sia aumentata di volume. Nei casi dovuti all’aumento di volume di entrambe le ghiandole il trattamento è in genere con farmaci come antagonisti dell’aldosterone come spironolattone o eplerenone. Possono anche essere necessari altri farmaci per la gestione dell’alta pressione sanguigna e una dieta a basso contenuto di sale. Alcune persone con iperaldosteronismo familiare possono essere trattate con uno steroide come il Desametasone.
Leggi anche:
- Pressione arteriosa: i momenti della giornata in cui è più alta
- Come si misura la pressione arteriosa? Guida facile
- Ipertensione: quali farmaci usare per abbassare la pressione arteriosa?
- Sarò iperteso per tutta la vita? Dovrò continuare ad assumere il farmaco per sempre?
- Non riesco a controllare la pressione arteriosa alta
- Surrene: anatomia, funzioni e patologie in sintesi
- Asse ipotalamo-ipofisi-surrene: funzionamento ed ormoni rilasciati
- Cos’è l’adrenalina ed a cosa serve?
- Adrenalina e “combatti o fuggi”: ecco cosa accade nel nostro corpo quando siamo terrorizzati
- Vasopressina (ormone antidiuretico o ADH): funzioni e patologie
- Differenza tra beta bloccanti, ace inibitori, calcio antagonisti, sartani e diuretici
- Testosterone basso, alto, valori normali ed interpretazione
- Ormoni estrogeni: cosa sono e quali funzioni svolgono?
- Progesterone: cos’è, a cosa serve, valori e quali funzioni ha in gravidanza?
- Sistema renina-angiotensina-aldosterone: schema ed effetti
- Quando la donna ha troppi peli dove non dovrebbero essere: irsutismo, cause, trattamenti e differenze con ipertricosi
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Ipotalamo: anatomia, struttura e funzioni
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Asse ipotalamo-ipofisi-gonade: funzionamento ed ormoni rilasciati
- Asse ipotalamo-ipofisi-testicolo: funzionamento ed ormoni rilasciati
- Asse ipotalamo-ipofisi-tiroide: funzionamento ed ormoni rilasciati
- Differenze tra adrenalina e noradrenalina
- Apparato urinario: anatomia e fisiologia [SCHEMA]
- Rene: anatomia, funzioni e patologie in sintesi
- Differenza tra surrene e rene
- Dopammina: cos’è ed a che serve?
- Neurotrasmettitori: cosa sono ed a che servono
- Si può vivere senza reni? Conseguenze della nefrectomia
- Dopammina: biosintesi, rilascio nello spazio sinaptico e degradazione
- Sistema dopamminergico: i circuti nervosi della dopammina
- Colesterolo: cos’è ed a cosa serve?
- Adrenalina ed epinefrina sono la stessa cosa?
- Ormone della crescita (GH) a che serve e da cosa è prodotto?
- Serotonina e triptofano: cosa sono e in quali cibi trovarli
- Glutamina: a che serve, quando assumerlo, dosi ed effetti collaterali
- Creatinina alta o bassa: cos’è, cosa indica e come si corregge
- Rene: anatomia, funzioni e patologie in sintesi
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
