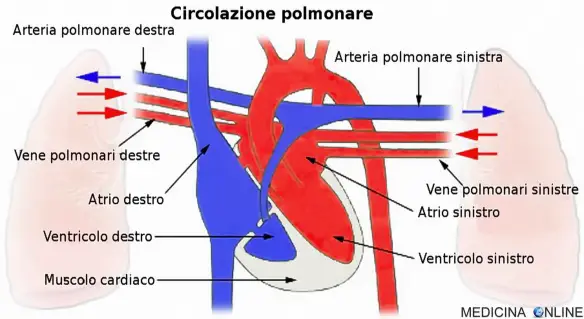
 Lo scompenso cardiaco (o “insufficienza cardiaca“) è una condizione patologica caratterizzata dalla incapacità del cuore a pompare una quantità di sangue sufficiente a fare fronte alle richieste metaboliche dell’organismo: in conseguenza a ciò si verifica uno shock circolatorio (insufficienza circolatoria) che in questo caso viene denominato “cardiogeno”.
Lo scompenso cardiaco (o “insufficienza cardiaca“) è una condizione patologica caratterizzata dalla incapacità del cuore a pompare una quantità di sangue sufficiente a fare fronte alle richieste metaboliche dell’organismo: in conseguenza a ciò si verifica uno shock circolatorio (insufficienza circolatoria) che in questo caso viene denominato “cardiogeno”.
Fisiopatologia
Il risultato della perfomance della pompa cardiaca è la gittata cardiaca (Qr) o flusso esterno ventricolare espresso
in litri/minuto. La gittata cardiaca è principalmente influenzata dalla frequenza cardiaca (HR) e dalla gittata pulsatoria
(SV). La descrizione matematica di questa interazione è data dal seguente semplice prodotto:
QT= HRxSV
La frequenza cardiaca è regolata dal sistema di stimolazione del cuore ed influenzata dai neurotrasmettitori (norepinefrina ed acetilcolina) rilasciati dal sistema nervoso autonomo. La gittata pulsatoria è influenzata dal ritorno venoso (pressione di riempimento, precarico), dalla resistenza al flusso (postcarico), dalla contrattilità miocardica e distensibilità ventricolare. Nel cuore normale esiste un eccezionale grado di autoregolazione della gittata cardiaca tra le sezioni destra e sinistra, così da prevenire la comparsa di squilibri di gittata. La differenza infatti, di 1 solo millilitro/minuto può portare alla comparsa di congestione venosa a monte del ventricolo insufficiente. L’esistenza di un più ridotto circuito di riserva a monte del ventricolo sinistro porta alla comparsa di sintomi in presenza di un minore grado di disfunzione rispetto a quella necessaria per le sezioni destre del cuore. La più spessa parete ventricolare sinistra è, però, in grado di sostenere un maggior carico di lavoro rispetto alla più sottile parete ventricolare destra. Inoltre, la limitata capacità funzionale del ventricolo destro lo predispone alla insufficienza ogni qualvolta esso viene sottoposto a crescenti livelli di precarico, postcarico o entrambi. In conseguenza di ciò è frequente la comparsa di una insufficienza ventricolare destra, secondaria all’insufficienza ventricolare sinistra primitiva. È interessante notare, però, che la comparsa dell’insufficienza ventricolare destra riduce il grado di congestione polmonare e quindi il precarico del ventricolo sinistro insufficiente e, pertanto, fornisce essa stessa un certo tipo di compenso. Raramente uno scompenso primitivo del cuore destro porta alla comparsa di una insufficienza ventricolare sinistra.
Performance miocardica
Le fibre miocardiche del cuore scompensato presentano caratteristicamente una riduzione delle capacità lunghezza-tensione e forza-velocità allorquando vengono stimolate a contrarsi: ciò porta il cuore scompensato a presentare ridotta contrattilità e ridotta capacità di produrre una normale frazione di eiezione (percentuale del volume telediastolico pompato dal ventricolo in una contrazione sistolica). La normale frazione di eiezione è approssimativamente del 70% e può ridursi a valori del 20% o inferiori nei casi di severa insufficienza cardiaca. Tre tipi di meccanismi di compenso migliorano l’efficienza miocardica, sia durante le condizioni di aumentata richiesta oppure in caso di scompenso cardiaco.
1) Risposta del sistema nervoso simpatico
Il rilascio di norepinefrina stimola i β-recettori del sistema di stimolazione cardiaco e il miocardio. Ciò determina, quindi, un aumento della frequenza cardiaca e della forza di contrazione miocardica che, a sua volta, determina un aumento della gittata cardiaca. Durante un episodio acuto di insufficienza cardiaca si osserva un aumento dell’attività simpatica e delle concentrazioni plasmatiche di norepinefrina, sia a riposo che dopo sforzo. Questa risposta aumenta inizialmente l’efficienza cardiaca ma, a lungo andare, porta ad una diminuita risposta del cuore a queste stesse sostanze. Successivamente, la stimolazione simpatica può portare alla comparsa di sintomi ischemici, quando il metabolismo miocardico supera la capacità del circolo coronarico di rifornirlo di una adeguata quantità di sangue. Nello scompenso cardiaco di lunga data, molti pazienti sviluppano quindi una persistente tachicardia che non risponde alla stimolazione bradicardizzante parasimpatica. Ciò conduce, in definitiva, ad una condizione in cui il cuore non è più in grado di modificare la propria frequenza a riposo o durante l’attività fisica.
2) Risposta di Frank-Starling
Quando le fibre miocardiche vengono stirate da pressione e volume ventricolare telediastolici crescenti, esse si contraggono con maggiore forza. La figura che vedete qui in basso illustra questa relazione nel cuore normale con aumentata contrattilità (ad esempio sotto l”influsso dell’epinefrina o della digossina) ed in un cuore con ridotta contrattilità (ad esempio nello scompenso cardiaco).
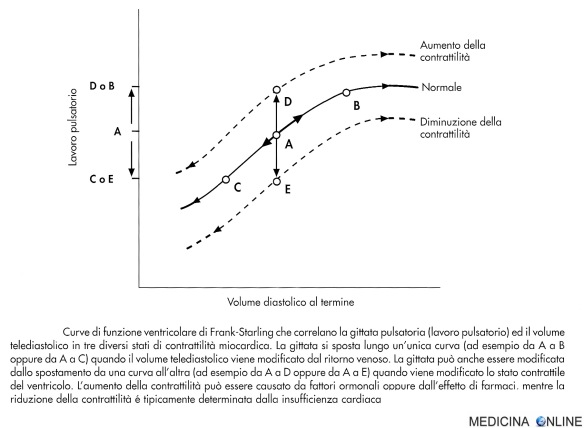
Nel cuore normale, l’aumentato ritorno venoso e il conseguente riempimento ventricolare che accompagnano lo sforzo fisico oppure altre forme di stress, vengono facilmente compensati per intero da questi meccanismi. L’insufficienza ventricolare provoca, invece, un progressivo aumento del volume telediastolico ventricolare ed una conseguente dilatazione del ventricolo. Per complicare ulteriormente l’efficienza cardiaca, un volume telediastolico eccessivamente elevato riduce la distensibilità ventricolare, il che a sua volta porta alla riduzione della contrattilità e vanifica o riduce notevolmente il riflesso di Frank-Starling, contribuendo ulteriormente alla genesi dello scompenso cardiaco congestizio.
3) Risposta ventricolare ipertrofica
L’ipertrofìa, aumento dello spessore e della massa muscolare cardiaca, è prodotta
dalla esposizione cronica ad elevate pressioni vascolari, ad alti volumi ematici e ad un incremento del rilascio di neurotrasmettitori (ad esempio norepinefrina e dopamina). Sebbene l’ipertrofia migliori la forza di contrazione miocardica nelle fasi precoci dello scompenso cardiaco tale beneficio viene, alla fine, superato dalla riduzione della distensibilità ventricolare e dalla accresciuta forza necessaria per comprimere il ventricolo dilatato. Questa condizione è, spesso, ulteriormente esacerbata dalle modificazioni ischemiche causate dall’inadeguato apporto di ossigeno ad un miocardio dilatato ed iperespanso in condizioni di aumentato lavoro cardiaco. L’ipertrofia non è necessariamente un fenomeno permanente nel caso in cui essa si instauri in breve tempo e può essere quindi successivamente corretta. Tale regressione non è, infatti, infrequente, ad esempio dopo sostituzione protesica valvolare di una valvola aortica stenotica.
Circolazione polmonare e periferica
Nello scompenso cardiaco congestizio si verifica una significativa ridistribuzione del flusso ematico che agisce come importante meccanismo compensatorio. Questa modificazione provoca la deviazione di una già ridotta gittata cardiaca dalla circolazione renale e cutanea verso i più importanti circoli coronarico e cerebrale. Ciò non si verifica soltanto a riposo ma anche, in misura ancora maggiore, durante sforzo oppure nelle altre forme di incremento metabolico mediate dalla attivazione del sistema nervoso simpatico. Durante lo scompenso cardiaco le resistenze vascolari sistemiche solitamente aumentano, in seguito agli effetti vasoattivi degli elevati livelli plasmatici di noradrenalina e per l’imbibizione della parete vasale ad opera dell’aumentato assorbimento di sodio ed acqua. Tale complesso di eventi porta alla generalizzata incapacità dell’apparato circolatorio di vasodilatazione, il che limita la capacità di aumentare il trasporto di ossigeno e disperdere calore durante l’attività fisica e le altre forme di stress. Questi pazienti, pertanto, sono spesso molto sensibili al calore e presentano una ridotta tolleranza allo sforzo. L’insufficienza ventricolare destra determina ipertensione venosa e congestione capillare periferica, con comparsa di stasi epatica, ipertensione portale, riduzione del drenaggio linfatico verso il sistema venoso e ritenzione di fluidi nello spazio extracellulare di varie sedi (ad esempio estremità declivi, cavità peritoneale e pleurica). L’insufficienza ventricolare sinistra, invece, determina la comparsa di stasi ed ipertensione del circolo polmonare con possibile cuore polmonare. Inizialmente, l’ipertensione polmonare porta ad un incremento del flusso verso i lobi polmonari superiori o nelle zone non declivi. Un ulteriore aggravamento dell’insufficienza ventricolare sinistra conduce, invece, ad un ancora maggiore incremento delle pressioni vascolo-polmonari, il che può portare alla comparsa di congestione ed edema polmonare.
Equilibrio idro-elettrolitico
Nello scompenso cardiaco congestizio, la riduzione della gittata cardiaca e la vasocostrizione generalizzata determinano l’ipoperfusione renale. Tale modificazione circolatoria porta, a sua volta, alla riduzione della ftltrazione glomerulare ed alla successiva ritenzione di sodio ed acqua. La stasi venosa sistemica, che compare durante lo scompenso ventricolare destro, può portare invece alla comparsa di ipertensione venosa renale che può contribuire alla riduzione della ftltrazione glomerulare ed all’aumento del riassorbimento del sodio. Sono pertanto l’ipoperfusione sistemica e la stasi venosa, oppure entrambe, a determinare le modificazioni renali che caratterizzano la componente congestizia della scompenso cardiaco.
Durante lo scompenso cardiaco, in aggiunta alle modificazioni vascolari renali causate dalla norepinefrina, numerosi altri cambiamenti ormonali sono in grado di modificare la funzionalità renale. La riduzione della perfusione renale stimola, infatti, la produzione di renina da parte dell’apparato iuxta-glomerulare renale, la quale – a sua volta – stimola la produzione di angiotensina I, successivamente convertita ad angiotensina II dopo il passaggio attraverso il circolo polmonare. L’angiotensina II, a sua volta, stimola il riassorbimento tubulare di sodio, causa una vasocostrizione che aggrava l’ipoperfusione renale e stimola la secrezione surrenalica di aldosterone. L’aldosterone induce, infine, una ulteriore ritenzione di sodio da parte del rene.
In conseguenza di queste modificazioni renali, i pazienti in scompenso cardiaco presentano spesso un aumento del volume ematico (aumento della volemia), del liquido interstiziale ed un aumento del quantitativo totale di sodio dell’organismo. Tale alterazione dell’equilibrio idro-elettrolitico, associato ad una scadente funzionalità cardiaca, può facilmente condurre alla formazione di edema sistemico o polmonare, conseguenza, rispettivamente, dell’insufficienza ventricolare sinistra e destra.
Formazione dell’edema
Il movimento di fluidi attraverso la parete dei vasi dal compartimento intravascolare a quello interstiziale è un fenomeno fisiologico. Il movimento dell’acqua è governato dalla permeabilità della parete capillare e dall’equilibrio tra la pressione idrostatica e la pressione osmotica. L’esistenza di tale equilibrio di proprietà e forze dà origine ad una forza netta verso l’esterno del vaso, di intensità di circa 10 mmHg, la quale porta al movimento di circa 150 ml/ora di liquido verso l’interstizio. In condizioni normali il liquido viene drenato dai linfatici verso la circolazione venosa sistemica stabilizzando il volume dei liquidi interstiziali.
Si definisce edema la evidenziazione clinica dell’accumulo di liquido negli spazi interstiziali dell’organismo. Numerose diverse condizioni possono portare alla formazione dell’edema:
- Aumento della permeabilità capillare (ad esempio per effetto dell’istamina)
- Aumento della pressione idrostatica capillare
- Riduzione della concentrazione proteica del plasma (ad esempio ipoalbuminemia) che provoca una riduzione della ritenzione osmotica dell’acqua intravascolare
- Ostruzione linfatica
Lo scompenso cardiaco congestizio è caratterizzato dall’aumento della pressione capillare polmonare che, quando raggiunge valori di 18-25 mmHg determina un accumulo di liquidi lungo le pareti dei vasi, intorno alle piccole vie aeree e nello spazio pleurico. Tale fenomeno avviene, inizialmente, nelle regioni declivi del polmone a livello delle quali, per azione della forza di gravità, la pressione è tendenzialmente più elevata già in condizioni fisiologiche. Con il peggiorare della gravità dello scompenso ventricolare sinistro, compare l’edema polmonare nelle regioni del polmone dove la pressione supera i 25 mmHg.
Disfunzione polmonare
Nel corso dell’insufficienza ventricolare sinistra la funzionalità polmonare è spesso alterata, come intuibile dalla tabella riportata di seguito:

Disfunzioni polmonari durante lo scompenso cardiaco ventricolare sinistro
Nelle fasi avanzate dello scompenso cardiaco congestizio, tale alterazione funzionale è marcata mentre, al contrario, nelle fasi precoci della patologia congestizia la presenza di una lieve ipertensione polmonare (ad esempio pressione di incuneamento polmonare di 15-22 mmHg) può in realtà migliorare lo scambio gassoso, a causa di un incremento del volume ematico polmonare e del miglioramento dell’equilibrio ventilazione/perfusione [V/Q]. Al peggiorare dello scompenso cardiaco congestizio e dell’aumento della congestione polmonare, si osserva un aumento del contenuto di acqua nei polmoni. L’edema polmonare riduce il volume di quest’organo e la capacità di diffusione gassosa, aumenta la resistenza a livello delle vie aeree e provoca uno squilibrio [V/Q]. Una grave insufficienza cardiaca ed il franco inondamento intralveolare portano, invece, ad un drammatico deterioramento della capacità vitale forzata, della distensibilità polmonare ed alla comparsa di una acidosi mista respiratoria e metabolica. Tali modificazioni causano, a loro volta, una ulteriore disfunzione cardiopolmonare ed innescano un circolo vizioso di insufficienza cardiaca e respiratoria.
Per approfondire:
- Scompenso cardiaco (insufficienza cardiaca): cause e fattori di rischio
- Scompenso cardiaco (insufficienza cardiaca): sintomi, segni, diagnosi, esami
- Scompenso cardiaco: trattamento farmacologico e chirurgico
- Shock circolatorio (insufficienza circolatoria): cause, sintomi, diagnosi, cure
- Gittata cardiaca, indice cardiaco, pre-carico, post-carico e contrattilità
- Cuore polmonare: cause, sintomi, diagnosi, esami, trattamento
Leggi anche:
- Com’è fatto il cuore, a che serve e come funziona?
- Shock ipovolemico, emorragico, allergico, anafilattico, cardiogeno, ostruttivo, distributivo, settico
- Shock ipovolemico emorragico: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock ipovolemico non emorragico: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock settico e sepsi: sintomi, terapia, conseguenze, si può guarire
- Shock settico e tossico: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock ostruttivo: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock da ustione: cos’è, quando si verifica, sintomi e cure
- Shock cardiogeno: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Scompenso cardiaco: cause, sintomi iniziali, tipi, cure
- Infarto cardiaco: sintomi premonitori, cause, cosa fare, enzimi, cure
- Sindrome coronarica acuta: sintomi, terapia, classificazione, cura
- Insufficienza cardiaca (scompenso cardiaco): cause, sintomi iniziali, tipi, cure
- Palpitazioni (cardiopalmo) a riposo, da ansia, notturne, dopo mangiato
- Cardiopatia ischemica: cronica, definizione, sintomi, conseguenze
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Differenza tra sindrome coronarica acuta ed infarto
- Infarto, ischemia, necrosi, aterosclerosi, trombo, embolo, ictus, miocardio… Facciamo chiarezza
- Esame obiettivo cardiovascolare: guida completa all’esecuzione
- Semeiotica del cuore: i focolai di auscultazione cardiaca
- Semeiotica del cuore: i 4 toni cardiaci ed i toni aggiunti
- Semeiotica del cuore: i soffi cardiaci sistolici e diastolici
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Come si muove il sangue all’interno del cuore?
- Che differenza c’è tra sistole e diastole?
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Come funziona uno sfigmomanometro (apparecchio per la pressione)
- Differenza tra pressione venosa centrale e periferica
- Cos’è la pressione venosa centrale e perché si misura?
- Cos’è la pressione sistemica di riempimento?
- Perché la pressione venosa è inferiore a quella arteriosa
- Qual è la differenza tra arteria e vena?
- Emorragia interna: definizione, cause, sintomi, diagnosi, gravità, terapia
- Emorragia interna: rischi, morte per dissanguamento, compressione, danni
- Emorragia interna: diagnosi, colore del sangue, sintomi e segni
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!
