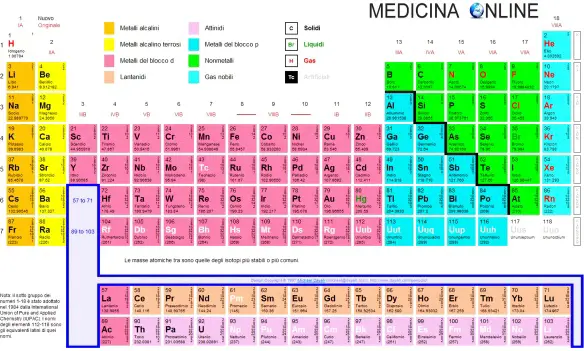
 Dimitri Mendeleev, scienziato russo, concepì il primo modello di tavola periodica nel 1869, disponendo gli allora 63 elementi noti verticalmente, per poi passare alla schematizzazione orizzontale che è quella odierna che vedete nell’immane in alto, che è ad alta risoluzione e stampabile. La tavola periodica è lo schema secondo il quale sono ordinati gli elementi i quali vengono disposti uno accanto all’atro, secondo il numero atomico (z) che indica il numero dei protoni presenti nel nucleo e conseguentemente quello degli elettroni che orbitano intorno ad esso.
Dimitri Mendeleev, scienziato russo, concepì il primo modello di tavola periodica nel 1869, disponendo gli allora 63 elementi noti verticalmente, per poi passare alla schematizzazione orizzontale che è quella odierna che vedete nell’immane in alto, che è ad alta risoluzione e stampabile. La tavola periodica è lo schema secondo il quale sono ordinati gli elementi i quali vengono disposti uno accanto all’atro, secondo il numero atomico (z) che indica il numero dei protoni presenti nel nucleo e conseguentemente quello degli elettroni che orbitano intorno ad esso.
Gli elementi della tavola periodica sono 118, alcuni sono solamente ipotetici, mentre altri sono stati scoperti di recente. Gli elementi sono organizzati in proporzione della legge periodica, del 1868, la quale afferma che le proprietà fisiche e chimiche degli stessi variano in funzione periodica secondo il numero atomico. La periodicità è dovuta alla struttura elettronica degli elementi, che si ripresenta periodicamente a intervalli regolari. In accordo con ciò la tavola periodica è costituita da periodi e gruppi.
Sono dette periodi le 7 righe orizzontali. Il numero di ciascun periodo indica il livello principale di energia sul quale è possibile trovare gli elettroni di valenza di tutti gli elementi del periodo.
Prendono invece il nome di gruppi le colonne verticali. I gruppi hanno una doppia numerazione: la prima in numeri arabi da 1 a 18 e la seconda in numeri arabi da I a VIII. Al numero romano corrisponde il numero degli elettroni di valenza. Gli elementi che si trovano nello stesso gruppo hanno quindi la stessa configurazione elettronica esterna.
I gruppi possiedono proprietà fisiche e chimiche simili e si dividono in due sezioni: gruppo A con elementi significativi e gruppo B con elementi di transizione.
Nel gruppo IA e IIA troviamo i metalli (eccetto l’Idrogeno), nel gruppo IIIA e VIIIA troviamo i non metalli (eccetto l’Elio). Gli elementi dell’VIII gruppo sono i gas nobili, i quali possiedono un’alta stabilità dovuta alla tendenza di non combinarsi con gli altri poiché hanno l’ottetto completo ovvero otto elettroni sull’orbitale esterno. Sono quindi poco reattivi e possono legarsi solo tra di loro.
Gli elementi del VII gruppo sono gli alogeni e tendono a legarsi con i metalli.
La tavola periodica ha una linea di “gradini” rossa che va dal Boro all’Astato e segna i metalli dai non metalli, semi-metalli, metalloidi.
Ai sette periodi sono aggiunte, nella parte inferiore, due righe ch includono gli elementi di transizione interna, dei Lantanidi e Attinidi.
I Lantanidi sono 14 elementi che vanno dal Cerio al Lutezio. Sono piuttosto reattivi ed hanno proprietà chimiche simili tra loro.
Gli Attinidi sono 14 elementi che vanno dall’Orio al Laurenzio e sono quasi tutti di origine artificiale.
Per approfondire, leggi anche:
- Differenza tra elemento, composto e miscuglio con esempi
- Differenza tra minerale, roccia, cristallo, vetro, metallo, elemento chimico
- Differenza tra atomo e elemento
- Differenza tra atomo e molecola con esempi
- Differenza tra atomo e nucleo
- Differenza tra anfipatica ed anfotera
- Differenza tra elemento chimico e composto
- Differenza tra miscuglio omogeneo ed eterogeneo con esempi
- Liquido in chimica: definizione e caratteristiche fisiche
- Differenza tra fluido e liquido
- Differenza tra liquidi volatili e non volatili in chimica
- Differenza tra fluido newtoniano e non newtoniano con esempi
- Differenza tra fluido ideale e reale
- Differenza tra soluzione ipertonica, ipotonica ed isotonica in chimica
- Differenza tra soluzione, sospensione aerosol ed emulsione in chimica
- Differenza tra soluzione e miscuglio in chimica con esempi
- Differenza tra soluzione e miscela in chimica con esempi
- Differenza tra miscela omogenea ed eterogenea
- Differenza tra soluzione e dispersione in chimica con esempi
- Sali minerali: definizione, funzioni, alimenti, integratori [GUIDA COMPLETA]
Leggi anche:
- Ferro: alimenti ricchi di ferro, fabbisogno giornaliero, integratore
- Integratore di zinco: proprietà sessuali e sintomi della sua carenza
- Iodio importante per prevenire le malattie della tiroide: in quali alimenti trovarlo?
- Selenio: benefici, integratore in compresse, controindicazioni
- Manganese: integratore, benefici, proprietà, alimenti, dose
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Classifica dei cibi con maggior quantità di fluoro esistenti
- Beta carotene: cos’è, a cosa serve e in quali cibi lo trovo?
- Anemia da carenza di ferro: cause, sintomi e cure
- Spirulina: cos’è, proprietà, dove comprarla, posologia, controindicazioni
- Integratori per la fertilità che aumentano le possibilità di gravidanza
- Integratore di Colina: efficace per aumentare la memoria
- Integratore di Inositolo: benefici, dimagrimento e controindicazioni
- Glucomannano: l’integratore che nel tuo stomaco aumenta di 100 volte il proprio volume, ti sazia e ti impedisce di mangiare troppo
- La stevia ti aiuta a smettere di fumare sigarette: come assumerla
- Melatonina 1 e 2mg per insonnia: quando assumerla e controindicazioni
- Ecco come il nostro corpo ci segnala la carenza di vitamine
- Misurazione della pressione: i migliori sfigmomanometri automatici
- Sarò iperteso per tutta la vita? Dovrò continuare ad assumere il farmaco per sempre?
- Non riesco a controllare la pressione arteriosa alta
- Cosa fare in caso di picco di pressione arteriosa elevato?
- Emocromo: valori di riferimento e significato clinico [SCHEMA]
- Ematocrito (HCT): basso, alto, in gravidanza, valori normali e interpretazione
- Emoglobina bassa, alta, cause e valori normali
- Ormoni tiroidei: differenza T3 e T4, valori normali e patologici
- TSH alto, basso e valori normali: qual è il significato clinico?
- Tireoglobulina alta, bassa, valori normali ed interpretazione
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
- Ecografia della tiroide: a cosa serve, come si svolge e come ci si prepara all’esame
- Ipotiroidismo: sintomi, diagnosi, cura farmacologica e consigli dietetici
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- VES alta o bassa: cause, sintomi e valori normali della velocità di eritrosedimentazione
- Esame delle urine completo con urinocoltura: come fare e capire i risultati
- Scura o chiara, liquida o schiumosa: la tua urina rivela la tua salute
- Le tue feci dicono se sei in salute: con la Scala di Bristol impara ad interpretarle
- Parassiti e vermi nelle feci: sintomi e come eliminarli con farmaci e rimedi naturali
- Coprocoltura e antibiogramma: procedura e perché si eseguono
- Esame e raccolta delle feci: come si fa nel modo corretto ed a che serve
- Paratiroidi: anatomia e funzioni in sintesi
- Paratiroidectomia: intervento, convalescenza e conseguenze
- Feedback negativo ed omeostasi: spiegazione ed esempi
- Differenza tra acidosi ed alcalosi, metabolica e respiratoria
- Osteoporosi: cause, diagnosi, cure, osteopenia e valori T-score
- Dibase (vitamina D): posologia, effetti collaterali [FOGLIETTO ILLUSTRATIVO]
- Vitamina D: sintomi che indicano la sua carenza e cibi che la contengono
- Ipoparatiroidismo e ipocalcemia post chirurgici ed autoimmuni: sintomi e cure
- Tiroidectomia totale: complicanze, postoperatorio e aumento di peso
- Tiroide: anatomia, funzioni e patologie in sintesi
- Paratormone: cos’è, alto, basso, cause, valori normali e patologici
- Alterazioni dell’equilibrio acido-base: acidosi ed alcalosi respiratorie e metabolica
- Ipoparatiroidismo primitivo, secondario autoimmune, cure
- Iperparatiroidismo primitivo, secondario normocalcemico, cure, dieta
- Tiroidectomia: cosa cambierà nella mia vita dopo l’intervento?
- Tiroidectomia: cosa mi succederà prima, durante e dopo l’intervento chirurgico
- Eutirox: quando si usa, dosaggio ed effetti collaterali (foglio illustrativo)
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Nodulo Tiroideo – sintomi e cure
- Cos’è l’adrenalina ed a cosa serve?
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Dopammina: cos’è ed a che serve?
- Neurotrasmettitori: cosa sono ed a che servono
- Quali sono le funzioni della Dopammina?
- Dopammina: biosintesi, rilascio nello spazio sinaptico e degradazione
- Acetilcolina: cos’è ed a cosa serve?
- Serotonina e triptofano: cosa sono e in quali cibi trovarli
- Glutamina: a che serve, quando assumerlo, dosi ed effetti collaterali
- Creatinina alta o bassa: cos’è, cosa indica e come si corregge
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!
