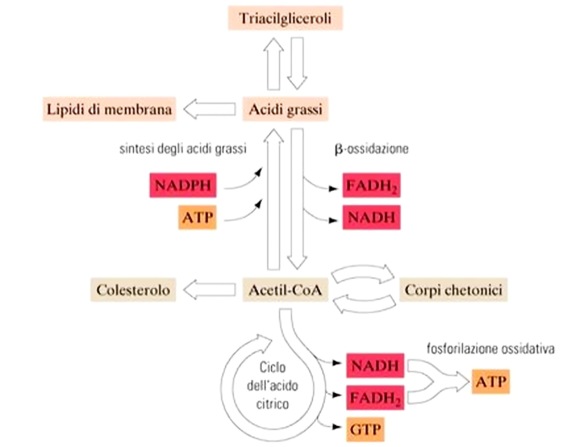
 La lipogenesi, chiamata anche “sintesi degli acidi grassi” o liposintesi, è una via metabolica della cellula che, a partire da molecole di acetil-CoenzimaA, sintetizza acidi grassi, e successivamente lipidi. Questa molecola viene prodotta durante il metabolismo dei vari nutrienti assunti con l’alimentazione e/o depositati nelle riserve corporee: qualsiasi sostanza capace di trasformarsi in acetil-CoA è potenzialmente precorritrice di lipidi ed acidi grassi, come ad esempio i carboidrati, motivo per cui i carboidrati in eccesso assunti con la dieta, determinano la formazione di tessuto adiposo in eccesso; anche alcuni amminoacidi e l’alcol – se assunti in eccesso – possono fornire l’acetil-CoA necessario alla lipogenesi. Gli enzimi chiave della lipogenesi sono la acetil-CoA carbossilasi e la acido grasso sintasi. Il processo di sintesi avviene nel citoplasma delle cellule del fegato e del tessuto adiposo.
La lipogenesi, chiamata anche “sintesi degli acidi grassi” o liposintesi, è una via metabolica della cellula che, a partire da molecole di acetil-CoenzimaA, sintetizza acidi grassi, e successivamente lipidi. Questa molecola viene prodotta durante il metabolismo dei vari nutrienti assunti con l’alimentazione e/o depositati nelle riserve corporee: qualsiasi sostanza capace di trasformarsi in acetil-CoA è potenzialmente precorritrice di lipidi ed acidi grassi, come ad esempio i carboidrati, motivo per cui i carboidrati in eccesso assunti con la dieta, determinano la formazione di tessuto adiposo in eccesso; anche alcuni amminoacidi e l’alcol – se assunti in eccesso – possono fornire l’acetil-CoA necessario alla lipogenesi. Gli enzimi chiave della lipogenesi sono la acetil-CoA carbossilasi e la acido grasso sintasi. Il processo di sintesi avviene nel citoplasma delle cellule del fegato e del tessuto adiposo.
Dal momento che l’acetil-CoA viene sintetizzato all’interno del mitocondrio, la cellula deve attivare prima meccanismi in grado di trasportare la molecola all’esterno del mitocondrio stesso (in condizioni normali l’acetil-CoA non è in grado di attraversare spontaneamente la doppia membrana mitocondriale). Allo stesso modo, la cellula deve garantire il reclutamento presso il citoplasma anche di molecole sufficienti di NADPH, necessarie per la biosintesi.
In seguito, l’acetil-CoA viene convertito in malonil-CoA ed ha inizio il processo di biosintesi vero e proprio, che consta dell’aggiunta progressiva di molecole di malonil-CoA all’estremità carbossilica della catena nascente.
La reazione complessiva di sintesi del palmitato è la seguente:
- 8 acetil-CoA + 7 ATP + 14 NADPH + 14 H+ → palmitato + 8 CoA + 7 ADP + 7 Pi + 6 H20 + 14 NADP+
Si noti che sono prodotte 6 molecole H20, non 7, in quanto una viene utilizzata per idrolizzare il legame tioestere tra il palmitato prodotto dalla reazione e l’enzima.
Essa comprende la prima reazione di conversione di sette molecole di acetil-CoA ad altrettante di malonil-CoA
- 7 acetil-CoA + 7 CO2 + 7 ATP → 7 malonil-CoA + 7 ADP + 7 Pi + 14 H+
ed i cicli di elongazione successivi
- acetil-CoA + 7 malonil-CoA + 14 NADPH + 20 H+ → palmitato + 8 CoA + 6 H20 + 14 NADP+ + 7 CO2
Leggi anche:
Reclutamento nel citoplasma di acetil-CoA e NADPH
L’uscita dell’acetil-CoA è susseguente alla sua conversione in acido citrico, molecola in grado di fuoriuscire dal mitocondrio, in un processo definito navetta del citrato, giungendo nel citoplasma della cellula. Ciò è possibile tramite l’enzima citrato sintasi, che utilizza come substrati l’acetil-CoA e l’ossalacetato. Una volta raggiunto il citoplasma, l’acido citrico si scinde di nuovo in acetil-CoA (che rimane nel citoplasma) ed ossalacetato.
Quest’ultimo, per poter essere riportato nel mitocondrio, deve essere sottoposto a diverse reazioni, dal momento che la membrana mitocondriale è impermeabile anche ad esso. Dapprima, esso viene ridotto a malato in presenza di NADH. Tale reazione è catalizzata da una malato deidrogenasi citosolica. In seguito, il malato subisce una decarbossilazione ossidativa ad opera dell’enzima malico, con produzione di piruvato (in grado di entrare nel mitocondrio ed essere ri-convertito ad ossaloacetato dalla piruvato carbossilasi) ed il rilascio di una molecola di NADPH.
Per ogni molecola di acetil-CoA trasportata nel citoplasma, dunque, viene prodotta una molecola di NADPH utile per la biosintesi dell’acido grasso. Per produrre una molecola di palmitato, ad esempio, vengono reclutati otto NADPH. Le sei ulteriori molecole necessarie provengono dalla via dei pentoso fosfati.
Produzione del malonil-CoA
L’acetil-CoA trasportato nel citoplasma viene carbossilato (viene aggiunta una molecola di CO2) in presenza dell’enzima acetil-CoA carbossilasi, che contiene il cofattore biotina(legato covalentemente al gruppo ε-aminico di una lisina, come nella piruvato carbossilasi e nella propionil-CoA carbossilasi) che viene coinvolto direttamente nella reazione. Il prodotto è il malonil-CoA (la reazione prevede il consumo di una molecola di ATP e la liberazione di ADP e fosfato inorganico) e la reazione è virtualmente irreversibile in quanto esoergonica. Si tratta di una reazione chiave nella regolazione dell’intero metabolismo degli acidi grassi.
Elongazione
Similarmente a quanto avviene nella β-ossidazione, l’elongazione ha luogo attraverso reazioni cicliche, catalizzate dalla acido grasso sintasi (un unico polipeptide negli eucarioti, un complesso multienzimatico nei procarioti). Per semplicità nel testo si descriveranno i singoli enzimi procariotici. In coda si descriverà la struttura della acido grasso sintasi eucariotica, che li comprende tutti in un’unica proteina.
Tappe dell’elongazione
La prima fase dell’elongazione è catalizzata dalla acetil transacilasi e dalla malonil transacilasi, che generano acetil-ACP e malonil-ACP. La prima, a differenza della seconda, ha una bassa specificità: essa è infatti usata anche per trasferire molecole diverse dagli acetili (come avviene ad esempio nella formazione di propionil-ACP). Le due molecole condensano a formare acetoacetil-ACP, in una reazione catalizzata dalla β-chetoacil-ACP sintasi.
Le tre reazioni successive portano il gruppo chetonico al C3 a gruppo metilenico. Dapprima, l’acetoacetil-ACP è ridotto a d-3-idrossibutirril-ACP (NADPH è usato come riducente). In seguito il d-3-idrossibutirril-ACP è disidratato a formare crotonil-ACP, un trans-Δ2-enoil-ACP. Il passaggio finale converte il crotonil-ACP a butirril-ACP. Ancora una volta NADPH è il riducente. L’enzima che catalizza quest’ultimo passaggio, la enoil-ACP reduttasi, è inibito dal triclosan, un agente antibatterico a largo spettro utilizzato ad esempio nei dentifrici, nei saponi o nelle creme per la pelle. Le quattro reazioni sono riepilogate nella tabella sottostante.
| Passaggio | Descrizione | Diagramma | Enzima |
| Condensazione | Il primo passaggio è la condensazione dell’acetil-ACP e del malonil-ACP. Ciò risulta nella formazione dell’acetoacetil-ACP. Sebbene questa reazione sia termodinamicamente sfavorita, essa viene spinta nella direzione dei prodotti dalla bassa concentrazione cellulare di CO2. |
FattyAcid-MB-Condensation.png
|
β-chetoacil-ACP sintasi |
| Riduzione dell’acetoacetil-ACP | L’acetoacetil-ACP è ridotto dal NADPH in D-3-idrossibutirril-ACP. Il doppio legame è ridotto ad un gruppo ossidrile. Viene formato solo l’isomero D. |
FattyAcid-MB-Reduction1.png
|
β-chetoacil-ACP reduttasi |
| Disidratazione | Il D-3-idrossibutirril-ACP è disidratato a crotonil-ACP. |
FattyAcid-MB-Dehydration.png
|
3-idrossiacil-ACP deidrasi |
| Riduzione del crotonil-ACP | Durante l’ultimo passaggio, il crotonil-ACP è ridotto dal NADPH in butirril-ACP. |
FattyAcid-MB-Reduction2.png
|
Enoil-ACP reduttasi |
Al termine di queste quattro reazioni (condensazione, riduzione, disidratazione, riduzione) si ha la conclusione del primo ciclo di elongazione. Nel secondo ciclo, il butirril-ACP formato durante il primo condensa con una nuova molecola di malonil-ACP, formando C6-β-chetoacil-ACP. Questa reazione è del tutto simile a quella che, nel primo ciclo, ha portato alla formazione di C4-β-chetoacil-ACP. Dopo reazioni analoghe di riduzione, disidratazione e riduzione, si forma un C6-acil-ACP, pronto per il terzo ciclo di elongazione. Tali ripetizioni procedono fino alla formazione di C16-acil-ACP (sette cicli complessivi). Tale intermedio è un ottimo substrato per una tioesterasi, che scinde la molecola in palmitato ed ACP. In questa chiave, tale tioesterasi agisce come metro per interrompere i cicli una volta raggiunta la lunghezza corretta dell’acido grasso. La produzione di acidi grassi diversi dal palmitato avviene in altri distretti corporei (ad esempio sul reticolo endoplasmatico) proprio a partire da questa molecola a 16 atomi di carbonio.
Ruolo della ACP
Gli intermedi di reazione sono legati ad una acyl carrier protein (ACP, proteina trasportante acili). Nel dettaglio, essi sono legati allo zolfo terminale di un gruppo fosfopantoteinico a sua volta legato ad un peptide di 77 amminoacidi, denominato appunto ACP. Questo legame ricorda quello con il CoA (anch’esso contenente un gruppo fosfopantoteinico) necessario per la degradazione degli acidi grassi. In questa chiave, l’ACP può dunque essere considerato come grande coenzima (una sorta di macro-CoA).
Leggi anche:
- Trigliceridi: cosa sono, alti, bassi, valori normali e dieta
- Colesterolo e trigliceridi: valori normali, alti, bassi ed interpretazione
- Colesterolo: cos’è ed a cosa serve?
- Colesterolo alto: i cibi che lo abbassano e quelli da evitare
- Abbassare colesterolo LDL e trigliceridi in modo naturale
- Dieta per abbassare il colesterolo: cibi consigliati e da evitare
- Differenza tra colesterolo HDL “buono” e LDL “cattivo”
- Eccesso di colesterolo (ipercolesterolemia): perché è pericoloso?
- Qual è la giusta percentuale di grasso che dobbiamo avere nel corpo?
- Distribuzione del grasso nell’uomo e nella donna: androide e ginoide
- Dislipidemia: significato, sintomi, cura, terapie, familiare, dieta
- Sono normopeso, sottopeso o sovrappeso? Come si calcola l’Indice di Massa Corporea (BMI)?
- Differenza tra obesità e sovrappeso
- Differenza tra obesità di primo, secondo e terzo grado
- La dieta ti sta facendo perdere massa magra o massa grassa? Scoprilo con la bioimpedenziometria
- Perché non riesco a dimagrire? I nove errori tipici di chi è a dieta
- Si può vivere senza stomaco? Conseguenze della gastrectomia
- Chirurgia bariatrica: complicanze, costi, interventi, rischi
- Ulcera a stomaco, intestinale, da stress, perforante e sanguinante
- Esofago di Barrett, tumore e reflusso gastroesofageo
- Capacità massima dello stomaco: si può “mangiare fino a scoppiare”?
- Stomaco: anatomia e funzioni in sintesi
- Differenza tra bypass gastrico, bendaggio, gastrectomia e diversione biliopancreatica
- Bypass gastrico: complicanze, peso minimo, costo, conseguenze
- Bendaggio gastrico: rischi, costi, peso minimo, complicanze
- Gastroplastica verticale: rischi, costi, indicazioni, complicanze
- Sleeve gastrectomy: rischi, costi, controindicazioni, complicanze
- Diversione biliopancreatica: complicanze, alimentazione
- Dimagrire riducendo le dimensioni dello stomaco senza chirurgia e bendaggio gastrico
- Glucomannano: l’integratore che nel tuo stomaco aumenta di 100 volte il proprio volume, ti sazia e ti impedisce di mangiare troppo
- Reflusso gastroesofageo: dieta, stress, alcolici, latte e notte
- Reflusso gastroesofageo: sintomi, diagnosi e cura
- Reflusso gastroesofageo: terapia farmacologica e chirurgica
- Cosa succede al cibo nello stomaco dopo averlo ingerito?
- Peristalsi intestinale ed antiperistalsi: caratteristiche e funzioni
- Acidità di stomaco e bruciore: tutti i farmaci antiacidi
- Bruciore di stomaco: cosa mangiare, come dormire e rimedi naturali
- Acidità di stomaco: come combatterla con i farmaci antiacidi
- Si può vivere senza pancreas? Conseguenze della pancreasectomia
- Si può vivere senza reni? Conseguenze della nefrectomia
- Si può vivere senza cistifellea?
- Glomerulo renale: schema, funzione e flusso ematico renale
- Com’è fatto un rene? [SCHEMA]
- Azotemia (Urea) alta o bassa: valori, cause, sintomi e cosa fare
- Azotemia alta e reni: cibi da evitare per abbassarla
- Clearance della creatinina: alta o bassa, valori, calcolo e sintomi
- Creatinina alta o bassa: cure e terapie per correggere i valori
- Sindrome post-colecistectomia: conseguenze dell’asportazione della cistifellea
- Cistifellea: cos’è, a cosa serve e dove si trova
- Apparato digerente: cos’è, com’è fatto, a che serve e come funziona?
- Cosa succede al cibo nello stomaco dopo averlo ingerito?
- Differenza tra laringe, faringe e trachea
- Esofago: anatomia e funzioni in sintesi
- Esofago e trachea: zona, anatomia, rapporti e differenze
- Duodeno: anatomia e funzioni in sintesi
- Pancreas: anatomia e funzioni in sintesi
- Differenza tra intestino tenue e crasso
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
