 Attualmente non esiste una terapia definitiva per il morbo di Parkinson, ma il trattamento farmacologico, la chirurgia e la gestione multidisciplinare sono in grado di fornire un parziale sollievo ai sintomi. I farmaci principalmente utilizzati nel trattamento di sintomi motori sono la levodopa (di solito in combinazione con un inibitore della dopa-decarbossilasi e un inibitore delle COMT), gli agonisti della dopamina e gli inibitori MAO-B (Inibitore della monoamino ossidasi). La fase della malattia determina quale famiglia di farmaci sia più utile. Due fasi sono di solito distinte:
Attualmente non esiste una terapia definitiva per il morbo di Parkinson, ma il trattamento farmacologico, la chirurgia e la gestione multidisciplinare sono in grado di fornire un parziale sollievo ai sintomi. I farmaci principalmente utilizzati nel trattamento di sintomi motori sono la levodopa (di solito in combinazione con un inibitore della dopa-decarbossilasi e un inibitore delle COMT), gli agonisti della dopamina e gli inibitori MAO-B (Inibitore della monoamino ossidasi). La fase della malattia determina quale famiglia di farmaci sia più utile. Due fasi sono di solito distinte:
- una prima fase in cui l’individuo con la malattia ha già sviluppato qualche disabilità e per la quale vi è la necessità di un trattamento farmacologico;
- una seconda fase in cui in un individuo si sviluppano complicanze motorie legate all’utilizzo della levodopa.
Leggi anche:
- Morbo di Parkinson: cause, sintomi, decorso, terapie
- Morbo di Alzheimer: cause, sintomi, decorso, terapie
- Demenza senile: cause, sintomi, decorso e cure
Il trattamento nella fase iniziale ha come obiettivo un compromesso ottimale tra il buon controllo dei sintomi e gli effetti collaterali derivanti dalla valorizzazione della funzione dopaminergica. L’inizio del trattamento con levodopa (o L-DOPA) può essere ritardato utilizzando altri farmaci come gli inibitori MAO-B e gli agonisti della dopamina, nella speranza di ritardare la comparsa delle discinesie. Nella seconda fase l’obiettivo è quello di ridurre i sintomi. Quando i farmaci non sono più sufficienti a controllarli, la chirurgia e la stimolazione cerebrale profonda possono rivelarsi utili. Nelle fasi finali della malattia, le cure palliative vengono offerte per migliorare la qualità di vita.
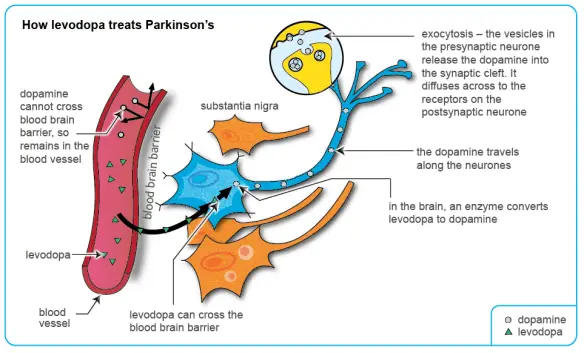
- Levodopa. La Levodopa è il trattamento più ampiamente usato fin dagli anni settanta. L-DOPA è convertito in dopamina nei neuroni dopaminergici (neuroni che producono dopamina) mediante DOPA-decarbossilasi. Poiché i sintomi motori sono prodotti da una mancanza di dopamina nella substantia nigra, la somministrazione di L-DOPA diminuisce temporaneamente i sintomi motori. Solo il 5-10% dell’L-DOPA attraversa la barriera ematoencefalica. Il resto è spesso metabolizzato altrove in dopamina, provocando una serie di effetti collaterali tra cui nausea, discinesia e rigidità articolare. La carbidopa e la benserazide sono inibitori periferici della DOPA-decarbossilasi, che aiutano a bloccare il metabolismo della L-DOPA, prima che raggiunga i neuroni dopaminergici, riducendo pertanto gli effetti collaterali e aumentando la biodisponibilità. Essi sono generalmente somministrati in preparazioni associate alla levodopa.I preparati esistenti sono carbidopa/levodopa (co-careldopa) e benserazide/levodopa (co-beneldopa). La levodopa è stata correlata alla sindrome da disregolazione dopaminergica, che consiste in un uso eccessivo e compulsivo del farmaco. Vi sono alcune versioni a rilascio controllato e lento di levodopa, tuttavia esse non hanno mostrato un maggiore controllo dei sintomi e delle complicanze motorie rispetto a preparazioni a rilascio immediato. Il tolcapone inibisce l’enzima COMT, degradante la dopamina, prolungando gli effetti della levodopa. Tuttavia, la sua utilità è limitata da effetti collaterali, come ad esempio i possibili danni al fegato. L’uso dell’entacapone, un farmaco altrettanto efficace, non evidenzia alterazioni significative della funzionalità epatica. I preparati a base di levodopa portano a lungo termine allo sviluppo di complicanze motorie caratterizzate da movimenti involontari chiamati discinesie e fluttuazioni nella risposta al trattamento farmacologico. In questo caso, un paziente affetto da malattia di Parkinson può sperimentare dei periodi con buona risposta ai farmaci con alcuni sintomi (fase on) e periodi con nessuna risposta al trattamento e sintomi motori significativi (fase off). Per questo motivo, le dosi di levodopa vengono somministrate in quantità minime. È pratica comune ritardare l’inizio della terapia con levodopa utilizzando alternative, come gli agonisti dopaminergici e gli inibitori della monoamino ossidasi. Una strategia utilizzata in passato per ridurre le complicanze motorie era quella di sospendere il trattamento con L-DOPA per un certo tempo. Ora ciò è sconsigliato, dal momento che può portare a effetti collaterali pericolosi, come la sindrome neurolettica maligna.
- Agonisti dopaminergici. Numerosi agonisti della dopamina, che si legano ai recettori dopaminergici post-sinaptici del cervello, hanno effetti simili a quelli della levodopa.. Inizialmente venivano usati, come terapia complementare alla levodopa, negli individui che accusano fluttuazioni on-off e discinesie, ora sono utilizzati principalmente come terapia unica iniziale per i sintomi motori, con l’obiettivo di ritardare l’assunzione di levodopa e le sue complicazioni motorie. Gli agonisti dopaminergici stimolano, con diversa specificità rispetto ai diversi tipi, i recettori per la dopamina. Si dividono in ergolinici (bromocriptina, pergolide, lisuride, cabergolina) e non ergolinici (pramipexolo, ropinirolo, apomorfina). Gli agonisti della dopamina producono significativi, anche se di solito lievi, effetti collaterali, tra cui sonnolenza, allucinazioni, insonnia, nausea e stipsi. A volte gli effetti collaterali appaiono anche con una minima dose clinicamente efficace, che porta il prescrivente alla ricerca di un farmaco diverso. Rispetto alla levodopa, gli agonisti della dopamina possono ritardare le complicanze motorie, ma sono meno efficaci nel controllare i sintomi. Tuttavia, solitamente appaiono sufficienti per gestire i sintomi nei primi anni di malattia. Essi tendono ad essere più costosi della levodopa. Tali farmaci sono stati correlati a disturbi del controllo degli impulsi, come l’ipersessualità, l’alimentazione compulsiva e il gioco d’azzardo e lo shopping patologici, in maniera anche più importante rispetto alla levodopa. Apomorfina, un agonista della dopamina, somministrata attraverso iniezioni sottocutanee, può essere utilizzata nella malattia avanzata per ridurre le fasi off e la discinesia. Dato che gli effetti secondari, come la confusione e le allucinazioni sono comuni, i pazienti che ricevono l’apomorfina devono essere attentamente monitorati. Recentemente sono stati trovati due agonisti della dopamina che vengono somministrati attraverso cerotti (lisuride e rotigotina) e risultano essere utili nei pazienti nella fase iniziale della malattia, mentre vi sono ancora degli studi alla fase preliminare riguardo alla loro efficacia nei pazienti in stato avanzato.
- Inibitori della monoamino ossidasi (inibitori MAO-B). Gli inibitori della monoamino ossidasi (inibitori MAO-B), selegilina e rasagilina, sono in grado di aumentare il livello di dopamina nei gangli della base, bloccandone il metabolismo. Essi bloccano la deaminazione ossidativa delle ammine endogene catalizzata dalle monoaminossidasi mitocondriali. La riduzione della attività della monoamino ossidasi, comporta un aumento di L-DOPA nello striato. Come gli agonisti della dopamina, gli inibitori MAO-B sono utilizzati in monoterapia per migliorare i sintomi motori e ritardare la necessità di assumere levodopa nella malattia precoce, ma producono effetti più negativi e sono meno efficaci rispetto alla levodopa. Vi sono pochi studi sulla loro efficacia in fase avanzata, anche se i risultati suggeriscono che essi sono utili per ridurre le fluttuazioni tra le fasi on e off. Uno studio iniziale ha indicato che la selegilina, in associazione con levodopa, aumenta il rischio di morte, ma ciò è stato in seguito smentito.
- Altri farmaci. Altri farmaci, come l’amantadina e gli anticolinergici, possono essere utili nel trattamento dei sintomi motori. Tuttavia, le prove a loro sostegno mancano di qualità e ciò comporta che non siano considerati trattamenti di prima scelta. Oltre ai sintomi motori, la malattia di Parkinson è accompagnata da una vasta gamma di sintomi. Un certo numero di farmaci sono stati utilizzati per il trattamento di alcuni di questi problemi. Ne sono un esempio l’uso della clozapina nella psicosi, degli inibitori della colinesterasi per la demenza e il modafinil per l’eccessiva sonnolenza diurna. Una meta-analisi del 2010, ha riscontrato che l’uso di farmaci anti-infiammatori non steroidei (tranne il paracetamolo e l’aspirina), sono stati correlati ad almeno il 15% di una minore incidenza di sviluppo della malattia di Parkinson.
Il farmaco levodopa e le proteine utilizzano, in concorrenza, lo stesso sistema di trasporto nell’intestino e nella barriera emato-encefalica. Questo comporta che, se assunti insieme, l’efficacia del farmaco appaia ridotta. Pertanto, quando si fa uso di levodopa, si sconsiglia il consumo eccessivo di proteine e viene raccomandata una dieta mediterranea equilibrata.
Leggi anche:
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Differenza tra morbo di Alzheimer, demenza senile, vascolare e reversibile
- Differenza tra morbo di Alzheimer e morbo di Parkinson: sintomi comuni e diversi
- Cervelletto: anatomia esterna ed interna
- Cervelletto: le lesioni cerebellari più comuni
- Le funzioni del cervelletto: apprendimento e correzione dei movimenti del corpo
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

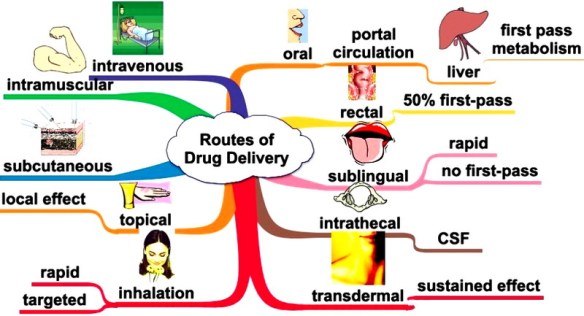 La somministrazione di un farmaco (in inglese “route of administration”) è quel processo che porta uno xenobiotico, cioè una sostanza estranea all’organismo, a raggiungere il suo bersaglio all’interno dell’organismo, cioè il sito d’azione a cui esso è destinato.
La somministrazione di un farmaco (in inglese “route of administration”) è quel processo che porta uno xenobiotico, cioè una sostanza estranea all’organismo, a raggiungere il suo bersaglio all’interno dell’organismo, cioè il sito d’azione a cui esso è destinato.