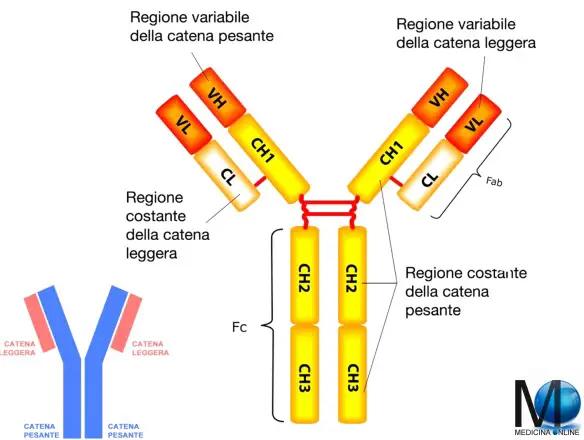
La struttura di un anticorpo
Un allergene è una sostanza solitamente innocua per la maggior parte delle persone, ma che in taluni individui (i soggetti atopici) è in grado di produrre manifestazioni allergiche di varia natura (asma, orticaria, etc.).
Un aptene è una molecola a basso peso molecolare che di per sé non induce una risposta anticorpale, cioè non ha proprietà immunogeniche, ma se legata ad un carrier è in grado di stimolare la formazione di anticorpi specifici e di reagire con essi.
Un epitopo è quella piccola parte di antigene che lega l’anticorpo specifico. La singola molecola di antigene può contenere diversi epitopi riconosciuti da anticorpi differenti.
Un antigene è qualsiasi molecola in grado di legarsi a specifici componenti del sistema immunitario, quali anticorpi o cellule immunocompetenti, comprendendo sia sostanze esogene che endogene (come nel caso di patologia autoimmuni). Più precisamente qualunque sostanza in grado di suscitare una risposta immune viene definita immunogenica e viene chiamata IMMUNOGENO. Un antigene viene chiamato APTENE (molecola a basso peso molecolare, di norma inferiore a 4 kD) quando riesce a stimolare la produzione di anticorpi solo se si lega ad una molecola (detta CARRIER) che lo rende in tal modo immunogeno.
Quindi IMMUNOGENICITA’ significa che quella sostanza è in grado di indurre una risposta immunitaria; ANTIGENICITA’ significa che quella sostanza è in grado di reagire con componenti del sistema immunitario.
EPITOPO o DETERMINANTE ANTIGENICO: come già prima accennato rappresenta una porzione di un antigene che entra in contatto con il sito di legame di un Anticorpo o con il recettore per l’Antigene delle cellule T (lo vedremo più avanti), pertanto è la parte più importante dell’antigene, ijn quano capace di indurre la risposta immunitaria.
Un antigene in genere possiede più di un epitopo, pertanto la risposta indotta viene detta POLICLONALE in quanto attiverà più cloni cellulari (linfociti).
Vi sono tuttavia alcune molecole antigeniche che possiedono uno o pochi epitopi immunodominanti e quindi in grado di indurre una risposta monoclonale (se attivato un solo clone) od oligoclonale(quando sono attivasti pochi cloni).
Pertanto in una molecola antigenica possiamo avere una maggiore o minore attivazione preferenziale di alcuni cloni rispetto ad altri e questa viene detta IMMUNODOMINANZA DEGLI EPITOPI.
Leggi anche:
- Sistema immunitario, immunità innata e specifica: riassunto, schema e spiegazione
- Immunodeficienza primaria e secondaria: sintomi, cause e terapie
- Immunità innata (aspecifica): barriere, infiammazione e complemento
- Immunità innata (aspecifica): neutrofili, macrofagi e linfociti natural killer
- Immunità specifica (acquisita): linfociti, T killer, T helper, T γδ, B ed anticorpi
- Immunità specifica (acquisita): memoria passiva, attiva ed immunizzazione
- Immunità specifica (acquisita) umorale e cellulare
- Patologie del sistema immunitario: immunodeficienze, autoimmunità ed ipersensibilità
- Anticorpi: (immunoglobuline): tipi, caratteristiche e funzioni
- Aptene: cos’è e perché è importante per il sistema immunitario
- Antigene: cos’è e perché è importante per il sistema immunitario
- Differenza tra antigeni esogeni, endogeni, tumorali, nativi ed autoantigeni
- Epitopi sequenziali e conformazionali: cosa sono e come funzionano
- HIV: dopo quanto si manifestano i sintomi? I 4 stadi dell’infezione
- Differenza tra HIV e AIDS: sono uguali?
- Si muore di AIDS? Qual è l’aspettativa di vita?
- HIV: sintomi iniziali in donne e uomini
- Differenza tra malattia, sindrome e disturbo con esempi
- Differenza tra virus HIV1 e HIV2
- Sesso e AIDS: l’HIV si trasmette anche tramite il rapporto orale
- Il liquido pre-eiaculatorio può indurre gravidanza e trasmettere l’HIV?
- HIV e AIDS: come, dove e quando si eseguono i test per la diagnosi?
FATTORI CHE INFLUENZANO L’IMMUNOGENICITA’
Normalmente il sistema immunitario discrimina tra ciò che è suo (self) e ciò che non è suo (non-self): pertanto sono immunogeniche le molecole ESTRANEE al self.
In generale più grande è la molecola, più evidenzia di essere immunogena, anche se nella realtà non esiste una grandezza oltre la quale una sostanza diviene immunogena.
La natura chimica dell’immunogeno è importante.
Le PROTEINE rappresentano di gran lunga la maggioranza degli immunogeni. Possono essere proteine pure, oppure glicoproteine o lipoproteine. Nelle proteine si deve tener conto della loro struttura, assai importante come vedremo successivamente parlando degli epitopi.
Le proteine sono polimeri i cui monomeri sono costituiti dai 20 diversi tipi di amminoacidi presenti in natura. Gli amminoacidi sono composti che contengono nella loro molecola sia il gruppo carbossilico –COOH sia il gruppo amminico –NH2 , basico. Entrambi questi gruppi funzionali sono legati a un carbonio, chiamato carbonio-α. A questo carbonio, sono legati, inoltre, un atomo di idrogeno e un gruppo denominato genericamente R che, essendo diverso nei 20 amminoacidi, ci consente di differenziarli. Durante la sintesi delle proteine, un amminoacido lega il suo gruppo carbossilico con quello amminico di un altro amminoacido, formando il legame peptidico con eliminazione di acqua come si può vedere in figura.
Nonostante gli amminoacidi siano solo 20, la varietà di proteine è elevatissima, in quanto gli amminoacidi si combinano tra loro in sequenze e quantità diverse. Le proteine rappresentano una classe di composti assai versatile e di grande interesse biologico: concorrono a formare l’impalcatura del corpo: ad es. il collagene è il principale componente fibroso delle ossa, dei tendini, della pelle, delle cartilagini, dei denti; i capelli e le unghie sono costituiti da α-cheratina; svolgono funzione catalitica: gli enzimi, infatti, indispensabili catalizzatori biologici sono costituiti da proteine; agiscono come mezzo di trasporto di altre molecole: nel sangue, ad esempio, l’ossigeno viene trasportato dall’emoglobina; provocano il movimento: ad esempio la contrazione muscolare è resa possibile da due proteine ovvero dall’actina e dalla miosina; hanno funzioni protettive: gli anticorpi, come le immunoglobuline che sono i più importanti mezzi di difesa dell’organismo sono costituiti da proteine; fanno parte del sistema endocrino: vari ormoni, tra cui l’insulina sono costituiti da proteine; rappresentano un sistema di controllo del pH del sangue perché limitano le eccessive variazioni di ioni H+ dovute al metabolismo cellulare, ecc.
Le proteine esplicano le loro specifiche funzioni grazie alla loro forma che dipende dalla successione di amminoacidi, dai ripiegamenti della catena proteica e dalla sua organizzazione nello spazio.
Possiamo pertanto individuare successivi livelli di organizzazione denominati: struttura primaria, secondaria, terziaria e quaternaria.
La pura e semplice successione degli amminoacidi costituisce la struttura primaria della proteina. La struttura primaria, cioè tipo e sequenza degli aminoacidi, condiziona la configurazione spaziale e la forma globale della molecola, dalle quali dipendono le proprietà biologiche.
L’avvolgimento a spirale, o la disposizione regolare di tratti più o meno lunghi della catena proteica costituiscono la struttura secondaria della proteina. Questo livello di organizzazione è una conseguenza dei legami a idrogeno tra gli amminoacidi appartenenti a una stessa catena, o tra gli amminoacidi di catene diverse. Due tipi di struttura secondaria delle proteine sono l’α-elica e il β-foglietto.
Nella struttura ad α-elica la proteina è avvolta a spirale: tra l’atomo di idrogeno legato all’azoto di ogni legame peptidico e l’ossigeno del gruppo –C=O del legame peptidico sovrastante ( che si trova a distanza di quattro amminoacidi lungo la catena) si instaura un legame a idrogeno. L’effetto stabilizzante dei molti legami a idrogeno che sono presenti nella proteina è la causa principale dell’esistenza di tale tipo di struttura. Tuttavia se gli amminoacidi che si succedono lungo un tratto di catena proteica hanno gruppi R voluminosi, come avviene nella prolina, o gruppi R dotati della stessa carica elettrica, come avviene negli amminoacidi lisina e arginina, l’α-elica non può formarsi, a causa delle forze di repulsione che si generano tra i gruppi R.
Nella struttura β-foglietto si ha una disposizione di catene proteiche l’una accanto all’altra. Ciascuna delle catene è totalmente estesa e presenta una conformazione a zig-zag, dovuta alla geometria dei legami attorno a ciascun atomo di carbonio e di azoto nella catena. In questo caso, i legami a idrogeno si formano tra gli amminoacidi di due catene adiacenti. Le proteine dotate di questa struttura non possono essere allungate ulteriormente, senza che si rompano i legami covalenti della loro catena. Esistono proteine la cui molecola ha una forma globulare che è il risultato di ulteriori ripiegamenti della catena proteica, compresi tratti di catena che già possiedono una loro struttura secondaria. Questo terzo livello di organizzazione è la struttura terziaria della proteina.
La struttura terziaria di una proteina è la conseguenza di interazioni attrattive tra i gruppi R di amminoacidi anche molto distanti tra loro nella sequenza della struttura primaria della proteina. A stabilizzare la struttura terziaria della proteina possono concorrere quattro tipi di forze:
- Interazioni idrofobe o idrofile: nell’ambiente acquoso della cellula, i gruppi R non polari, idrofobi, della molecola proteica tendono a raggrupparsi all’interno della proteina, in modo da ridurre al minimo i contatti con le molecole d’acqua che la circondano. Invece, i gruppi polari, idrofili, tendono a disporsi verso l’esterno della proteina a contatto con l’acqua.
- Attrazioni ioniche: si instaurano in genere tra due gruppi, come –NH3+ e –COO-, l’uno carico positivamente e l’altro negativamente, dei gruppi R di due diversi amminoacidi.
- Legami idrogeno: derivano dall’attrazione tra gruppi R o si instaurano tra gruppi peptidici come nel caso delle strutture α e β.
- Ponti disolfuro: si formano tra gruppi –SH di due molecole dell’amminoacido cisteina; in seguito a una reazione di ossidazione, i due gruppi –SH perdono i rispettivi atomi di idrogeno e si legano tra loro mediante un legame covalente –S-S- come si può vedere in figura:
Alcune proteine sono formate da più di una catena di amminoacidi. Le catene possono essere uguali fra loro, o anche diverse. La disposizione reciproca delle varie catene che compongono una proteina di questo tipo costituisce la struttura quaternaria della proteina. Le interazioni possono essere legami deboli come legami idrogeno e forze di Van der Waals, oppure forti ossia ionico o covalente. Ad esempio una proteina con struttura quaternaria è l’emoglobina: essa è costituita da quattro catene proteiche, a due a due uguali, denotate rispettivamente dalle lettere α e β come si può vedere in figura :
Ognuna di queste catene contiene un gruppo eme, cioè una struttura ciclica, chiamata anello porfirinico, con al centro uno ione Fe2+; a questo ione si lega una molecola di ossigeno, che viene trasportata dai polmoni alle cellule del corpo.
- Anche i polisaccaridi puri e i lipopolisaccaridi sono buoni immunogeni.
- Gli acidi nucleici di solito sono poco immunogeni. Lo possono diventare quando si complessano con proteine.
- I lipidi in generale non sono immunogeni, ma possono essere apteni.
- Gli antigeni particolati in genere sono più immunogenici di quelli solubili e gli antigeni denaturatisono più immunogenici di quelli in forma nativa.
- Gli antigeni che sono più facilmente fagocitati sono in generale più immunogeni, in quanto per la maggior parte degli antigeni (antigeni T-dipendenti, vedi oltre) lo sviluppo di una risposta immune richiede che gli antigeni siano fagocitati, processati e presentati alle cellule T helper attraverso l’azione delle “cellule che presentano l’antigene”, in sigla APC .
- Anche la genetica ha importanza: alcune sostanze sono immunogene in un individuo ma non in altri (vengono gli uni e gli altri chiamati rispettivamente responders e non responders). Alcuni individui possono non avere o avere alterati dei geni che codificano per i recettori dell’antigene sulle cellule B o sulle cellule T oppure possono non avere quegli appropriati geni necessari per le “cellule che presentano l’antigene” di presentare l’antigene alle cellule T helper.
- Anche l’ETA’ può influire sulla immunogenicità. Infatti di solito individui molto giovani o molto vecchi hanno una diminuita capacità di indurre risposte immuni a stimoli immunogeni.
- La DOSE stessa dell’immunogeno somministrato può influenzare l’immunogenicità; vi è una dose di antigene al di sopra o al di sotto della quale la risposta immune non risulta ottimale,
- La VIA DI SOMMINISTRAZIONE è importante : di solito la via sottocutanea è migliore rispetto a quella endovenosa o intragastrica. La via di somministrazione antigenica può talora alterare la natura della riposta.
- Vi sono poi delle sostanze chiamate ADIUVANTI che hanno la proprietà di aumentare la risposta immune verso un immunogeno. L’uso degli adiuvanti tuttavia è spesso ostacolato da effetti collaterali indesiderati quali febbre e infiammazione.
CARATTERISTICHE DEGLI EPITOPI
I determinanti antigenici devono essere accessibili agli anticorpi. Già nel 1960 Sela e Arnon studiarono la immunogenicità di varie catene laterali legate ad uno scheletro polilisinico, ricordando come il sistema immunitario non reagisce contro polimeri di molecole identiche ripetute. Dimostrarono come se il determinate antigenico delle catene (rappresentato da residui di acido glutammico o di tirosina legati a polialanina) risulta inaccessibile agli anticorpi non si aveva risposta immunitaria, risposta invece che compariva a seguito dello smascheramento degli epitopi, aumentando ad es, la distanza tra le catene.
I determinanti antigenici possono essere continui o discontinui. Sempre negli anni ’60 A.Tassi fece degli studi sulla mioglobina di balena e trovò che in questa molecola di 153 aminoacidi erano presenti 5 regioni in grado di provocare una risposta anche dopo la frammentazione della molecola e che queste regioni risultavano trovarsi su zone esposte e flessibili. Questi tipi di determinanti antigenici sono detti continui o lineari, in quanto rappresentati da aminoacidi disposti in modo lineare, cioè uno dopo l’altro nella sequenza primaria della proteina. Esistono altri tipi di determinanti che sono stati dimostrati successivamente, utilizzando molecole di lisozima, e che sono detti discontinui o conformazionali, formati da aminoacidi che erano discontinui nella struttura primaria (quindi non erano uno accanto all’altro nella disposizione lineare) ma che diventano contigui nella struttura terziaria perché indotti ad unirsi grazie al ripiegamento tridimensionale della proteina come ad es. 2 regioni legate da ponti disolfuro.
Gli epitopi lineari, in particolare, sono riconosciuti sia dai linfociti T che dai linfociti B; mentre quelli conformazionali solo dai linfociti B.
I determinanti antigenici che possiedono alcuni residui più importanti di altri vengono chiamati epitopi dominanti verso i quali gli anticorpi dimostrano una maggiore affinità e che si trovano prevalentemente su porzioni idrofiliche degli antigeni e quindi più facilmente raggiungibili dagli anticorpi. La mobilità del sito antigenico: l’antigene è dotato di una certa mobilità strutturale in modo da consentire all’anticorpo di “incastrarsi” correttamente.
TIPI DI ANTIGENI
ANTIGENI T-INDIPENDENTI
Gli antigeni T-indipendenti sono quelli che possono direttamente stimolare le B cellule a produrre anticorpi senza aver bisogno dell’aiuto delle T cellule. In generale i polisaccaridi sono antigeni T-indipendenti. Le risposte verso questi antigeni sono diverse dalle risposte verso altri antigeni. Hanno una struttura polimerica, cioè caratterizzati dallo stesso determinante antigenico ripetuto più volte. Molti di questi antigeni sono in grado di attivare cloni di B linfociti specifici per altri antigeni (= attivazione policlonale). Questi antigeni T-indipendenti possono quindi essere suddivisi i tipo 1 e tipo 2 sulla base della loro capacità di attivare cellule B policlonali. Gli antigeni T-indipendenti di tipo 1 sono attivatori policlonali; quelli di tipo 2 no. Gli antigeni T-indipendenti sono in generale più resistenti alla degradazione e pertanto possono persistere per un tempo più lungo continuando a stimolare il sistema immunitario. Esempi di questi sono il polisaccaride e il liposaccaride del pneumococco, i flagelli dei microorganismi.
ANTIGENI T-DIPENDENTI
Gli antigeni T-dipendenti sono quelli che non sono in grado di stimolare direttamente la produzione di anticorpi, ma hanno bisogno dell’aiuto dei T linfociti.
Le proteine sono antigeni T-dipendenti.
Dal punto di vista strutturale questi antigeni sono caratterizzati dall’avere poche copie di molti differenti determinati antigenici. Esempi di questi antigeni sono le proteine microbiche, le proteine non self o le self-proteine alterate.
Leggi anche:
- Che significa malattia autoimmune? Spiegazione ed esempi
- Differenza tra immunità specifica ed immunità aspecifica
- Differenza tra linfociti B e T
- Differenza tra immunità umorale e cellulare
- Fattore reumatoide alto o basso? Valori normali e Reuma test
- Reuma test positivo o negativo? Cos’è e come si interpreta il valore?
- Differenza tra anticorpo ed autoanticorpo
- Differenza tra self non self in immunologia
- Che significa malattia terminale?
- Artrite reumatoide: sintomi iniziali, cause, cure e mortalità
- Differenze tra artrite ed artrosi: sintomi comuni e diversi
- Differenza artrite reumatoide e artrite psoriasica: sintomi comuni e diversi
- Artrite psoriasica e spondiloartriti sieronegative: sintomi, diagnosi e cura
- Terapia con Infrarossi per il dolore
- Ti piace scrocchiare le dita? Ecco cosa succede alle tue ossa e i danni che rischi
- Dolore: cos’è, da cosa è causato, quanti tipi di dolore esistono?
- Nove cose che non sai sul tuo sistema immunitario
- Malattie reumatiche: cosa sono, come si curano, sono pericolose?
- Lupus eritematoso sistemico (LES): cause, sintomi e terapie
- Sclerodermia: cause, sintomi e cura
- Sindrome di Sjögren: sintomi, invalidità, terapia e mortalità
- Fibromialgia: sintomi, cause, cura e tender points
- Fibromialgia: dove si trovano i tender points che provocano dolore alla palpazione?
- Dita ippocratiche congenite e secondarie: cause, sintomi e terapie
- Fenomeno di Raynaud: cause, sintomi e trattamento
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

 L’aptene è una molecola a basso peso molecolare (inferiore a 10.000 uma) che di per sé non induce una risposta anticorpale, cioè non ha proprietà immunogeniche, ma se legata ad un carrier è in grado di stimolare la formazione di anticorpi specifici e di reagire con essi.
L’aptene è una molecola a basso peso molecolare (inferiore a 10.000 uma) che di per sé non induce una risposta anticorpale, cioè non ha proprietà immunogeniche, ma se legata ad un carrier è in grado di stimolare la formazione di anticorpi specifici e di reagire con essi.