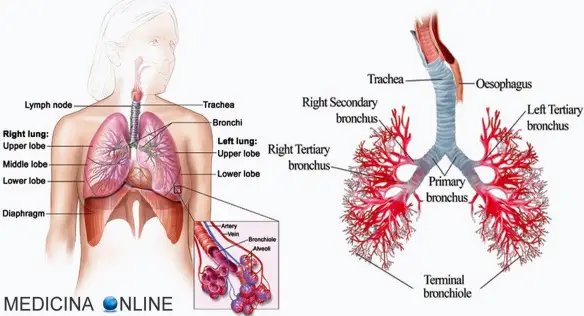
 La bronchiolite è un’infezione dei piccoli passaggi presenti nei polmoni (bronchioli), di solito causata da un’infezione virale. La bronchiolite è una malattia stagionale, diffusa soprattutto nei mesi autunnali e invernali. È una causa molto comune di ricovero ospedaliero di neonati e bimbi con meno di due anni.
La bronchiolite è un’infezione dei piccoli passaggi presenti nei polmoni (bronchioli), di solito causata da un’infezione virale. La bronchiolite è una malattia stagionale, diffusa soprattutto nei mesi autunnali e invernali. È una causa molto comune di ricovero ospedaliero di neonati e bimbi con meno di due anni.
Cause
Colpisce prevalentemente i bambini di età inferiore ai 2 anni, costringendo spesso a ricovero ospedaliero quando contratta nei primi 6 mesi di vita; il periodo più a rischio è infatti fra i 3 ed i 6 mesi. È una comune, e a volte anche grave, malattia causata principalmente dal virus respiratorio sinciziale (RSV). Altri virus che potrebbero causare la bronchiolite sono:
- adenovirus,
- virus dell’influenza,
- virus responsabili di parainfluenza.
Sebbene l’RSV nell’adulto sia in genere causa di una sintomatologia lieve, nei bambini può essere responsabile di problemi molto più severi.
Fattori di rischio
I fattori di rischio principali in età pediatrica sono:
- esposizione al fumo di sigaretta,
- età inferiore ai 6 mesi,
- vivere in condizioni affollate,
- non essere mai stati allattati al seno,
- famigliarità per asma,
- nati prematuri (prima delle 37 settimane di gestazione).
Sintomi e segni
L’incubazione dura generalmente da 6 a 10 giorni (mediamente 4 in caso di infezione da virus respiratorio sinciziale). Alcuni bambini manifestano un’infezione associata a pochi e lievi sintomi iniziali, principalmente rinorrea (naso che cola) e sintomi comuni alle classiche malattie invernali, che tende a risolversi spontaneamente. In casi più severi la bronchiolite inizia con una leggera infezione respiratoria superiore che, in 2 o 3 giorni, può svilupparsi in una crescente difficoltà a respirare che causa affanno ed una forte tosse ansimante. Il ritmo di respirazione può aumentare di molto (tachipnea) ed il bambino potrebbe diventare irritabile o dall’aspetto ansioso. Se la malattia è abbastanza grave il viso potrebbe assumere colore bluastro (cianotico) richiedendo immediato intervento medico. L’aumentata difficoltà respiratoria si manifesta visivamente a livello della narici e delle costole (rientramenti intercostali), segno che il malato soffre per aumento degli sforzi nella respirazione. Questo può essere spossante per il bambino ed i neonati possono diventare cosi stanchi da avere difficoltà nel mantenere il respiro.
I sintomi tipici della bronchiolite includono:
- pelle bluastra dovuta alla mancanza di ossigeno (cianosi);
- tosse;
- malessere generale;
- inappetenza;
- affanno;
- respiro corto;
- dispnea (difficoltà di respirazione);
- febbre;
- retrazioni intercostali;
- respirazione accelerata (tachipnea);
- rientramenti intercostali;
- respiro sibilante;
- sintomi e segni di otite media;
- sintomi e segni di congiuntivite;
- sintomi e degni di faringite.
Trasmissione
I virus che causano bronchiolite si trasmettono tipicamente per via aerea, ad esempio tramite colpi di tosse o particelle di saliva immessi nell’ambiente che vanno a finire su oggetti come asciugamani o giocattoli. Le due più comuni modalità di trasmissione della malattia sono:
- attraverso gocce di saliva inalate per via aerosolica durante contatti interpersonali ravvicinati;
- attraverso il contatto con secrezioni infette (ad esempio secrezioni nasali) che può avvenire tramite il contatto interpersonale oppure toccando del materiale infetto.
L’infezione si verifica solitamente quando il virus entra in contatto con la congiuntiva (il bianco dell’occhio) o le mucose attraverso particelle aeree oppure per contatto diretto. Sebbene il virus sia molto labile (fragile) esso resta potenzialmente infettivo sui vestiti e sulla carta per più di 30 minuti ed è ancora contagioso nelle secrezioni nasali dopo 6 ore.
Gravità
La gravità di una infezione da RSV è molto varia in base a molti fattori come età del paziente, presenza di eventuali altre malattie ed efficienza del sistema immunitario. Negli adulti, nei bambini più grandi e negli adolescenti, la malattia è solitamente leggera e può manifestarsi solamente come un comune raffreddore. In pazienti adulti sani la malattia può essere addirittura asintomatica, cioè non determinare alcun sintomo, o si può presentare come un semplice malessere generale o come un raffreddore in assenza di febbre. Al contrario i bambini più piccoli tendono ad avere forme più severe di infezione e, se non trattati rapidamente, possono sviluppare distress respiratorio grave ed andare incontro a morte per insufficienza respiratoria.
Fattori di rischio per forme gravi di infezione da RSV, sono:
- lattanti di età inferiore ai 3 mesi;
- cardiopatia congenita;
- displasia broncopolmonare (BPD);
- fibrosi cistica;
- prematurità;
- immunodeficienza congenita o acquisita;
- immunosoppressione;
- chemioterapia in corso;
- terapia iniziata tardivamente.
Prevenzione
La maggior parte dei casi di bronchiolite non sono facilmente prevenibili, perché i virus che causano la malattia sono diffusi nell’ambiente. Porre molta attenzione nel lavarsi le mani, soprattutto dove ci sono bambini, può aiutare a prevenire la diffusione dei virus che causano le malattie respiratorie. Soprattutto i membri della famiglia con un’infezione respiratoria dovrebbero stare molto attenti ad evitare il contagio (ad esempio fratelli e sorelle). Lavate spesso le mani, soprattutto prima di toccare il bambino. I virus che causano bronchiolite possono essere trasmessi facilmente a scuola, tra i vari bambini. Al giorno d’oggi, non è ancora disponibile un vaccino contro l’RSV.
Reinfezione dopo guarigione
Il bambino può infettarsi nuovamente dopo essere guarito? Si, può reinfettarsi. L’immunità acquisita dopo una infezione da RSV è infatti incompleta e di breve durata. L’infezione con RSV di adulti volontari ha dimostrato che la reinfezione si verifica facilmente anche nei volontari che, della inoculazione del virus, avevano livelli di anticorpi neutralizzanti da moderati ad alti: in parole semplici, i bambini che hanno avuto bronchioliti e polmoniti da RSV e sono successivamente guariti, possono nuovamente infettarsi ed ammalarsi della stessa patologia. La severità del quadro patologico – tuttavia – in genere decresce con il recidivare delle stesse. Semplificando: il paziente – pur potendosi nuovamente ammalare dopo essere guarito – ha in genere una malattia più lieve la seconda volta ed ancora più lieve la terza e così via.
Continua la lettura con:
- Infezione da virus respiratorio sinciziale: sintomi, segni, gravità
- Infezione da virus respiratorio sinciziale: esami e diagnosi
- Infezione da virus respiratorio sinciziale: trattamento, precauzioni, reinfezione dopo guarigione
- Infezione da virus respiratorio sinciziale: prevenzione, prognosi, complicanze
Leggi anche:
- Apparato respiratorio: anatomia in sintesi, struttura e funzioni
- Asma bronchiale: spirometria e diagnosi differenziale
- Bronchi polmonari: anatomia, posizione e funzioni in sintesi
- Bronchioli e ramificazioni dell’albero bronchiale: anatomia e funzioni
- Bronchioli terminali: anatomia, posizione e funzioni in sintesi
- Polmoni: differenza tra funzioni respiratorie e non respiratorie
- Surfattante, compliance polmonare, alveoli, composizione e funzioni
- Differenza tra vie aeree superiori ed inferiori
- Differenza tra pneumociti di tipo I e di tipo II
- Diramazioni delle vie aeree inferiori: spiegazione e schema
- Bronchiolite nei bimbi: mortalità, pericoli, complicazioni e durata
- Bronchiolite nei bambini: quando chiamare il medico?
- Bronchiolite nei bambini: qual è la migliore terapia?
- Drenaggio toracico (toracostomia): a che serve, quando si rimuove
- Valvola di Heimlich: com’è fatta, a che serve e come funziona
- Versamento pleurico, scompenso cardiaco, neoplastico, conseguenze
- Chilotorace: cause, sintomi e trattamento
- Empiema pleurico, subdurale, della colecisti: cause e cure
- Differenza tra empiema ed ascesso
- Emotorace (sangue nella cavità pleurica): sintomi, cause e cura
- Idrotorace: cause, patologie, sintomi, diagnosi e cure
- Embolia polmonare: massiva, diagnosi, da tumore, terapia
- Polmoniti nosocomiali: cause, terapie e linee guida ATS
- Polmonite interstiziale, atipica, senza febbre: sintomi e cure in bimbi ed adulti
- Polmonite in bimbi ed adulti: quando chiamare subito il medico
- Polmonite in bimbi ed adulti: quando diventa davvero pericolosa
- Esofago e trachea: zona, anatomia, rapporti e differenze
- Spirometria diretta ed indiretta: come si esegue ed a cosa serve
- Differenza tra BPCO ed asma: terapia e sintomi comuni e diversi
- Broncopneumopatia cronica ostruttiva (BPCO): sintomi, diagnosi e cura
- Asma bronchiale in bambini e adulti: cause, sintomi e cura
- Differenza tra inspirazione e espirazione: l’atto respiratorio
- Tumore al polmone in chi non fuma: da cosa viene causato?
- Differenza tra ventilazione polmonare e alveolare: spazio morto anatomico e fisiologico
- Broncoscopia polmonare con biopsia: a cosa serve, fa male, è pericolosa?
- Tutti gli articoli sullo smettere di fumare
- Enfisema polmonare: sintomi, tipi, cause, diagnosi e terapia
- Alveoli polmonari: cosa sono e che funzioni svolgono?
- Enfisema polmonare: cure, complicazioni, quando chiamare il medico
- Spirometria diretta ed indiretta: come si esegue ed a cosa serve
- Che significa malattia autoimmune? Spiegazione ed esempi
- Parametri della spirometria: capacità, volumi, rapporti e flussi
- Polmoni: anatomia e funzioni in sintesi
- Differenza tra laringe, faringe e trachea
- Differenza tra costola incrinata e rotta
- Cos’è una costa? Differenza tra costole e coste
- Gabbia toracica: dove si trova, a che serve e da cosa è composta
- Costola rotta (frattura costale): sintomi, diagnosi e terapia
- Costola incrinata: sintomi, terapia e tempi di recupero
- Differenza tra costole e vertebre
- Muscoli respiratori volontari ed involontari
- Frattura costale multipla, volet costale e pneumotorace
- Pneumotorace spontaneo primario, secondario ed iperteso: cause, sintomi, terapie
- Sangue dal naso (epistassi) in bambini e adulti: cause, rimedi naturali, cosa fare e cosa NON fare
- Differenza tra dispnea, apnea e tachipnea
- Differenza apnea statica, dinamica e profonda
- Differenza tra ipossiemia, ipossia ed anossia
- Differenza tra ipossiemia e ipercapnia
- Differenza tra insufficienza respiratoria di tipo 1 e 2
- Crisi respiratoria acuta e rischio di morte: cosa fare?
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!

 Gli pneumociti sono le cellule che, insieme ai macrofagi alveolari, costituiscono l’epitelio degli alveoli polmonari. In base alla morfologia cellulare si dividono in pneumociti di tipo I e di tipo II.
Gli pneumociti sono le cellule che, insieme ai macrofagi alveolari, costituiscono l’epitelio degli alveoli polmonari. In base alla morfologia cellulare si dividono in pneumociti di tipo I e di tipo II.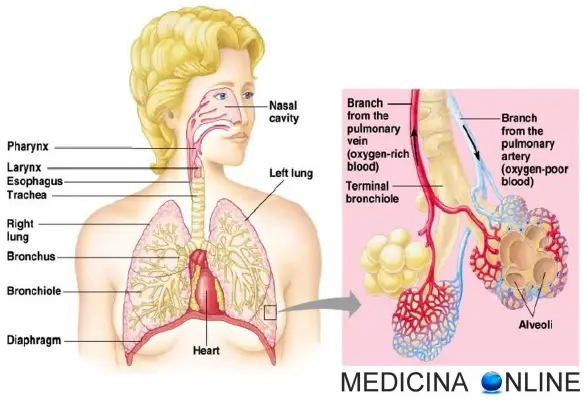 Le vie aeree sono varie strutture anatomiche formate da organi cavi in cui le sostanze gassose, vengono trasportate da o verso i polmoni. Devono essere mantenute costantemente pervie, cioè libere da ostruzioni, motivo per cui sono sostenute esternamente da una struttura ossea o cartilaginea e muscolare. Pur essendo in continuità tra di loro, vengono suddivise in vie aeree superiori ed inferiori, in base ad aspetti organogenetici e clinici.
Le vie aeree sono varie strutture anatomiche formate da organi cavi in cui le sostanze gassose, vengono trasportate da o verso i polmoni. Devono essere mantenute costantemente pervie, cioè libere da ostruzioni, motivo per cui sono sostenute esternamente da una struttura ossea o cartilaginea e muscolare. Pur essendo in continuità tra di loro, vengono suddivise in vie aeree superiori ed inferiori, in base ad aspetti organogenetici e clinici.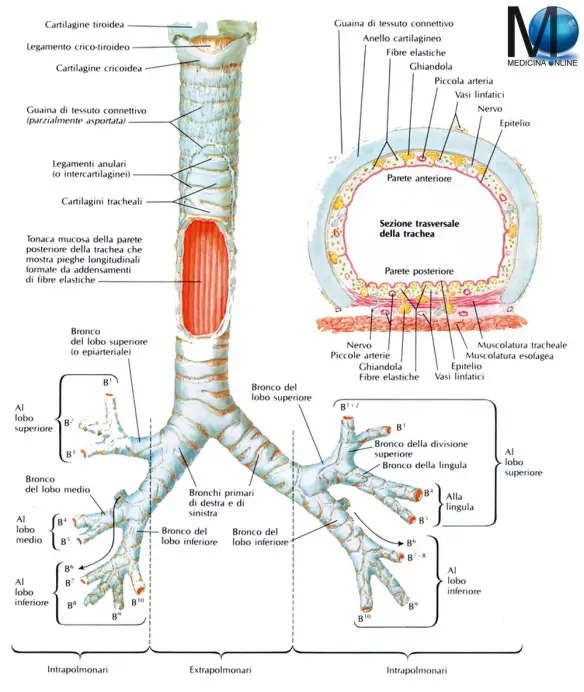 Con “bronco” in anatomia umana si intende ciascuna delle due ramificazioni terminali della trachea, il condotto che trasporta l’aria inspirata verso i polmoni e l’aria espirata verso l’esterno. La trachea si divide a livello della 4ª-5ª vertebra toracica formando il bronco sinistro e nel bronco destro. I due bronchi, di uguale struttura, si dirigono verso l’ilo polmonare dove si dividono ulteriormente per formare un’arborizzazione all’interno dei polmoni: l’albero bronchiale. I due bronchi principali e parte della prima ramificazione sono chiamati bronchi extrapolmonari, mentre la parte dell’albero dentro i polmoni bronchi intrapolmonari. In completa continuità con la trachea, permettono all’aria inspirata di arrivare ad entrambi i polmoni dopo essere passata per la faringe, la laringe e la trachea stessa.
Con “bronco” in anatomia umana si intende ciascuna delle due ramificazioni terminali della trachea, il condotto che trasporta l’aria inspirata verso i polmoni e l’aria espirata verso l’esterno. La trachea si divide a livello della 4ª-5ª vertebra toracica formando il bronco sinistro e nel bronco destro. I due bronchi, di uguale struttura, si dirigono verso l’ilo polmonare dove si dividono ulteriormente per formare un’arborizzazione all’interno dei polmoni: l’albero bronchiale. I due bronchi principali e parte della prima ramificazione sono chiamati bronchi extrapolmonari, mentre la parte dell’albero dentro i polmoni bronchi intrapolmonari. In completa continuità con la trachea, permettono all’aria inspirata di arrivare ad entrambi i polmoni dopo essere passata per la faringe, la laringe e la trachea stessa.