 Con il termine “overdose” in medicina si indica la dose di una sostanza (ad esempio farmaci come gli antidepressivi o droghe come cocaina o eroina) che risulta eccessiva Continua a leggere
Con il termine “overdose” in medicina si indica la dose di una sostanza (ad esempio farmaci come gli antidepressivi o droghe come cocaina o eroina) che risulta eccessiva Continua a leggere
Archivi tag: concentrazione
Cause di overdose accidentale e intenzionale: situazioni tipiche

Alcuni tentano il suicidio assumendo dosi eccessive di farmaci
Con il termine “overdose” in medicina si indica la dose di una sostanza (ad esempio farmaci come gli antidepressivi o droghe come cocaina o eroina) che risulta eccessiva Continua a leggere
Sintomi di overdose da sostanze eccitanti e deprimenti
 Con il termine “overdose” in medicina si indica la dose di una sostanza (ad esempio farmaci come gli antidepressivi o droghe come cocaina o eroina) che risulta eccessiva Continua a leggere
Con il termine “overdose” in medicina si indica la dose di una sostanza (ad esempio farmaci come gli antidepressivi o droghe come cocaina o eroina) che risulta eccessiva Continua a leggere
Quando si verifica una overdose?
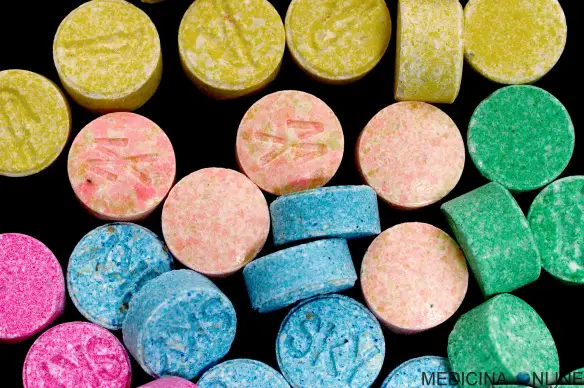 Una overdose si verifica quando viene assunta una quantità eccessiva di una data sostanza, ad esempio stupefacenti (droghe come cocaina, ecstasy ed eroina) o Continua a leggere
Una overdose si verifica quando viene assunta una quantità eccessiva di una data sostanza, ad esempio stupefacenti (droghe come cocaina, ecstasy ed eroina) o Continua a leggere
Cosa significa “overdose” e “andare in overdose”?
Cos’è una overdose?
Con il termine “overdose” in medicina si indica la dose di una sostanza (ad esempio farmaci antidepressivi o droghe come cocaina o eroina) che risulta eccessiva Continua a leggere
Nevrastenia (esaurimento nervoso): cause, diagnosi, cure
 Con il termine “nevrastenia” (anche chiamata “scompenso nervoso”, “astenia mentale”, “astenia nervosa” o Continua a leggere
Con il termine “nevrastenia” (anche chiamata “scompenso nervoso”, “astenia mentale”, “astenia nervosa” o Continua a leggere
Ginkgo biloba: a cosa serve, indicazioni, dosaggio, effetti collaterali
 Il ginkgo biloba (a volte chiamato “ginko biloba”) è una pianta antichissima le cui origini risalgono a 250 milioni di anni fa nel Permiano e per questo è considerato un Continua a leggere
Il ginkgo biloba (a volte chiamato “ginko biloba”) è una pianta antichissima le cui origini risalgono a 250 milioni di anni fa nel Permiano e per questo è considerato un Continua a leggere
Differenza tra soluzione ipertonica, ipotonica ed isotonica in chimica
 Si definisce “soluzione” in chimica una miscela omogenea in cui una o più sostanze sono contenute in una fase liquida o solida o gassosa; una soluzione contiene particelle diverse mescolate e distribuite in modo uniforme nello spazio disponibile in modo che ogni volume di soluzione abbia la medesima composizione degli altri. La misura della quantità di soluto rispetto alla quantità di soluzione è detta concentrazione e viene misurata sia tramite unità fisiche che tramite unità chimiche.
Si definisce “soluzione” in chimica una miscela omogenea in cui una o più sostanze sono contenute in una fase liquida o solida o gassosa; una soluzione contiene particelle diverse mescolate e distribuite in modo uniforme nello spazio disponibile in modo che ogni volume di soluzione abbia la medesima composizione degli altri. La misura della quantità di soluto rispetto alla quantità di soluzione è detta concentrazione e viene misurata sia tramite unità fisiche che tramite unità chimiche.
In chimica si possono distinguere tre tipi di soluzione, in base alla concentrazione di soluto:
- soluzioni isotoniche: sono due soluzioni con stessa concentrazione di soluto tra loro;
- soluzione ipertonica: è una soluzione con maggiore concentrazione di soluto rispetto ad un’altra soluzione;
- soluzione ipotonica: è una soluzione con minore concentrazione di soluto rispetto ad un’altra soluzione.
Passaggio di acqua da una soluzione all’altra
Il passaggio dell’acqua attraverso una membrana posta tra due ambienti (ad esempio cellula e spazio extracellulare), dipende dal tipo di ambiente ipertonico, ipotonico o isotonico:
- se la soluzione è isotonica rispetto alla cellula, ci sarà la medesima concentrazione di soluto da entrambe le parti venendosi a creare un equilibrio idrico;
- se la soluzione è ipertonica rispetto alla cellula, l’acqua si muoverà verso l’esterno della cellula che può essere danneggiata dalla disidratazione;
- se la soluzione è ipotonica rispetto alla cellula, l’acqua si muoverà verso l’interno della cellula che si rigonfia e può scoppiare (lisi cellulare).
Leggi anche:
- Differenza tra pressione idrostatica, oncotica ed osmotica
- Differenza tra elemento, composto e miscuglio con esempi
- Differenza tra miscuglio omogeneo ed eterogeneo con esempi
- Differenza tra aldosi e chetosi con esempi
Per sopravvivere in un ambiante ipertonico o ipotonico la cellula deve quindi continuamente regolare l’equilibrio idrico, tramite l’osmoregolazione. Le cellule vegetali hanno una parete cellulare che limita il loro volume e ne definisce la forma.
Turgore : pressione interna alla cellula contro la parete cellulare che impedisce l’ingresso di altra acqua.
- se la soluzione è isotonica rispetto alla cellula vegetale, quest’ultima perde il proprio turgore;
- se la soluzione è ipertonica rispetto alla cellula vegetale perde acqua e raggrinzisce e la membrana si stacca dalla parete cellulare mediante un fenomeno detto plasmolisi;
- Se la soluzione è ipotonica rispetto alla cellula vegetale, la cellula è turgida.
Le proteine di trasporto consentono una diffusione facilitata, cioè permettono a una sostanza di attraversare la membrana secondo il gradiente di concentrazione. È un tipo di trasporto passivo, non richiede energia. La diffusione facilitata è utilizzata da zuccheri, amminoacidi, ioni e acqua. Le proteine di trasporto più comuni agiscono da canale per queste sostanze; la proteina da trasporto “ carrier” si lega al proprio passeggero, cambia forma e lo lascia all’altro lato della membrana. Le proteine di trasporto dette acquaporine rendono rapida la diffusione dell’acqua. La proteina di trasporto è specifica per la sostanza di cui facilita il passaggio; più proteine di trasporto ci sono, più rapida è la diffusione.
Leggi anche:
- Differenza tra soluzione, sospensione aerosol ed emulsione in chimica
- Differenza tra soluzione e miscuglio in chimica con esempi
- Differenza tra soluzione e miscela in chimica con esempi
- Differenza tra miscela omogenea ed eterogenea
- Differenza tra soluzione e dispersione in chimica con esempi
- Liquido in chimica: definizione e caratteristiche fisiche
- Differenza tra fluido e liquido
- Differenza tra liquidi volatili e non volatili in chimica
- Differenza tra fluido newtoniano e non newtoniano con esempi
- Differenza tra fluido ideale e reale
- Differenza tra densità e viscosità di un fluido con esempi
- Cos’è la densità in chimica? Densità di acqua ed aria a varie temperature
- Massa e peso di un corpo sulla Luna rispetto alla Terra
- Massa e peso sui vari pianeti del Sistema Solare rispetto alla Terra
- Differenza tra densità e peso specifico
- Differenza tra densità reale ed assoluta con esempi
- Esempio di esercizio svolto sul calcolo della densità
- Differenza tra densità e concentrazione
- Differenza tra massa e peso in fisica ed in medicina
- Quanto pesa un litro di acqua liquida o ghiacciata?
- Differenza tra acqua distillata e demineralizzata e loro usi
- E’ più difficile e pesante nuotare a mare o in piscina?
- Perché l’acqua di mare non si può bere?
- Differenza tra orbita ed orbitale (in chimica ed astronomia)
- Differenza tra elettrone, fotone, protone e ione
- Differenza tra acidi e basi
- Differenza tra stella, pianeta e satellite con esempi
- Perché l’acqua di mare è salata?
- Quante volte l’uomo è stato sulla Luna?
- Perché si verificano le maree?
- Perché la luna ci rivolge sempre la stessa faccia? Com’è il lato oscuro?
- Cos’è una eclissi solare? Come e quando si verifica?
- Vi spiego come far entrare sette miliardi di persone nello spazio di una palla da tennis
- Quante persone vivono a Roma, in Italia, in Europa e nel mondo?
- Teoria del Tempo Fantasma: 297 anni di storia non sono mai esistiti, ora siamo nel 1717
- Cosa sono e qual è la differenza tra massa magra e massa grassa? Tutte le percentuali di grasso, ossa e muscoli
- Un atomo si può dividere? Cosa succede se si divide?
- Differenza tra atomo e molecola con esempi
- Differenza tra atomi e ioni e regola dell’ottetto
- Differenza tra atomo e elemento
- Differenza tra atomo e nucleo
- Differenza tra anfipatica ed anfotera
- Differenze tra H2O e H2S in chimica
- Differenze e punti in comune tra chimica e fisica
- Differenza tra fisica classica e quantistica
- Differenza tra fisica classica e meccanica quantistica
- Differenza tra microscopio ottico ed elettronico
- Differenza tra microscopio elettronico a scansione e a trasmissione
- Differenza tra raggi x e gamma
- L’uomo più grasso del mondo pesa 368 kg
- Lina Medina è la mamma più giovane al mondo: ha partorito il suo primo figlio a 5 anni
- La persona più intelligente al mondo mai esistita nella storia dell’uomo
- Jon Brower Minnoch: quanto è arrivato a pesare l’uomo più grasso del mondo?
- Le 20 droghe più potenti e pericolose al mondo
- Lo scivolo trasparente più alto e pauroso del mondo
- Valeria Levitina pesa 25 kg: è la ragazza più anoressica del mondo [VIDEO]
- Differenza tra eclissi solare e lunare (spiegazione semplice)
- Differenza tra eclissi totale, parziale, anulare e penombrale
- Com’è fatta la tuta degli astronauti?
- Cos’è una galassia? Di cosa è fatta?
- Cos’è e dove si trova la Stella Polare? Come individuarla?
- Cos’è una eclissi lunare? Come e quando si verifica?
- Perché la notte di San Lorenzo cadono le stelle? Cos’è una stella cadente?
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
