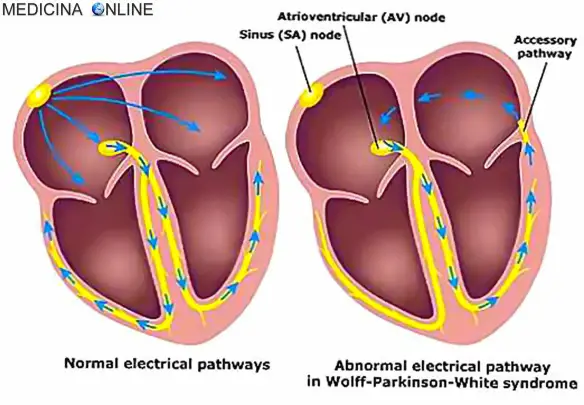
 La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti. I pazienti con sindrome di WPW spesso hanno più di una via accessoria, ed in alcuni possono essere anche più di otto; questo è stato dimostrato in soggetti affetti dall’anomalia di Ebstein. La sindrome di WPW è talora associata alla neuropatia ottica ereditaria di Leber (LHON),una forma di malattia mitocondriale.
La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti. I pazienti con sindrome di WPW spesso hanno più di una via accessoria, ed in alcuni possono essere anche più di otto; questo è stato dimostrato in soggetti affetti dall’anomalia di Ebstein. La sindrome di WPW è talora associata alla neuropatia ottica ereditaria di Leber (LHON),una forma di malattia mitocondriale.
Fisiopatologia
In condizioni normali la conduzione dell’impulso elettrico dagli atrii ai ventricoli del cuore percorre una via costituita dal nodo atrio-ventricolare e fascio di His. Il nodo atrio-ventricolare ha caratteristiche elettrofisiologiche di velocità di conduzione e tempo di refrattarietà tali da costituire un filtro in grado di proteggere i ventricoli dalla conduzione di impulsi atriali troppo rapidi e potenzialmente pericolosi. In alcuni casi esistono vie di conduzione dette accessorie (VA) tra atrii e ventricoli che possono essere localizzate in vari siti degli anelli valvolari tricuspidalico e mitralico. Per le loro caratteristiche elettrofisiologiche, simili alle cellule del muscolo cardiaco comune, queste vie accessorie non svolgono la funzione di filtro tipica del nodo atrioventricolare, e in certi casi possono condurre gli impulsi ai ventricoli a frequenze molto elevate. Durante il ritmo sinusale una via accessoria si manifesta all’elettrocardiogramma con la pre-eccitazione ventricolare e la presenza di un’onda “delta”: la conduzione attraverso la via accessoria non subisce un rallentamento come all’interno del nodo atrioventricolare e l’intervallo PQ dell’elettrocardiogramma (che rappresenta appunto il percorso dell’impulso elettrico dagli atrii ai ventricoli) è più breve del normale (pre-eccitazione). Inoltre l’estremità ventricolare della via accessoria si inserisce nel muscolo cardiaco comune anziché essere in continuità con il sistema specializzato di conduzione: per questo motivo la depolarizzazione di una parte dei ventricoli avviene più lentamente, e si traduce in un aspetto elettrocardiografico detto onda “delta”. Se la presenza di una via accessoria si associa a episodi di palpitazione si parla di Sindrome di Wolff-Parkinson-White. Le palpitazioni possono dipendere da “aritmie da rientro“, ossia determinate da un corto circuito in cui l’impulso generalmente raggiunge i ventricoli attraverso il nodo atrioventricolare e rientra negli atrii attraverso la via accessoria percorsa in senso inverso. L’aritmia si perpetua fino a quando una delle due vie (nodo o via accessoria) non è più in grado di condurre. In alcuni casi meno frequenti il circuito è percorso all’inverso, ossia la via accessoria è utilizzata nel senso dagli atrii ai ventricoli, mentre l’impulso rientra agli atrii attraverso il fascio di His e il nodo atrioventricolare. In altri casi la via accessoria non partecipa direttamente al meccanismo che perpetua l’aritmia, ma può contribuire alla conduzione ai ventricoli di aritmie degli atrii (fibrillazione atriale/flutter atriale/tachicardia atriale). Se le capacità di conduzione della VA sono molto elevate (breve tempo di refrattarietà) la frequenza ventricolare risultante può essere molto rapida (> 250 battiti al minuto) e mettere a rischio di aritmie ventricolari rapide e di arresto cardiaco.
Sintomi di Wolff-Parkinson-White
Clinicamente tale sindrome si può manifestare con fibrillazione atriale e palpitazioni secondarie alle sopra citate aritmie da rientro. Non è raro che sia totalmente asintomatica e che venga scoperta durante un elettrocardiogramma eseguito per altri motivi, ad esempio in una visita di medicina sportiva.
Diagnosi di Wolff-Parkinson-White
La diagnosi di sindrome di WPW è clinica ma soprattutto si avvale dell’elettrocadiogramma, che può scovarla anche in un soggetto asintomatico: in questi casi si manifesta come un’onda delta, che corrisponde all’ampliamento della fase di ascesa del complesso QRS associato all’accorciamento dell’intervallo PR. Tutto questo è dovuto al fluire dell’impulso elettrico attraverso la via accessoria piuttosto che attraverso il nodo atrio-ventricolare.
Se il paziente accusa episodi di fibrillazione atriale, l’ECG mostra una tachicardia rapida polimorfica (senza torsione di punta). Questa combinazione di fibrillazione atriale e sindrome di WPW è considerata pericolosa, e molti farmaci antiaritmici sono controindicati.
Quando un soggetto è in normale ritmo sinusale le caratteristiche della sindrome di WPW sono un intervallo PR corto, uno slargamento del complesso QRS (più di 120msec in lunghezza) con ampliamento della fase di ascesa del QRS stesso, e cambiamenti della ripolarizzazione che si riflettono in alterazioni del tratto ST e dell’onda T.
In soggetti affetti l’attività elettrica che inizia nel nodo seno-atriale passa attraverso il fascio accessorio tanto bene quanto nel nodo atrio-ventricolare. Poiché il fascio accessorio non blocca l’impulso quanto il nodo, i ventricoli vengono attivati da questo, e subito dopo dal nodo. Questo causa le alterazioni ECG sopra descritte.
Altra tecnica di diagnosi è lo studio elettrofisiologico: per questo esame, il medico inserisce un catetere sottile e flessibile, dotato di elettrodi all’estremità, attraverso i vasi sanguigni fino a raggiungere diverse parti del cuore dove sono in grado di mappare gli impulsi elettrici.
Leggi anche:
- Pressione arteriosa: valori normali e patologici
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
Trattamenti di Wolff-Parkinson-White
Il trattamento degli episodi acuti di aritmie da rientro nella Sindrome di WPW si avvale di farmaci che agiscono bloccando la conduzione attraverso il nodo atrioventricolare, interrompendo uno dei bracci dell’aritmia. Questi farmaci sono invece da evitare in caso di fibrillazione atriale condotta rapidamente attraverso la via accessoria, poiché possono in certi casi aumentare la frequenza di conduzione ai ventricoli attraverso la via accessoria.
In presenza di pre-eccitazione ventricolare e indipendentemente dalla presenza di sintomi aritmici è raccomandato sottoporsi a studio elettrofisiologico per indagare le capacità conduttive della via accessoria e la inducibilità di aritmie. Se la via accessoria ha capacità conduttive elevate con un rischio di frequenze ventricolari elevate durante eventuali episodi di fibrillazione atriale, o in presenza sintomi e di aritmie da rientro, è indicato procedere alla ablazione della via accessoria.
Lo studio elettrofisiologico è in grado di identificare la sede della via accessoria, da cui dipenderà l’approccio utilizzato per l’ablazione: in presenza di una via situata nelle sezioni destre del cuore l’accesso è generalmente dalla vena femorale destra.
Per le vie sinistre saranno possibili un accesso venoso e successiva puntura transettale per passare dall’atrio destro all’atrio sinistro, oppure un approccio “retrogrado” attraverso le arterie femorale e aorta. L’energia utilizzata per l’ablazione è generalmente la radiofrequenza. Dopo un’ablazione efficace saranno prevenuti episodi di aritmia da rientro attraverso la via accessoria e all’elettrocardiogramma non sarà più visibile l’onda delta. L’efficacia a lungo termine dell’ablazione è in genere molto elevata e supera il 95%.
Dopo un’ablazione efficace e in assenza di altri tipi di aritmia o di cardiopatia, non è necessaria alcuna terapia farmacologica.
Leggi anche:
- Sapresti riconoscere un infarto del miocardio? Impara ad identificarlo e salverai una vita (anche la tua)
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Wolff-Parkinson-White: nei bambini, rischi, sport, morte improvvisa
- Wolff-Parkinson-White: elettrocardiogramma (ECG) ed alterazioni
- Differenza tra cardioversione spontanea, elettrica e farmacologica
- Il defibrillatore non funziona: muore a 51 anni per un infarto
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Il massaggio cardiaco si esegue in assenza di…
- Flutter atriale: cause, terapie, cosa fare, cura, ablazione e sintomi
- Differenza tra fibrillazione atriale e flutter
- Differenza tra fibrillazione atriale ed extrasistole
- Differenza tra fibrillazione atriale ed aritmia
- Differenza tra fibrillazione atriale e fibrillazione ventricolare
- Differenza tra tachicardia e fibrillazione atriale e ventricolare
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Differenza tra pacemaker e defibrillatore ICD
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Differenza tra sintomo e segno con esempi
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!

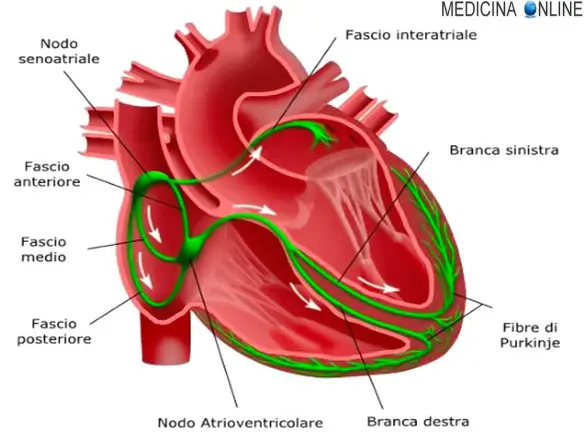 Una bradiaritmia è un’aritmia cardiaca caratterizzata da un rallentamento patologico della frequenza cardiaca causato da un disturbo nella formazione o nella conduzione dell’impulso elettrico cardiaco. La diminuzione della frequenza cardiaca può essere talmente severa da non permettere il corretto pompaggio del sangue non solo sotto sforzo, ma perfino con soggetto a riposo, ad esempio mentre è steso su un letto. Il deficit di funzione di pompa del cuore porta l’organismo (e soprattutto il cervello) a non avere adeguato nutrimento ed ossigeno con possibile perdita di coscienza e – se il normale ritmo non viene ripristinato e la bradiaritmia è severa – al decesso del paziente, anche a causa dell’accumulo di liquidi a livello polmonare (
Una bradiaritmia è un’aritmia cardiaca caratterizzata da un rallentamento patologico della frequenza cardiaca causato da un disturbo nella formazione o nella conduzione dell’impulso elettrico cardiaco. La diminuzione della frequenza cardiaca può essere talmente severa da non permettere il corretto pompaggio del sangue non solo sotto sforzo, ma perfino con soggetto a riposo, ad esempio mentre è steso su un letto. Il deficit di funzione di pompa del cuore porta l’organismo (e soprattutto il cervello) a non avere adeguato nutrimento ed ossigeno con possibile perdita di coscienza e – se il normale ritmo non viene ripristinato e la bradiaritmia è severa – al decesso del paziente, anche a causa dell’accumulo di liquidi a livello polmonare (