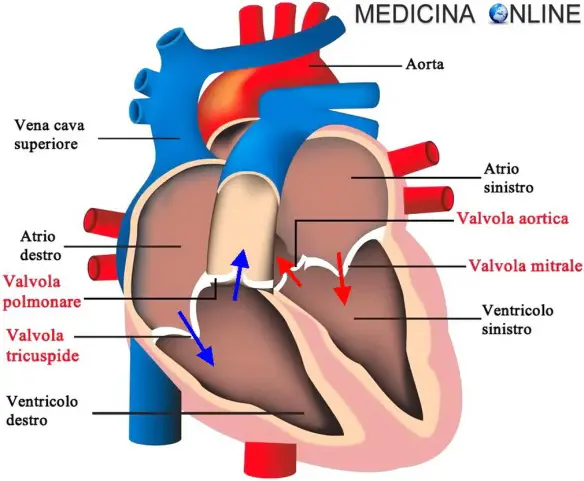
 In un cuore sano la valvola mitrale, quella che collega atrio sinistro e ventricolo sinistro, si apre per far passare il sangue dall’atrio al ventricolo, per poi chiudersi durante la contrazione ventricolare in modo che il sangue passi dal ventricolo verso l’arteria aorta. Nei soggetti con prolasso mitralico il lembo posteriore (o entrambi i Continua a leggere
In un cuore sano la valvola mitrale, quella che collega atrio sinistro e ventricolo sinistro, si apre per far passare il sangue dall’atrio al ventricolo, per poi chiudersi durante la contrazione ventricolare in modo che il sangue passi dal ventricolo verso l’arteria aorta. Nei soggetti con prolasso mitralico il lembo posteriore (o entrambi i Continua a leggere
Archivi tag: atrio
Differenza tra fibrillazione atriale e fibrillazione ventricolare
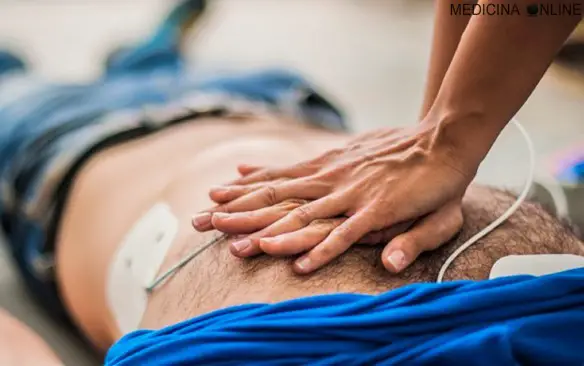 Con “fibrillazione atriale” in medicina si intende una aritmia cardiaca, cioè una alterazione del ritmo cardiaco normale (ritmo sinusale), che origina dagli atri del cuore. È una complessa patologia elettrica degli atri che presenta costantemente tre caratteristiche principali:
Con “fibrillazione atriale” in medicina si intende una aritmia cardiaca, cioè una alterazione del ritmo cardiaco normale (ritmo sinusale), che origina dagli atri del cuore. È una complessa patologia elettrica degli atri che presenta costantemente tre caratteristiche principali:
- l’attivazione elettrica rapida ed apparentemente caotica del tessuto atriale, che provoca il caratteristico sintomo di cuore “palpitante” ed è riscontrabile con un comune elettrocardiogramma (ECG);
- la diminuita efficienza dell’attività di pompa del cuore (diminuzione della gittata cardiaca);
- se la fibrillazione atriale si prolunga nel tempo determina l’aumento del rischio tromboembolico, causato dal rallentamento del flusso ematico nel cuore che porta ad aumentato rischio di coagulazione. L’eventuale formazione di embolo può portare a ictus cerebrale o infarto del miocardio.
La fibrillazione atriale è il risultato di un gran numero di disordini cardiaci ed extracardiaci: da malattie strutturali, come le valvulopatie e le cardiomiopatie, all’ipertensione arteriosa, a malattie genetiche ereditarie, a ernia iatale, patologie della tiroide, ai distiroidismi, fino ai casi in cui non è possibile determinare la causa, detti idiopatici.
Con “fibrillazione ventricolare” (FV o VF) in medicina si intende una gravissima aritmia che si caratterizza per un ritmo cardiaco rapidissimo, caotico e disorganizzato che origina dai ventricoli. La rapidità e la disorganizzazione dell’impulso elettrico rendono il cuore incapace di espellere il sangue all’interno del circolo arterioso, portando ad un arresto cardiaco. I tessuti corporei e cerebrali, durante un arresto cardiaco, non sono più perfusi da sangue ed ossigeno: questo comporta una veloce perdita di coscienza e delle capacità respiratorie. Un arresto cardiaco è una urgenza medica: se non si interviene immediatamente con la rianimazione cardiopolmonare e con un defibrillatore, nel giro di pochissimi minuti provoca danni permanenti al cervello e – successivamente – il decesso del paziente. L’arresto cardiaco improvviso è una delle principali cause di morte nel mondo industrializzato, dove la maggior parte delle volte è secondario ad infarto miocardico acuto.
Da quanto detto entrambi i tipi di fibrillazione sono aritmie – una ad origine dagli atri, l’altra ad origine dai ventricoli, entrambe ben visibili con un elettrocardiogramma – tuttavia la differenza è sostanziale: mentre la fibrillazione atriale, pur di lunga durata, può rappresentare un problema di aumentato rischio di formazione di emboli, è la fibrillazione ventricolare ad essere estremamente più grave dal momento che in essa la capacità del cuore di pompare sangue è totalmente inefficiente (mentre nella fibrillazione atriale è – pur se in parte – conservata). La fibrillazione ventricolare porta di fatto ad un arresto cardiaco che è una urgenza medica: il mancato ritorno ad un ritmo sinusale (tramite cardioversione con defibrillatore, massaggio cardiaco o pugno precordiale) porta al decesso del paziente.
Leggi anche:
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Flutter atriale: cause, terapie, cosa fare, cura, ablazione e sintomi
- Differenza tra fibrillazione atriale e flutter
- Differenza tra fibrillazione atriale ed extrasistole
- Differenza tra fibrillazione atriale ed aritmia
- Differenza tra tachicardia e fibrillazione atriale e ventricolare
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Sapresti riconoscere un infarto del miocardio? Impara ad identificarlo e salverai una vita (anche la tua)
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Differenza tra cardioversione spontanea, elettrica e farmacologica
- Il defibrillatore non funziona: muore a 51 anni per un infarto
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Il massaggio cardiaco si esegue in assenza di…
- Sindrome di Wolff-Parkinson-White: cos’è, cosa fare, come si cura
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Differenza tra pacemaker e defibrillatore ICD
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Differenza tra sintomo e segno con esempi
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Flutter atriale: cause, terapie, cosa fare, cura, ablazione e sintomi
 Con “flutter atriale” si intende una “aritmia ectopica sopraventricolare” cioè una:
Con “flutter atriale” si intende una “aritmia ectopica sopraventricolare” cioè una:
- aritmia (alterazione del ritmo cardiaco sinusale)
- ectopica (che origina da un sito diverso dal normale pacemaker fisiologico, il nodo del seno atriale)
- sopraventricolare (cioè ad origine atriale)
con contrazione degli atri estremamente rapida: la frequenza atriale in corso di flutter può arrivare anche a superare i 300 impulsi al minuto. Gli impulsi sono irregolari e compaiono all’improvviso, quasi sempre senza alcun sintomo premonitore. Generalmente si instaura un blocco nella conduzione atrioventricolare, per cui la frequenza percepita è normalmente di circa 150 battiti al minuto. A causa del rallentamento della conduzione dell’impulso attraverso il nodo atrioventricolare, non tutte le attività elettriche del flutter si trasmettono dagli atri ai ventricoli. Generalmente il rapporto tra l’attività elettrica degli atri e quella dei ventricoli è 2:1 (cioè due attività atriali ed una ventricolare), talvolta 3:1 o 3:2, molto raramente 1:1 (di solito quando la frequenza del flutter è stata portata, attraverso la somministrazione di farmaci, sotto i 200 battiti al minuto).
Rispetto alla fibrillazione atriale, le modificazioni del ritmo sono meno marcate. Infatti, se durante una fibrillazione atriale la frequenza del battito cardiaco atriale può raggiungere i 400 battiti al minuto, durante un flutter atriale la frequenza del battito cardiaco atriale si innalza solitamente tra i 200 ed i 200 battiti al minuto.
Una frequenza inferiore si traduce in un numero inferiore di impulsi di contrazione. Pertanto, ciò che cambia rispetto ad una fibrillazione atriale è anche il maggior tempo concesso al muscolo del cuore (il miocardio) per “ricaricarsi” e tornare recettivo ad un nuovo stimolo (tempo di refrattarietà). Questo lasso di tempo permette al battito di risultare meno disordinato.
Un’altra importante differenza tra flutter e fibrillazione, riguarda l’impatto che hanno sul ventricolo. Durante queste due forme aritmiche, parte degli impulsi viene bloccata a livello del nodo atrioventricolare, che ferma parte degli impulsi diretti verso il ventricolo. Questo blocco è assai maggiore nel flutter atriale, tanto che la contrazione ventricolare può essere anche ¼ di quella atriale. Il medico, infatti, definisce il flutter con le dizioni di 2:1, 3:1 o 4:1, per indicare che può passare per il blocco atrioventricolare uno stimolo, rispettivamente, ogni 2, ogni 3 o ogni 4. Le conseguenze del blocco atrioventricolare riguardano la gittata cardiaca, che sarà più o meno influenzata in base al numero degli stimoli che raggiungono il ventricolo. Può apparire complicato comprendere questo dettaglio, ma è assai importante dal punto di vista sintomatologico: infatti, maggiore è la frequenza ventricolare, più evidenti sono i sintomi. In altre parole, la frequenza ventricolare può variare notevolmente, da 180 battiti per minuto a meno di 100. Il fatto che la frequenza ventricolare possa rientrare nell’intervallo di normalità, non deve stupire: spesso accade che il flutter passi inosservato proprio per questo motivo.
Tipi di flutter atriale
A seconda della modalità di comparsa, si possono distinguere due tipi di flutter atriale:
- flutter atriale parossistico: il flutter compare bruscamente e repentinamente, in forma isolata. La frequenza del battito è molto alta; le contrazioni atriali superano il blocco atriventricolare con notevole efficacia, di 2:1 e, in alcuni rari casi, anche di 1:1. La frequenza ventricolare, quindi, può raggiungere anche i 120-180 battiti per minuto. La forma parossistica caratterizza le manifestazioni isolate, che si verificano in un individuo sano. Dura qualche ora, al massimo qualche giorno, molto spesso si esaurisce da sola. Ciò esclude l’uso di farmaci o di altri interventi terapici;
- flutter atriale permanente: la sua comparsa è più graduale ed ha frequenza è più bassa rispetto alla forma parossistica. Le contrazioni superano il blocco del nodo atrioventricolare con un’efficienza di 3:1, 4:1 e anche 5:1. Quindi, la frequenza ventricolare è più bassa rispetto alla forma parossistica e può non superare, in alcuni casi, i 100 battiti per minuto. La forma permanente può durare anni e passare inosservata, nonostante sia sinonimo, nella maggior parte dei casi, di un patologia associata. Serve una terapia specifica e una terapia generale: la prima per agire contro la patologia associata; la seconda per agire contro il flutter.
Fisiopatologia
Il meccanismo elettrofisiologico alla base del flutter è un rientro dello stimolo elettrico all’interno dell’atrio (rientro intra-atriale) che può interessare tutto l’atrio o una parte di esso. Il disturbo artitmico si trasmette fino al ventricolo, da ciò ne deriva che è alterata anche la gittata cardiaca e di conseguenza anche la circolazione sanguigna polmonare e sistemica.
Leggi anche:
- Differenza tra fibrillazione atriale e flutter
- Differenza tra fibrillazione atriale ed extrasistole
- Differenza tra fibrillazione atriale ed aritmia
- Differenza tra fibrillazione atriale e fibrillazione ventricolare
- Differenza tra tachicardia e fibrillazione atriale e ventricolare
Cause di flutter atriale
Il flutter atriale può svilupparsi in un cuore sano, in forma generalmente isolata, spesso legate a:
- stress,
- ansia,
- alcuni tipi di farmaci,
- abuso di caffè,
- abuso di droghe,
- fumo di sigarette.
Può presentarsi anche in cuori con anomalie degli atri (per es. dilatazione) o alterazioni del sistema di conduzione. Come avviene per la fibrillazione atriale, l’insorgenza può essere dovuta a varie patologie e condizioni, come:
- cardiopatia reumatica;
- cardiopatia valvolare (o valvulopatia);
- infarto del miocardio;
- coronaropatie;
- pericarditi;
- ipertensione;
- ipertiroidismo;
- obesità;
- reflusso gastroesofageo;
- malattie respiratorie;
- squilibri elettrolitici.
Sintomi di flutter atriale
Generalmente il paziente non ha sintomi premonitori. Il flutter compare improvvisamente e la persona avverte irregolarità nel ritmo (nel caso di blocco variabile 2:1 e 3:1) oppure frequenza accelerata. È da notarsi che spesso molti pazienti non avvertono alcuna alterazione del ritmo (flutter atriale asintomatico). Possono riscontrarsi disturbi legati ad ischemia cardiaca (tipo angina pectoris, infarto miocardico acuto..) e/o sintomi di uno scompenso cardiaco. I sintomi più diffusi di flutter atriale sono:
- palpitazione;
- senso di vertigine;
- disorientamento (specie negli anziani);
- malessere generale;
- dispnea;
- sincope;
- dolore toracico;
- mancanza di forze (astenia).
Rischi e complicanze del flutter atriale
Il flutter atriale, seppur meno della fibrillazione atriale è considerato un ritmo emboligeno, ovvero, una condizione che determina rallentamento del flusso ematico, aumento della coagulazione sanguigna ed aumentato rischio di formazione di trombi nell’atrio sinistro che possono spostarsi nel circolo sanguigno e causare ictus cerebrale ed infarto del miocardio. Le altre complicanze della presenza di flutter atriale sono principalmente un blocco A-V 1:1 ed il passaggio a fibrillazione atriale o a fibrillazione ventricolare. Da non sottovalutare infine che, un flutter causa una minore efficienza cardiaca, che si riflette in una diminuzione della gittata cardiaca: ciò fornisce in modo alterato il corretto nutrimento a tutti i tessuti del corpo, a partire dal cuore stesso e dal cervello. Ciò può causare, specie nei soggetti anziani, un mancamento che porta a cadute che possono determinare fratture di femore ed altri traumi potenzialmente gravi.
Diagnosi di flutter atriale
Il sospetto di flutter si instaura anche semplicemente grazie al polso radiale o carotideo del paziente, ma per chiarire l’esatta entità del flutter atriale serve un’accurata visita cardiologica, che si avvale dei risultati di:
- elettrocardiogramma (ECG);
- ecoccolordoppler cardiaco;
- radiografia del torace.
Nell’ECG in particolare, il flutter appare evidente: le onde che si visualizzano sono a dente di sega e si nota la continua attività elettrica (più onde P per ogni complesso QRST), ancora più chiara in II, III o V derivazione. Normalmente la frequenza ventricolare si stabilizza (nei casi blocco A-V fisso) tra i 145-150 (se blocco A-V 2:1) oppure 95-100 (se blocco A-V 3:1), oppure circa 75 (se blocco A-V 4:1).
Uno strumento molto utile per la diagnosi è infine l’elettrocardiogramma dinamico secondo Holter. Si tratta di un normale ECG, con la differenza, assai vantaggiosa, che il monitoraggio si protrae per 24-48 ore, senza impedire al paziente di svolgere le normali attività di vita quotidiana. È utile qualora gli episodi di flutter atriale siano sporadici e non prevedibili: ciò può portare il paziente a fare un normale ECG quando il ritmo non è più in flutter. Con l’Holter invece si riesce ad individuare un qualsiasi episodio di aritmia durante l’intero periodo di monitoraggio.
Cura del flutter atriale
La terapia del flutter va scelta caso per caso in base alla causa che la determina.
Come intervento immediato è utile la cardioversione sincronica con corrente diretta a bassa energia, sempre minori di 50 joule; come terapia farmacologica si usano generalmente farmaci betabloccanti e calcioantagonisti per rallentare l’alta frequenza. In individui con forme isolate e cuore sano, generalmente è sufficiente il controllo dell’ansia, la limitazione del peso corporeo o la diminuzione delle sigarette fumate, per determinare un rischio minore di aritmia.
Cura del flutter atriale permanente ed ablazione transcatetere
Se il flutter atriale è di tipo permanente, molto spesso significa che all’origine del disturbo c’è una cardiopatia o una patologia di altra natura. Risolvere tale condizione, con un approccio terapeutico scelto caso per caso, è il passo fondamentale per aiutare il ripristino del normale ritmo cardiaco. La terapia, invece, mirata a curare il flutter atriale, fa da supporto e mantenimento. Essa è la seguente:
- Somministrazione di farmaci:
- Digitale.
- Antiaritmici: derivati della chinidina, dofetilide, ibutilide, flecainide, propafenone e amiodarone.
- Anticoagulanti. Le forme permanenti possono creare situazione di trombo-embolia. Si usano in presenza di particolari cardiopatie, le valvulopatie mitraliche, che potrebbero generare trombi o emboli.
- Beta-bloccanti e calcio-antagonisti. Rallentano il ritmo cardiaco, agendo a livello del nodo atrioventricolare. Si somministrano a coloro che sono tolleranti alla digitale.
- Trattamento elettrico:
- Cardioversione. Non è più indicata, quando il paziente è affetto da una cardiopatia che altera la struttura del cuore, come per esempio le valvulopatie.
- Ablazione a radiofrequenza transcatetere. Si fa uso di un catetere che, una volta condotto fino al cuore, è in grado di infondere una scarica a radiofrequenza colpendo proprio l’area di miocardio che genera il flutter atriale. La zona colpita viene distrutta e questo dovrebbe riordinare il numero degli impulsi di contrazione da parte del nodo seno atriale. È un tecnica invasiva.
Leggi anche:
- Sapresti riconoscere un infarto del miocardio? Impara ad identificarlo e salverai una vita (anche la tua)
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Differenza tra cardioversione spontanea, elettrica e farmacologica
- Il defibrillatore non funziona: muore a 51 anni per un infarto
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Il massaggio cardiaco si esegue in assenza di…
- Sindrome di Wolff-Parkinson-White: cos’è, cosa fare, come si cura
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Differenza tra pacemaker e defibrillatore ICD
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Differenza tra sintomo e segno con esempi
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Differenza tra tachicardia e fibrillazione atriale e ventricolare
 Il cuore è un muscolo che ha come compito fondamentale quello di far circolare il sangue in tutto il corpo e per raggiungere tale obiettivo si contrae in maniera adeguata grazie ad un circuito elettrico, detto sistema eccito-conduzione, che attiva e regola la contrazione cardiaca. Tale contrazione è regolata, dal punto di vista temporale:
Il cuore è un muscolo che ha come compito fondamentale quello di far circolare il sangue in tutto il corpo e per raggiungere tale obiettivo si contrae in maniera adeguata grazie ad un circuito elettrico, detto sistema eccito-conduzione, che attiva e regola la contrazione cardiaca. Tale contrazione è regolata, dal punto di vista temporale:
- nella frequenza (cioè nel numero di contrazioni al minuto);
- nel ritmo (cioè nella pari distanza temporale tra un battito ed il successivo, rispetto a tutti gli altri battiti, che si traduce nella regolarità delle contrazioni).
Normalmente la frequenza cardiaca varia tra i 60 e i 100 battiti al minuto e le contrazioni si susseguono in modo regolare e ritmico (ad esempio distanziate sempre da un secondo una dall’altro nel caso di una frequenza di 60 battiti al minuto), con solo leggere variazioni fisiologiche legate alla respirazione (i battiti tendono a rallentare durante una espirazione profonda). Alterazioni fisiologiche o ritardi/blocchi dell’impulso elettrico che si verificano in varie patologie, vanno ad alterare uno od entrambi questi fattori, determinando appunto aritmia. L’aritmia cardiaca è quindi un disturbo:
- della frequenza cardiaca aumentata (tachicardia) in cui la frequenza supera i 100 battiti al minuto a riposo;
- della frequenza cardiaca diminuita (bradicardia) in cui la frequenza è inferiore ai 60 battiti al minuto a riposo.
- del ritmo cardiaco, in cui i battiti non sono ritmici (ad esempio: fibrillazione atriale o ventricolare).
Tali alterazioni sono riscontrabili semplicemente grazie al polso radiale o un elettrocardiogramma (ECG). E’ importante ricordare che non tutte le aritmie sono determinate da patologie. Un aumento fisiologico della frequenza cardiaca si verifica ad esempio compiendo un grosso sforzo o durante la gravidanza, mentre è abbastanza frequente riscontrare una bradicardia fisiologica in atleti e sportivi particolarmente allenati.
Con “fibrillazione atriale” in medicina si intende una aritmia cardiaca, cioè una alterazione del ritmo cardiaco normale (ritmo sinusale), che origina dagli atri del cuore. È una complessa patologia elettrica degli atri che presenta costantemente tre caratteristiche principali:
- l’attivazione elettrica rapida ed apparentemente caotica del tessuto atriale, che provoca il caratteristico sintomo di cuore “palpitante” ed è riscontrabile con un comune elettrocardiogramma (ECG);
- la diminuita efficienza dell’attività di pompa del cuore (diminuzione della gittata cardiaca);
- se la fibrillazione atriale si prolunga nel tempo determina l’aumento del rischio tromboembolico, causato dal rallentamento del flusso ematico nel cuore che porta ad aumentato rischio di coagulazione. L’eventuale formazione di embolo può portare a ictus cerebrale o infarto del miocardio.
La fibrillazione atriale è il risultato di un gran numero di disordini cardiaci ed extracardiaci: da malattie strutturali, come le valvulopatie e le cardiomiopatie, all’ipertensione arteriosa, a malattie genetiche ereditarie, a ernia iatale, patologie della tiroide, ai distiroidismi, fino ai casi in cui non è possibile determinare la causa, detti idiopatici.
Leggi anche:
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
Con “fibrillazione ventricolare” (FV o VF) in medicina si intende una gravissima aritmia che si caratterizza per un ritmo cardiaco rapidissimo, caotico e disorganizzato che origina dai ventricoli. La rapidità e la disorganizzazione dell’impulso elettrico rendono il cuore incapace di espellere il sangue all’interno del circolo arterioso, portando ad un arresto cardiaco. I tessuti corporei e cerebrali, durante un arresto cardiaco, non sono più perfusi da sangue ed ossigeno: questo comporta una veloce perdita di coscienza e delle capacità respiratorie. Un arresto cardiaco è una urgenza medica: se non si interviene immediatamente con la rianimazione cardiopolmonare e con un defibrillatore, nel giro di pochissimi minuti provoca danni permanenti al cervello e – successivamente – il decesso del paziente. L’arresto cardiaco improvviso è una delle principali cause di morte nel mondo industrializzato, dove la maggior parte delle volte è secondario ad infarto miocardico acuto.
Da quanto detto entrambi i tipi di fibrillazione sono aritmie – una ad origine dagli atri, l’altra ad origine dai ventricoli, entrambe ben visibili con un elettrocardiogramma – tuttavia la differenza è sostanziale: mentre la fibrillazione atriale, pur di lunga durata, può rappresentare un problema di aumentato rischio di formazione di emboli, è la fibrillazione ventricolare ad essere estremamente più grave dal momento che in essa la capacità del cuore di pompare sangue è totalmente inefficiente (mentre nella fibrillazione atriale è – pur se in parte – conservata). La fibrillazione ventricolare porta di fatto ad un arresto cardiaco che è una urgenza medica: il mancato ritorno ad un ritmo sinusale (tramite cardioversione con defibrillatore, massaggio cardiaco o pugno precordiale) porta al decesso del paziente.
Dovrebbe ora essere anche chiara la differenza tra “aritmia” ed i tue tipi di fibrillazione: questi ultimi sono un tipo particolare di aritmia. Tutte le fibrillazioni (atriali e ventricolari) sono aritmie, ma non tutte le aritmie sono fibrillazioni.
Leggi anche:
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Flutter atriale: cause, terapie, cosa fare, cura, ablazione e sintomi
- Differenza tra fibrillazione atriale e flutter
- Differenza tra fibrillazione atriale ed extrasistole
- Differenza tra fibrillazione atriale ed aritmia
- Differenza tra fibrillazione atriale e fibrillazione ventricolare
- Sapresti riconoscere un infarto del miocardio? Impara ad identificarlo e salverai una vita (anche la tua)
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Differenza tra cardioversione spontanea, elettrica e farmacologica
- Il defibrillatore non funziona: muore a 51 anni per un infarto
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Il massaggio cardiaco si esegue in assenza di…
- Sindrome di Wolff-Parkinson-White: cos’è, cosa fare, come si cura
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Differenza tra pacemaker e defibrillatore ICD
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Differenza tra sintomo e segno con esempi
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
 Con “extrasistole” in medicina si intende un battito cardiaco prematuro, che avviene prima del previsto andando così ad alterare la fisiologica successione regolare dei battiti cardiaci tipici del “ritmo sinusale” (cioè il ritmo cardiaco normale). L’impulso cardiaco normale nasce dal nodo seno-atriale (il pacemaker naturale del cuore), invece, nelle extrasistoli, l’impulso origina da sedi diverse dette sedi ectopiche e tale diversa origine dà avvio al battito prematuro. Tali contrazioni anomale, o extrasistoli, sono separate dalla successiva contrazione regolare da una pausa più lunga del normale.In mancanza di una conferma elettrocardiografica che permetta una diagnosi differenziale, un episodio di extrasistolia prolungata può essere scambiato per fibrillazione atriale (in questo caso il ritmo cessa di essere sinusale), anche se generalmente la seconda tende a durare più a lungo.
Con “extrasistole” in medicina si intende un battito cardiaco prematuro, che avviene prima del previsto andando così ad alterare la fisiologica successione regolare dei battiti cardiaci tipici del “ritmo sinusale” (cioè il ritmo cardiaco normale). L’impulso cardiaco normale nasce dal nodo seno-atriale (il pacemaker naturale del cuore), invece, nelle extrasistoli, l’impulso origina da sedi diverse dette sedi ectopiche e tale diversa origine dà avvio al battito prematuro. Tali contrazioni anomale, o extrasistoli, sono separate dalla successiva contrazione regolare da una pausa più lunga del normale.In mancanza di una conferma elettrocardiografica che permetta una diagnosi differenziale, un episodio di extrasistolia prolungata può essere scambiato per fibrillazione atriale (in questo caso il ritmo cessa di essere sinusale), anche se generalmente la seconda tende a durare più a lungo.
Raramente le extrasistoli possono dare l’innesco ad aritmie sostenute: un’extrasistole atriale può dare inizio a una tachicardia parossistica sopraventricolare, a un flutter, a una fibrillazione atriale o a una tachicardia giunzionale; un’extrasistole ventricolare può scatenare una tachicardia da rientro AV o una tachicardia ventricolare. In rari casi, cioè quando sono presenti in numero estremamente elevato (molte migliaia al giorno), le extrasistoli potrebbero determinare lo sviluppo di una cardiomiopatia dilatativa. In tali casi, la riduzione o l’eliminazione delle extrasistole (ad esempio tramite ablazione radioelettrica) determina solitamente la progressiva regressione della cardiomiopatia, nelle fasi iniziali della patologia.
Leggi anche:
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
Tipi di extrasistole
Le extrasistoli possono essere:
- isolate: quando l’extrasistole compare in maniera sporadica, con un singolo battito prematuro inserito in un ritmo normale;
- non isolate: l’extrasistole compare più volte.
Esempi di extrasistoli non isolate, sono:
- extrasistoli bigemine: compaiono dopo ogni battito sinusale;
- extrasistoli trigemine: compaiono ogni due battiti sinusali.
Le extrasistoli possono presentarsi anche sotto forma di “scariche”:
- coppia di extrasistoli;
- tripletta di extrasistoli;
- più extrasistoli (extrasistoli “a salve”).
In genere, a una extrasistole fa seguito una pausa che può essere:
- compensatoria: se la somma del periodo dell’extrasistole più la pausa è uguale a due cicli sinusali);
- non compensatoria: se la somma del periodo dell’extrasistole più la pausa è minore a due cicli sinusali.
Le extrasistoli che originano dall’atrio hanno di solito una pausa non compensatoria, quelle ad origine ventricolare hanno invece una pausa compensatoria. L’extrasistole viene detta “extrasistole interpolata” se non vi è pausa, se cioè l’extrasistole si inserisce semplicemente fra due battiti sinusali successivi.
In base alla sede di origine, le extrasistoli vengono comunemente distinte in extrasistoli atriali, giunzionali e ventricolari.
- Extrasistoli atriali: all’ECG questi impulsi anomali appaiono come onde P premature, con morfologia differente rispetto alle onde P sinusali. Gli impulsi possono arrivare ai ventricoli attraverso le normali vie di conduzione (in tal caso alla P anomala segue un regolare complesso QRS), oppure possono bloccarsi nel nodo AV che si trova ancora in periodo refrattario (extrasistole atriale non condotta). Oppure possono giungere ai ventricoli in un momento in cui il nodo AV è uscito dal periodo refrattario, ma una delle due branche si trova ancora in fase refrattaria; in tal caso lo stimolo raggiungerà i ventricoli attraverso l’altra branca, per cui si verifica un complesso ventricolare con morfologia tipo blocco di branca. Questo tipo di conduzione viene definito “aberranza”, per cui si parla di extrasistole atriale condotta con aberranza.
- Extrasistoli giunzionali: l’impulso origina nel fascio di His e va ai ventricoli dando luogo a un complesso QRS di morfologia regolare. Può verificarsi la retroattivazione degli atri, o lo stimolo può estinguersi, “scontrandosi” con quello sinusale nel nodo seno-atriale.
- Extrasistoli ventricolari: in questo tipo di contrazioni premature (sovente abbreviate in CVP o Contrazione Ventricolare Prematura) l’impulso origina nei ventricoli, a valle della biforcazione del fascio di His. All’ECG si rilevano complessi QRS larghi, non preceduti dall’onda P e pertanto chiaramente distinguibili da quelli sinusali. Anche in questo caso può verificarsi o non verificarsi la retroattivazione degli atri.
Leggi anche:
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
In quali condizioni si verifica?
Questo disturbo del ritmo cardiaco può osservarsi sporadicamente in soggetti sani di qualsiasi età, anche nei bambini. In soggetti sani, la maggior probabilità di singoli eventi autoconclusivi di extrasistole compaiono in caso di:
- ansia;
- stress;
- astenia (stanchezza);
- sforzi fisici intensi;
- mancanza prolungata di sonno;
- consumo di elevate quantità di sigarette;
- uso di stupefacenti;
- abuso di caffè e tè.
In soggetti assolutamente sani le extrasistoli possono comparire frequentemente dopo un pasto abbondante (extrasistole post-prandiale), e possono essere legate a distensione del fondo gastrico o alla presenza di un’ernia iatale.
Extrasistoli in gravidanza: c’è pericolo per il feto?
Anche donne che non hanno mai avuto episodi di extrasistole, possono “subirne” uno o più di uno durante la gravidanza: ciò è un fatto piuttosto comune dal momento che la gravidanza apporta una serie di cambiamenti fisiologici importanti, e tali cambiamenti potrebbero influenzare anche il lavoro cardiovascolare, e provocare appunto la classica extrasistole. Inoltre l’ansia e stress, assolutamente “normali” durante la gravidanza, possono aumentare la possibilità di aritmie. Le future mamme devono stare tranquille, perché episodi sporadici di extrasistole non sono pericolosi per il feto. Diverso è il discorso nel caso le aritmie durino a lungo e si ripresentino più volte nell’arco della giornata: in quel caso è conveniente avvertire il proprio ginecologo e consultare un cardiologo per una visita più approfondita che escluda patologie.
In quali patologie si verifica?
Quello che abbiamo appena chiarito non deve però farci sottovalutare la presenza di extrasistoli, specie se compaiono più volte e durano a lungo: anche se raramente, le extrasistoli possono infatti essere campanello di allarme di varie patologie:
- malattie cardiache,
- disturbi elettroliticoi(ad es. carenza di potassio),
- alterazioni ormonali,
- malattie della tiroide (ipotiroidismo),
- intossicazione da digitale,
- patologie della colecisti.
Leggi anche:
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Differenza tra cardioversione spontanea, elettrica e farmacologica
Quando preoccuparsi?
Come già anticipato, una extrasistole sporadica non ci deve far troppo preoccupare. Diverso è il discorso nel caso di episodi di extrasistolie prolungate e spesso recidivanti: in questo caso la condizione abbisogna di ulteriori chiarimenti, specie se associata ad altri sintomi come ad esempio:
- dolore al petto,
- costrizione toracica,
- improvvisa mancanza di forza,
- perdita di coscienza.
La condizione potrebbe essere tanto più pericolosa quanto siano presenti:
- altre condizioni o patologie di interesse cardiologico;
- casi in famiglia di malattie cardiache (aritmie, infarto del miocardio…);
- sovrappeso od obesità;
- episodi frequenti e prolungati di extrasistolia, soprattutto se compaiono senza nessuna apparente causa (ad esempio senza sforzi, senza ansia, senza consumo eccessivo di caffè).
Sintomi di extrasistole
L’extrasistole può non provocare alcun sintomo nel paziente che si sente bene e può non accorgersi mai delle contrazioni anomale del suo ritmo cardiaco, specie se è solo una ed il soggetto in quel momento è distratto da qualche attività. Più spesso invece determina una sensazione spiacevole, descritta come un “battito più forte di altri” alla regione precordiale, un “tuffo al cuore”, una sensazione di apparente arresto/ripresa del battito che crea una profonda ansia – specie se si avverte per la prima volta – ed una generale sensazione di instabilità corporea in questi casi, infatti, il paziente – specie l’anziano – tende a cercare un appoggio.
Leggi anche: Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
Diagnosi di extrasistole
L’esame del polso permette di apprezzare, intercalate alle pulsazioni normali, pulsazioni di scarsa ampiezza, anticipate, seguite da una pausa più o meno lunga e quindi da una pulsazione più energica. Per lo studio delle extrasistoli è tuttavia indispensabile l’esame elettrocardiografico, che consente di stabilirne con esattezza la sede d’origine, la posizione nel ciclo cardiaco, il modo di raggrupparsi, se cioè sono isolate “a salve” o se si inseriscono regolarmente nel ciclo cardiaco, dando luogo ad un ritmo bigemino o trigemino. Grazie al tracciato dell’elettrocardiogramma si può quindi capire cause ed impostare conseguenti terapie delle extrasistoli.
Alterazioni elettrocardiografiche nell’extrasistolia
L’ECG permette di rilevare un complesso QRS prematuro. In base alle sue caratteristiche, si può distinguere l’origine dell’extrasistole.
- Se il QRS prematuro è preceduto da un’onda P, l’extrasistole è sicuramente atriale. Se non è preceduto da onda P, si può determinare l’origine dell’extrasistole dalla larghezza del QRS.
- Se il complesso QRS è stretto, l’extrasistole è atriale. Se è largo, ma ugualmente preceduto da un’onda P anomala, l’extrasistole è atriale ma verosimilmente ha trovato una delle branche del fascio di His ancora in periodo refrattario ed è stata condotta ai ventricoli con aberranza (“blocco di branca funzionale”).
- Se vi sono più complessi QRS prematuri, e tutti presentano la stessa morfologia e lo stesso ritardo, si parla di extrasistoli monomorfe, hanno un solo focus d’origine ectopica e possono manifestarsi in soggetti sani o possono essere sintomo di una cardiopatia sottostante; al contrario, se i complessi QRS hanno morfologia differente, si parla di extrasistoli polimorfe, possiedono diversi centri ectopici ed hanno quasi sempre genesi organica, molte volte indicano la presenza di un danno miocardico.
- Se si riscontrano extrasistoli isolate, monomorfe, in un paziente con un’obiettività cardiovascolare normale, le extrasistoli non hanno alcun significato e il paziente non ha bisogno di ulteriori indagini.
Terapia delle extrasistoli
Le extrasistoli sporadiche in soggetti sani, sono solitamente autoconclusive e non necessitano di alcuna cura. Le extrasistoli tendono a scomparire in seguito a generiche cure sedative contro l’ansia, associate a misure igieniche e dietetiche, maggior riposo, pasti regolari e leggeri e un adeguato movimento fisico. La terapia nei casi più gravi, recidivanti ed invalidanti fa uso di farmaci quali la chinidina, la procainamide, l’ajmalina.
Leggi anche:
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Il massaggio cardiaco si esegue in assenza di…
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Differenza tra pacemaker e defibrillatore ICD
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra sintomo e segno con esempi
- Pressione arteriosa: valori normali e patologici
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Wolff-Parkinson-White: nei bambini, rischi, sport, morte improvvisa
 La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti.
La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti.
Leggi anche: Come si muove l’impulso elettrico cardiaco nel cuore?
Sport e Wolff-Parkinson-White
Con la Sindrome di Wolff-Parkinson-White sia il bambino che l’adulto possono praticare sport, come ad esempio calcio e nuoto, ma è importante che si eseguano sempre i controlli medici. Importante valutazione si ha, oltre all’elettrocardiogramma standard e all’elettrocardiogramma sotto sforzo, anche attraverso il SETE, cioè lo studio elettrofisiologico trans-esofageo, che trova una vantaggiosa applicazione in cardiologia dello sport
I rischi del Wolff-Parkinson-White
I soggetti con WPW, rispetto alla popolazione sana, hanno un maggior rischio di fibrillazione atriale, di aritmie ventricolari rapide e di arresto cardiaco, oltre ad una probabilità più elevata di morte cardiaca improvvisa.
Wolff-Parkinson-White e morte improvvisa
La sindrome di Wolff-Parkinson-White espone il soggetto ad un rischio maggiore di morte cardiaca improvvisa, rispetto alla popolazione sana. Se la presenza di sintomi nei pazienti con preeccitazioni ventricolari è un elemento predittivo di eventi avversi e impone quindi una terapia adeguata, come quella ablativa, non significa che l’assenza di sintomi identifichi necessariamente soggetti scevri da eventi avversi. In altre parole i soggetti sintomatici hanno un rischio più elevato di morte cardiaca improvvisa rispetto a quelli asintomatici, ma questi ultimi hanno comunque un rischio maggiore rispetto alla popolazione sana: secondo uno studio del prof. Carlo Pappone presso il Maria Cecilia Hospital di Cotignola e pubblicato su Circulation, anche i pazienti asintomatici sono infatti a rischio di sviluppare aritmie maligne.
Leggi anche:
- Sindrome di Wolff-Parkinson-White: cos’è, cosa fare, come si cura
- Wolff-Parkinson-White: elettrocardiogramma (ECG) ed alterazioni
- Differenza tra cardioversione spontanea, elettrica e farmacologica
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Differenza tra sintomo e segno con esempi
- Pressione arteriosa: valori normali e patologici
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Sindrome di Wolff-Parkinson-White: cos’è, cosa fare, come si cura
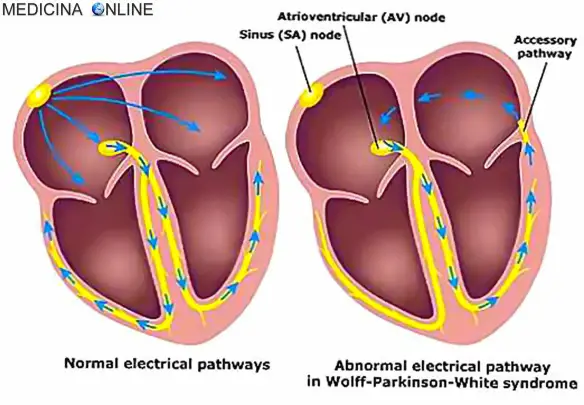 La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti. I pazienti con sindrome di WPW spesso hanno più di una via accessoria, ed in alcuni possono essere anche più di otto; questo è stato dimostrato in soggetti affetti dall’anomalia di Ebstein. La sindrome di WPW è talora associata alla neuropatia ottica ereditaria di Leber (LHON),una forma di malattia mitocondriale.
La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti. I pazienti con sindrome di WPW spesso hanno più di una via accessoria, ed in alcuni possono essere anche più di otto; questo è stato dimostrato in soggetti affetti dall’anomalia di Ebstein. La sindrome di WPW è talora associata alla neuropatia ottica ereditaria di Leber (LHON),una forma di malattia mitocondriale.
Fisiopatologia
In condizioni normali la conduzione dell’impulso elettrico dagli atrii ai ventricoli del cuore percorre una via costituita dal nodo atrio-ventricolare e fascio di His. Il nodo atrio-ventricolare ha caratteristiche elettrofisiologiche di velocità di conduzione e tempo di refrattarietà tali da costituire un filtro in grado di proteggere i ventricoli dalla conduzione di impulsi atriali troppo rapidi e potenzialmente pericolosi. In alcuni casi esistono vie di conduzione dette accessorie (VA) tra atrii e ventricoli che possono essere localizzate in vari siti degli anelli valvolari tricuspidalico e mitralico. Per le loro caratteristiche elettrofisiologiche, simili alle cellule del muscolo cardiaco comune, queste vie accessorie non svolgono la funzione di filtro tipica del nodo atrioventricolare, e in certi casi possono condurre gli impulsi ai ventricoli a frequenze molto elevate. Durante il ritmo sinusale una via accessoria si manifesta all’elettrocardiogramma con la pre-eccitazione ventricolare e la presenza di un’onda “delta”: la conduzione attraverso la via accessoria non subisce un rallentamento come all’interno del nodo atrioventricolare e l’intervallo PQ dell’elettrocardiogramma (che rappresenta appunto il percorso dell’impulso elettrico dagli atrii ai ventricoli) è più breve del normale (pre-eccitazione). Inoltre l’estremità ventricolare della via accessoria si inserisce nel muscolo cardiaco comune anziché essere in continuità con il sistema specializzato di conduzione: per questo motivo la depolarizzazione di una parte dei ventricoli avviene più lentamente, e si traduce in un aspetto elettrocardiografico detto onda “delta”. Se la presenza di una via accessoria si associa a episodi di palpitazione si parla di Sindrome di Wolff-Parkinson-White. Le palpitazioni possono dipendere da “aritmie da rientro“, ossia determinate da un corto circuito in cui l’impulso generalmente raggiunge i ventricoli attraverso il nodo atrioventricolare e rientra negli atrii attraverso la via accessoria percorsa in senso inverso. L’aritmia si perpetua fino a quando una delle due vie (nodo o via accessoria) non è più in grado di condurre. In alcuni casi meno frequenti il circuito è percorso all’inverso, ossia la via accessoria è utilizzata nel senso dagli atrii ai ventricoli, mentre l’impulso rientra agli atrii attraverso il fascio di His e il nodo atrioventricolare. In altri casi la via accessoria non partecipa direttamente al meccanismo che perpetua l’aritmia, ma può contribuire alla conduzione ai ventricoli di aritmie degli atrii (fibrillazione atriale/flutter atriale/tachicardia atriale). Se le capacità di conduzione della VA sono molto elevate (breve tempo di refrattarietà) la frequenza ventricolare risultante può essere molto rapida (> 250 battiti al minuto) e mettere a rischio di aritmie ventricolari rapide e di arresto cardiaco.
Sintomi di Wolff-Parkinson-White
Clinicamente tale sindrome si può manifestare con fibrillazione atriale e palpitazioni secondarie alle sopra citate aritmie da rientro. Non è raro che sia totalmente asintomatica e che venga scoperta durante un elettrocardiogramma eseguito per altri motivi, ad esempio in una visita di medicina sportiva.
Diagnosi di Wolff-Parkinson-White
La diagnosi di sindrome di WPW è clinica ma soprattutto si avvale dell’elettrocadiogramma, che può scovarla anche in un soggetto asintomatico: in questi casi si manifesta come un’onda delta, che corrisponde all’ampliamento della fase di ascesa del complesso QRS associato all’accorciamento dell’intervallo PR. Tutto questo è dovuto al fluire dell’impulso elettrico attraverso la via accessoria piuttosto che attraverso il nodo atrio-ventricolare.
Se il paziente accusa episodi di fibrillazione atriale, l’ECG mostra una tachicardia rapida polimorfica (senza torsione di punta). Questa combinazione di fibrillazione atriale e sindrome di WPW è considerata pericolosa, e molti farmaci antiaritmici sono controindicati.
Quando un soggetto è in normale ritmo sinusale le caratteristiche della sindrome di WPW sono un intervallo PR corto, uno slargamento del complesso QRS (più di 120msec in lunghezza) con ampliamento della fase di ascesa del QRS stesso, e cambiamenti della ripolarizzazione che si riflettono in alterazioni del tratto ST e dell’onda T.
In soggetti affetti l’attività elettrica che inizia nel nodo seno-atriale passa attraverso il fascio accessorio tanto bene quanto nel nodo atrio-ventricolare. Poiché il fascio accessorio non blocca l’impulso quanto il nodo, i ventricoli vengono attivati da questo, e subito dopo dal nodo. Questo causa le alterazioni ECG sopra descritte.
Altra tecnica di diagnosi è lo studio elettrofisiologico: per questo esame, il medico inserisce un catetere sottile e flessibile, dotato di elettrodi all’estremità, attraverso i vasi sanguigni fino a raggiungere diverse parti del cuore dove sono in grado di mappare gli impulsi elettrici.
Leggi anche:
- Pressione arteriosa: valori normali e patologici
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
Trattamenti di Wolff-Parkinson-White
Il trattamento degli episodi acuti di aritmie da rientro nella Sindrome di WPW si avvale di farmaci che agiscono bloccando la conduzione attraverso il nodo atrioventricolare, interrompendo uno dei bracci dell’aritmia. Questi farmaci sono invece da evitare in caso di fibrillazione atriale condotta rapidamente attraverso la via accessoria, poiché possono in certi casi aumentare la frequenza di conduzione ai ventricoli attraverso la via accessoria.
In presenza di pre-eccitazione ventricolare e indipendentemente dalla presenza di sintomi aritmici è raccomandato sottoporsi a studio elettrofisiologico per indagare le capacità conduttive della via accessoria e la inducibilità di aritmie. Se la via accessoria ha capacità conduttive elevate con un rischio di frequenze ventricolari elevate durante eventuali episodi di fibrillazione atriale, o in presenza sintomi e di aritmie da rientro, è indicato procedere alla ablazione della via accessoria.
Lo studio elettrofisiologico è in grado di identificare la sede della via accessoria, da cui dipenderà l’approccio utilizzato per l’ablazione: in presenza di una via situata nelle sezioni destre del cuore l’accesso è generalmente dalla vena femorale destra.
Per le vie sinistre saranno possibili un accesso venoso e successiva puntura transettale per passare dall’atrio destro all’atrio sinistro, oppure un approccio “retrogrado” attraverso le arterie femorale e aorta. L’energia utilizzata per l’ablazione è generalmente la radiofrequenza. Dopo un’ablazione efficace saranno prevenuti episodi di aritmia da rientro attraverso la via accessoria e all’elettrocardiogramma non sarà più visibile l’onda delta. L’efficacia a lungo termine dell’ablazione è in genere molto elevata e supera il 95%.
Dopo un’ablazione efficace e in assenza di altri tipi di aritmia o di cardiopatia, non è necessaria alcuna terapia farmacologica.
Leggi anche:
- Sapresti riconoscere un infarto del miocardio? Impara ad identificarlo e salverai una vita (anche la tua)
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Wolff-Parkinson-White: nei bambini, rischi, sport, morte improvvisa
- Wolff-Parkinson-White: elettrocardiogramma (ECG) ed alterazioni
- Differenza tra cardioversione spontanea, elettrica e farmacologica
- Il defibrillatore non funziona: muore a 51 anni per un infarto
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Il massaggio cardiaco si esegue in assenza di…
- Flutter atriale: cause, terapie, cosa fare, cura, ablazione e sintomi
- Differenza tra fibrillazione atriale e flutter
- Differenza tra fibrillazione atriale ed extrasistole
- Differenza tra fibrillazione atriale ed aritmia
- Differenza tra fibrillazione atriale e fibrillazione ventricolare
- Differenza tra tachicardia e fibrillazione atriale e ventricolare
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Differenza tra pacemaker e defibrillatore ICD
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Differenza tra sintomo e segno con esempi
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Semeiotica del cuore: i focolai di auscultazione cardiaca
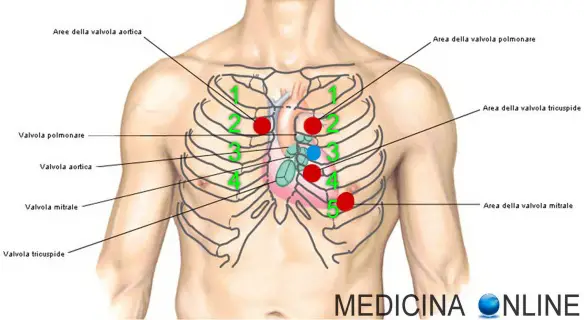
I numeri in verde corrispondono agli spazi intercostali. In azzurro il focolaio di Erb, nel 3° spazio intercostale sinistro
L’auscultazione del cuore, durante l’esame obiettivo, va effettuata sui focolai cardiaci, 5 zone specifiche che corrispondono ai focolai valvolari:
Focolaio aortico
E’ presente nel II spazio intercostale destro sulla linea margino-sternale o parasternale (è importante auscultare questo focolaio nel soggetto anziano perché la patologia aterosclerotica può colpire facilmente questo focolaio, dando origine ad un soffio, mentre in un paziente iperteso di vecchia data in questo focolaio possiamo sentire un tono scoccante, un primo tono accentuato)
Focolaio polmonare
Si trova sul II spazio intercostale sinistro sulla linea marginosternale o parasternale sinistra.
Focolaio tricuspidale
E’ presente sul IV spazio intercostale destro al margine dello sterno.
Focolaio mitralico
Si trova sul quarto-quinto spazio intercostale all’altezza della linea emiclaveare di sinistra (rappresenta l’itto della punta del cuore).
Focolaio di Erb
Rappresenta il focolaio elettivo dei soffi aortici, appartiene al mesocardio e si trova al centro del quadrilatero determinato dai restanti quattro punti di auscultazione. E’ posto a livello del terzo spazio intercostale sinistro sulla linea parasternale, immediatamente al di sotto del focolaio dell’arteria polmonare. Alcune fonti lo localizzano a livello del quarto spazio intercostale. E’ il punto in cui è possibile effettuare l’auscultazione della componente aortica del secondo tono cardiaco e di soffi cardiaci causati da alterazioni della valvola aortica.
Altri articoli che potrebbero interessarti:
Semeiotica del cuore:
- Esame obiettivo cardiovascolare: guida completa all’esecuzione
- Semeiotica del cuore: i 4 toni cardiaci ed i toni aggiunti
- Semeiotica del cuore: i soffi cardiaci sistolici e diastolici
- Semeiotica del cuore: l’esame obiettivo cardiaco completo
- Elettrocardiogramma: posizionamento degli elettrodi dell’ECG
- Manovra di Valsalva in medicina (tachicardia e nervo vago)
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Differenza tra sintomo e segno con esempi
- Esame obiettivo generale: come farlo, importanza ed esempi
- Esame obiettivo: come si fa l’ispezione ed a cosa serve?
- Esame obiettivo: cos’è la percussione e perché si fa?
- Palpazione nell’esame obiettivo: cos’è ed a che serve?
- Auscultazione nell’esame obiettivo: cos’è ed a che serve?
Leggi anche:
- Com’è fatto il cuore, a che serve e come funziona?
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Ecocolordoppler cardiaco (ecocardio): funzioni, preparazione, gravidanza
- Pressione arteriosa: valori normali e patologici
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
