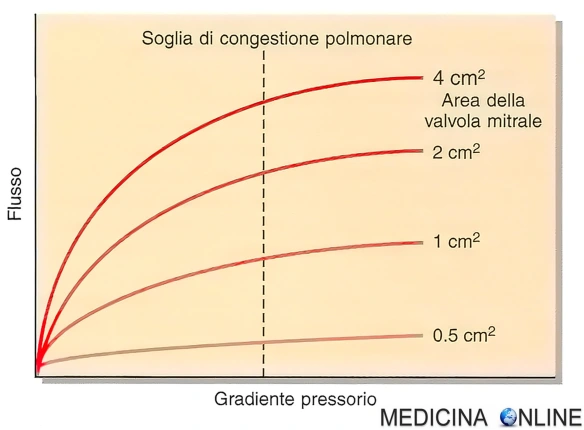
Grafico che illustra la relazione tra gradiente diastolico attraverso la valvola mitrale e il flusso transmitralico. Quando la stenosi della valvola mitrale peggiora, il gradiente pressorio transvalvolare deve aumentare per mantenere un flusso adeguato al ventricolo sinistro. Quando l’area della valvola mitrale non supera 1,0 cm2, il flusso al ventricolo sinistro non può aumentare in modo significativo, nonostante un aumento significativo del gradiente pressorio transvalvolare.
La stenosi mitralica (o “stenosi mitrale” o “stenosi della valvola mitrale” o “stenosi della valvola mitralica”, in inglese “mitral stenosis” da cui l’acronimo “MS“) è una patologia del cuore caratterizzata da un restringimento (stenosi) dell’orifizio mitralico causato da ispessimento e immobilità dei lembi mitralici. Tale restringimento impediscono il flusso di sangue dall’atrio sinistro al ventricolo sinistro. La causa più frequente è la febbre reumatica. Oltre il 60% dei pazienti con MS è composto da donne.
Cause e fattori di rischio
La febbre reumatica era di gran lunga la causa più comune di MS in era pre-antibiotica. Gli streptococchi di gruppo A possiedono antigeni di superficie strutturalmente simili ad alcune proteine presenti nella struttura valvolare; la reazione antigene – anticorpo che ne deriva causa la formazione di numerosi piccoli noduli fibrotici sui lembi valvolari, che con il tempo vanno incontro a calcificazione e retrazione. Il processo può estendersi alle corde tendinee, che rappresentano il supporto meccanico delle valvole, provocandone il loro irrigidimento fibrotico, con conseguente arresto del movimento dei lembi valvolari, i quali, una volta calcificati, danno alla valvola l’aspetto a “bocca di pesce“. Altre cause includono:
- anomalie congenite;
- patologie del tessuto connettivo;
- riparazioni eccessivamente aggressive di una valvola insufficiente (vasculoplastica chirurgica restrittiva).
Possono portare ad ostruzione della valvola mitrale anche:
- endocardite;
- LES (lupus eritematoso sistemico);
- artrite reumatoide;
- mixoma;
- sindrome da carcinoide;
- sarcoidosi;
- malattia di Fabry;
- malattia di Whipple;
- calcificazioni degenerative dell’anulus;
- uso di metisergide.
Le alterazioni patologiche che si verificano con la MS reumatica comprendono fusione delle commissure dei lembi e ispessimento, fibrosi e calcificazione dei lembi mitralici e delle corde tendinee. Queste alterazioni si verificano nell’arco di molti anni prima che la disfunzione divenga emodinamicamente rilevante.
Fisiopatologia
L’iniziale alterazione emodinamica che compare con la MS è costituita da un innalzamento della pressione atriale sinistra, creato da ostruzione all’afflusso ventricolare sinistro (vedi figura in alto in questo articolo).
Questa modificazione pressoria viene trasmessa in modo retrogrado al sistema venoso polmonare e può condurre a congestione polmonare. Inizialmente, questa alterazione può comparire soltanto con le frequenze cardiache più elevate, come con l’esercizio fisico o le aritmie atriali, quando si sviluppa una maggior pressione atriale sinistra durante il periodo diastolico abbreviato. Quando la MS diviene più
grave, la pressione atriale sinistra rimane elevata anche a frequenze cardiache normali, e i sintomi correlati ad innalzamento delle pressioni venose polmonari possono essere presenti anche a riposo. Innalzamenti cronici nelle pressioni venose polmonari possono condurre ad un aumento delle resistenze vascolari polmonari e delle pressioni nell’arteria polmonare. Se la MS non è corretta, possono verificarsi alterazioni irreversibili nella vascolarizzazione polmonare, e possono svilupparsi segni e sintomi di insufficienza cardiaca destra. Per contro, le pressioni di riempimento ventricolare sinistro sono in genere normali o ridotte con una MS da lieve a moderata. Con l’aggravamento della stenosi, il riempimento del ventricolo sinistro è compromesso e la gittata sistolica e la gittata cardiaca sono ridotte.
Sintomi e segni
La conseguenza della stenosi valvolare è un aumento di pressione nell’atrio sinistro: tale aumento si rende necessario per superare la resistenza opposta dalla valvola stenotica. L’aumento pressorio, con il progredire della patologia, si trasmette per via retrograda a tutto il sistema circolatorio del polmone e si associa a ridotta gittata cardiaca, determinando una serie di sintomi:
- mancanza di respiro per piccoli sforzi (dispnea da sforzo);
- facile affaticamento;
- ortopnea;
- dispnea parossistica notturna;
- emoftoe;
- tachicardia.
I pazienti con MS di origine reumatica in genere divengono sintomatici durante il terzo o il quarto decennio di vita. Dispnea, ortopnea e fibrillazione atriale sono i sintomi più comuni. Alcuni pazienti possono presentare improvvisa emottisi, conseguente a rottura di vene bronchiali dilatate (apoplessia polmonare), o escreato screziato di sangue associato a edema polmonare. Un’embolia polmonare per un
trombo dell’atrio sinistro può comparire anche in assenza di fibrillazione atriale. Nella MS grave di lunga durata, i pazienti possono sviluppare edema periferico conseguente all’innalzamento delle pressioni ventricolari destre e alla disfunzione ventricolare destra. La compressione del nervo laringeo ricorrente sinistro da parte di un atrio sinistro fortemente dilatato può portare a raucedine (sindrome di Ortner).
Diagnosi
La diagnosi si basa su anamnesi, esame obiettivo ed esami come l’ecografia cardiaca e l’elettrocardiogramma.
Esame obiettivo
All’esame obiettivo, S1 è sonoro nelle prime fasi della MS perché i lembi rimangono completamente aperti per tutta la diastole e quindi si chiudono rapidamente. Quando i lembi divengono più calcificati e immobili, S1 diviene meno sonoro o completamente assente. Lo schiocco di apertura è un suono di alta frequenza successivo a S2 e riflette l’improvvisa apertura della valvola mitrale. Quando la MS diviene più grave, l’intervallo fra S2 e lo schiocco di apertura diviene più breve perché la pressione atriale sinistra supera la pressione ventri colare in una fase più precoce della diastole. Il caratteristico soffio ronzante a bassa frequenza della MS è udito meglio all’apice ventricolare sinistro, con il paziente in posizione di decubito laterale sinistro. Il soffio è più sonoro nella protodiastole, quando si verifica il rapido riempimento ventricolare. Se il ritmo è sinusale, il soffio può aumentare di intensità dopo contrazione atriale (accentuazione presistolica). In alcuni pazienti il soffio può essere udito solamente in momenti di aumento del flusso ematico attraverso la valvola mitrale, come dopo esercizio fisico. Se le pressioni nell’arteria polmonare sono elevate, può essere rilevato un P2 palpabile al margine sternale superiore sinistro. All’auscultazione, la componente polmonare di S2 è prevalente, e può essere presente un galoppo ventricolare destro.
Ecografia cardiaca
L’ecocardiografia è lo strumento più utile per la valutazione patologica dell’apparato mitralico, nonché della gravità della stenosi. La caratteristica deformità reumatica osservata con l’immagine bidimensionale è l’aspetto a cupola (ovvero deformità a bastone di hockey) del lembo mitralico anteriore, che è conseguente alla fusione delle commissure e all’anco raggio degli apici del lembo (vedi immagine in basso).
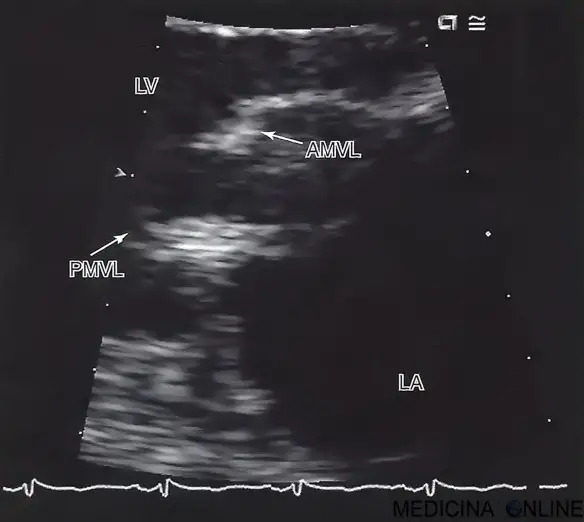
Esempio di deformità a bastone di hockey della valvola mitrale nella cardiopatia reumatica cronica come viene presentata all’ecocardiografia. Gli apici del lembo mitralico anteriore (Anterior Mitral Valve Leaflet, AMVL) risultano ancorati, restringendo così l’apertura valvolare. Il lembo mitralico posteriore (Posterior Mitral Valve Leaflet, PMVL) si presenta ispessito ed ha una mobilità ridotta. L’atrio sinistro (LA) è tipicamente dilatato.
L’ecocardiografia, inoltre, permette di valutare la mobilità dei lembi e l’estensione della calcificazione valvolare e utilizzarle per determinare le opzioni terapeutiche. Le tecniche Doppler consentono il calcolo dell’area della valvola mitrale e del gradiente transvalvolare. L’ecocardiografia transesofagea è uno strumento utile per studiare l’apparato mitralico ed esaminare l’atrio sinistro alla ricerca di trombi prima di una valvuloplastica percutanea.
Elettrocardiogramma
L’ECG, quando il paziente è in ritmo sinusale, evidenzia un’alterazione dell’onda P molto caratteristica, tanto da definirla P mitralica.
Radiografia del torace
L’RX del torace nel paziente con stenosi della mitrale, è una tecnica utile per osservare la situazione polmonare, in particolare per individuare eventuali edemi polmonari. La radiografia del torace permetta anche di vedere i volumi aumentati dei vasi a monte della stenosi valvolare, dovuti all’ipertrofia e al ristagno ematico.
Cateterismo cardiaco
La gravità della MS e delle alterazioni emodinamiche associate può anche essere valutata con il cateterismo cardiaco. Le misurazioni della gittata cardiaca e del gradiente transvalvolare possono essere utilizzate per calcolare l’area valvolare attraverso la formula di Gorlin. L’area di una valvola mitrale normale è di 4-6 cm-, e una stenosi critica è definita da un’area inferiore a l cm2.
Complicanze
Le complicanze più frequenti della stenosi della valvola mitralica, sono:
- ipertensione polmonare;
- fibrillazione atriale;
- embolia polmonare;
- tromboembolia;
- ictus cerebrale;
- edema polmonare.
L’edema polmonare, cioè un passaggio di liquido dai capillari all’interno degli alveoli polmonari, per improvviso aumento della pressione nei capillari stessi, con conseguente grave sintomatologia dispnoica, può intervenire nei casi più gravi e si può associare emoftoe, ovvero sputo ematico, quando si instaura ipertensione polmonare; causa importante di complicanze e morte sono le embolie polmonari ricorrenti in caso di insufficienza del ventricolo destro. Frequente è la comparsa di fibrillazione atriale, causata dalla valvulopatia e dall’ingrandimento dell’atrio sinistro con possibile comparsa di trombi sulle pareti dell’atrio sinistro o più propriamente all’interno dell’auricola sinistra. La fibrillazione causa sintomatologia soggettiva di cardiopalmo, mentre i trombi possono staccarsi come emboli e migrare soprattutto verso il cervello e provocare un ictus cerebrale o polmonare.
Trattamento
Il trattamento di una stenosi mitralica dipende molto dalla gravità della situazione. Generalmente stenosi lievi e moderate non hanno bisogno di trattamento chirurgico, cosa che invece può avvenire in caso di stenosi severe.
Terapia delle stenosi mitraliche lievi o moderate
I pazienti con MS da lieve a moderata possono in genere essere gestiti con terapia medica, evitando chirurgia percutanea o a cielo aperto. Il controllo della frequenza cardiaca è imperativo in questi pazienti, perché frequenze più rapide riducono la lunghezza del periodo di riempimento diastolico. Questo è particolarmente vero in pazienti con fibrillazione atriale, nei quali la perdita di contrazione atriale può ridurre ulteriormente il riempimento ventricolare sinistro. Per prevenire gli episodi di fibrillazione atriale possono essere utilizzati dei farmaci antiaritmici, ma quando l’aritmia è cronica si userà solo la digossina. La terapia anticoagulante è indicata per pazienti con fibrillazione atriale e per quelli con ritmo sinusale che sono andati in precedenza incontro ad eventi embolici, o che presentano una MS da moderata a grave. I diuretici sono utili nell’alleviare una congestione polmonare e i segni di insufficienza cardiaca destra. Tutti i pazienti devono essere istruiti sull’importanza della profilassi contro l’endocardite. La profilassi contro puntate recidivanti di febbre reumatica può essere usata nei pazienti di età inferiore ai 30 anni. Utili gli antibiotici, ma è importante una quotidiana igiene orale e dentale, per evitare la predisposizione alle infezioni batteriche.
Terapia della stenosi mitralica grave
Nei pazienti con sintomi gravi (classi III e IV della New York Heart Association) e MS da moderata a grave deve essere preso in considerazione un intervento percutaneo o chirurgico a cielo aperto. Sono possibili diversi approcci:
- commissurotomia,
- valvuloplastica,
- riparazione valvolare,
- sostituzione valvolare.
Commissurotomia
Un’opzione chirurgica è costituita dalla commissurotomia a cielo aperto della valvola mitrale. Tramite una toracotomia anteriore-laterale sinistra, si accede al torace attraverso lo spazio di resezione della V costa. Aperto il pericardio attraverso l’auricola sinistra, si introduce nell’ostio mitralico un divulsore che, aprendosi, forza i lembi valvolari in modo da separare le commissure fuse; il chirurgo è in grado inoltre di ripulire la valvola e asportare trombi nell’atrio sinistro. Benché la valvola rimanga anormale, questa procedura è associata a una bassa mortalità operatoria e a buoni risultati emodinamici, e può risparmiare per molti anni al paziente una sostituzione valvolare. Oggi tale approccio viene spesso sostituito dalla valvuloplastica a palloncino.
Valvuloplastica percutanea con palloncino
La valvuloplastica percutanea con palloncino è una tecnica simile all’angioplastica quindi meno invasiva della chirurgia open, in cui un catetere con palloncino posto attraverso la valvola mitrale viene rapidamente gonfiato, portando a separazione delle cuspidi fuse. Risultati ottimali a breve e lungo termine sono ottenuti nei pazienti con lembi e corde flessibili, non calcificati, minimo rigurgito mitralico e senza evidenza di trombi nell’atrio sinistro.
Riparazione valvolare
La riparazione della valvola mitralica dà risultati migliori nelle insufficienze mitraliche da prolasso e rottura di una corda tendinea (intervento per il quale rappresenta la prima scelta terapeutica). Non può essere attuata nella valvulopatia reumatica, dove la deformazione non è riparabile. L’intervento è eseguito in CEC (circolazione extra corporea). Può comprendere:
- accorciamento di corde tendinee allungate;
- sezione di parte di un lembo valvolare;
- trasposizione delle corde tendinee o sostituzione con corde sintetiche;
- uso di anelli contenitrici per ridurre o rimodellare l’annulus dilatato e deformato;
- anello di Carpentier.
Sostituzione valvolare
Se le tecniche fin qui elencate non rappresentano un’opzione valida, si può realizzare la sostituzione valvolare mitralica con una protesi biologica o meccanica. La sostituzione valvolare prevede una toracotomia antero-laterale sinistra con escissione sotto-periostale della V costa; il paziente viene posto in circolazione extracorporea (CEC). La valvola viene sostituita con una protesi di misura congrua all’annulus naturale.
Per approfondire:
- Valvole cardiache: cosa sono, quali sono ed a che servono?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
- Insufficienza mitralica lieve, moderata, severa e sport
- Insufficienza polmonare lieve, severa, acuta: sintomi e cura
- Stenosi e insufficienza tricuspidale: cause, sintomi, diagnosi e terapia
- Stenosi polmonare, insufficienza polmonare e patologia multivalvolare
- Cardiopatia reumatica, valvole cardiache protesiche e profilassi per l’endocardite
- Prolasso mitralico: gravità, sintomi, sport, ansia, intervento minivasivo
- Insufficienza aortica: lieve, sport, pressione differenziale, acuta
- Insufficienza tricuspidale: lieve, severa, sport, soffio, sintomi
- Stenosi aortica: lieve, severa, sintomi, intervento, nell’anziano
- Stenosi aortica congenita e valvola aortica bicuspide
- Stenosi congenita della valvola polmonare e anomalia di Ebstein
- Differenza tra prolasso e insufficienza mitralica
- Differenza tra insufficienza e stenosi valvolare
Leggi anche:
- Com’è fatto il cuore, a che serve e come funziona?
- Come si muove il sangue all’interno del cuore?
- Differenza tra circolazione sistemica, polmonare ed intracardiaca
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Sindrome del QT lungo: valorie, cause, cura, farmaci, sportivi
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Ecocolordoppler cardiaco (ecocardio): funzioni, preparazione, gravidanza
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Difetto del setto interventricolare: cause, sintomi, diagnosi, rischi, terapie, prognosi
- Difetti del setto interventricolare: cause, sintomi, diagnosi e terapie
- Sindrome di Eisenmenger: diffusione, cause, sintomi, segni, diagnosi, terapia, attività sportiva
- Tetralogia di Fallot: caratteristiche, diffusione, comorbilità, etimologia e cenni storici
- Difetti del setto interatriale: cause, sintomi, diagnosi, terapia, rischi, prognosi, mortalità
- Coartazione aortica: cause, sintomi, diagnosi, terapie complicanze e rischi
- Dotto arterioso pervio: cause, sintomi, diagnosi, terapie complicanze e rischi
- Tetralogia di Fallot: cause, sintomi, diagnosi, terapie complicanze e rischi
- Trasposizione completa e corretta delle grandi arterie, cuore univentricolare e intervento di Fontain
- Differenza tra difetto del setto interatriale, interventricolare e dotto arterioso pervio SCHEMA
- Ipertensione polmonare persistente nel neonato: trattamento, prognosi, mortalità
- Pervietà del dotto di Botallo: cause, sintomi, diagnosi, terapia, prognosi, rischi nell’adulto
- Forame ovale pervio: cause, sintomi, diagnosi, rischi, terapie, prognosi
- Mediastino: anatomia, suddivisione, inferiore, anteriore, superiore
- Sindrome mediastinica: cause, sintomi e cura delle malattie del mediastino
- Tumori del mediastino: timomi e neurinomi, sintomi e cure
- Mediastinite acuta, cronica e fulminante: diagnosi, sintomi e cura
- Massa mediastinica: sintomi, cause, localizzazione, terapie
- Cardiomiopatia dilatativa: cause, sintomi, diagnosi e terapia
- Cardiomiopatia ipertrofica: cause, sintomi, diagnosi, terapia e prognosi
- Cardiomiopatia restrittiva: classificazione, cause, sintomi, diagnosi e terapia
- Cardiomiopatia alcolica e cardiomiopatia ventricolare destra aritmogena
- Miocardite: cause, sintomi, diagnosi e terapia
- Miocardite: terapia, conseguenze, recupero, morte
- Pericardite acuta: cause, sintomi, diagnosi e terapia
- Pericardite fulminante e cronica: ECG, cura, contagio
- Pericardite costrittiva e pericardite essudativa costrittiva
- Versamento pericardico: cause, sintomi, diagnosi e terapia
- Versamento pericardico lieve moderato severo: cura e riassorbimento
- Tamponamento cardiaco: cause, sintomi, diagnosi e terapia
- Tamponamento cardiaco: sintomi, ECG, polso paradosso, linee guida
- Cardiomegalia: sintomi, congenita, cura, diagnosi con RX
- Traumi del torace: epidemiologia, cause e cenni di medicina legale
- Fisiopatologia dei traumi toracici: lesioni della parete toracica, polmonari e delle vie aeree
- Fisiopatologia dei traumi toracici: lesioni del cuore, dei grossi vasi e del diaframma
- Traumi del torace: aspetti clinici, terapia, assistenza alle vie aeree e ventilatoria
- Morte cardiaca improvvisa: cause, sintomi premonitori e cure
- Rottura di cuore: cos’è, sintomi, terapia
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Anatomia macroscopica del cuore, sistema circolatorio e circolazione coronarica
- Sistema di conduzione dell’impulso elettrico nel cuore e innervazione del miocardio
- Miocardio, miofibrilla, sarcomero e contrazione muscolare calcio-dipendente
- Fisiologia della circolazione: ciclo cardiaco e performance cardiaca
- Fisiologia della circolazione coronarica, sistemica e polmonare
- Risposta cardiovascolare allo sforzo ed all’esercizio fisico
- Di cosa è composto il sangue e quali sono le sue funzioni?
- Saturazione dell’ossigeno: valori normali e patologici in anziani e bambini
- Circolazione coronarica, arterie e vene coronarie: anatomia e funzioni
- Riduzione della riserva coronarica: cos’è e come si studia
- Gruppi sanguigni: cosa sono e quali sono compatibili tra loro
- Cardiopatia ischemica: cronica, definizione, sintomi, conseguenze
- Infarto cardiaco: sintomi premonitori, cause, cosa fare, enzimi, cure
- Sindrome coronarica acuta: sintomi, terapia, classificazione, cura
- Insufficienza cardiaca (scompenso cardiaco): cause, sintomi iniziali, tipi, cure
- Insufficienza cardiaca: sintomi iniziali, sinistra, acuta, cronica
- Angina pectoris stabile, instabile, secondaria: sintomi, interpretazione e terapia
- Palpitazioni (cardiopalmo) a riposo, da ansia, notturne, dopo mangiato
- Differenza tra ipossiemia e ipercapnia
- Differenza tra ipossiemia, ipossia, anossiemia ed anossia
- Ipossia: valori, conseguenze, sintomi, cure
- Ipossiemia: significato, valori, sintomi, conseguenze, rischi, cure
- Ipercapnia: valori, terapia, conseguenze e trattamento
- Anossia: definizione, cause, sintomi, sinonimo, cure
- Ipocapnia: significato, cause, valori, alcalosi respiratoria
- Ossigenoterapia: uso, controindicazioni, domiciliare, con maschera
- Ipertensione polmonare: lieve, severa, terapia, aspettativa di vita
- Shunt in medicina: cardiaco, cerebrale, polmonare ed altre tipologie
- Pentalogia di Cantrell: il cuore batte fuori dal corpo [VIDEO]
- Sindrome di Wolff-Parkinson-White: cos’è, cosa fare, come si cura
- Bimba nata con organi fuori dal corpo, glieli avvolgono con una pellicola
- Il miracolo della bambina nata con mezzo cuore
- Anastomosi vascolare arteriosa e venosa: tipi e differenze
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Endocardite batterica: profilassi in bambini ed adulti
- Plasma e cellule (elementi corpuscolati) che compongono il sangue
- Plasma e suoi derivati (plasmaderivati)
- Differenza tra sangue, plasma e siero
- Come si ottiene il plasma?
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Enzimi cardiaci: alti, bassi, tempi, risultati, ogni quante ore
- Coronarografia: preparazione, stent, angioplastica, è pericolosa
- Angioplastica coronarica: convalescenza, dieta, stent, dolori, durata
- Holter cardiaco (ECG dinamico) 24 ore: lettura risultati, valori, costo
- Radiografia del torace: come si fa, indicazioni, bisogna spogliarsi, costo
- Farmaci trombolitici (fibrinolitici): nomi commerciali e indicazioni
- Antiaggreganti piastrinici: nomi commerciali, effetti collaterali
- Farmaci anticoagulanti : elenco ed effetti collaterali
- Cardiopatia ischemica: cronica, definizione, sintomi, conseguenze
- Infarto, ischemia, necrosi, aterosclerosi, trombo, embolo, ictus, miocardio… Facciamo chiarezza
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
