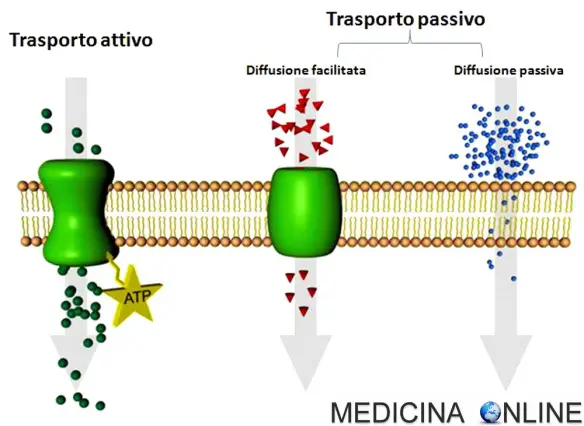
Quando una sostanza riesce ad attraversare la membrana plasmatica cellulare solo impiegando una certa quota di energia (sotto forma di ATP) si parla di trasporto attivo; quando invece la sostanza può attraversare la membrana Continua a leggere


Quando una sostanza riesce ad attraversare la membrana plasmatica cellulare solo impiegando una certa quota di energia (sotto forma di ATP) si parla di trasporto attivo; quando invece la sostanza può attraversare la membrana Continua a leggere
 Tra l’interno e l’esterno di ogni cellula c’è un continuo traffico di sostanze di varia grandezza e natura chimica. Il loro passaggio è regolato dalla membrana plasmatica (o cellulare) e può essere di due tipi principali: Continua a leggere
Tra l’interno e l’esterno di ogni cellula c’è un continuo traffico di sostanze di varia grandezza e natura chimica. Il loro passaggio è regolato dalla membrana plasmatica (o cellulare) e può essere di due tipi principali: Continua a leggere
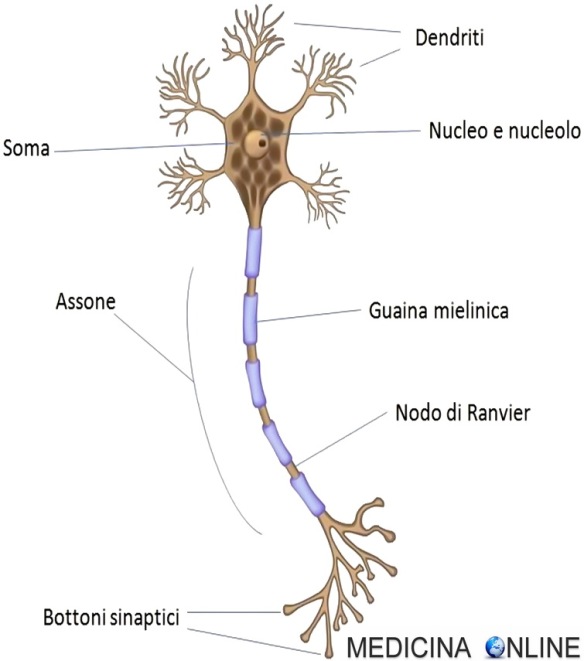 Il termine “neurone” identifica un tipo particolare di cellula che costituisce il tessuto nervoso, il quale concorre alla formazione del sistema nervoso, insieme con le cellule gliali. Il nostro cervello contiene circa 100 miliardi di neuroni, variabili per forma e posizione ma accomunati da alcune caratteristiche. Grazie alle loro peculiari proprietà fisiologiche e chimiche, i neuroni sono in grado di ricevere e trasmettere impulsi nervosi attraverso le sinapsi. La parte centrale del neurone è chiamata soma, ed è costituita Continua a leggere
Il termine “neurone” identifica un tipo particolare di cellula che costituisce il tessuto nervoso, il quale concorre alla formazione del sistema nervoso, insieme con le cellule gliali. Il nostro cervello contiene circa 100 miliardi di neuroni, variabili per forma e posizione ma accomunati da alcune caratteristiche. Grazie alle loro peculiari proprietà fisiologiche e chimiche, i neuroni sono in grado di ricevere e trasmettere impulsi nervosi attraverso le sinapsi. La parte centrale del neurone è chiamata soma, ed è costituita Continua a leggere
 Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
I recettori possono essere suddivisi in due grandi categorie, a seconda della loro localizzazione cellulare:
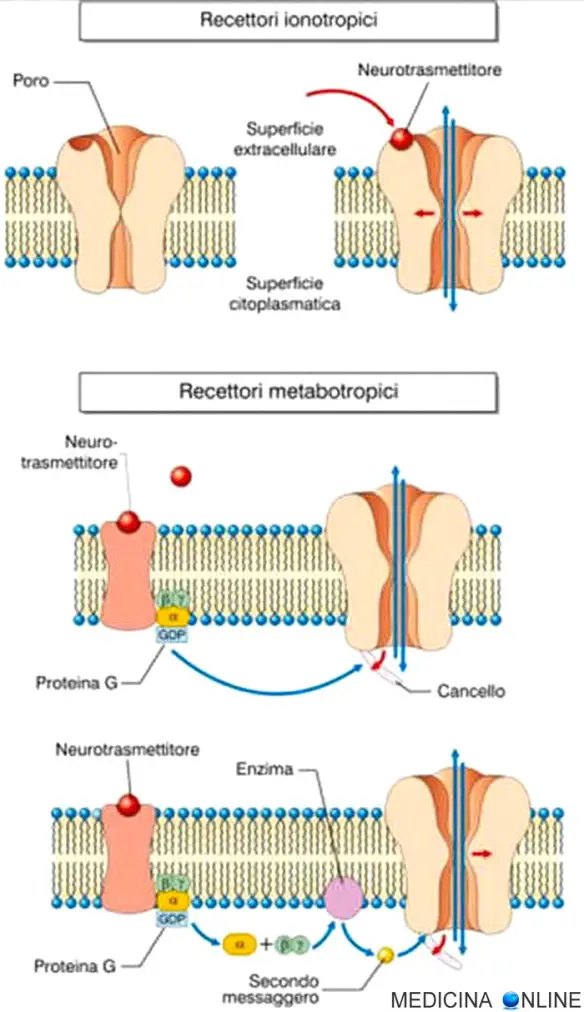
I recettori transmembrana sono suddivisibili in due differenti classi: ionotropi e metabotropici. I recettori ionotropi, definiti anche recettori-canale, sono recettori la cui apertura causa il flusso di ioni. Esistono sei tipi principali di recettori ionotropi:
I recettori metabotropici sono una classe di recettori che, in seguito all’interazione con lo specifico ligando, inducono una cascata di reazioni cellulari. Sono riconducibili a quattro tipologie recettoriali principali:
Da quanto detto appare chiaro che i recettori ionotropici ed i recettori metabotropici hanno punti in comune ma anche differenze. Entrambi sono localizzati a livello della membrana citoplasmatica (e non nel nucleo o nel citosol) e sono perciò entrambi recettori transmembrana.
Nei recettori ionotropici il legame con il ligando causa l’apertura del canale racchiuso dal recettore stesso, invece il recettore metabotropico, al contrario del recettore ionotropico, una volta legato il ligando, avvia una serie di reazioni a cascata intracellulari mediata da un secondo messaggero ed alla base della trasduzione del segnale. Inoltre mentre il recettore ionotropo è un canale ionico, invece il recettore metabotropico non è un canale.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
I recettori possono essere suddivisi in due grandi categorie, a seconda della loro localizzazione cellulare:
I recettori intracellulari possono essere a loro volta distinti in recettori citosolici o nucleari, in base alla loro localizzazione rispettivamente nel citosol o nel nucleo della cellula.
I recettori intracellulari citosolici sono il recettore dei glucocorticoidi ed il recettore dei mineralcorticoidi.
I recettori intracellulari nucleari sono: il recettore degli ormoni steroidei, il recettore della vitamina D, il recettore degli ormoni tiroidei ed il recettore dell’acido retinoico.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
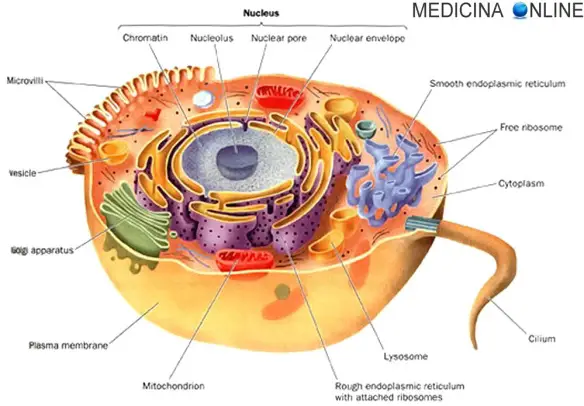 Cosa sono i recettori?
Cosa sono i recettori?
In biologia ed in medicina i recettori sono delle proteine localizzate sulla superficie o all’interno delle cellule che sono in grado di riconoscere e legare in maniera selettiva una particolare sostanza – definita ligando – di varia natura (per esempio un ormone, un antigene, uno zucchero) ma anche un microrganismo (un virus o un batterio).
Cosa avviene quando il recettore si lega al suo ligando?
Il legame di una sostanza al proprio recettore provoca una cascata di reazioni che culminano in una precisa risposta della cellula alla sostanza legata, che agisce da segnale. Un esempio classico è il legame di un ormone come l’insulina ai propri recettori situati nel fegato: tale legame indica all’organismo che è necessario immagazzinare all’interno delle cellule il glucosio ingerito con un pasto e circolante nel sangue. La risposta delle cellule epatiche a questo segnale è l’assunzione al loro interno del glucosio circolante, con un conseguente ristabilirsi dei valori normali di glicemia.
Il ruolo dei recettori in oncologia
Nel caso dei tumori, i recettori possono avere un ruolo determinante. Spesso, infatti, la trasformazione neoplastica induce la cellula a produrre recettori modificati, che mandano segnali del tutto sregolati: può accadere per esempio che un recettore che normalmente risponde agli stimoli di crescita esterni venga mutato e sia quindi sempre attivo, inviando alla cellula stimoli proliferativi continui. Mutazioni in alcuni tipi di recettori possono quindi essere alla base dello sviluppo dei tumori. Conoscere queste mutazioni può essere utile per sintetizzare farmaci mirati che, una volta legati ai recettori modificati, siano in grado di bloccarne l’attività che favorisce la crescita tumorale.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 Si definisce “soluzione” in chimica una miscela omogenea in cui una o più sostanze sono contenute in una fase liquida o solida o gassosa; una soluzione contiene particelle diverse mescolate e distribuite in modo uniforme nello spazio disponibile in modo che ogni volume di soluzione abbia la medesima composizione degli altri. La misura della quantità di soluto rispetto alla quantità di soluzione è detta concentrazione e viene misurata sia tramite unità fisiche che tramite unità chimiche.
Si definisce “soluzione” in chimica una miscela omogenea in cui una o più sostanze sono contenute in una fase liquida o solida o gassosa; una soluzione contiene particelle diverse mescolate e distribuite in modo uniforme nello spazio disponibile in modo che ogni volume di soluzione abbia la medesima composizione degli altri. La misura della quantità di soluto rispetto alla quantità di soluzione è detta concentrazione e viene misurata sia tramite unità fisiche che tramite unità chimiche.
In chimica si possono distinguere tre tipi di soluzione, in base alla concentrazione di soluto:
Il passaggio dell’acqua attraverso una membrana posta tra due ambienti (ad esempio cellula e spazio extracellulare), dipende dal tipo di ambiente ipertonico, ipotonico o isotonico:
Leggi anche:
Per sopravvivere in un ambiante ipertonico o ipotonico la cellula deve quindi continuamente regolare l’equilibrio idrico, tramite l’osmoregolazione. Le cellule vegetali hanno una parete cellulare che limita il loro volume e ne definisce la forma.
Turgore : pressione interna alla cellula contro la parete cellulare che impedisce l’ingresso di altra acqua.
Le proteine di trasporto consentono una diffusione facilitata, cioè permettono a una sostanza di attraversare la membrana secondo il gradiente di concentrazione. È un tipo di trasporto passivo, non richiede energia. La diffusione facilitata è utilizzata da zuccheri, amminoacidi, ioni e acqua. Le proteine di trasporto più comuni agiscono da canale per queste sostanze; la proteina da trasporto “ carrier” si lega al proprio passeggero, cambia forma e lo lascia all’altro lato della membrana. Le proteine di trasporto dette acquaporine rendono rapida la diffusione dell’acqua. La proteina di trasporto è specifica per la sostanza di cui facilita il passaggio; più proteine di trasporto ci sono, più rapida è la diffusione.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
La respirazione aerobica è il processo che permette di sfruttare il contenuto energetico delle molecole utilizzate nel metabolismo. Per questa via metabolica è necessaria la presenza dell’ossigeno e per questo motivo l’apparizione degli organismi fotosintetici ossigenici è stato un passaggio fondamentale nell’evoluzione dei viventi. La respirazione permette infatti di ossidare il piruvato proveniente dai processi di glicolisi, sfruttando così al massimo il contenuto energetico iniziale del glucosio, zucchero esoso intorno al quale ruota il metabolismo centrale della maggior parte degli esseri viventi.
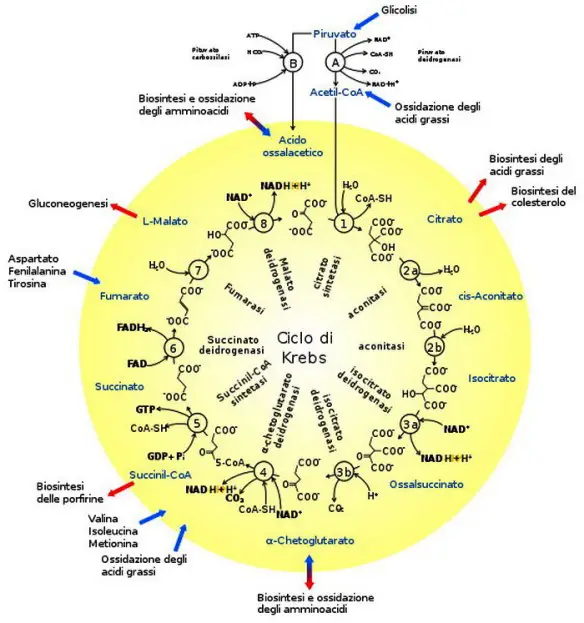
Negli eucarioti gli enzimi di che intervengono in queste reazioni si trovano nei mitocondri, dove avviene il ciclo di Krebs, o ciclo dei TCA (acidi tricarbossilici) e ciclo dell’acido citrico. Il ciclo è costituito da 8 passaggi. Ma prima di inserirsi in questa via, il piruvato deve essere trasportato attraverso la doppia membrana del mitocondrio, sin nella parte più interna, chiamata matrice mitocondriale. Il piruvato viene poi trasformato in acetilcoenzima A (AcetilCoA) dall’enzima piruvato deidrogenasi, liberando CO2 e NADH. Questo passaggio è necessario, poiché l’energia contenuta nel legame tioestere (che coinvolge uno zolfo) fra l’acetile e il coenzima A viene usata per il legame con l’ossalacetato, uno degli intermedi del ciclo di Krebs. In quanto ciclo, non si può dire che esso abbia un vero substrato di partenza e un vero prodotto di arrivo.
I vari passaggi di ossidazione, catalizzati dalle deidrogenasi, producono cofattori ridotti: 3 NADH e 1 FADH2 per ogni piruvato utilizzato, il doppio per ogni glucosio, dato che la glicolisi permette di ottenere 2 molecole di piruvato per ogni glucosio. Gli altri prodotti ottenuti sono 2 CO2 (che diffonde dalle membrane) e 1 GTP (guanosintrifosfato) dal quale indirettamente si ottiene 1 ATP.
Leggi anche:
Il ciclo di Krebs è costituito da 8 reazioni catalizzate da enzimi, i cui intermedi sono spesso substrato di altre vie metaboliche: per questo motivo è necessario che la cellula li sostituisca mediante reazioni di “riempimento” chiamate reazioni anaplerotiche.
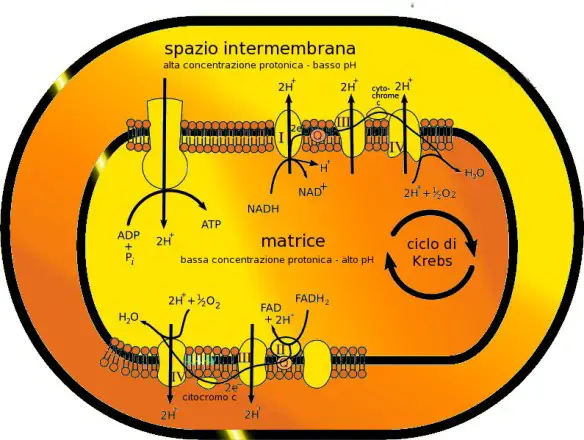
Visto che non risulta conveniente coinvolgere così tanti enzimi per guadagnare solo 1 ATP, la cellula sfrutta i cofattori ridotti accumulati nella glicolisi e nel ciclo di Krebs per produrre altro ATP. Sulla membrana interna sono presenti un gruppo di proteine integrali che svolgono il ruolo di deidrogenasi. Esse sono in grado di ossidare il NADH e il FADH2 e di utilizzare l’energia potenziale degli elettroni che da essi ottengono, i quali derivano in origine dall’ossidazione del glucosio e del piruvato. Queste proteine sono enzimi che vengono chiamati nel loro insieme catena di trasporto degli elettroni.
I complessi I, III e IV sono in realtà delle pompe protoniche in grado di sfruttare l’energia delle reazioni redox che catalizzano per trasportare protoni (H+) dalla matrice allo spazio intermembrana, creando così un gradiente di concentrazione ad alta energia potenziale. I protoni infatti subiscono forte repulsione elettrostatica e cercano una “valvola di sfogo” per allontanarsi, cedendo la propria energia a qualcun altro.
L’enzima ATP sintasi, anch’esso nella membrana interna del mitocondrio, è in grado di usare questo gradiente per legare un gruppo fosfato all’ADP, sintetizzando l’ATP, la cui energia è proprio contenuta nel legame dell’ultimo gruppo fosfato, che qui si forma. Questo tipo di aggiunta di un gruppo fosfato viene chiamato fosforilazione ossidativa. La reazione completa, a partire dal glucosio e comprendendo quindi la glicolisi e la catena di trasporto degli elettroni, è la seguente:
C6H12O6 + 6O2 → 6CO2 + 6H2O + 36 (o 38) ATP
Leggi anche:
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Reddit, su Tumblr e su Pinterest, grazie!