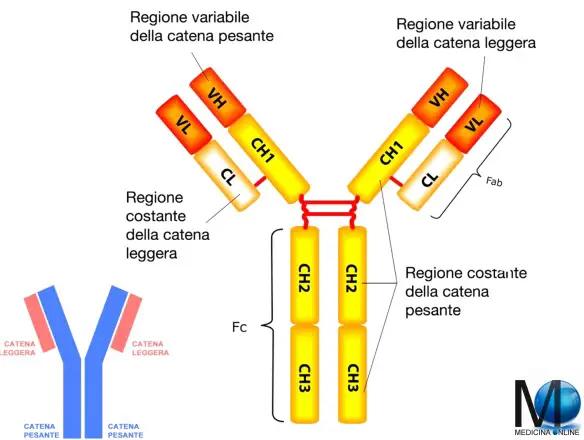
Struttura di una immunoglobulina (anticorpo)
Le “sindromi reattive pseudoallergiche” o “pseudoallergie” o “PAR” (acronimo dall’inglese “Pseudo-Allergic Reactions”) costituiscono un gruppo di Continua a leggere


Struttura di una immunoglobulina (anticorpo)
Le “sindromi reattive pseudoallergiche” o “pseudoallergie” o “PAR” (acronimo dall’inglese “Pseudo-Allergic Reactions”) costituiscono un gruppo di Continua a leggere
 Patogenesi
PatogenesiIl termine “patogenesi” descrive i modi ed i processi fisiopatologici attraverso cui avvengono le alterazioni dello stato fisiologico che portano allo stabilirsi e allo svilupparsi di una malattia a partire dalle sue cause e fattori di rischio; ad esempio la patogenesi di una infezione virale descrive il modo Continua a leggere

Che differenza c’è tra i termini eziologia, patogenesi ed eziopatogenesi?
Il termine “eziologia” in medicina descrive la parte della scienza che si occupa di ricercare tutti gli avvenimenti, i motivi e le variabili che hanno causato una patologia, sia in modo diretto che indiretto. Esempi di fattori eziologici sono: Continua a leggere
 Il diabete mellito abbreviato DM è una forma di diabete ovvero un gruppo di disturbi metabolici accomunati dal fatto di presentare una persistente instabilità del livello glicemico del sangue, passando da condizioni di iperglicemia, più frequente, a condizioni di ipoglicemia. La patogenesi del diabete mellito non è ancora chiarita completamente ma molti meccanismi sono certamente noti.
Il diabete mellito abbreviato DM è una forma di diabete ovvero un gruppo di disturbi metabolici accomunati dal fatto di presentare una persistente instabilità del livello glicemico del sangue, passando da condizioni di iperglicemia, più frequente, a condizioni di ipoglicemia. La patogenesi del diabete mellito non è ancora chiarita completamente ma molti meccanismi sono certamente noti.
Il glucosio rappresenta la più importante fonte di energia per le cellule del nostro organismo e proprio per questo, oltre ad essere utilizzato immediatamente, viene anche immagazzinato in riserve di glicogeno. Il glucosio, dunque, dal sangue (nel quale viene disciolto dopo il processo di digestione degli alimenti) deve essere trasportato all’interno delle cellule per essere utilizzato e immagazzinato.
L’insulina è il principale ormone che regola l’ingresso del glucosio dal sangue nelle cellule (principalmente le cellule muscolari e adipose; non nelle cellule del sistema nervoso), il deficit di secrezione insulinica o l’insensibilità alla sua azione sono proprio i due meccanismi principali attraverso cui si espleta il DM. La gran parte dei carboidrati nel cibo viene convertita entro un paio di ore in glucosio. L’insulina è prodotta dalle cellule β del pancreas come esatta risposta all’innalzamento dei livelli di glucosio nel sangue (per esempio dopo un pasto), le cellule β del pancreas sono infatti stimolate dagli alti valori di glicemia e inibite dai valori bassi.
Se la disponibilità di insulina è insufficiente (deficit di insulina) o se le cellule rispondono inadeguatamente ad essa (insulinoresistenza) o se l’insulina prodotta è difettosa, il glucosio non può essere efficacemente utilizzato dal nostro organismo: la conseguenza di ciò è uno stato di carenza di glucosio nei tessuti con elevati valori nel torrente sanguigno.
Quando la glicemia a digiuno supera i 126 mg/dl si parla di DM, mentre per valori compresi tra 110 e 125 mg/dl si parla di “alterata glicemia a digiuno” (fattore di rischio per la futura comparsa di DM). Il glucosio compare nelle urine (glicosuria) per valori di glicemia maggiori di 180/200 mg/dl.
Leggi anche:
La ridotta capacità dell’insulina di agire in maniera efficace sui tessuti bersaglio (muscoli e fegato) è la caratteristica principale del DM di tipo 2 e viene chiamata insulinoresistenza. Si tratta di una resistenza “relativa” in quanto livelli sovrafisiologici di insulinemia provocano una normalizzazione della glicemia. Si ritiene che questo tipo di resistenza sia dovuto a difetti post-recettoriali, per la precisione sembra coinvolto il gene IRS-1, indispensabile per la sintesi delle proteine IRS coinvolte in una serie di vie metaboliche che in ultima istanza promuovono l’ingresso del glucosio nelle cellule diminuendo così la glicemia.
La resistenza cronica all’insulina è definita come un fabbisogno giornaliero di insulina superiore a 200 Ui per parecchi giorni in assenza di infezione o chetoacidosi.
Le cause più comuni sono rappresentate dall’obesità e da anticorpi antinsulina di tipo IgG. La conseguenza più importante è il mancato controllo della glicemia.
In quasi tutti i pazienti diabetici, entro i 60 giorni dall’inizio della terapia insulinica, si sviluppano anticorpi. Si pensa che il loro legame all’insulina sia la causa più importante di severa resistenza, ma la correlazione fra il titolo anticorpale e la resistenza non è sempre stretta. Studi recenti individuano come una precoce terapia insulinica possa scongiurare una progressione delle due forme di diabete, per questo l’assunzione di zuccheri deve essere diminuita.
Nel momento in cui si instaura una insulino-resistenza si ha inizialmente un aumento compensatorio di secrezione di insulina (iperinsulinemia) da parte delle cellule β pancreatiche, tuttavia la patologia ha un decorso ingravescente che porta a una vera e propria insufficienza dei meccanismi di compenso. Nella patogenesi del progressivo deficit della secrezione insulinica hanno un ruolo determinante la necrosi e l’apoptosi della cellule beta, alle quali concorrono la dislipidemia (lipotossicità) e la iperglicemia cronica (glucotossicità), attraverso meccanismi biochimici complessi, che, tra l’altro, provocano un aumento della produzione di radicali liberi (stress ossidativo), un disaccoppiamento della fosforilazione ossidativa mitocondriale e alterazioni del reticolo endoplasmatico (stress reticolare).
Come si vedrà in seguito, il DM provoca un aumento di corpi chetonici in circolo, ciò metabolicamente equivale allo sviluppo di una ingannevole condizione di “digiuno cronico” (anche se il paziente si nutre normalmente): in condizioni di digiuno si assiste a un aumento della glicogenolisi (liberazione di riserve glucidiche) e gluconeogenesi (sintesi ex novo di glucosio). Tutto ciò provoca un ulteriore peggioramento dello stato di iperglicemia.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 La schizofrenia è una psicosi cronica caratterizzata dalla persistenza di sintomi di alterazione del pensiero, del comportamento e dell’affettività, da un decorso superiore ai sei mesi, con forte disadattamento della persona ovvero una gravità tale da limitare le normali attività di vita della persona.
La schizofrenia è una psicosi cronica caratterizzata dalla persistenza di sintomi di alterazione del pensiero, del comportamento e dell’affettività, da un decorso superiore ai sei mesi, con forte disadattamento della persona ovvero una gravità tale da limitare le normali attività di vita della persona.
Leggi anche:
Tra le ipotesi delle cause fisiopatologiche della schizofrenia vi è un deficit e/o alterata funzione dell’acido folico che comporta:
Una recente ricerca indica una correlazione tra l’aumento di IL-6 e TNF-α con i livelli di omocisteina patologici dovuti alla mutazione genica C677>T dell’enzimaMTHFR. Uno studio mette in relazione la comparsa della sintomatologia schizofrenica con un deficit di attività della glutamato carbossipeptidasi II (GCPII), enzima chiave per l’assorbimento dell’acido folico Un altro gruppo di ricerca del Massachusetts General Hospital and Harvard Medical School di Boston mette in relazione i sintomi negativi della schizofrenia con il deficit di acido folico dovuto al deficit dell’enzima MTHFR. L’uso dell’acido folico nell’ambito della terapia complementare e alternativa (CAM), sembra avere un ruolo definito e interessante, certamente meritevole di ulteriori sviluppi di ricerca. Vi sono alcuni studi che mettono in relazione l’infezione da Toxoplasma gondii con lo sviluppo della schizofrenia.
Secondo uno studio dell’Università dell’Ulster e dell’University of Southern Denmark, una delle possibili cause dello sviluppo di alcuni disturbi mentali, tra cui la schizofrenia, ci siano traumi sessuali subiti anche molti anni addietro. I ricercatori hanno analizzato la salute mentale di donne che erano ricorse ai centri di crisi dopo aver subito uno stupro o violenza sessuale e hanno scoperto che proprio il trauma sessuale può giocare un ruolo chiave nello sviluppo di disturbi psicotici come la schizofrenia. In più, la tendenza ad allontanarsi dal luogo in cui sono state vittime della violenza influisce ancora di più sulla possibilità di sviluppare disturbi mentali a causa del mancato sostegno causato dall’interruzione dei rapporti sociali. I risultati di questo studio sono stati pubblicati sulla prestigiosa rivista scientifica “Schizophrenia Bulletin”, dove si apprende che i dati sono stati ricavati dal database del Danish Civil Registration System (CRS) che raccoglie informazioni ufficiali sui cittadini danesi dal 1968 in poi.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 Eziologia della tubercolosi
Eziologia della tubercolosi
L’agente eziologico principale della tubercolosi (TBC) è il Mycobacterium tuberculosis, un batterio aerobiotico che si divide ogni 16-20 ore, una velocità estremamente lenta in confronto ad altri batteri, che solitamente si dividono in meno di un’ora (uno dei più veloci batteri a replicarsi è un ceppo del batterio Escherichia coli, che si divide circa ogni 20 minuti). Poiché l’MTB ha una parete cellulare, ma non una membrana esterna, viene classificato come un batterio Gram-positivo. Tuttavia, se viene applicata una colorazione di Gram, l’MTB risulta o Gram-positivo in modo estremamente debole, o non mantiene la colorazione, a causa dell’elevato contenuto di lipidi e acido micolico della sua parete cellulare. L’MTB è un piccolo bacillus a forma di bastoncello, che può resistere a deboli disinfettanti e sopravvivere in uno stato disidratato per settimane. In natura, il batterio può crescere solo all’interno delle cellule di un organismo ospite, ma l’M. tuberculosis può essere coltivato in vitro.
Usando pigmenti istologici su campioni di espettorato, gli scienziati possono identificare l’MTB con un normale microscopio. Poiché l’MTB conserva certi pigmenti dopo essere stato trattato con soluzioni acide, viene classificato come un bacillus acido-alcolico. La tecnica di pigmentazione più comune, la colorazione di Ziehl-Neelsen, tinge i bacilli acido-alcolici di un rosso acceso che risalta chiaramente su sfondo blu. Altri metodi per evidenziare questi bacilli sono la colorazione con auramina-rodamina e l’osservazione mediante microscopio a fluorescenza.
Il complesso MTB include tre micobatteri causa di tubercolosi: Mycobacterium bovis, Mycobacterium africanum e Mycobacterium microti. I primi due causano la malattia in persone immunocompetenti solo in casi rarissimi. Tuttavia, nonostante il M. microti non sia normalmente patogenico, è possibile che la prevalenza di infezioni da esso causate sia stata sottovalutata.
Altri micobatteri patogenici conosciuti comprendono Mycobacterium leprae, Mycobacterium avium complex e Mycobacterium kansasii. Gli ultimi due fanno parte del gruppo di micobatteri non tubercolari (MOTT, mycobacteria other than tuberculosis). I micobatteri non tubercolari non causano TBC o lebbra, ma provocano malattie polmonari simili alla tubercolosi.
Per approfondire:
Patogenesi della tubercolosi
Circa il 90% delle persone infette dal Mycobacterium tuberculosis ha un’infezione TBC asintomatica (chiamata anche LTBI, da latent tuberculsis infection), e solamente il 10% di possibilità nella vita che un’infezione latente si sviluppi in TBC. Tuttavia, se non trattata, il tasso di mortalità dei casi attivi di TBC è superiore al 50%.
L’infezione tubercolare inizia quando i micobatteri raggiungono gli alveoli polmonari, dove attaccano e si replicano all’interno dei macrofagialveolari. Il sito primario di infezione nei polmoni è chiamato focolaio di Ghon. I batteri vengono raccolti dalle cellule dendritiche, che non permettono la loro replicazione ma che possono trasportare i bacilli ai linfonodi mediastinici locali. L’ulteriore diffusione attraverso il flusso sanguigno si dirige verso i tessuti e gli organi più distanti, dove lesioni secondarie di TBC si possono sviluppare negli apici polmonari, nei linfonodi periferici, nei reni, nel cervello e nelle ossa. Ogni parte del corpo può essere influenzata dalla malattia, che tuttavia raramente colpisce il cuore, i muscoli scheletrici, il pancreas e la tiroide.
La tubercolosi è classificata come una delle condizioni infiammatorie granulomatose. Macrofagi, linfociti T, linfociti B e fibroblasti sono le cellule aggredite che formano il granuloma, con i linfociti che circondano i macrofagi infetti. Il granuloma non solo impedisce la diffusione dei micobatteri, ma fornisce un ambiente locale per la comunicazione delle cellule del sistema immunitario. Dentro al granuloma, i linfociti T (CD4+) producono citochine come l’interferone gamma, che provoca un tentativo di distruzione da parte dei macrofagi dei batteri fagocitati, senza però riscontri significativi, dal momento che i Mycobacterium tuberculosis sono batteri Catalasi positivi (resistenti quindi agli enzimi killer dei polimorfonucleati). I linfociti T (CD8+) possono anche uccidere direttamente le cellule infette.
Significativamente, i batteri non vengono sempre eliminati all’interno del granuloma, ma possono diventare dormienti, e svilupparsi in infezione latente. Un’altra caratteristica dei granulomi della tubercolosi umana è lo sviluppo di necrosi, cioè della morte delle cellule, al centro dei tubercoloma. A occhio nudo la necrosi ha l’aspetto di formaggio bianco, ed è stata quindi chiamata necrosi caseosa.
Se i batteri della TBC riescono ad accedere al flusso sanguigno da un’area di tessuto danneggiato, si diffondono nell’organismo e creano molti focolai di infezione, tutti con l’aspetto di piccoli tubercoli bianchi nei tessuti. Questa grave forma di tubercolosi è molto diffusa nei bambini e negli anziani, ed è chiamata tubercolosi miliare. I pazienti con la TBC disseminata hanno una mortalità del 20% circa, persino con un trattamento intensivo.
In molti pazienti l’infezione cresce e diminuisce. La distruzione dei tessuti e la necrosi è bilanciata dalla guarigione e dalla fibrosi. I tessuti affetti vengono rimpiazzati da cicatrici e le cavità riempite di materiale necrotico bianco. Nella malattia attiva parte del materiale necrotico si unisce all’aria passante per i bronchi, e questo viene tossito. Esso contiene batteri attivi, e quindi può diffondere l’infezione. Un trattamento con antibiotici appropriati uccide i batteri e permette la guarigione. Durante questa, le aree affette vengono lentamente rimpiazzate da tessuto cicatriziale.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!