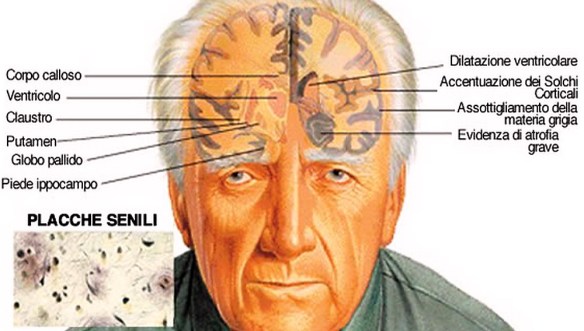
 Con “demenza senile” si indica una patologia neurodegenerativa dell’encefalo, tipica dell’età avanzata e caratterizzata da una riduzione graduale ed irreversibile delle facoltà cognitive di una persona. La demenza senile rientra nella più ampia categoria delle demenze le quali sono patologie neurodegenerative dell’encefalo che possono colpire persone anziane ma non solo, e che determinano un progressivo declino delle facoltà cognitive di un individuo. E’ importante ricordare che non tutte le demenze sono irreversibili, sono reversibili ad esempio alcune forme di demenza da idrocefalo normoteso o da cause metaboliche. Un tempo “demenza senile” era sinonimo di malattia di Alzheimer. Successivamente, con la scoperta di altre forme di demenza tipiche dell’età avanzata, e con l’individuazione di una forma di Alzheimer giovanile, la dicitura demenza senile ha assunto un significato leggermente diverso, riportato nella definizione iniziale. Pur non essendo la demenza una causa diretta di morte, nella maggior parte dei casi sono i disturbi della deglutizione ad essa associata ad essere fatali per l’anziano. Tali disturbi, infatti, concorrono allo sviluppo di polmoniti da inalazione (o da aspirazione).
Con “demenza senile” si indica una patologia neurodegenerativa dell’encefalo, tipica dell’età avanzata e caratterizzata da una riduzione graduale ed irreversibile delle facoltà cognitive di una persona. La demenza senile rientra nella più ampia categoria delle demenze le quali sono patologie neurodegenerative dell’encefalo che possono colpire persone anziane ma non solo, e che determinano un progressivo declino delle facoltà cognitive di un individuo. E’ importante ricordare che non tutte le demenze sono irreversibili, sono reversibili ad esempio alcune forme di demenza da idrocefalo normoteso o da cause metaboliche. Un tempo “demenza senile” era sinonimo di malattia di Alzheimer. Successivamente, con la scoperta di altre forme di demenza tipiche dell’età avanzata, e con l’individuazione di una forma di Alzheimer giovanile, la dicitura demenza senile ha assunto un significato leggermente diverso, riportato nella definizione iniziale. Pur non essendo la demenza una causa diretta di morte, nella maggior parte dei casi sono i disturbi della deglutizione ad essa associata ad essere fatali per l’anziano. Tali disturbi, infatti, concorrono allo sviluppo di polmoniti da inalazione (o da aspirazione).- Morbo di Parkinson: cause, sintomi, decorso, terapie
- Morbo di Alzheimer: cause, sintomi, decorso, terapie
- Sclerosi laterale amiotrofica (SLA): cause, sintomi, diagnosi e prognosi
- Demenza da corpi di Lewy: cause, decorso, Parkinson, aspettativa di vita
Demenza senile o fisiologico invecchiamento?
Nonostante determinino manifestazioni simili, la demenza senile e il cosiddetto declino cognitivo legato all’età avanzata sono due condizioni mediche differenti.
Infatti, il declino cognitivo legato all’età avanzata – noto anche come deterioramento cognitivo dell’età avanzata – è un normale processo involutivo a cui va incontro il cervello di una persona sana, durante l’invecchiamento. Tale normale processo involutivo interessa tutte le persone anziane e comporta una graduale riduzione del volume cerebrale, la perdita di diversi neuroni e un’inefficiente trasmissione dei segnali nervosi; ovviamente questi processi possono essere più o meno gravi in funzione di molti fattori: un anziano in peso forma, che svolge attività fisica regolare, si alimenta bene e continua a mantenersi attivo (ad esempio leggendo libri, avendo hobby ed amici con cui parlare), avrà un declino più lento di un anziano obeso, pigro e sedentario, a parità di età biologica. Al contrario del fisiologico deterioramento cognitivo legato all’età avanzata, la demenza senile è una vera e propria patologia. Mentre tutti noi da anziani andremo incontro ad un deterioramento cognitivo, non tutti noi avremo la demenza senile.
TIPI DI DEMENZA SENILE
Le principali malattie neurodegenerative dell’encefalo, che fanno capo alla voce “demenza senile”, sono:
- Il morbo di Alzheimer o malattia di Alzheimer. Il morbo di Alzheimer può colpire anche adulti giovani, trentenni. In questi frangenti, la malattia è nota come Alzheimer giovanile, ha probabilmente cause di tipo genetico e non rientra tra le forme di demenza senile.
- La demenza vascolare.
- La demenza a corpi di Lewy.
Leggi anche:
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Differenza tra morbo di Alzheimer, demenza senile, vascolare e reversibile
- Differenza tra morbo di Alzheimer e morbo di Parkinson: sintomi comuni e diversi
- Cervelletto: anatomia esterna ed interna
EPIDEMIOLOGIA
Dati epidemiologici relativi, specificatamente, alla demenza senile non esistono.
Tuttavia, è possibile trarre alcune conclusioni interessanti dai numerosi studi statistici riguardanti la più ampia categoria delle demenze
Secondo tali studi, datati 2010, le persone dementi sparse in tutto il mondo sarebbero circa 36 milioni.
Di questi 36 milioni:
- Il 3% ha tra i 65 e i 74 anni, il 19% ha tra i 75 e gli 84 anni e più della metà ha dagli 85 anni in su.
- 6,8 milioni vivono negli Stati Uniti. Più della metà di queste persone con demenza è ultraottantenne.
- 750.000-800.000 vivono nel Regno Unito.
- Il 50-70% soffre di morbo di Alzheimer, il 25% di demenza vascolare, il 15% di demenza a corpi di Lewy e la restante percentuale è affetta dalle altre forme di demenza esistenti.
Per effetto dell’allungamento delle vita media dell’essere umano, gli esperti ritengono che il numero di persone con demenza senile sarà destinato ad aumentare progressivamente.
Per quanto concerne le demenze in generale, alcune previsioni sostengono che, nel 2020, il numero mondiale di dementi raggiungerà i 48 milioni circa.
In Italia, le persone con una forma di demenza sono circa l’1,5% della popolazione sopra i 65 anni e più del 30% della popolazione sopra gli 80 anni.
Cause
Le precise cause di demenza senile sono ancora poco chiare. A renderne difficile lo studio e la comprensione è la complessità strutturale dell’encefalo.
Al momento, il solo dato certo, in merito ai fattori scatenanti, è che la demenza senile è la conseguenza di due eventi: la morte delle cellule nervose cerebrali e/o un loro malfunzionamento a livello di comunicazione intercellulare (cioè la comunicazione esistente tra cellula e cellula).
CAUSE IPOTETICHE: AGGREGATI PROTEICI E PROBLEMI CEREBROVASCOLARI
Studiando i vari tipi di demenza senile sopraccitati, i ricercatori hanno fatto alcuni importanti ritrovamenti e hanno ipotizzato, per questi, un possibile ruolo causale.
Per quanto concerne il morbo di Alzheimer e la demenza da corpi di Lewy, questi ritrovamenti consistono nei cosiddetti aggregati proteici, ossia aggregati di proteine con sede all’esterno e/o all’interno dei neuroni cerebrali.
L’idea degli studiosi è che questi aggregati vadano a interferire con il normale funzionamento dei neuroni, determinandone, in alcuni frangenti, anche la morte.
Tra le proteine costituenti gli aggregati proteici, rientrano: l’APP (o proteina precursore della beta amiloide), la proteina tau e l’alfa-sinucleina. L’APP e la proteina tau caratterizzano il morbo di Alzheimer, mentre l’alfa-sinucleina contraddistingue la demenza a corpi di Lewy.
Per quanto concerne invece la demenza vascolare, i ritrovamenti che potrebbero in qualche modo spiegare l’insorgenza della malattia consistono nelle alterazioni vascolari (cioè a carico dei vasi sanguigni), rinvenute in sede cerebrale. Secondo gli studiosi, queste alterazioni andrebbero a pregiudicare il normale flusso sanguigno cerebrale, il tutto con serie conseguenze a carico del tessuto nervoso del cervello.
All’origine delle alterazioni vascolari cerebrali possono esserci episodi di ictus omini-ictus, la cosiddetta malattia dei piccoli vasi sanguigni o l’aterosclerosi.
Leggi anche:
- Sclerosi multipla: cause, sintomi, diagnosi e prognosi
- Differenze tra sclerosi laterale amiotrofica e sclerosi multipla
- Atrofia muscolare progressiva: cause, sintomi, cura, aspettativa di vita
- Differenze tra atrofia muscolare progressiva e sclerosi laterale amiotrofica
Sintomi
I sintomi e i segni della demenza senile subiscono un peggioramento graduale, che è strettamente dipendente dalla progressiva morte delle cellule nervose cerebrali.
In genere, l’evoluzione sintomatologica della demenza senile è un percorso a tre stadi: iniziale, intermedio e avanzato.
Allo stadio iniziale, le manifestazioni più caratteristiche consistono in:
- Piccoli problemi di memoria a breve termine (in genere amnesie);
- Sporadici cambiamenti di personalità;
- Occasionale mancanza di giudizio;
- Lievi difficoltà di linguaggio, calcolo, ragionamento e comprensione di nuovi concetti;
- Tendenza alla passività e alla mancanza d’iniziativa.
Allo stadio intermedio, i sintomi e i segni più comuni sono:
- Perdita evidente di parte delle abilità cognitive, dalle capacità di ragionamento e apprendimento a quelle di giudizio;
- Peggioramento dei problemi di memoria a breve termine;
- Problemi di memoria a lungo termine;
- Aggravamento delle difficoltà di linguaggio;
- Problemi visivi, dall’incapacità di riconoscere i colori e leggere a quella di quantificare approssimativamente una distanza;
- Confusione (o disorientamento) spazio-temporale, con il paziente che fatica a realizzare dove si trova, a dire con certezza il giorno della settimana ecc;
- Difficoltà nel quotidiano, anche nelle attività più banali;
- Lieve instabilità emotiva.
Infine, allo stadio avanzato, i disturbi tipici consistono in:
- Perdita totale o quasi totale delle capacità cognitive;
- Incapacità di accudire alla propria persona, quindi problemi nel mangiare, lavarsi ecc;
- Incapacità di riconoscere le persone care;
- Difficoltà di deglutizione;
- Perdita di controllo della funzione intestinale e vescicale (incontinenza);
- Perdita del controllo motorio, con il paziente che cammina sempre meno.
È importante precisare che ciascun tipo di demenza senile presenta alcune particolarità sintomatologiche.
Per esempio, chi soffre di morbo di Alzheimer può manifestare anche: aggressività insolita, agitazione, depressione, insonnia e/o delusione.
Chi è affetto da demenza vascolare può manifestare allucinazioni e una serie di disturbi dipendenti dall’area cerebrale interessata dalle alterazioni vascolari.
Infine, i malati di demenza a corpi di Lewy possono evidenziare problematiche analoghe alle persone con morbo di Parkinson (quindi andatura ricurva, passo strascicato ecc).
Leggi anche:
- Sindrome dell’idiota sapiente: cause, caratteristiche e sintomi
- Sindrome del tramonto o del crepuscolo: cause, sintomi e cura
- Ritardo mentale nei bambini lieve, moderato, grave: si guarisce?
- Cervelletto: le lesioni cerebellari più comuni
- Le funzioni del cervelletto: apprendimento e correzione dei movimenti del corpo
DURATA DEL DECLINO COGNITIVO
La durata del graduale declino cognitivo dipende dal tipo di demenza senile in atto.
Ad esempio, la malattia di Alzheimer impiega, tipicamente, tra i 7 e i 10 anni per pregiudicare del tutto le capacità cognitive; dopodiché causa la morte.
La demenza vascolare agisce in maniera differente da paziente a paziente: in alcuni soggetti, il declino è molto rapido (pochi anni); in altri soggetti, invece, è decisamente più lento.
Infine, la demenza a corpi di Lewy presenta un declino cognitivo che raggiunge il suo apice nel giro di 7 anni.
Diagnosi
Non potendo contare su un test specifico per diagnosticare le demenze, i medici ricorrono a una lunga serie di esami molto diversi tra loro, che valutano le condizioni in cui versa il paziente e permettono l’esclusione di malattie differenti ma dai sintomi analoghi (N.B: questo modo di procedere, per esclusione, è noto come diagnosi differenziale).
- Un esame obiettivo accurato.
Consiste nell’analisi dei sintomi e dei segni, riportati o manifestati dal paziente. Nonostante non fornisca alcun dato certo, rappresenta un passaggio obbligato e spesso ricco di informazioni diagnostiche utili. - L’analisi della storia clinica.
Consiste nell’indagare: come e quando i sintomi hanno fatto la loro prima comparsa; se il paziente soffre o ha sofferto in passato di altre particolari patologie; se il paziente assume farmaci ecc. - Un esame neurologico completo.
Consiste nell’analisi dei riflessi tendinei, delle abilità motorie (equilibrio ecc) e delle funzioni sensoriali. - Un esame cognitivo e neuropsicologico.
Consiste nello studio del comportamento, delle capacità di memoria, delle abilità di linguaggio e della facoltà di ragionamento. - La risonanza magnetica nucleare (RMN) e la tomografia assiale computerizzata (TAC), entrambe riferite all’encefalo.
Sono due procedure di diagnostica per immagini che permettono di valutare lo stato di salute dell’encefalo. Infatti, sono in grado di evidenziare eventuali processi di atrofia della corteccia cerebrale (tipici del morbo di Alzheimer) o eventuali alterazioni cerebrovascolari (tipiche della demenza vascolare). - Esami di laboratorio.
Consistono in: analisi del sangue, misura della glicemia, analisi delle urine, test tossicologici, analisi del liquido cerebrospinale e, infine, misura degli ormoni tiroidei.
La loro esecuzione è importante dal punto di vista della diagnosi differenziale.
Trattamento
Allo stato attuale, la demenza senile è una condizione che è possibile curare soltanto sotto il profilo dei sintomi, in quanto non è stato ancora trovato un trattamento specifico in grado di arrestare la neurodegenerazione e far regredire le sue conseguenze (ossia la riduzione delle facoltà cognitive).
Tra i vari tipi di terapia sintomatica a disposizione dei pazienti con demenza senile, rientrano:
- Farmaci. I più noti e prescritti sono gli inibitori dell’acetilcolinesterasie la memantina, un preparato farmacologico che agisce sul sistema glutamminergico.
La somministrazione di altri medicinali dipende dal tipo di demenza senile in atto.
Per esempio, la demenza vascolare prevede l’impiego di antipertensivi e anticoagulanti (per far fronte ai problemi di natura cerebrovascolare), mentre la demenza a corpi di Lewy prevede l’uso di levodopa (per contrastare i problemi di natura parkinsoniana).
Altri farmaci e preparati farmaceutici potenzialmente utili sono: gli antidepressivi, gli antipsicotici e le vitamine antiossidanti. - Fisioterapia
- Terapia occupazionale
- Terapia comportamentale
- Terapia del linguaggio
- Stimolazione cognitiva.
DIETA E STILE DI VITA
Diversi team di ricerca stanno cercando di capire se la dieta e lo stile di vita influiscano sulla demenza senile.
Nella fattispecie, stanno testando se, in qualche modo, il tipo di alimentazione e una regolare attività fisica siano capaci di rallentare il processo neurodegenerativo, indotto dal morbo di Alzheimer.
Prognosi e prevenzione
Date l’impossibilità di curarla in maniera specifica e l’inesorabile neurodegenerazione che provoca, la demenza senile ha, inevitabilmente, una prognosi negativa. Svariati studi scientifici hanno dimostrato che esistono alcune strategie per posticipare la comparsa della demenza senile.
Leggi anche:
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
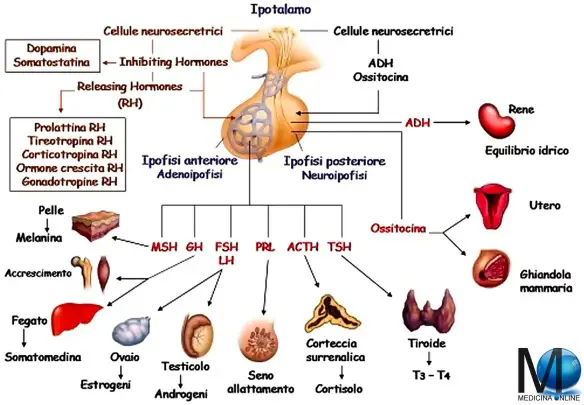
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Epilessia infantile ed in adulti: cause, sintomi, diagnosi, cosa fare
- Epilessia: come riconoscere un attacco e soccorrere un ammalato
- Differenza tra epilessia e convulsioni
- Differenza tra epilessia e sincope
- Differenza tra epilessia parziale e generalizzata
- Epilessia: riconoscere in tempo l’arrivo di una crisi e come comportarsi
- Epilessia infantile: come comportarsi col proprio figlio?
- Si può morire di epilessia?
- Tumore al cervello: operato mentre suona la chitarra e canta Yesterday
- Che cos’è l’intelligenza umana: definizione, significato e psicologia
- Quoziente d’intelligenza: valori, significato, test ed ereditarietà
- Problem solving: cos’è, caratteristiche, tecniche, fasi ed esempi
- Sindrome di Tourette: cause, sintomi, diagnosi e trattamento
- Sindrome di Tourette: si può guarire definitivamente? Come si guarisce?
- Disturbi cognitivi congeniti e acquisiti: ritardo mentale e demenza
- Riabilitazione cognitiva: Token Economy e tecniche per incrementare comportamenti adeguati
- Riabilitazione cognitiva: tecniche per incrementare comportamenti adeguati non presenti
- Terapia occupazionale: caratteristiche, attività, obiettivi, dispositivi
- Riabilitazione cognitiva: tecniche per incrementare attenzione, memoria, linguaggio
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!

 La malattia di Alzheimer e la malattia di Parkinson sono patologie spesso confuse tra i meno esperti, anche perché possono effettivamente avere sintomi simili, specie nelle fasi terminali, tuttavia eziologia, zona colpita, trattamenti e sintomi caratteristici sono diversi.
La malattia di Alzheimer e la malattia di Parkinson sono patologie spesso confuse tra i meno esperti, anche perché possono effettivamente avere sintomi simili, specie nelle fasi terminali, tuttavia eziologia, zona colpita, trattamenti e sintomi caratteristici sono diversi. Con demenza senile si indica un gruppo di patologie neurodegenerative dell’encefalo causate da diversi fattori eziologici; colpisce le persone anziane determinando in esse una riduzione graduale ed irreversibile delle facoltà cognitive.
Con demenza senile si indica un gruppo di patologie neurodegenerative dell’encefalo causate da diversi fattori eziologici; colpisce le persone anziane determinando in esse una riduzione graduale ed irreversibile delle facoltà cognitive.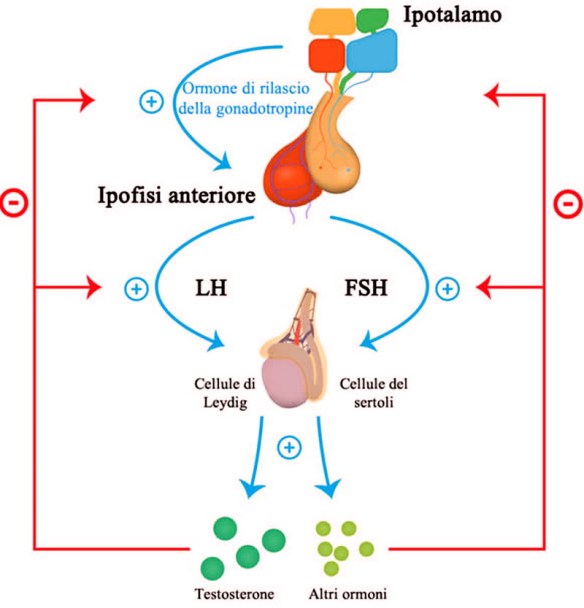 L’ipotalamo rilascia il GnRh, ormone rilasciante le gonadotropine Lh ed FSH rilasciate dall’ipofisi. Le due gonadotropine a livello del testicolo si indirizzano verso (LH) le cellule del Leydig e (FSH) tubulo seminifero, quindi l’LH controlla la steroidogenesi che avviene nelle cellule del Leydig mentre l’FSH controlla la spermatogenesi nel tubulo seminifero con il mantenimento dell’ABP che lega il testosterone.
L’ipotalamo rilascia il GnRh, ormone rilasciante le gonadotropine Lh ed FSH rilasciate dall’ipofisi. Le due gonadotropine a livello del testicolo si indirizzano verso (LH) le cellule del Leydig e (FSH) tubulo seminifero, quindi l’LH controlla la steroidogenesi che avviene nelle cellule del Leydig mentre l’FSH controlla la spermatogenesi nel tubulo seminifero con il mantenimento dell’ABP che lega il testosterone.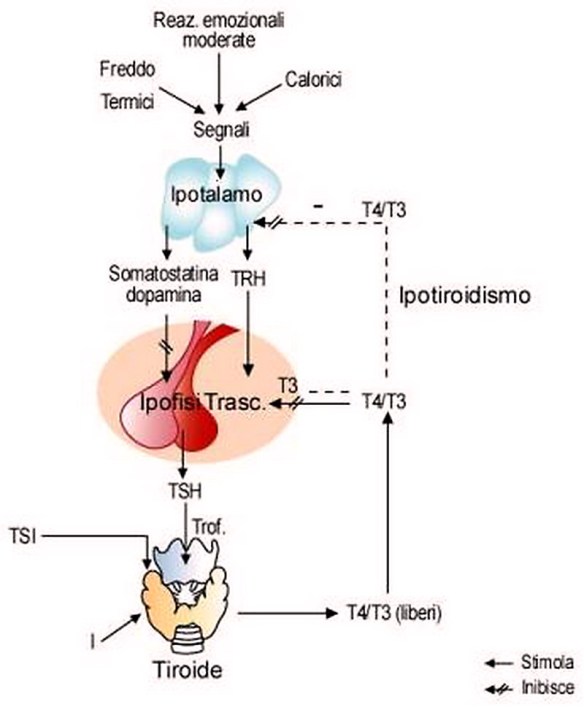 Quando l’ipotalamo rileva bassi livelli circolanti di ormoni tiroidei triiodotironina (T3) e tiroxina (T4), accade che:
Quando l’ipotalamo rileva bassi livelli circolanti di ormoni tiroidei triiodotironina (T3) e tiroxina (T4), accade che: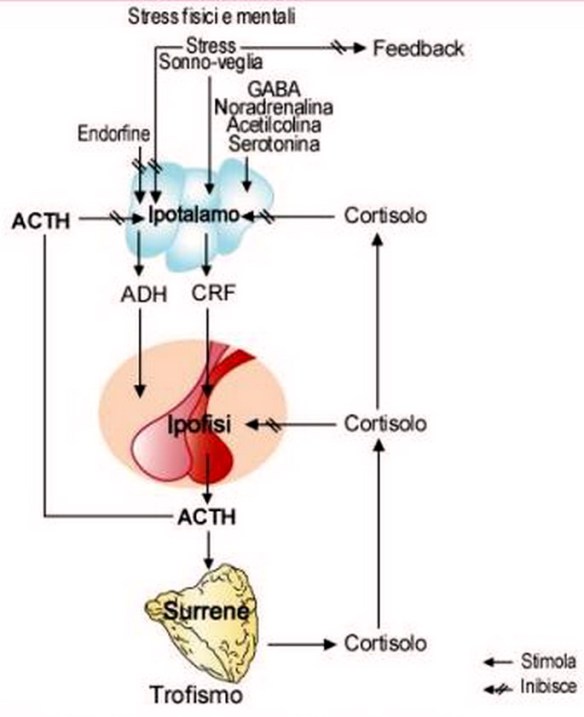 L’ipotalamo rilascia il fattore CRF che sta per fattore rilasciante la corticotropina o CRH che stimola l’adenoipofisi a rilasciare l’ormone ACTH, ormone adrenocorticotropo. Quest’ormone è importantissimo perché stimola poi la sintesi degli steroidi.
L’ipotalamo rilascia il fattore CRF che sta per fattore rilasciante la corticotropina o CRH che stimola l’adenoipofisi a rilasciare l’ormone ACTH, ormone adrenocorticotropo. Quest’ormone è importantissimo perché stimola poi la sintesi degli steroidi.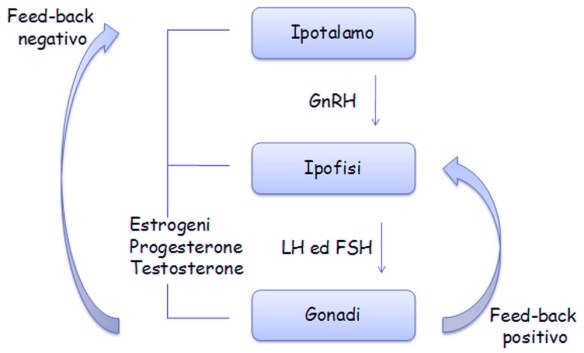 L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.
L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.