 Con “fibra alimentare“, o più semplicemente “fibra“, si indicano i polisaccaridi non a base di amido componenti le pareti cellulari, il parenchima Continua a leggere
Con “fibra alimentare“, o più semplicemente “fibra“, si indicano i polisaccaridi non a base di amido componenti le pareti cellulari, il parenchima Continua a leggere
Archivi tag: sazietà
Differenza tra fibre solubili ed insolubili
 Con “fibra alimentare“, o più semplicemente “fibra“, si indicano i polisaccaridi non a base di amido componenti le Continua a leggere
Con “fibra alimentare“, o più semplicemente “fibra“, si indicano i polisaccaridi non a base di amido componenti le Continua a leggere
Fibre solubili per stipsi e dimagrire: dieta, integratori, fabbisogno
 Le fibre alimentari non sono tutte uguali ed in base alla loro solubilità vengono classificate in due tipologie molto differenti per funzioni: fibre insolubili e Continua a leggere
Le fibre alimentari non sono tutte uguali ed in base alla loro solubilità vengono classificate in due tipologie molto differenti per funzioni: fibre insolubili e Continua a leggere
Asse ipotalamo-ipofisi-testicolo: funzionamento ed ormoni rilasciati
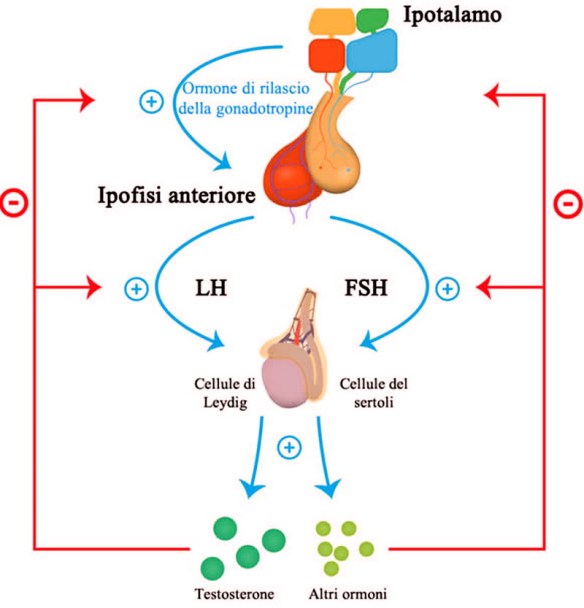 L’ipotalamo rilascia il GnRh, ormone rilasciante le gonadotropine Lh ed FSH rilasciate dall’ipofisi. Le due gonadotropine a livello del testicolo si indirizzano verso (LH) le cellule del Leydig e (FSH) tubulo seminifero, quindi l’LH controlla la steroidogenesi che avviene nelle cellule del Leydig mentre l’FSH controlla la spermatogenesi nel tubulo seminifero con il mantenimento dell’ABP che lega il testosterone.
L’ipotalamo rilascia il GnRh, ormone rilasciante le gonadotropine Lh ed FSH rilasciate dall’ipofisi. Le due gonadotropine a livello del testicolo si indirizzano verso (LH) le cellule del Leydig e (FSH) tubulo seminifero, quindi l’LH controlla la steroidogenesi che avviene nelle cellule del Leydig mentre l’FSH controlla la spermatogenesi nel tubulo seminifero con il mantenimento dell’ABP che lega il testosterone.
All’interno del testicolo vediamo che le due cellule sono in contatto fisico e funzionale in quanto il testosterone prodotto dal Leydig giunge nel tubulo seminifero, viene legato dalla proteine ABP e qui serve a controllare la produzione degli spermatozoi.
Questi sono effetti positivi. La spermatogenesi e sia LH che FSH dipendente perché l’LH guida la steroidogenesi e il testosterone assicura una corretta spermatogenesi.
La dopamina e la serotonina (neurotrasmettitori) hanno un effetto inibitorio sull’ipotalamo e sul rilascio di GnRH mentre la norepinefrina ha effetto positivo sul rilascio di GnRH.
Leggi anche:
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
Abbiamo feedback negativi che mantengono l’omeostasi della funzione gonadale, quindi un elevata concentrazione e sintesi di testosterone ed estradiolo innesca un feed – quindi viene rilasciato meno LH ma anche un feed – a livello ipotalamico quindi viene rilasciato meno GnRH. L’FSH inibito dall’inibina prodotta a livello della cellula del Sertoli che serve in modo specifico ad inibire l’FSH e mantenere livelli fisiologici.
Anche gli androgeni testosterone e DHT e anche la minima parte di estradiolo sono in grado di inibire l’FSH ipofisario, è ovvio che se ci sono elevate concentrazioni di androgeni la prima gonadotropina inibita è l’LH, anche se il controllo specifico sull’FSH è dato dall’inibina. Non si sa però ancora se l’inibina è in grado di indurre un freno inibitorio sul GnRH.
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Asse ipotalamo-ipofisi-tiroide: funzionamento ed ormoni rilasciati
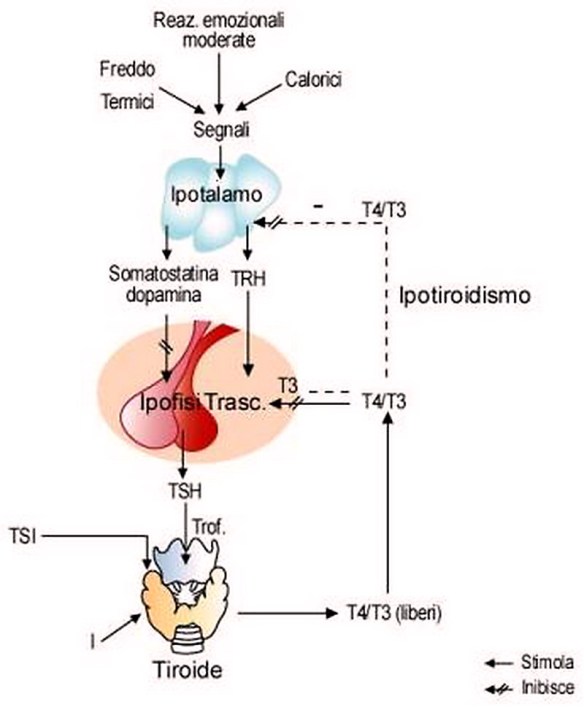 Quando l’ipotalamo rileva bassi livelli circolanti di ormoni tiroidei triiodotironina (T3) e tiroxina (T4), accade che:
Quando l’ipotalamo rileva bassi livelli circolanti di ormoni tiroidei triiodotironina (T3) e tiroxina (T4), accade che:
- l’ipotalamo rilascia l’ormone di rilascio della tireotropina (TRH);
- il TRH stimola l’ipofisi a produrre l’ormone tireostimolante (TSH o tireotropina);
- il TSH rilasciato dall’ipofisi stimola la tiroide;
- la tiroide, stimolata dal TSH ipofisario, produce e rilascia maggior quantità di triiodotironina (T3) e tiroxina (T4).
Gli ormoni tiroidei esercitano un controllo di tipo feedback negativo sull’ipotalamo e l’ipofisi anteriore, controllando così il rilascio sia di TRH che di TSH: quanto triiodotironina (T3) e tiroxina (T4) sono in quantità elevate, il rilascio di TRH e di TSH diminuiscono raggiungendo l’omeostasi, cioè l’equilibrio.
Leggi anche:
- Tiroide: dove si trova, com’è fatta e quali funzioni svolge?
- Differenza tra ipotiroidismo primario, secondario e terziario
- Ormoni tiroidei: differenza T3 e T4, valori normali e patologici
- TSH alto, basso e valori normali: qual è il significato clinico?
- Tireoglobulina alta, bassa, valori normali ed interpretazione
- Metabolismo basale: cos’è, definizione, calcolo, alto, basso, totale
- Asse ipotalamo-ipofisi-tiroide: funzionamento ed ormoni rilasciati
- Ipertiroidismo: cause, cura, valori diagnosi, sintomi iniziali, conseguenze
- Ipertiroidismo nell’uomo: sintomi, conseguenze sulla libido, cure
- Ipotiroidismo: sintomi, diagnosi, cura farmacologica e consigli dietetici
- Esame obiettivo del collo: palpazione della tiroide, video e spiegazione
- Ecografia della tiroide: a cosa serve, come si svolge e come ci si prepara all’esame
- Scintigrafia tiroidea: risultati, captazione, noduli, costo
- Agoaspirato tiroideo: esito, complicanze, dolore, referto, prezzo
- Tiroidite di Hashimoto: esami, cura, conseguenze, dieta, guarire
- Tiroidite di De Quervain (subacuta): sintomi, dieta, si guarisce, è contagiosa?
- Tireotossicosi autoimmune, iatrogena, factitia, valori, cura
- Differenza tra ipertiroidismo e tireotossicosi
- Morbo di Basedow: alimentazione, cura, occhi, si guarisce, rimedi
- Gozzo tiroideo: semplice, tossico, endemico, rimedi, intervento, immagini
- Gozzo tossico nodulare e multinodulare: sintomi, diagnosi e cura
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Feedback negativo ed omeostasi: spiegazione ed esempi
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Asse ipotalamo-ipofisi-surrene: funzionamento ed ormoni rilasciati
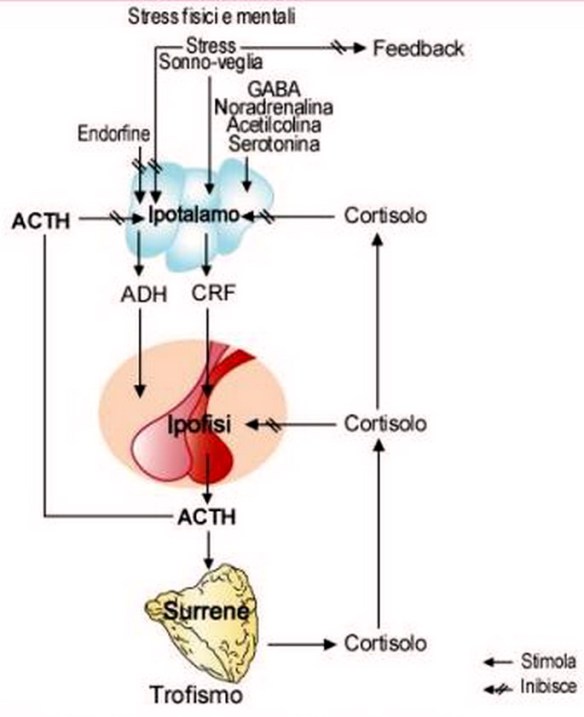 L’ipotalamo rilascia il fattore CRF che sta per fattore rilasciante la corticotropina o CRH che stimola l’adenoipofisi a rilasciare l’ormone ACTH, ormone adrenocorticotropo. Quest’ormone è importantissimo perché stimola poi la sintesi degli steroidi.
L’ipotalamo rilascia il fattore CRF che sta per fattore rilasciante la corticotropina o CRH che stimola l’adenoipofisi a rilasciare l’ormone ACTH, ormone adrenocorticotropo. Quest’ormone è importantissimo perché stimola poi la sintesi degli steroidi.
Il CRH o CRF nasce sottoforma di pre – pro CRH di 196 aa. e al carbossi term.troviamo la sequenza vera e propria dell’ormone ad attività biologica. Il crf agisce tramite recettori di membrana sull’adenoipofisi e quando viene rilasciato si lega e innesca l’attivazione della proteina G che attivando l’adenilato ciclasi innesca la produzione di cAMP che facilità il rilascio e la sintesi di ACTH da parte dell’adenoipofisi. Questo ACTH a sua volta nasce anch’esso come molecola precursore che è molto grossa e prende il nome di propio-melanocortina (POMC) dal gene che codifica per questa grossa proteina, siamo a livello dell’adenoipofisi.
Leggi anche:
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
Tramite peptidasi viene rilasciato l’ACTH ma vengono rilasciati anche frammenti carbossi-terminale che prende il nome di Beta-Lph che sta per Beta-lipotrofina. abbiamo diversi tagli molecolari che questa molecola subisce a livello adenoipofisario e questo prodotto lo troviamo anche a livello di tessuti extraipofisario, e livello gastroenterico, a livello del surrene e dell’ipofisi intermedia. In questi tessuti la molecola viene ulteriormente clivato dando origine ad altri prodotti di minore taglia come la beta – endorfina e la gamma – endorfina che si originano dalla beta – lipotrofina; dal peptide corrispondente all’ACTH si originano l’alfa MSH (melanocita stimolante) e il clip e infine si origina anche a partire dalla beta lipotropina il beta MSH soprattutto a livello dell’ipofisi intermedia.
A noi interessa soprattutto l’ACTH. L’ACTH rilasciato dall’adenoipofisi agisce con il suo recettore di membrana localizzato sulle cellule della corticale del surrene e anche in qst caso il recettore è accoppiato con l’cAMP che va ad attivare la PKA che va a fosforilare delle proteine importanti per la sintesi degli steroidi, fosforila delle proteine che rendono libera la molecola precursore che è il colesterolo presente immagazzinato nelle cellule come estere del colesterolo quindi la PKA agisce attivando le esterasi in modo tale che i legami di tipo estereo vengano rotti in modo tale che il colesterolo venga reso disponibile.
La sintesi del cortisolo e dell’ACTH è una sintesi non sempre uguale nelle 24h ma è elevata nelle prime ore del mattino, c’è una perfetta sincronia tra picchi dell’ACTH e picchi del cortisolo. Intorno alle 24 siccome gli ormoni glucocorticoidi sono ormoni che mantengono desta l’attenzione sono molto importanti per mantenere sveglia la memoria e l’attenzione, è quindi ovvio che naturalmente intorno alle 24 raggiungono dei livelli molto basali, si ha un livello basale del cortisolo che mantiene un livello molto basso del cortisolo.
È importante che le concentrazioni ormonali di questi ormoni aumentino al momento del risveglio, infatti intorno alle primissime ore del mattino, intorno alle 6, si ha un incremento delle concentrazioni di ACTH e di cortisolo. Infatti intorno alle 2 – 3 di notte c’è un sonno molto pesante che viene dato anche dalla mancanza di ormoni glucocorticoidi perché siamo ad un livello basale; man mano che inizia ad aumentare la sintesi di glucocorticoidi diventiamo più desti. Abbiamo quindi una ciclicità di secrezione impartita dal nostro orologio biologico impartito dal nucleo sovra-chiasmatico a livello celebrale da cui provengono anche i nostri ritmi sonno-veglia.
Da alcuni esperimenti su animali si è visto che un ritmo biologico di secrezione viene proprio mantentuo dalle cellule della corticale del surrene, cioè cellule della corticale del surrene messe in coltura hanno attività secretoria ciclica.
L’ ASSE IPOTALAMO IPOFISI SURRENE è un asse neuroendocrino controllato molto dallo stress, dall’ansia che influiscono sulla secrezione di glucocorticoidi e sui ritmi circadiani. Di tutti i neurotrasmettitori la serotonina e l’acetilcolina hanno un effetto positivo che potenzia a livello ipotalamico il rilascio di CRH, mentre il GABA è solitamente inibitorio unitamente alla noradrenalina hanno effetto inibitorio sul CRH.
Il CRH rilasciato dall’ipotalamo a livello dell’adenoipofisi controlla il rilascio dell’ACTH che subisce anche l’influenza positiva dell’adrenalina. L’ACTH a livello del surrene mantiene attiva la secrezione ormonale del cortisolo. Quando le concentrazioni di cortisolo tendono ad aumentare il cortisolo agisce con un controllo negativo sull’ACTH ipofisario o sul CRH ipotalamico. Anche l’ACTH se presente in eccesso è in grado di inibire il rilascio di CRH. La vasopressina è un potente stimolatore.
Questo asse neuroendocrino ricordiamo che ha una certa ciclicità, anche se ci sono situazioni che possono alterarlo, ad esempio lo stress impone un’ ipersecrezione di CRH e ACTH quindi lo stress governa quest’asse e anche quando la sera tardi i livelli di questi ormoni dovrebbero essere basali se siamo nervosi, aumenta la secrezione di catecolamine e lo stress impone un maggiore rilascio di ACTH e CRH.
L’ACTH soprattutto controlla il ritmo di sonno ma la ghiandola corticosurrenale libera cortisolo e mineralcorticoidi come l’aldosterone e questo ormone è sotto il controllo di ipotalamo e ipofisi ma l’ACTH controlla questo ormone solo quando raggiunge delle concentrazioni molto elevate e ne può ridurre il rilascio anche se il mineralcorticoide è sottoposto ad un altro tipo di controllo che vedremo che non è questo ipotalamico.
Leggi anche:
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Asse ipotalamo-ipofisi-gonade: funzionamento ed ormoni rilasciati
- Ormone della crescita (GH) a che serve e da cosa è prodotto?
- Ormone della crescita (GH): body building e doping in palestra
- Ormone della crescita (GH): effetti avversi nel body building e nello sport
- Quando essere troppo alti è una malattia: il gigantismo
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Cos’è l’adrenalina ed a cosa serve?
- L’altezza media italiana nel 2017 di maschi e femmine
- L’altezza media italiana 2017 da 1 a 19 anni di maschi e femmine
- L’altezza media mondiale nel 2017 di maschi e femmine [TABELLA]
- Altezza: quando si può parlare di nanismo o gigantismo
- Differenza tra midollo osseo e spinale
- Differenza tra sistema nervoso centrale e periferico: anatomia e funzioni in sintesi
- A cosa serve il midollo osseo?
- Differenza tra midollo osseo e cellule staminali
- Differenza tra midollo spinale e allungato
- Differenza tra epifisi, diafisi, metafisi ed ipofisi
- Quanto è alto l’uomo più alto del mondo?
- Quanto è alto l’uomo più basso del mondo?
- Nanismo: sintomi, cura, cause, terapia, diagnosi e prevenzione
- Charlotte, la bambina più piccola del mondo
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, segui la nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Asse ipotalamo-ipofisi-gonade: funzionamento ed ormoni rilasciati
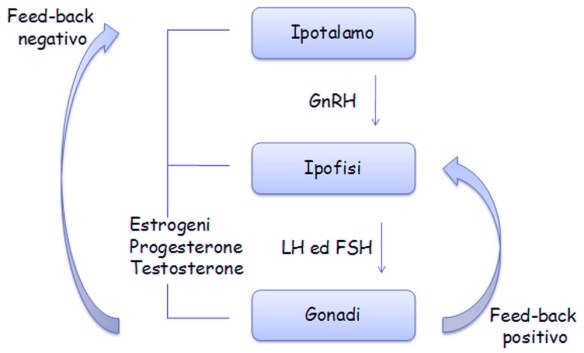 L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.
L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.
La secrezione di GnRH da parte dell’ipotalamo inizia nella 4° settimana di gestazione; questo rilascio pian piano sollecita l’ipofisi a rilasciare LH ed FSH e la loro sintesi inizia verso la 10 – 12 settimana di gestazione; poco prima della nascita questi valori decadono per mantenersi basse durante la prima infanzia e la secrezione si mantiene bassa anche durante la seconda infanzia e anche nell’età peri-puberale, momento in cui l’asse inizia a svegliarsi. Durante l’infanzia la quantità di FSH circolante supera quella dell’LH, in effetti l’FSH ha effetti sull’attività maturativa dei gameti. Durante la pubertà vediamo che l’attività secretoria del GnRH diventa più consistente probabilmente perché ci sono fattori di tipo inibitorio che vengono rimossi anche se ci sono ancora molti studi in corso.
L’LH a livello gonadale inizia la sintesi degli steroidi gonadici, testosterone nel testicolo, estrogeni e progesterone nelle ovaie. Nella donna la secrezione di LH ed FSH è ciclica mentre nell’uomo questa ciclicità non c’è. Nella tarda età nella donna l’attività riproduttiva cessa, nella menopausa infatti la quantità di gameti femminili è stata consumata o comunque è andata incontro ad un processo degenerativo per cui la donna non è più in grado di concepire; l’uomo invece mantiene la sua attività maturativa anche al di là dei 60 anni.
Il GnRH è un decapeptide, una proteina di 10 aa. che tramite la circolazione portale ipofisaria raggiunge l’ipofisi dove induce sintesi e rilascio di LH ed FSH che sono due glicoproteine costituite da una sub unità alfa e una beta quindi sono etero dimeri e includono nella molecola anche residui carboidratici; la subunità alfa è costituita da uno stesso numero di aa. che sono sempre gli stessi e quindi questa subunità alfa è comune alla subunità alfa del TSH e della gonadotropina corionica CG, quella che cambia è la subunità beta che si differenzia sia per lunghezza in aa. che per sequenza.
Il GnRH induce a recettori specifici di membrana sulle cellule ipofisarie e la risposta che dà quando si lega è che va ad attivare il metabolismo dei fosfolipidi, in generale tutti i fattori di rilascio ipotalamici vanno ad attivare recettori di membrana connessi con l’attivazione dei fosfolipidi di membrana quindi formazione di DAG, attivazione proteina chinasi C e di IP3 ma anche attivazione dell’cAMP mentre LH ed FSH hanno recettori di membrana è il meccanismo di traduzione che attivano è quello dell’adenilato ciclasi con incremento di cAMP.
Leggi anche:
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Asse ipotalamo-ipofisi-surrene: funzionamento ed ormoni rilasciati
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Virilizzazione (mascolinizzazione): tipi, cause, sintomi, diagnosi e terapie
- Irsutismo: cause, sintomi, diagnosi e trattamenti
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Ormone della crescita (GH) a che serve e da cosa è prodotto?
- Ormone della crescita (GH): body building e doping in palestra
- Ormone della crescita (GH): effetti avversi nel body building e nello sport
- Quando essere troppo alti è una malattia: il gigantismo
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Cos’è l’adrenalina ed a cosa serve?
- L’altezza media italiana nel 2017 di maschi e femmine
- L’altezza media italiana 2017 da 1 a 19 anni di maschi e femmine
- L’altezza media mondiale nel 2017 di maschi e femmine [TABELLA]
- Altezza: quando si può parlare di nanismo o gigantismo
- Differenza tra midollo osseo e spinale
- Differenza tra sistema nervoso centrale e periferico: anatomia e funzioni in sintesi
- A cosa serve il midollo osseo?
- Differenza tra midollo osseo e cellule staminali
- Differenza tra midollo spinale e allungato
- Differenza tra epifisi, diafisi, metafisi ed ipofisi
- Quanto è alto l’uomo più alto del mondo?
- Quanto è alto l’uomo più basso del mondo?
- Nanismo: sintomi, cura, cause, terapia, diagnosi e prevenzione
- Charlotte, la bambina più piccola del mondo
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!
Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
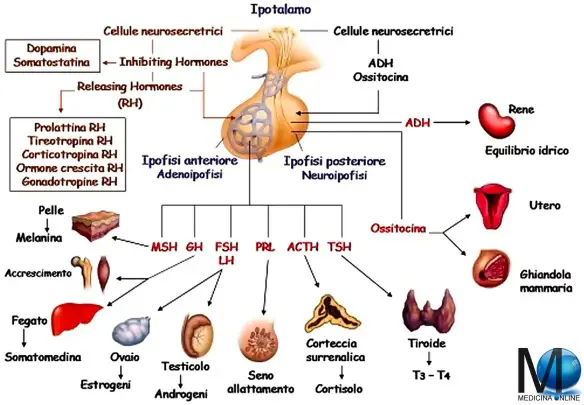
Fonte dell’immagine: dr. Mauro Amato – Centro Analisi Cliniche AMATO sas – Via Tattoli 6/o Molfetta (Bari)
Il SNC (sistema nervoso centrale), in funzione degli stimoli che riceve dall’esterno e dall’interno del nostro corpo, trasmette dei messaggi – tramite neurotrasmettitori – all’ipotalamo, che esercita a sua volta un influenza sulla ghiandola sottostante l’ipotalamo stesso, che si chiama ipofisi, attraverso altri neurotrasmettitori da esso liberati, in un complesso sistema che lega le due strutture, chiamato asse ipotalamo-ipofisario o asse ipotalamo-ipofisi (hypothalamic–pituitary axis in inglese).
L’ipotalamo appartiene al sistema nervoso centrale ma, da un punto di vista funzionale, i suoi neuroni sono capaci di ricevere segnali che arrivano sia dalle strutture nervose superiori, sia dalle ghiandole del sistema endocrino (ipofisi e gonadi per esempio), che non sono strutture nervose. Esso è quindi la sede in cui si verificano le connessioni tra sistema nervoso centrale e sistema endocrino (ormonale).
Gli ormoni prodotti dall’ipotalamo sono di natura proteica (mentre quelli prodotti dalle gonadi sono dei derivati del colesterolo, e quindi di natura lipidica) ed agiscono sull’ipofisi. Essa è suddivisa in due porzioni, una anteriore, o adenoipofisi, ed una posteriore, o neuroipofisi.
L’adenoipofisi è collegata all’ipotalamo da un sistema di vasi sanguigni nel quale vengono immessi gli ormoni ipotalamici che arrivano così all’ipofisi. Allo stesso modo, sempre attraverso questo sistema, gli ormoni prodotti dall’ipofisi possono giungere all’ipotalamo ed influenzarne la funzione.
Gli ormoni ipotalamici determinano, a livello dell’adenoipofisi, la sintesi, l’accumulo, quindi la immissione nel sangue di una serie di prodotti che vengono chiamate tropine in quanto agiscono su altre ghiandole del sistema endocrino che sono dipendenti dall’ipofisi (ovaio, testicolo, tiroide, mammella, corticale del surrene, funzione dell’ accrescimento ecc…).
Gli ormoni ipotalamici sono indicati come Relasing Hormones (RH) e cioè sostanze che stimolano la dismissione e l’ingresso nel sangue degli ormoni ipofisari.
Gli RH sono:
- Il GnRH o relasing hormone per le due gonadotropine ipofisarie LH ed FSH, agenti sulle ovaie per l’induzione dell’ovulazione;
- Un relasing hormone per la tireostimolina ipofisaria o TRH agente sulla tiroide;
- Un relasing hormone per l’ormone ipofisario della crescita o GHRH;
- Un relasing hormone per la tropina che stimola la corticale del surrene o CRH, inducendola a sua volta a produrre l’ormone cortisolo;
Allo stesso modo, esistono anche ormoni che inibiscono la secrezione dell’ipofisi qualora ciò risulti necessario.
Sotto lo stimolo o l’inibizione dell’ipotalamo, l’adenoipofisi produce una serie di ormoni o tropine di natura proteica ed altre sostanze, come per esempio le endorfine, che si trovano anche nel cervello ed hanno una struttura chimica che assomiglia a quella degli oppioidi.
Gli ormoni ipofisari sono rappresentati da:
- Gonadotropina FSH (ormone stimolante il follicolo);
- Gonadotropina LH (ormone luteinizzante);
- ICSH (ormone stimolante le cellule interstiziali del testicolo) nell’uomo;
- Prolattina, importante nella preparazione della ghiandola mammaria durante la gravidanza e nella sua funzione durante l’allattamento. Al di fuori dello stato gravidico, i livelli di prolattina non fisiologici possono influenzare negativamente i meccanismi della fertilità, quindi della riproduzione;
- Il TSH (tropina stimolante la tiroide);
- L’ACTH (tropina stimolante la corticale del surrene);
- Il GH (tropina stimolante l’accrescimento corporeo);
Inoltre, l’ipofisi produce peptidi oppioidi (endorfine) e fattori che influenzano il fegato ed il pancreas.
Le gonadotropine agiscono sulle gonadi (ovaio e testicolo). L’ovaio, sotto lo stimolo delle gonadotropine, secerne tre ormoni che derivano dal colesterolo: estrogeni, androgeni, progesterone e suoi derivati.
Esiste nell’ipofisi anche un lobo posteriore a struttura nervosa, chiamata neuroipofisi, a cui arrivano direttamente dall’ipotalamo, stavolta non attraverso il sangue ma tramite dei prolungamenti di neuroni, una serie di sostanze prodotte dai neuroni dell’ipotalamo stesso. Queste, vengono poi immesse nel circolo sanguigno ed hanno azioni su tutto l’organismo. Fra esse, le più importanti sono l’ADH o ormone antidiuretico o vasopressina, responsabile della ritenzione di sodio, e l’ossitocina, che stimola la contrazione della muscolatura dell’utero durante il parto e delle cellule muscolari (mioepiteliali) della mammella durante l’allattamento per favorire l’uscita del latte.
Per approfondire, continua la lettura con:
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisi-gonade: funzionamento ed ormoni rilasciati
- Asse ipotalamo-ipofisi-surrene: funzionamento ed ormoni rilasciati
- Asse ipotalamo-ipofisi-testicolo: funzionamento ed ormoni rilasciati
- Asse ipotalamo-ipofisi-tiroide: funzionamento ed ormoni rilasciati
- Vasopressina (ormone antidiuretico o ADH): funzioni e patologie
- Ormone adrenocorticotropo o corticotropina (ACTH) cos’è e quali sono le sue funzioni
- Ormone della crescita (GH) a che serve e da cosa è prodotto?
- Ormone della crescita (GH): body building e doping in palestra
- Ormone della crescita (GH): effetti avversi nel body building e nello sport
- TSH alto, basso e valori normali: qual è il significato clinico?
- Differenza tra ipotiroidismo primario, secondario e terziario
Leggi anche:
- Surrene: anatomia, funzioni e patologie in sintesi
- Cos’è l’adrenalina ed a cosa serve?
- Adrenalina e “combatti o fuggi”: ecco cosa accade nel nostro corpo quando siamo terrorizzati
- Differenza tra beta bloccanti, ace inibitori, calcio antagonisti, sartani e diuretici
- Testosterone basso, alto, valori normali ed interpretazione
- Ormoni estrogeni: cosa sono e quali funzioni svolgono?
- Progesterone: cos’è, a cosa serve, valori e quali funzioni ha in gravidanza?
- Quando la donna ha troppi peli dove non dovrebbero essere: irsutismo, cause, trattamenti e differenze con ipertricosi
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Differenze tra adrenalina e noradrenalina
- Apparato urinario: anatomia e fisiologia [SCHEMA]
- Rene: anatomia, funzioni e patologie in sintesi
- Differenza tra surrene e rene
- Dopammina: cos’è ed a che serve?
- Neurotrasmettitori: cosa sono ed a che servono
- Si può vivere senza reni? Conseguenze della nefrectomia
- Dopammina: biosintesi, rilascio nello spazio sinaptico e degradazione
- Sistema dopamminergico: i circuti nervosi della dopammina
- Quando essere troppo alti è una malattia: il gigantismo
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Differenza tra sistema nervoso centrale e periferico: anatomia e funzioni in sintesi
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Reddit, su Tumblr e su Pinterest, grazie!
