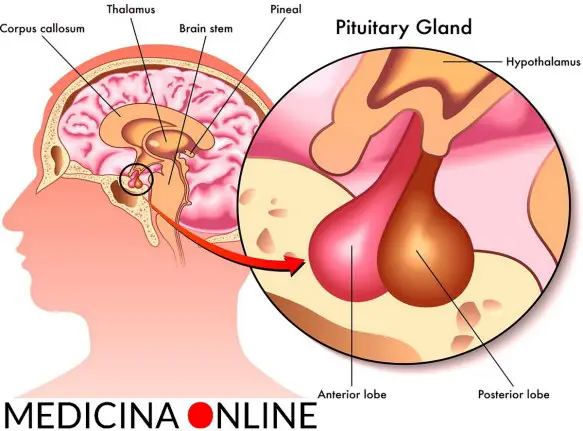
 L’ipofisi (con l’accento sulla o), anche chiamata ghiandola pituitaria (hypophysis o pituitary gland in inglese), è una ghiandola endocrina situata alla base del cranio, nella fossa ipofisaria della sella turcica dell’osso sfenoide. Si può dividere in due lobi, diversi per sviluppo embrionale, struttura e funzioni, che controllano – attraverso la secrezione di numerosi ormoni – l’attività endocrina e metabolica di tutto l’organismo:
L’ipofisi (con l’accento sulla o), anche chiamata ghiandola pituitaria (hypophysis o pituitary gland in inglese), è una ghiandola endocrina situata alla base del cranio, nella fossa ipofisaria della sella turcica dell’osso sfenoide. Si può dividere in due lobi, diversi per sviluppo embrionale, struttura e funzioni, che controllano – attraverso la secrezione di numerosi ormoni – l’attività endocrina e metabolica di tutto l’organismo:
- lobo anteriore (adenoipofisi): nello sviluppo embrionale si forma per invaginazione dell’ectoderma dello stomodeo (membrana faringea);
- lobo posteriore (neuroipofisi): formazione neuro-ectodermica diencefalica.
Essi sono divisi da una pars intermedia, piccola e poco vascolarizzata.
Anatomia della ghiandola pituitaria
La ghiandola si trova inferiormente al chiasma ottico. È di dimensioni abbastanza piccole e pesa non più di 0,9 g. È separata dall’encefalo da una porzione della dura madre, che la sovrasta ad ombrello e attraverso un peduncolo vascolo-nervoso comunica con l’ipotalamo, che regola attraverso altre sostanze ormonali l’ipofisi stessa. Intorno alla sella turcica si trovano i seni cavernosi da cui defluiscono le carotidi interne e i nervi cranici III, IV, V e VI; è facile immaginare che alterazioni a carico dell’ipofisi possono quindi causare diversi effetti secondari sulla funzione visiva (compromissione del chiasma), vascolare, neurologica.
Vasi sanguigni e nervi dell’ipofisi
L’ipofisi è irrorata da arterie ipofisarie, superiori e inferiori.
- Le arterie ipofisarie superiori nascono dal circolo di Willis e penetrano nel peduncolo ipofisario come arterie anteriori e posteriori che si capillarizzano nel peduncolo stesso e nell’infundibolo, dando origine a grappoli capillari. Questi ultimi si aprono in venule che portano nel lobo anteriore sboccando nei sinusoidi della parte distale. Si realizza così la circolazione portale ipofisaria che permette al sangue di scorrere in capillari situati nel peduncolo e nell’infundibolo prima di raggiungere, tramite le venule, la rete sinusoidale del lobo anteriore. In questo modo i fattori di rilascio o inibenti ipotalamici possono raggiungere, attraverso il sangue, l’adenoipofisi.
- Le arterie ipofisarie inferiori derivano dalla carotide interna e si distribuiscono con i loro rami al lobo anteriore ma specialmente a quello posteriore, senza entrare a far parte della circolazione portale.
- Le vene reflue dall’ipofisi fanno capo ai circostanti seni venosi della dura madre.
- Non sono presenti vasi linfatici nell’ipofisi.
- L’innervazione dell’adenoipofisi è povera ed è rappresentata solo da fibre vasomotrici originate dal plesso carotideo. La neuroipofisi, invece, riceve cospicui fasci ipotalamo-neuroipofisari e rami vasomotori.
Leggi anche:
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
Ipofisectomia
Per ben definire l’azione dell’ipofisi, secondo il metodo classico della fisiologia sperimentale, si è proceduto all’asportazione chirurgica della ghiandola in animali da laboratorio (ipofisectomia) . Gli effetti dell’ablazione del lobo anteriore sono in parte caratterizzati dalla diminuita attività delle altre ghiandole endocrine: la tiroide si atrofizza, e così pure i surreni e le gonadi, con scomparsa della spermatogenesi nel maschio e dell’ovulazione nella femmina; aumenta la sensibilità all’insulina per la compromissione delle isole pancreatiche, e insorge una lieve forma di diabete insipido. L’ipofisectomia comporta inoltre arresto dello sviluppo somatico negli animali giovani, con alterazioni scheletriche e muscolari. Queste osservazioni hanno permesso di individuare i diversi ormoni secreti dall’ipofisi.
Leggi anche:
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
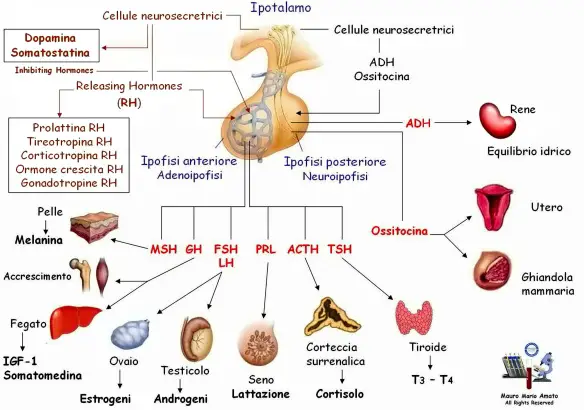
Fonte dell’immagine: dr. Mauro Amato – Centro Analisi Cliniche AMATO sas – Via Tattoli 6/o Molfetta (Bari)
Ormoni secreti dall’ipofisi
1) Ormoni agenti su organi e cellule bersaglio
Sono prodotti dalle cellule acidofile dell’adenoipofisi.
- Dalle cellule alfa l’ormone somatotropo (anche chiamato “somatotropina“, “ormone della crescita“, STH, oppure SH o GH (da “growth hormone”) o hGH (da “human growth hormone”)agisce direttamente sui tessuti ed è indipendente dall’attività delle altre ghiandole endocrine; stimola la deposizione del calcio nel tessuto osseo e la proliferazione delle cellule cartilaginee, aumenta la massa dei muscoli scheletrici e stimola la sintesi proteica. È detto anche ormone della crescita e la sua mancanza causa l’arresto dello sviluppo staturale e ponderale dell’individuo.
- Dalle cellule epsilon la prolattina (PRL) agisce sulla ghiandola mammaria stimolando la secrezione di latte dopo il parto.
- L’ormone melanotropo (MSH) ha effetto trofico sui melanociti, responsabili della pigmentazione della pelle. A differenza degli altri ormoni ipofisiari della sua classe questo è prodotto dalle cellule basofile dell’adenoipofisi
2) Ormoni trofici
Gli ormoni trofici sono ormoni glicoproteici (PAS positivi) che agiscono su altre ghiandole endocrine, e sono prodotti dalle cellule basofile:
- Dalle cellule delta l’ormone tireotropo (anche chiamato “ormone tireostimolante”, “ormone tireotropo”, “tireotropina” o “TSH”) agisce sulla tiroide, favorendo la liberazione degli ormoni che questa produce (tiroxina e triiodotironina).
- L’ormone adrenocorticotropo (“ACTH” o “corticotropina”) determina a sua volta la sintesi e la secrezione molto rapida degli ormoni della corteccia surrenale e stimola il metabolismo lipidico.
- Dalle cellule beta e gamma rispettivamente l’ormone follicolo-stimolante (FSH) e l’ormone luteinizzante (LH) sono invece gonadotropi (agiscono cioè sulle gonadi); nelle ovaie il primo stimola la formazione dei follicoli e la secrezione dei loro ormoni (estrogeni), il secondo la formazione del corpo luteo e la secrezione dell’ormone corrispondente, il progesterone; nel testicolo, l’LH agisce invece sulle cellule interstiziali (e viene perciò anche contraddistinto con la sigla ICSH), promuovendo la spermatogenesi e la secrezione dell’ormone testicolare (testosterone), mentre l’FSH favorisce la sintesi di una proteina (ABP) che lega il testosterone, attivando gli spermatozoi.
Patologie dell’ipofisi
Se questi meccanismi di regolazione sono alterati, o se l’ipofisi è in qualche modo danneggiata, si può verificare un’eccessiva produzione di ormoni (iperpituitarismo) o una loro carenza (ipopituitarismo).
- L’ipopituitarismo, in soggetti giovani, si manifesta essenzialmente con il nanismo ipofisario che dipende da deficienza di ormone somatotropo; se la deficienza riguarda invece l’ACTH si ha insufficienza surrenale, con diminuita capacità dell’organismo di rispondere alle infezioni e agli stress.
- L’iperpituitarismo, dovuto in genere ai tumori all’adenoipofisi, riguarda anch’esso gli ormoni somatotropo e corticotropo. L’eccesso di ormone somatotropo determina due fenomeni diversi: se l’ipersecrezione esordisce prima della maturazione delle ossa lunghe, lo scheletro continua ad accrescersi dando luogo alla caratteristica sindrome del gigantismo (alcuni giovani pazienti raggiungono altezze di 2,10-2,40 m); se invece la malattia insorge dopo la maturazione dell’organismo e dello scheletro, si manifesta acromegalia (aumento delle dimensioni dei segmenti ossei periferici) con dorso ricurvo, mascella prominente, mani e piedi enormemente sviluppati. Quando l’iperpituitarismo riguarda l’ormone corticotropo (ACTH), si verifica una iperplasia dei surreni (sindrome di Cushing), che dà luogo alla caratteristica faccia a “luna piena”, addome prominente, acne, irsutismo (vedi ipertricosi) e assottigliamento delle ossa.
Leggi anche:
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Asse ipotalamo-ipofisi-gonade: funzionamento ed ormoni rilasciati
- Asse ipotalamo-ipofisi-surrene: funzionamento ed ormoni rilasciati
- Asse ipotalamo-ipofisi-tiroide: funzionamento ed ormoni rilasciati
- Ormone della crescita (GH) a che serve e da cosa è prodotto?
- Ormone della crescita (GH): body building e doping in palestra
- Ormone della crescita (GH): effetti avversi nel body building e nello sport
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Cos’è l’adrenalina ed a cosa serve?
- Quando essere troppo alti è una malattia: il gigantismo
- Tiroide: anatomia, funzioni e patologie in sintesi
- Paratiroidi: anatomia e funzioni in sintesi
- Differenza tra tiroide e paratiroide
- Differenza tra midollo osseo e spinale
- Differenza tra sistema nervoso centrale e periferico: anatomia e funzioni in sintesi
- A cosa serve il midollo osseo?
- Differenza tra midollo osseo e cellule staminali
- Differenza tra midollo spinale e allungato
- Differenza tra epifisi, diafisi, metafisi ed ipofisi
- Paratiroidectomia: intervento, convalescenza e conseguenze
- L’altezza media italiana nel 2017 di maschi e femmine
- L’altezza media italiana 2017 da 1 a 19 anni di maschi e femmine
- L’altezza media mondiale nel 2017 di maschi e femmine [TABELLA]
- Altezza: quando si può parlare di nanismo o gigantismo
- Quanto è alto l’uomo più alto del mondo?
- Quanto è alto l’uomo più basso del mondo?
- Nanismo: sintomi, cura, cause, terapia, diagnosi e prevenzione
- Charlotte, la bambina più piccola del mondo
- Morbo di Parkinson: cause, sintomi, decorso, terapie
- Morbo di Alzheimer: cause, sintomi, decorso, terapie
- Differenza tra morbo di Alzheimer e morbo di Parkinson: sintomi comuni e diversi
- Differenza tra morbo di Alzheimer, demenza senile, vascolare e reversibile
- Demenza senile: cause, sintomi, decorso e cure
- Cervelletto: anatomia esterna ed interna
- Cervelletto: le lesioni cerebellari più comuni
- Le funzioni del cervelletto: apprendimento e correzione dei movimenti del corpo
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!

 Le patologie che possono colpire l’ipotalamo o l’ipofisi sono molte e differenti ma portano tutte alla medesima situazione : una iperfunzione o una ipofunzione del sistema ipotalamo-ipofisi.
Le patologie che possono colpire l’ipotalamo o l’ipofisi sono molte e differenti ma portano tutte alla medesima situazione : una iperfunzione o una ipofunzione del sistema ipotalamo-ipofisi.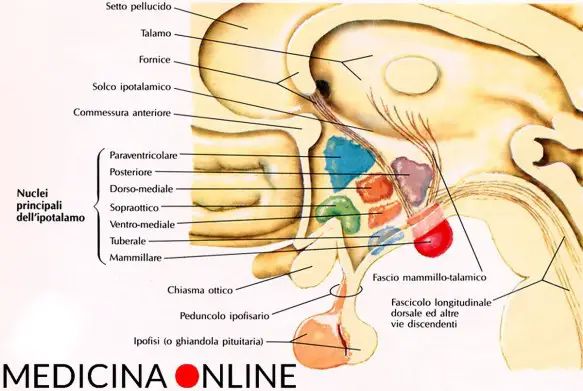 L’ipotalamo e l’ipofisi sono due strutture anatomiche, strettamente collegate fra loro, situate alla base del cranio. Si tratta di due strutture che rappresentano la più importante area di interconnessione fra il sistema nervoso e il sistema endocrino da cui partono gli impulsi e gli stimoli ormonali che governano l’intero sistema endocrino.
L’ipotalamo e l’ipofisi sono due strutture anatomiche, strettamente collegate fra loro, situate alla base del cranio. Si tratta di due strutture che rappresentano la più importante area di interconnessione fra il sistema nervoso e il sistema endocrino da cui partono gli impulsi e gli stimoli ormonali che governano l’intero sistema endocrino.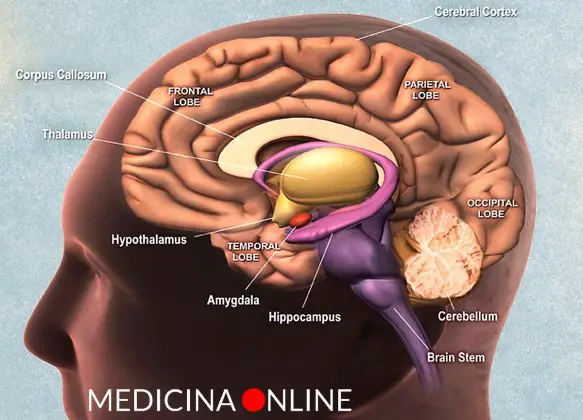 L’ipotalamo (hypothalamus in inglese) è una struttura del SNC (sistema nervoso centrale), situata nella zona centrale interna ai due emisferi cerebrali, e costituisce la parte ventrale del diencefalo. L’ipotalamo comprende molti nuclei che attivano, controllano e integrano i meccanismi autonomici periferici, l’attività endocrina e molte funzioni somatiche tra cui:
L’ipotalamo (hypothalamus in inglese) è una struttura del SNC (sistema nervoso centrale), situata nella zona centrale interna ai due emisferi cerebrali, e costituisce la parte ventrale del diencefalo. L’ipotalamo comprende molti nuclei che attivano, controllano e integrano i meccanismi autonomici periferici, l’attività endocrina e molte funzioni somatiche tra cui: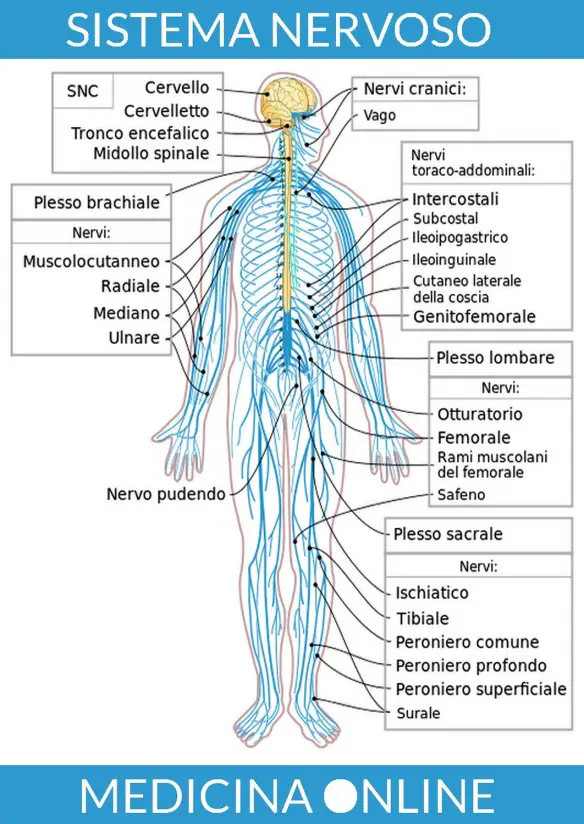 Il sistema nervoso negli esseri umani può essere anatomicamente suddiviso in
Il sistema nervoso negli esseri umani può essere anatomicamente suddiviso in
 C’è un luogo a Roma, dove ci si prende cura delle vite spezzate. Si chiama
C’è un luogo a Roma, dove ci si prende cura delle vite spezzate. Si chiama