 Cos’è la poliomielite e come si trasmette?
Cos’è la poliomielite e come si trasmette?
La poliomielite è una grave malattia infettiva altamente contagiosa che colpisce il sistema nervoso centrale e si trasmette per via oro-fecale (attraverso l’ingestione di prodotti contaminati, tramite saliva dei soggetti ammalati o tramite contatto con le feci di persone colpite dal virus). La poliomielite è stata riconosciuta come malattia da Jakob Heine nel 1840, mentre il suo agente eziologico, il poliovirus, è stato identificato nel 1908 da Karl Landsteine.
Leggi anche: Il calendario delle vaccinazioni obbligatorie per i vostri figli
Classificazione della poliomielite
La poliomielite si presenta, generalmente, in tre forme distinte: la prima (poliomielite abortiva) porta solo a febbre alta senza interessare il sistema nervoso, la seconda (meningite asettica) porta a una paralisi lieve e momentanea, mentre la terza – che è la forma più grave in assoluto – comporta sia febbre che “paralisi flaccida” acuta che porta gli arti inferiori a perdere molto velocemente tono muscolare fino a diventare, appunto, flaccide (oltre che paralizzate).
Sintomi della poliomielite
Sebbene circa il 90% delle infezioni da polio non causi sintomi, gli individui affetti possono presentare una serie di condizioni se il virus entra nella circolazione sanguigna. In circa l’1% dei casi, il virus penetra nel sistema nervoso centrale, dove colpisce di preferenza i neuroni motori, portando a debolezza muscolare e paralisi flaccida acuta. A seconda dei nervi coinvolti, possono presentarsi diversi tipi di paralisi. La polio spinale è la forma più comune, caratterizzata da paralisi asimmetrica che spesso coinvolge le gambe. La polio bulbare porta alla debolezza dei muscoli innervati dai nervi cranici. La polio bulbospinale è una combinazione di paralisi bulbare e spinale.
Leggi anche: Febbre alta nei bambini e neonati: quali farmaci e cosa fare
Cause della poliomielite
La poliomielite è causata dall’infezione con un virus appartenente al genere degli enterovirus, noto come poliovirus (PV). Questi virus a RNA colonizzano il tratto gastrointestinale, specificamente l’orofaringe e l’intestino. Il periodo di incubazione, ovverosia il tempo tra la prima esposizione e i primi sintomi, varia da tre a 35 giorni, con un arco più comune che va dai sei ai venti giorni. Il poliovirus infetta e provoca la malattia soltanto negli esseri umani. La sua struttura è molto semplice: è composto da un genoma a RNA racchiuso in un involucro proteico chiamato capside. Oltre a proteggere il materiale genetico del virus, le proteine del capside consentono al poliovirus di infettare alcuni tipi di cellule. Tre sierotipi di poliovirus sono stati identificati: il poliovirus di tipo 1 (PV1), di tipo 2 (PV2) e di tipo 3 (PV3), ognuno con una proteina del capside leggermente diversa. Tutti e tre sono estremamente virulenti e producono gli stessi sintomi della malattia. PV1 è la forma che si riscontra più frequente e quella più strettamente correlata alla paralisi. Gli individui che sono esposti al virus, tramite infezione o tramite l’immunizzazione con il vaccino antipolio, sviluppano l’immunità. Negli individui immuni, gli anticorpi IgA contro il poliovirus sono presenti nelle tonsille e nel tratto gastrointestinale e sono in grado di bloccare la replicazione del virus mentre gli anticorpi IgG e IgM possono prevenire la diffusione del virus ai neuroni motori del sistema nervoso centrale. L’infezione o la vaccinazione con un sierotipo di poliovirus non fornisce immunità contro gli altri sierotipi e l’immunità completa richiede l’esposizione a ciascun sierotipo.
Leggi anche: Meningite batterica e virale: sintomi, profilassi, cura e vaccini
Trasmissione della poliomielite
La poliomielite è altamente contagiosa e si può trasmettere per via oro-orale (fonte orofaringea) e fecale-orale (di origine intestinale). Nelle aree endemiche, il poliovirus può infettare praticamente l’intera popolazione umana. Il virus si presenta per lo più stagionalmente nelle fasce climatiche temperate, con il picco di trasmissione che si verifica in estate e in autunno. Queste differenze stagionali sono molto meno pronunciate nelle aree tropicali. Il periodo di incubazione è di solito compreso tra sei e venti giorni, con un intervallo massimo che va dai tre ai trentacinque giorni. Dopo l’infezione iniziale le particelle virali sono escrete, per diverse settimane, con le feci, che pertanto risultano infette. La malattia si trasmette principalmente per via fecale-orale, con l’ingestione di cibo contaminato o acqua. Talvolta viene trasmessa via oro-orale, una modalità di trasmissione più comune nelle zone in cui vi è una buona igiene. La poliomielite è maggiormente infettiva tra i sette e i dieci giorni prima e dopo la comparsa dei sintomi, ma la trasmissione è possibile finché il virus rimane nella saliva o nelle feci. I fattori che aumentano il rischio di infezione da polio o influenzano la gravità della malattia comprendono: deficienza immunitaria, malnutrizione, tonsillectomia, attività fisica subito dopo l’inizio della paralisi, lesioni muscolo-scheletriche a causa di iniezione di vaccini e la gravidanza. Anche se il virus può attraversare la placenta, il feto non sembra essere influenzato da una infezione materna o dalla vaccinazione contro la polio. Anche gli eventuali anticorpi materni possono attraversare la placenta, fornendo l’immunità passiva che protegge il neonato dalle infezioni da polio durante i primi mesi di vita. Come precauzione contro le infezioni, durante le epidemie di poliomielite le piscine pubbliche delle zone colpite sono state spesso chiuse.
Diagnosi della poliomielite
La poliomielite paralitica può essere clinicamente sospettata in individui che con insorgenza acuta di paralisi flaccida a livello di uno o più arti e riflessi tendinei diminuiti o assenti negli arti colpiti, con conservazione delle funzioni sensoriale o cognitiva e in assenza di altre cause apparenti. Una diagnosi di laboratorio può essere effettuata in seguito all’isolamento del poliovirus in un campione di feci o in un tampone faringeo. Gli anticorpi anti-poliovirus possono essere trovati nel sangue durante la fase infettiva. L’analisi del liquido cerebrospinale (CSF) del paziente, prelevato tramite puntura lombare, mostra un elevato numero di globuli bianchi (principalmente linfociti) e un lieve incremento nella concentrazione proteica. L’individuazione del virus nel liquor attesta l’avvenuta infezione del sistema nervoso centrale ed è pertanto diagnostica per la polio paralitica, sebbene ciò si verifichi raramente. Se il poliovirus è isolato da un paziente che presenta paralisi flaccida acuta, viene ulteriormente testato tramite mappatura genetica o, più recentemente, mediante reazione polimerasica a catena (PCR), per determinare se esso è “wild type” (cioè, il virus che si incontra in natura) o “da vaccino” (derivato da un ceppo del virus della poliomielite utilizzato per produrre il vaccino antipolio). È importante determinare l’origine del virus, poiché per ogni caso segnalato di polio paralitica causato da poliovirus selvaggi si stima che possano esistere altri 200 a 3000 portatori asintomatici contagiosi.
Vaccino poliomielite
Il vaccino anti-polio, contro la poliomielite, come quella contro la difterite, l’epatite b e il tetano fa parte delle vaccinazioni obbligatorie per i neonati. Per l’immunizzazione dei nuovi nati, infatti, viene utilizzato il vaccino esavalente che viene somministrato in tre dosi, da praticare entro il primo anno di vita (al 3, 5 e 11 mesi), e in un richiamo da effettuare tra il 5 e i 6 anni. Esistono due tipi diversi di vaccino, quello inattivato (o di Salk) e quello vivo attenuato (o di Sabin), ma in Italia viene praticato solo il primo, mentre il Ministero della Salute mantiene una scorta del secondo in caso di emergenza.
Leggi anche: Febbre dopo vaccino: come curarla e quanto dura?
Controindicazioni vaccino
Non esistono controindicazioni alla vaccinazione nei bambini sani che possono essere vaccinati senza alcun pericolo. Se sono invece presenti malattie infettive in forme acute, con febbre o con diarrea, è preferibile rimandare la vaccinazione al momento in cui il piccolo abbia recuperato la buona salute. Oltre a questo, poi, è consigliato attendere almeno 4 settimane dall’iniezione prima di sottoporsi all’asportazione di tonsille o adenoidi.
Leggi anche:
- Vaccini anti meningite: quanti sono, quando farli, quali sono indispensabili, effetti collaterali
- Cos’è il vaccino esavalente? Quando, come e perché farlo?
- Vaccini: servono davvero? Tutte le verità scientifiche
- Differenza tra virus e batteri: chi è più pericoloso? Diagnosi, sintomi e terapia
- Sistema immunitario, immunità innata e specifica: riassunto, schema e spiegazione
- Immunodeficienza primaria e secondaria: sintomi, cause e terapie
- Immunità innata (aspecifica): barriere, infiammazione e complemento
- Immunità innata (aspecifica): neutrofili, macrofagi e linfociti natural killer
- Immunità specifica (acquisita): linfociti, T killer, T helper, T γδ, B ed anticorpi
- Immunità specifica (acquisita): memoria passiva, attiva ed immunizzazione
- Immunità specifica (acquisita) umorale e cellulare
- Patologie del sistema immunitario: immunodeficienze, autoimmunità ed ipersensibilità
- Anticorpi: (immunoglobuline): tipi, caratteristiche e funzioni
- Differenza tra antigene, aptene allergene ed epitopo
- Aptene: cos’è e perché è importante per il sistema immunitario
- Antigene: cos’è e perché è importante per il sistema immunitario
- Differenza tra antigeni esogeni, endogeni, tumorali, nativi ed autoantigeni
- Epitopi sequenziali e conformazionali: cosa sono e come funzionano
- Differenza tra allele dominante e recessivo
- HIV: dopo quanto si manifestano i sintomi? I 4 stadi dell’infezione
- Differenza tra HIV e AIDS: sono uguali?
- Si muore di AIDS? Qual è l’aspettativa di vita?
- HIV: sintomi iniziali in donne e uomini
- Differenza tra malattia, sindrome e disturbo con esempi
- Differenza tra virus HIV1 e HIV2
- Sesso e AIDS: l’HIV si trasmette anche tramite il rapporto orale
- Il liquido pre-eiaculatorio può indurre gravidanza e trasmettere l’HIV?
- HIV e AIDS: come, dove e quando si eseguono i test per la diagnosi?
- Smegma: i rischi dell’accumulo di sporco sul pene
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!

 Vicino ad Amsterdam, nei Paesi Bassi, esiste una piccola città con 23 case, alcuni ristoranti, vari caffè, negozi, un salone di bellezza, un teatro e un cinema. Questa città si chiama Hogewey ed al suo interno ci vivono attualmente 152 persone, tutte anziane, e tutte affette da una grave demenza o da uno stadio avanzato di Alzheimer. Hogewey è letteralmente una casa di cura organizzata come un piccolo paese, così da permettere ai pazienti di condurre una vita quasi normale e di sentirsi a casa, e di ricevere nello stesso tempo le cure necessarie. Hogewey è stata fondata nel 2009 e da allora è diventata, specie per la sua particolare natura, un punto di riferimento importante a livello mondiale anche tra gli studiosi della demenza.
Vicino ad Amsterdam, nei Paesi Bassi, esiste una piccola città con 23 case, alcuni ristoranti, vari caffè, negozi, un salone di bellezza, un teatro e un cinema. Questa città si chiama Hogewey ed al suo interno ci vivono attualmente 152 persone, tutte anziane, e tutte affette da una grave demenza o da uno stadio avanzato di Alzheimer. Hogewey è letteralmente una casa di cura organizzata come un piccolo paese, così da permettere ai pazienti di condurre una vita quasi normale e di sentirsi a casa, e di ricevere nello stesso tempo le cure necessarie. Hogewey è stata fondata nel 2009 e da allora è diventata, specie per la sua particolare natura, un punto di riferimento importante a livello mondiale anche tra gli studiosi della demenza. Tanti pazienti vengono da me allarmati da una sorta di contrazione involontaria ripetuta, che avvertono spesso nell’ultimo periodo. Nella maggioranza dei casi, questi pazienti si riferiscono al mioclono: di cosa si tratta?
Tanti pazienti vengono da me allarmati da una sorta di contrazione involontaria ripetuta, che avvertono spesso nell’ultimo periodo. Nella maggioranza dei casi, questi pazienti si riferiscono al mioclono: di cosa si tratta? Sembra che a breve sarà possibile diagnosticare l’Alzheimer grazie ad un’analisi del sangue specifica che misura il tasso di peptide amiloide il cui livello nel sangue, secondo alcuni ricercatori spagnoli (agenzia spagnola di Araclon), è direttamente proporzionale alla possibilità di sviluppare la malattia. La spagnola Araclon ha sviluppato e brevettato un kit che consente di trovare 40-42 peptidi di beta amiloide nel sangue (ABtest) e stanno procedendo con degli studi su un campione di 400 persone per riuscire a dimostrare che l’ABtest è uno strumento in grado di diagnosticare l’Alzheimer. Il test potrebbe infatti distinguere i soggetti completamenti sani da quelli che presentano già un deficit cognitivo precursore della malattia.
Sembra che a breve sarà possibile diagnosticare l’Alzheimer grazie ad un’analisi del sangue specifica che misura il tasso di peptide amiloide il cui livello nel sangue, secondo alcuni ricercatori spagnoli (agenzia spagnola di Araclon), è direttamente proporzionale alla possibilità di sviluppare la malattia. La spagnola Araclon ha sviluppato e brevettato un kit che consente di trovare 40-42 peptidi di beta amiloide nel sangue (ABtest) e stanno procedendo con degli studi su un campione di 400 persone per riuscire a dimostrare che l’ABtest è uno strumento in grado di diagnosticare l’Alzheimer. Il test potrebbe infatti distinguere i soggetti completamenti sani da quelli che presentano già un deficit cognitivo precursore della malattia. Nella nona stagione del telefilm Grey’s Anatomy, la dottoressa Arizona Robbins – interpretata da Jessica Capshaw – si trova a fare i conti con l’amputazione di una gamba (in seguito ad i severi traumi riportati in un incidente aereo) ed a tutti i disagi che ne conseguono, tra cui il soffrire della “sindrome dell’arto fantasma”. Esiste davvero questa sindrome? Di cosa si tratta esattamente?
Nella nona stagione del telefilm Grey’s Anatomy, la dottoressa Arizona Robbins – interpretata da Jessica Capshaw – si trova a fare i conti con l’amputazione di una gamba (in seguito ad i severi traumi riportati in un incidente aereo) ed a tutti i disagi che ne conseguono, tra cui il soffrire della “sindrome dell’arto fantasma”. Esiste davvero questa sindrome? Di cosa si tratta esattamente?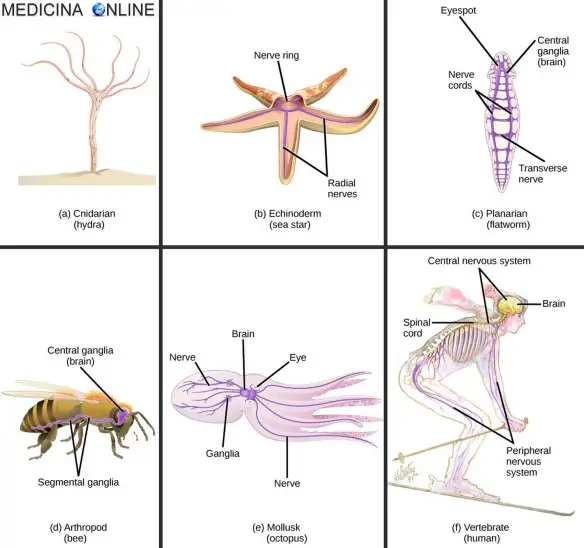 Il sistema nervoso degli invertebrati è di varia complessità: il più semplice modello organizzativo di sistema nervoso lo
Il sistema nervoso degli invertebrati è di varia complessità: il più semplice modello organizzativo di sistema nervoso lo