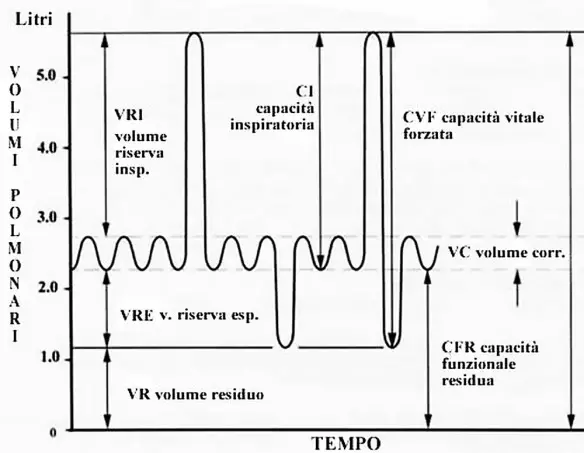
 Sono molti i parametri che possono essere misurati durante un esame spirometrico, i più frequenti sono:
Sono molti i parametri che possono essere misurati durante un esame spirometrico, i più frequenti sono:
- la Capacità Vitale (VC);
- la Capacità Vitale Forzata (FVC);
- il Volume Espiratorio Forzato (FEV) all’intervallo di 0.5, 1 (FEV1), 2, e 3 secondi;
- il Flusso Espiratorio Forzato al 25–75% (FEF 25–75);
- la Massima Ventilazione Volontaria (MVV), anche conosciuta come Massima Capacità Respiratoria.
Altri test possono essere eseguiti in situazioni particolari. I risultati sono generalmente forniti sia come dati grezzi (litri, litri al secondo) ed in percentuale rispetto ai valori predetti o attesi per i pazienti che hanno caratteristiche simili (altezza, età, sesso e, talvolta, razza e peso). L’interpretazione dei risultati può variare a seconda del medico e della fonte dei valori previsti. In generale, i risultati prossimi al 100% del valore predetto sono assolutamente normali, e spesso risultati oltre l’80% del valore atteso sono considerati normali. Tuttavia i risultati devono essere sempre correlati dal medico con anamnesi ed esame obiettivo del paziente, oltre ad altri eventuali esami come un RX torace.
Leggi anche: Differenza tra inspirazione e espirazione: l’atto respiratorio
Grado di reversibilità della broncocostrizione
Spesso, in determinate circostanze, si deve somministrare un broncodilatatore per via inalatoria e si esegue un confronto tra la prova ed il relativo grafico pre e post stimolo broncodilatatorio, per verificare l’efficacia del broncodilatatore ed il cosiddetto grado di reversibilità della broncocostrizione.
Altre tecniche
La capacità funzionale residua (FRC) non può essere misurata mediante la spirometria, ma può comunque essere misurata con un pletismografo oppure con un test di diluizione (ad esempio, la prova di diluizione dell’elio).
Leggi anche: Apparato respiratorio: anatomia in sintesi, struttura e funzioni
Capacità vitale forzata (FVC)
La capacità vitale forzata (FVC) è il volume di aria che può essere espirato con uno sforzo massimale, dopo che il paziente ha eseguito una piena ispirazione, misurata in litri.[20] La FVC è una manovra fondamentale nei test di spirometria.
Volume espiratorio massimo in 1 secondo (VEMS o FEV1)
Il FEV1 è il volume di aria che può essere espirato con uno sforzo massimale in un secondo, dopo che il paziente ha eseguito una piena ispirazione. I valori medi di FEV1 in persone sane dipendono principalmente dal sesso e dall’età. Valori compresi tra 80% e 120% del valore medio sono considerati normali. I valori normali previsti per il FEV1 possono essere calcolato online, dipendono da età, sesso, altezza, massa corporea ed etnia, e presentano anche alcune variazioni in base allo studio di ricerca.
Rapporto FEV1/FVC (FEV1%)
Il FEV1/FVC (FEV1% o Indice di Tiffeneau) è il rapporto tra il FEV1 e la FVC. In adulti sani questo rapporto dovrebbe essere di circa il 75-80%. Nelle malattie ostruttive (asma bronchiale, BPCO, bronchite cronica, enfisema) il FEV1 è diminuito a causa della maggiore resistenza delle vie aeree al flusso espiratorio. Nelle medesime malattie anche la FVC può essere diminuita, a causa della chiusura prematura della vie aeree durante l’espirazione, ma non nella stessa proporzione del FEV1. Tipicamente in queste malattie sia la FEV1 che la FVC sono ridotti, ma il primo è più colpito, a causa della maggiore resistenza delle vie aeree.
Leggi anche: Differenza tra ventilazione polmonare e alveolare: spazio morto anatomico e fisiologico
Flusso espiratorio forzato (FEF)
Il flusso espiratorio forzato (FEF) è il flusso (o velocità) con cui l’aria esce dal polmone durante la parte centrale di una espirazione forzata. Può essere misurato ad intervalli discreti (definiti) della capacità vitale forzata (FVC). Gli intervalli usuali sono 25%, 50% e 75% (FEF25, FEF50 e FEF75), o il 25% e il 50% della FVC. Può anche essere misurato come media del flusso durante un intervallo, generalmente delimitato da quante specifiche frazioni rimangono della FVC, di solito 25-75% (FEF25-75%). La gamma delle medie nella popolazione sana dipendono principalmente dal sesso e dall’età. Valori compresi tra 50-60% e fino al 130% della media sono considerati normali. I valori normali previsti per il FEF può essere calcolato online e dipendono dall’età, dal sesso, da altezza, massa ed etnia nonché da alcune variabili da studio di ricerca a studio di ricerca. MMEF o MEF è sinonimo di massimo (a metà) flusso espiratorio ed è il picco di flusso espiratorio, ricavato dalla curva flusso-volume e misurato in litri al secondo. Dovrebbe essere teoricamente identico al picco di flusso espiratorio (PEF), che è, invece, generalmente valutato con l’ausilio di un misuratore di picco e misurato in litri al minuto. Ricerche recenti suggeriscono che il FEF25 -75 % o FEF25 -50 % possa essere un parametro più sensibile rispetto al FEV1 (VEMS) nell’evidenziare la malattia ostruttiva a carico delle piccole vie aeree.Comunque, in assenza di concomitanti variazioni di altri marcatori standard, il rilevare alcune discrepanze nel flusso espiratorio centrale (il FEF 25-75%) potrebbe non essere sufficientemente specifico per parlare di malattia ostruttiva e, pertanto, le attuali indicazioni sottolineano l’opportunità di continuare ad utilizzare altri parametri (FEV1, VC, e FEV1/VC) come indicatori di malattia ostruttiva.
Flusso inspiratorio forzato 25–75% o 25–50%
Il flusso inspiratorio forzato 25–75% o 25–50% (FIF 25–75% o 25–50%) è per molti aspetti simile al FEF 25–75% or 25–50%, tranne, ovviamente, per il fatto che la misura viene presa durante la fase inspiratoria.
Flusso di picco espiratorio (PEF)
Il flusso di picco espiratorio (PEF) è il flusso (o la velocità) massima che può essere raggiunta durante l’esecuzione di una espirazione forzata che viene iniziata dopo una inspirazione completa, misurata in litri al minuto oppure in litri al secondo.
Leggi anche: Spirometria diretta ed indiretta: come si esegue ed a cosa serve
Volume corrente (VC)
Il volume corrente (in inglese tidal volume – TV) corrisponde al totale di aria inalata ed esalata normalmente con l’attività respiratoria.
Capacità polmonare totale (CPT)
La capacità polmonare totale (in inglese total lung capacity – TLC) equivale alla quantità (volume) massima d’aria presente nei polmoni.
Capacità di diffusione (DLCO)
La capacità di diffusione (o DLCO) equivale all’assorbimento di monossido di carbonio (CO) a seguito di un singolo respiro che viene effettuato per un tempo standard (in genere 10 secondi). Poiché l’aria è costituita da una quantità estremamente ridotta (tracce) di CO, è stato assunto il tempo di 10 secondi come tempo standard per l’inalazione, la quale deve essere poi seguita da una rapida espirazione. Il gas esalato dal paziente viene poi testato per determinare in quale quantità il gas tracciante sia stato assorbito durante il singolo respiro di 10 secondi. Questa prova è in grado di evidenziare eventuali alterazioni della capacità di diffusione come, ad esempio, può avvenire in caso di fibrosi polmonare. Si deve ricordare che questo parametro non ha un valore assoluto ma che deve essere correlato a determinate condizioni cliniche del paziente. In caso di anemia, ad esempio, il valore ottenuto necessita di essere corretto. L’anemia infatti altera il parametro in quanto la rapida diffusione del monossido di carbonio (CO) dipende dalla concentrazione di emoglobina contenuta nei globuli rossi: in caso di bassa concentrazione di emoglobina (ovvero in caso di anemia) si avrà una alterata e falsa riduzione del valore di DLCO). Nel caso, invece, di emorragia polmonare, si verifica un eccesso di eritrociti nell’interstizio o negli alveoli: queste cellule, dato l’alto contenuto di emoglobina, sono ovviamente in grado di assorbire la CO e artificiosamente dare un valore aumentato della capacità DLCO). La pressione atmosferica e/o l’altitudine sul livello del mare possono influire sulla misura di DLCO che viene registrata: si rende quindi necessario un fattore di correzione che tenga conto di questi valori. Sono disponibili online dei calcolatori che correggono le misure sulla base dei livelli di emoglobina e di altitudine e/o pressione con i quali è stata rilevata la misura.
Massima ventilazione volontaria (MVV)
La massima ventilazione volontaria (MVV) è una misura della quantità massima di aria che può essere inspirata ed espirata nell’arco temporale di un minuto. Una simile massima ventilazione può determinare discomfort nel paziente esaminato. Al fine di rendere più agevole l’esame per il paziente, la prova viene fatta eseguire per una durata massima di 15 secondi. I valori ottenuti vengono quindi estrapolati ad un valore per una prova di durata di un minuto ed espressi in litri/minuto. I valori medi per soggetti di sesso maschile sono pari a 140-180 litri/minuto e si riducono a valori di 80-120 litri/minuto in soggetti di sesso femminile.
Leggi anche:
Compliance polmonare statica (Cst)
Quando l’obiettivo è stimare la compliance polmonare statica, è necessario che alle canoniche misurazioni di volume effettuate attraverso lo spirometro si associno delle misurazioni simultanee della pressione transpolmonare effettuate grazie alla integrazione dello spirometro con dei trasduttori di pressione. Una volta costruita la curva con le relazioni tra le variazioni di volume e le relative variazioni di pressione transpolmonare, la Cst si ottiene valutando la pendenza della curva ad un dato volume, oppure, matematicamente, si ottiene dal differenziale ΔVolume/Δpressione. La compliance polmonare statica è probabilmente il parametro più sensibile per mettere in evidenza una meccanica polmonare anormale. È considerato nei limiti di norma se è compreso tra il 60% ed il 140% del valore medio della popolazione per una persona di simile età, sesso e composizione corporea.Nei soggetti in insufficienza respiratoria acuta ed in ventilazione meccanica, “la compliance statica del sistema respiratorio totale viene convenzionalmente ottenuta dividendo il volume corrente con la differenza tra il plateau di pressione, misurato all’apertura delle vie aeree (PaO) durante una occlusione a fine ispirazione e la pressione positiva di fine espirazione (PEEP) così come è stata impostata sul ventilatore”.
Capacità vitale lenta (SVC)
La capacità vitale lenta (SVC) è il volume massimo di aria che può essere espirata lentamente dopo aver eseguito una lenta inspirazione massimale.
Tempo espiratorio forzato (FET)
Il tempo di espirazione forzata (FET) misura la durata di una espirazione massimale, in secondi.
Pressione massima (Pmax e Pi)
Pmax è la pressione che tende ad avvicinarsi (asintotica) a quella massima che può essere sviluppata dai muscoli respiratori a qualsiasi volume polmonare. Pi è la pressione massima di inspirazione che può essere sviluppata a volumi polmonari specifici.[27] Questa misura richiede anche il contemporaneo utilizzo di trasduttori di pressione. È considerata normale se è compresa tra il 60% ed il 140% del valore medio della popolazione per qualsiasi persona della stessa età, sesso e composizione corporea. Un parametro derivato è il cosiddetto coefficiente di retrazione (CR), che è il rapporto tra Pmax/TLC.
Leggi anche:
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Condividi questo articolo:
 Prima di leggere quali sono i fattori di rischio per l’asma bronchiale, ti consiglio di leggere questo articolo: Asma bronchiale in bambini e adulti: cause, sintomi e cura
Prima di leggere quali sono i fattori di rischio per l’asma bronchiale, ti consiglio di leggere questo articolo: Asma bronchiale in bambini e adulti: cause, sintomi e cura
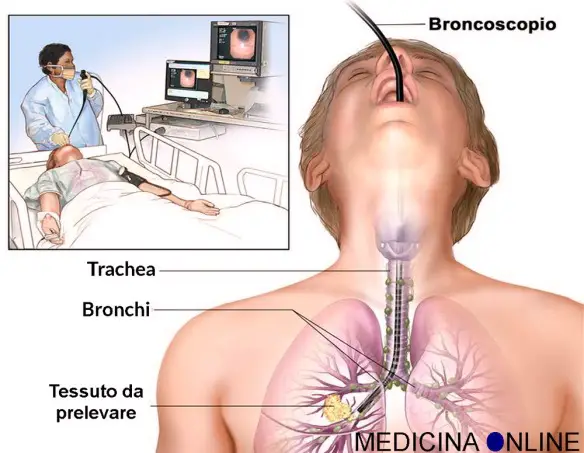 La broncoscopia (o videobroncoscopia o fibrobroncoscopia) è un esame mediamente invasivo con cui è possibile osservare direttamente le vie aeree – cioè laringe, trachea e bronchi – attraverso uno strumento, detto fibrobroncoscopio di forma tubolare flessibile composto da fibre ottiche e da un canale operativo, introdotto nel corpo tramite il naso o la bocca del paziente. La prima broncoscopia è stata eseguita da Gustav Killian nel 1887 utilizzando uno strumento rigido.
La broncoscopia (o videobroncoscopia o fibrobroncoscopia) è un esame mediamente invasivo con cui è possibile osservare direttamente le vie aeree – cioè laringe, trachea e bronchi – attraverso uno strumento, detto fibrobroncoscopio di forma tubolare flessibile composto da fibre ottiche e da un canale operativo, introdotto nel corpo tramite il naso o la bocca del paziente. La prima broncoscopia è stata eseguita da Gustav Killian nel 1887 utilizzando uno strumento rigido.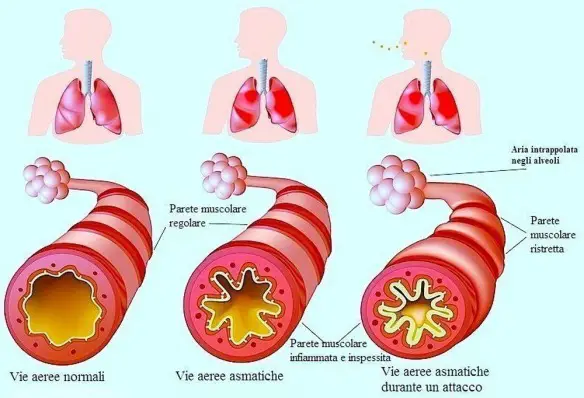 L’asma bronchiale è una patologia infiammatoria cronica dei bronchi, caratterizzata da ostruzione generalmente reversibile delle vie aeree inferiori spesso in seguito a sensibilizzazione da parte di allergeni, il cui sintomo principale è rappresentato da episodi di respiro sibilante e fischiante associato a dispnea (difficoltà respiratoria), senso di costrizione toracica e tosse. In alcuni casi l’ostruzione bronchiale può essere irreversibile. E’ una patologia conosciuta fin dai tempi dell’Antico Egitto, anche se è stato Ippocrate di Coo intorno al 450 a.C. a studiarla a fondo per primo: a lui si deve l’etimologia di “asma” che deriva da “ansimante”.
L’asma bronchiale è una patologia infiammatoria cronica dei bronchi, caratterizzata da ostruzione generalmente reversibile delle vie aeree inferiori spesso in seguito a sensibilizzazione da parte di allergeni, il cui sintomo principale è rappresentato da episodi di respiro sibilante e fischiante associato a dispnea (difficoltà respiratoria), senso di costrizione toracica e tosse. In alcuni casi l’ostruzione bronchiale può essere irreversibile. E’ una patologia conosciuta fin dai tempi dell’Antico Egitto, anche se è stato Ippocrate di Coo intorno al 450 a.C. a studiarla a fondo per primo: a lui si deve l’etimologia di “asma” che deriva da “ansimante”.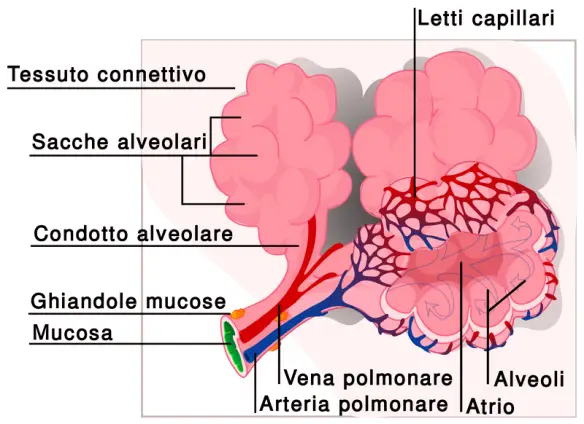 Gli alveoli sono delle piccole cavità polmonari che fanno parte del parenchima polmonare. Nell’albero respiratorio si trovano in posizione terminale, dopo i bronchioli polmonari, coi quali costituisce l’elemento base dell’architettura del polmone, il lobulo polmonare.
Gli alveoli sono delle piccole cavità polmonari che fanno parte del parenchima polmonare. Nell’albero respiratorio si trovano in posizione terminale, dopo i bronchioli polmonari, coi quali costituisce l’elemento base dell’architettura del polmone, il lobulo polmonare.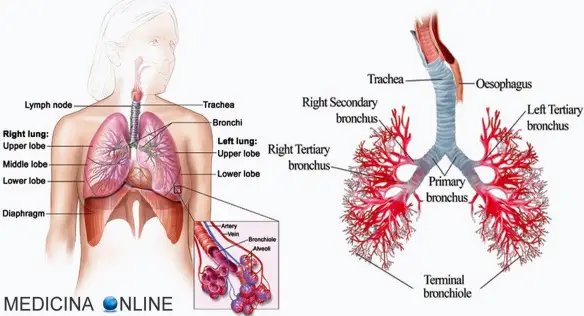
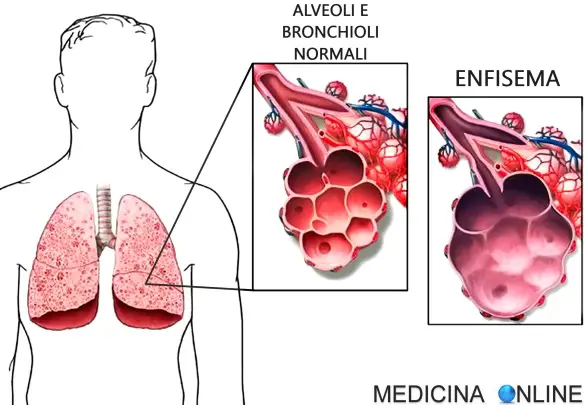 Con “enfisema polmonare” o, semplicemente “enfisema” (in inglese emphysema o pulmonary emphysema) si indica una grave patologia che interessa i polmoni, associata a deterioramento anatomico-funzionale degli alveoli polmonari e dei bronchioli terminali e classificata tra le malattie di tipo polmonare ostruttivo (BPCO). L’enfisema polmonare rappresenta uno stato morboso cronico e solitamente bilaterale (colpisce cioè entrambi i polmoni).
Con “enfisema polmonare” o, semplicemente “enfisema” (in inglese emphysema o pulmonary emphysema) si indica una grave patologia che interessa i polmoni, associata a deterioramento anatomico-funzionale degli alveoli polmonari e dei bronchioli terminali e classificata tra le malattie di tipo polmonare ostruttivo (BPCO). L’enfisema polmonare rappresenta uno stato morboso cronico e solitamente bilaterale (colpisce cioè entrambi i polmoni).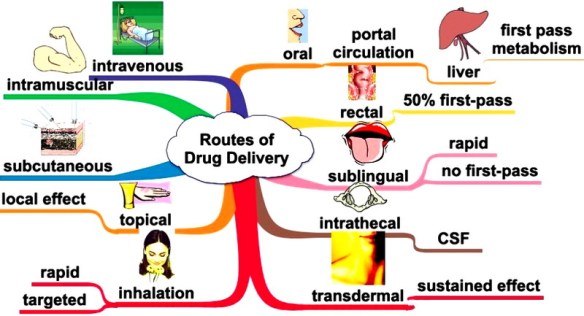 La somministrazione di un farmaco (in inglese “route of administration”) è quel processo che porta uno xenobiotico, cioè una sostanza estranea all’organismo, a raggiungere il suo bersaglio all’interno dell’organismo, cioè il sito d’azione a cui esso è destinato.
La somministrazione di un farmaco (in inglese “route of administration”) è quel processo che porta uno xenobiotico, cioè una sostanza estranea all’organismo, a raggiungere il suo bersaglio all’interno dell’organismo, cioè il sito d’azione a cui esso è destinato. Sono molti i parametri che possono essere misurati durante un esame spirometrico, i più frequenti sono:
Sono molti i parametri che possono essere misurati durante un esame spirometrico, i più frequenti sono: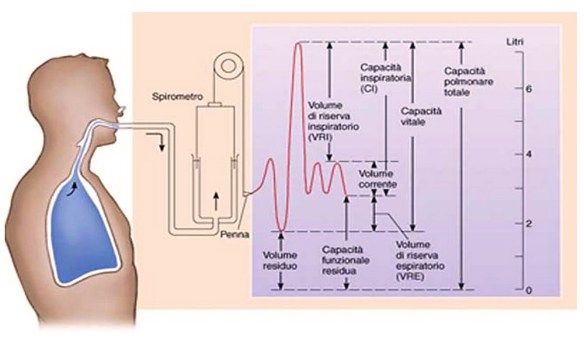 La spirometria è un esame molto diffuso, rapido, indolore ed economico che indaga la funzione respiratoria. Il test si esegue con l’ausilio di uno strumento chiamato spirometro. Grazie a questo esame si può misurare la funzione dei polmoni, in particolare il volume e/o la velocità con cui l’aria può essere inspirata o espirata da un soggetto. La spirometria può anche essere parte di un test di provocazione bronchiale, utilizzato per determinare l’eventuale presenza di iperreattività bronchiale, ad esempio per verificare la presenza di asma occupazionale. Il risultato della spirometria è normalmente corredato da un commento verbale aggiunto dal medico in cui si esprime un giudizio inerente ai valori ottenuti.
La spirometria è un esame molto diffuso, rapido, indolore ed economico che indaga la funzione respiratoria. Il test si esegue con l’ausilio di uno strumento chiamato spirometro. Grazie a questo esame si può misurare la funzione dei polmoni, in particolare il volume e/o la velocità con cui l’aria può essere inspirata o espirata da un soggetto. La spirometria può anche essere parte di un test di provocazione bronchiale, utilizzato per determinare l’eventuale presenza di iperreattività bronchiale, ad esempio per verificare la presenza di asma occupazionale. Il risultato della spirometria è normalmente corredato da un commento verbale aggiunto dal medico in cui si esprime un giudizio inerente ai valori ottenuti.