 L’ipersensibilità dell’amigdala è una condizione nella quale l’amigdala è iperattiva, provocando un senso costante di paura, caratterizzata dal rilascio costante di adrenalina nel circolo e relativi danni psichici e psicosomatici che si riflettono nel comportamento, comunemente definito come “timidezza”. Essa è poco conosciuta dagli psichiatri, che la generalizzano come depressione ed ansia, e la curano di conseguenza.
L’ipersensibilità dell’amigdala è una condizione nella quale l’amigdala è iperattiva, provocando un senso costante di paura, caratterizzata dal rilascio costante di adrenalina nel circolo e relativi danni psichici e psicosomatici che si riflettono nel comportamento, comunemente definito come “timidezza”. Essa è poco conosciuta dagli psichiatri, che la generalizzano come depressione ed ansia, e la curano di conseguenza.
Gravi crisi acute possono manifestarsi quando un soggetto, diagnosticato come depresso, è curato con antidepressivi inibitori della ricaptazione delle monoamine (pazienti ritenuti a torto “resistenti agli antidepressivi” cioè a un farmaco inutile, non essendo depressi) o che impediscono l’eliminazione dell’adrenalina (IMAO ed SNRI). La vita sociale è compromessa e quella lavorativa è preclusa a causa dell’ottundimento della lucidità proprio degli effetti dell’adrenalina sul sistema nervoso.
I danni somatici evidenti sono quelli tipici dell’ipersurrenalismo, riguardanti l’effetto vasocostrittore periferico e catabolizzante dell’adrenalina e del cortisolo (cachessia, ectomorfismo, ipertensione arteriosa, sofferenza cutanea e delle mucose, alito cattivo, carie dentaria, impotenza sessuale, calvizie).
Il ritmo circadiano è solitamente alterato a causa degli effetti a cascata che lo squilibrio ormonale ha sull’intero sistema endocrino. L’effetto a cascata può portare ad altri disturbi endocrini ed alimentari, ad esempio diabete. L’equilibrio minerale è alterato (forte deplezione di potassio e magnesio causata dal cortisolo). Gli stimoli ambientali sono ottusi dal sentimento preponderante, la paura; tipica è l’anoressia nel bambino, e la bulimia di risposta nell’adulto. Il soggetto è accondiscendente, non accetta la competizione, non è in grado di difendersi e di compiere atti ostili. Il trattamento prevederebbe principalmente di ristabilire l’equilibrio minerale (integrazione di potassio e magnesio); quello ambientale di evitare gli shock morali intensi (ad esempio l’interazione forzata, soprattutto con forme di autorità; il giudizio, la coercizione, le punizioni, la cattività). La legislazione italiana non prevede emolumenti pensionistici nonostante l’inabilità al lavoro (a meno che non sia fatta passare come depressione grave, il che dà diritto ad una pensione di 280 euro mensili).
Leggi anche:
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Emozioni: cosa sono, classificazione, importanza e stress
- Rabbia: differenza tra ira passiva ed ira aggressiva
- Paura: cause, gradi, timore, ansia, fobia, panico, terrore ed orrore
- Paure fisiologiche e patologiche nei bambini
- Paura dei luoghi chiusi e claustrofobia: cos’è e come si cura
- Fobie specifiche o semplici: cosa sono ed esempi di fobia
- Terrore notturno: sintomi, diagnosi e terapia
- Sono un sonnambulo: cause, sintomi, diagnosi e terapie
- Attacchi di panico: cosa sono, come riconoscerli e curarli
- Disturbo d’ansia generalizzato: sintomi, diagnosi e terapia
- Vertigine e perdita di equilibrio: tipi, cause, diagnosi e cure
- Debolezza senza perdita completa di coscienza: la lipotimia
- Preoccuparsi troppo per la propria salute: l’ipocondria
- Quando mancano le emozioni: l’alessitimia
- Connessione tra corpo e mente: la psicosomatica
- Disturbo da somatizzazione: caratteristiche, diagnosi e decorso
- Disturbo di conversione o isteria di conversione
- Isteria: significato e visione moderna
- Psiconeuroendocrinoimmunologia
- Personalità sottomessa: caratteristiche e descrizione
- Cosa significa “andare in iperventilazione”?
- Amigdala: connessioni, anatomia e funzioni in sintesi
- Perdita della coordinazione muscolare: l’atassia
- Atassia ottica: cos’è e da cosa è causata?
- Test di Romberg: cos’è, a che serve, come si esegue
- Cos’è il labirinto dell’orecchio ed a che serve?
- Ippocampo: anatomia, funzioni e ruolo nella memoria
- Nervo trigemino: anatomia, decorso, branche e funzioni
- Nervo faciale: anatomia, funzioni e patologie in sintesi
- Paralisi periferica del nervo faciale: cause e sintomi
- Quando l’occhio non riesce a lacrimare: la xeroftalmia
- Quando la bocca è secca per mancanza di saliva: la xerostomia
- Locus ceruleus: anatomia, funzioni e connessioni in sintesi
- Talamo: anatomia, struttura, nuclei e funzioni in sintesi
- Diencefalo: anatomia, struttura e funzioni in sintesi
- Ventricoli cerebrali: anatomia e funzioni in sintesi
- Differenza tra neocorteccia omotipica ed eterotipica
- Differenza tra memoria a breve termine ed a lungo termine
- Differenza tra nucleo genicolato mediale e laterale
- Cortisolo: funzioni, produzione, chimica, patologie, glicemia e dieta
- Quando la malattia deperisce l’organismo: la cachessia
- Ritmo circadiano: caratteristiche, durata, luce e melatonina
- La Sindrome da abbandono: cos’è e come si supera
- Liberarsi dalla dipendenza affettiva e dalla paura dell’abbandono
- Dipendenza affettiva: riconoscerla, affrontarla e superarla
- Gelosia patologica e delirio di infedeltà: la possessività esclusiva
- Differenza tra gelosia normale e patologica
- Cervello maschile e femminile: quali sono le differenze?
- Autostima: come ritrovarla dopo un fallimento ed avere successo al tentativo successivo
- La tua vita è difficile? Ti spiego tutti i segreti per ritrovare la fiducia in te stesso ed aumentare la tua autostima
- Scopri come affronti la vita e le sue difficoltà, con il “Test del bosco”
- I dieci comportamenti che comunicano agli altri che sei una persona introversa
- Differenza tra afasia, disartria ed aprassia
- Area di Broca: funzioni ed afasia di Broca
- Area di Wernicke: funzioni ed afasia di Wernicke
- Differenza tra afasia di Broca e di Wernicke
- Cervelletto: anatomia esterna ed interna
- Cervelletto: le lesioni cerebellari più comuni
- Le funzioni del cervelletto: apprendimento e correzione dei movimenti del corpo
- Differenza tra area di Broca e Wernicke
- Perché si piange? Per quale motivo si piange di gioia, di dolore e dal ridere?
- Paralisi del sonno e allucinazioni ipnagogiche: cause, pericoli, rimedi
- Morbo di Parkinson: cause, sintomi, decorso, terapie
- Morbo di Alzheimer: cause, sintomi, decorso, terapie
- Differenza tra morbo di Alzheimer e morbo di Parkinson: sintomi comuni e diversi
- Differenza tra morbo di Alzheimer, demenza senile, vascolare e reversibile
- Demenza senile: cause, sintomi, decorso e cure
- Emorragia cerebrale: cause, sintomi premonitori, diagnosi e cura
- Emorragia subaracnoidea: cause, sintomi, diagnosi e cura
- Quanti caffè devi bere in un giorno per morire?
- Malformazioni artero-venose cerebrali: sintomi e cura
- Aneurisma cerebrale rotto e non rotto: cause, sintomi, diagnosi e cura
- Differenza tra emorragia cerebrale e subaracnoidea
- Differenza tra emorragia cerebrale ed aneurisma
- Differenza tra emorragia cerebrale ed ictus
- Differenza tra ictus cerebrale ed attacco ischemico transitorio (TIA)
- Cocaina: effetti a breve e lungo termine e loro durata
- Meccanismo d’azione della cocaina: il reuptake della dopamina
- Cocaina: trattamenti psicoterapici per contrastare la dipendenza
- Cocaina in gravidanza: effetti sul feto e sul bambino
- Cocaina: trattamenti farmacologici per contrastare l’astinenza
- Differenza tra cocaina e crack
- Differenza tra midollo spinale e allungato
- Differenza tra epifisi, diafisi, metafisi ed ipofisi
- Differenza tra acetilcolina e noradrenalina
- Noradrenalina: cos’è ed a cosa serve?
- Differenza tra dopamina e dobutamina
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

 L’infiammazione, o flogosi, è un meccanismo di difesa non specifico innato, che costituisce una risposta protettiva, seguente all’azione dannosa di agenti fisici, chimici e biologici, il cui obiettivo finale è l’eliminazione della causa iniziale di danno cellulare o tissutale, nonché l’avvio del processo riparativo. L’infiammazione è cronica quando il processo flogistico è di lunga durata: in esso coesistono l’infiammazione attiva, la distruzione tissutale ed i tentativi di riparazione.
L’infiammazione, o flogosi, è un meccanismo di difesa non specifico innato, che costituisce una risposta protettiva, seguente all’azione dannosa di agenti fisici, chimici e biologici, il cui obiettivo finale è l’eliminazione della causa iniziale di danno cellulare o tissutale, nonché l’avvio del processo riparativo. L’infiammazione è cronica quando il processo flogistico è di lunga durata: in esso coesistono l’infiammazione attiva, la distruzione tissutale ed i tentativi di riparazione.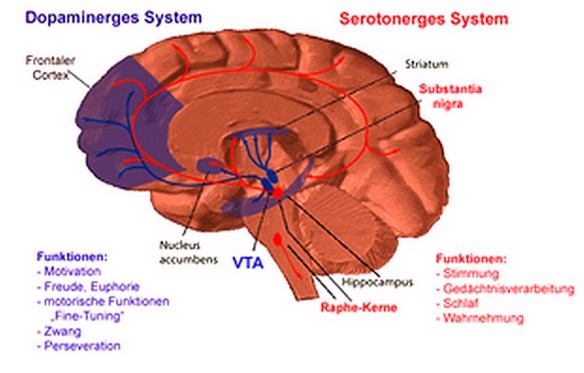 I neuroni dopamminergici formano un sistema di neuromodulazione che ha origine nella substantia nigra, nell’area tegmentale ventrale (VTA), e nell’ipotalamo. Questi sono collegati tramite assoni ad ampie zone del cervello attraverso quattro percorsi principali:
I neuroni dopamminergici formano un sistema di neuromodulazione che ha origine nella substantia nigra, nell’area tegmentale ventrale (VTA), e nell’ipotalamo. Questi sono collegati tramite assoni ad ampie zone del cervello attraverso quattro percorsi principali: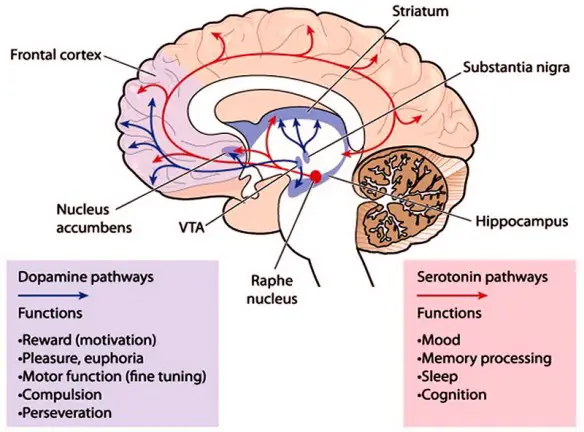 La dopamina (o dopammina) ha molte funzioni, specie a livello del cervello dove svolge un ruolo importante in comportamento, cognizione, movimento volontario, motivazione, punizione, nell’inibizione della produzione di prolattina (coinvolta nell’allattamento materno e nella gratificazione sessuale), sonno, umore, attenzione, memoria di lavoro e di apprendimento. Agisce sul sistema nervoso simpatico causando l’accelerazione del battito cardiaco e l’innalzamento della pressione del sangue. La dopammina viene rilasciata a livello centrale dalla substantia nigra e la sua azione è mirata a modulare l’attività inibitoria dei neuroni GABAergici. Neuroni dopamminergici (cioè, i neuroni il cui principale neurotrasmettitore è la dopammina) sono presenti soprattutto nella zona tegmentale ventrale del mesencefalo, nella substantia nigra, e nel nucleo arcuato dell’ipotalamo.
La dopamina (o dopammina) ha molte funzioni, specie a livello del cervello dove svolge un ruolo importante in comportamento, cognizione, movimento volontario, motivazione, punizione, nell’inibizione della produzione di prolattina (coinvolta nell’allattamento materno e nella gratificazione sessuale), sonno, umore, attenzione, memoria di lavoro e di apprendimento. Agisce sul sistema nervoso simpatico causando l’accelerazione del battito cardiaco e l’innalzamento della pressione del sangue. La dopammina viene rilasciata a livello centrale dalla substantia nigra e la sua azione è mirata a modulare l’attività inibitoria dei neuroni GABAergici. Neuroni dopamminergici (cioè, i neuroni il cui principale neurotrasmettitore è la dopammina) sono presenti soprattutto nella zona tegmentale ventrale del mesencefalo, nella substantia nigra, e nel nucleo arcuato dell’ipotalamo.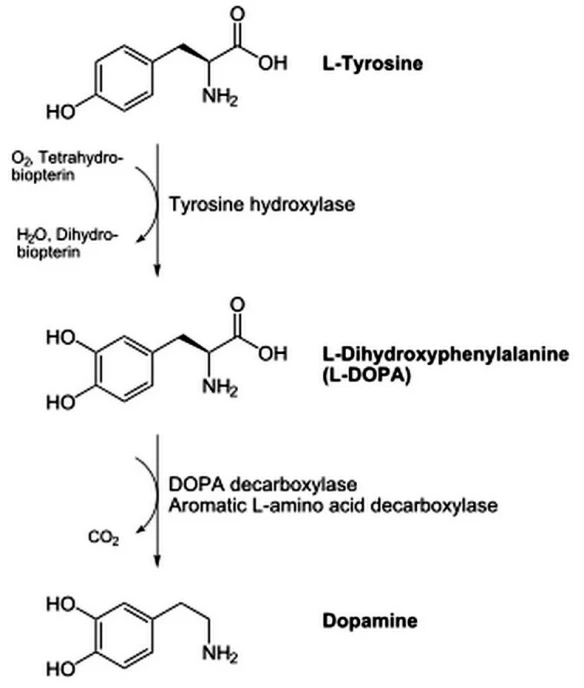
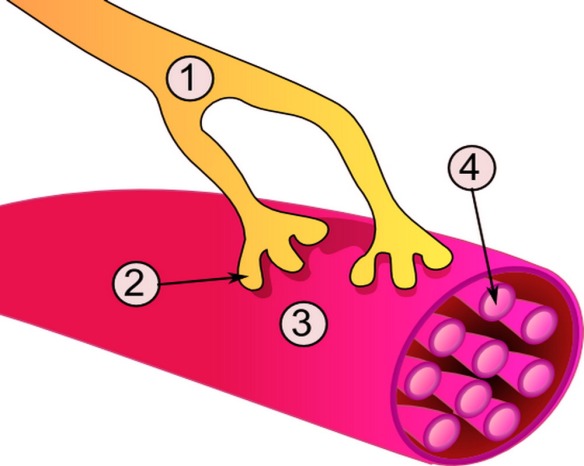
 Un neurotrasmettitore è una sostanza che trasmette le informazioni tra le varie cellule che compongono il nostro sistema nervoso, cioè i neuroni, attraverso la trasmissione sinaptica. All’interno del neurone, i neurotrasmettitori sono contenuti in vescicole dette vescicole sinaptiche che sono addensate alle estremità distali dell’assone nei punti in cui esso contrae rapporto sinaptico con altri neuroni.
Un neurotrasmettitore è una sostanza che trasmette le informazioni tra le varie cellule che compongono il nostro sistema nervoso, cioè i neuroni, attraverso la trasmissione sinaptica. All’interno del neurone, i neurotrasmettitori sono contenuti in vescicole dette vescicole sinaptiche che sono addensate alle estremità distali dell’assone nei punti in cui esso contrae rapporto sinaptico con altri neuroni.