
Kaori
All’apparenza potrebbe apparire come una invenzione stravagante, tuttavia potrebbe aprire la strada a grandi novità nel Continua a leggere


Kaori
All’apparenza potrebbe apparire come una invenzione stravagante, tuttavia potrebbe aprire la strada a grandi novità nel Continua a leggere
 Con “fluido” in chimica si definisce un materiale (generalmente costituito da una sostanza o da una miscela di più sostanze) che si deforma illimitatamente (fluisce) se sottoposto a uno sforzo di taglio, indipendentemente dall’entità di quest’ultimo. Il fluido è un particolare stato della materia che comprende
Con “fluido” in chimica si definisce un materiale (generalmente costituito da una sostanza o da una miscela di più sostanze) che si deforma illimitatamente (fluisce) se sottoposto a uno sforzo di taglio, indipendentemente dall’entità di quest’ultimo. Il fluido è un particolare stato della materia che comprende
La dinamica dei fluidi, o fluidodinamica, studia il comportamento dei fluidi in moto, in relazione alle cause che lo determinano. Per ricavare le equazioni che regolano il moto dei fluidi è necessario ricorrere ad un modello teorico di fluido, chiamato “fluido ideale” (anche chiamato “fluido perfetto“, sono sinonimi) del tutto incomprimibile e non viscoso, cioè senza attrito interno. La maggior parte dei fluidi reali non è appartenente al gruppo dei fluidi perfetti, ma il loro comportamento, benché a volte si discosti notevolmente da quello dei fluidi perfetti, in alcuni casi può essere assimilabile a quello dei fluidi perfetti.
La differenza principale tra un fluido perfetto e un fluido reale è la presenza della viscosità, che tende a ostacolare il moto del fluido imponendo che nelle equazioni del moto usate per i fluidi perfetti siano introdotti termini correttivi che tengano conto della dissipazione di energia causata dall’attrito interno tra le molecole. Inoltre, un fluido reale, a differenza di un fluido ideale, può presentare due modalità di scorrimento:
Semplificando:
- i fluidi ideali sono fluidi non viscosi (privi di attrito) e sempre incomprimibili;
- i fluidi reali sono viscosi, inoltre sono comprimibili nel caso dei gas o incomprimibili nel caso dei liquidi, infine possono scorrere con flusso laminare o turbolento.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 Con “fluido” in chimica si definisce un materiale (generalmente costituito da una sostanza o da una miscela di più sostanze) che si deforma illimitatamente (fluisce) se sottoposto a uno sforzo di taglio, indipendentemente dall’entità di quest’ultimo. Il fluido è un particolare stato della materia che comprende
Con “fluido” in chimica si definisce un materiale (generalmente costituito da una sostanza o da una miscela di più sostanze) che si deforma illimitatamente (fluisce) se sottoposto a uno sforzo di taglio, indipendentemente dall’entità di quest’ultimo. Il fluido è un particolare stato della materia che comprende
Con “liquido” in chimica si indica uno degli stati della materia, insieme a “solido” ed aeriforme (gas). Le sue proprietà principali sono: fluidità, elasticità ed incomprimibilità. Generalmente, una sostanza allo stato liquido è meno densa che allo stato solido, ma un’importante eccezione è costituita dall’acqua.
Da quanto detto appare chiaro che i liquidi fanno parte della grande famiglia dei fluidi: tutti i liquidi sono fluidi, ma non tutti i fluidi sono dei liquidi.
Consideriamo ad esempio un tipo particolare fluido: un gas. Il gas è un fluido, tuttavia non è un liquido, bensì è allo stato aeriforme. Immesso in un dato contenitore, il gas lo occupa tutto mentre invece, un altro particolare fluido, un liquido, ne occupa solo una parte, perché i liquidi mantengono il loro volume, i gas invece no.
Sinteticamente si può concludere dicendo che i liquidi sono quei particolari fluidi che mantengono il loro volume.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 La densità di un materiale è il rapporto tra la sua massa ed il suo volume (cioè massa diviso volume); l’unità di misura della densità è il kg/m³. Nell’uso comune si utilizza talvolta il kg/litro (kg/dm³), che corrisponde esattamente al g/cm³.
La densità di un materiale è il rapporto tra la sua massa ed il suo volume (cioè massa diviso volume); l’unità di misura della densità è il kg/m³. Nell’uso comune si utilizza talvolta il kg/litro (kg/dm³), che corrisponde esattamente al g/cm³.
Il materiale in esame può essere sia un liquido che un solido o un gas. La densità nella tavola periodica degli elementi tende a crescere nei gruppi dall’alto verso il basso (fanno eccezione berillio e magnesio), mentre nei periodi cresce da sinistra a destra fino a boro-alluminio-rame-rutenio-iridio, per poi decrescere.
I corpi con densità maggiore vanno a fondo se immersi in fluidi con densità minore; invece i corpi con densità minore galleggiano su fluidi che hanno densità maggiore, ciò è valido solo se l’esperimento viene effettuato sotto effetto della gravità, mentre ciò non è vero in assenza di gravità, ad esempio nello spazio. Questa proprietà è alla base del celebre Principio di Archimede:
«ogni corpo immerso parzialmente o completamente in un fluido (liquido o gas) riceve una spinta verticale dal basso verso l’alto, uguale per intensità al peso del volume del fluido spostato».
Leggi anche:
Nella tabella seguente è indicata la densità dell’acqua in grammi per centimetro cubo a varie temperature (in °C). I valori sotto 0 °C si riferiscono allo stato di acqua sottoraffreddata.
| Temperatura (°C) | Densità (g/cm3) | Volume specifico (cm3/g) |
|---|---|---|
| 100 | 0,9584 | 1,0434 |
| 80 | 0,9718 | 1,0290 |
| 60 | 0,9832 | 1,0171 |
| 40 | 0,9922 | 1,00786 |
| 30 | 0,9956502 | 1,00437 |
| 25 | 0,9970479 | 1,00296 |
| 22 | 0,9977735 | 1,00223 |
| 20 | 0,9982071 | 1,001796 |
| 15 | 0,9991026 | 1,000898 |
| 10 | 0,9997026 | 1,000297 |
| 4 | 0,9999720 | 1,0000280 |
| 0 | 0,9998395 | 1,00016 |
| −10 | 0,998117 | 1,001886 |
| −20 | 0,993547 | 1,006495 |
| −30 | 0,983854 | 1,01641 |
Nella tabella seguente è indicata la densità dell’aria in chilogrammi per metro cubo a varie temperature (in °C)
| Temperatura in °C | Densità in kg/m3 (a 1 atm) |
|---|---|
| –10 | 1,342 |
| –5 | 1,316 |
| 0 | 1,293 |
| 5 | 1,269 |
| 10 | 1,247 |
| 15 | 1,225 |
| 20 | 1,204 |
| 25 | 1,184 |
| 30 | 1,165 |
Il termine “densità” può essere applicato anche ad altre grandezze che hanno una distribuzione spaziale. Per esempio il rapporto tra il numero di elettroni in un dato volume e il volume stesso è detto densità di elettroni. Più in generale, considerando un insieme qualunque di oggetti, si parla di densità di numero. Il rapporto tra la carica totale distribuita in un volume e il volume medesimo viene comunemente indicato come densità di carica; l’energia luminosa per unità di volume è definita come densità di energia luminosa. Quindi in generale la massa volumica di una grandezza è espressa mediante il rapporto tra la quantità della grandezza contenuta in un volume assegnato e il valore di quest’ultimo.
In senso ancora più ampio il concetto è stato esteso anche ad altri ambiti quali la geografia: la densità di popolazione misura la popolazione di un territorio per unità di superficie.
Nel caso in cui una grandezza sia distribuita su una superficie si può parlare infine di densità superficiale di tale grandezza riferendosi al rapporto tra la grandezza stessa e l’area della superficie su cui è distribuita. Per esempio nel caso della carica elettrica si parla di densità superficiale di carica. Nel caso di una corrente elettrica attraverso un conduttore di sezione S si chiama densità di corrente il rapporto tra la corrente e la sezione S attraversata.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 La densità di un materiale è il rapporto tra la sua massa ed il suo volume (cioè massa diviso volume); l’unità di misura della densità è il kg/m³. Nell’uso comune si utilizza talvolta il kg/litro (kg/dm³), che corrisponde esattamente al g/cm³. Il materiale in esame può essere sia un liquido che un solido o un gas. Tale definizione di densità è riferita ad una quantità di materia solida massiccia, vale a dire senza vuoti interni, per tale motivo viene anche detta densità reale in quanto prende in considerazione solo il volume della frazione solida.
La densità di un materiale è il rapporto tra la sua massa ed il suo volume (cioè massa diviso volume); l’unità di misura della densità è il kg/m³. Nell’uso comune si utilizza talvolta il kg/litro (kg/dm³), che corrisponde esattamente al g/cm³. Il materiale in esame può essere sia un liquido che un solido o un gas. Tale definizione di densità è riferita ad una quantità di materia solida massiccia, vale a dire senza vuoti interni, per tale motivo viene anche detta densità reale in quanto prende in considerazione solo il volume della frazione solida.
In contrapposizione alla densità reale, la densità apparente di un corpo – pur venendo calcolata in maniera formalmente analoga alla densità reale – prende invece in considerazione il volume totale occupato dal solido ovvero il suo ingombro esterno, compresi quindi gli spazi vuoti (solidi con cavità chiuse, con cavità aperte o a struttura spugnosa).
Un esempio classico è la densità della sabbia contenuta in un barattolo. La sabbia ha una data densità reale data dalla sua massa diviso il volume che occupa realmente, ma ha anche una densità apparente data dalla sua massa diviso il volume che occupa nel suo contenitore, compresi gli spazi di aria tra i vari granelli. La densità apparente, comprendendo pari massa ma volume maggiore, è quindi più bassa rispetto alla densità reale.
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
 La densità di un materiale è il rapporto tra la sua massa ed il suo volume (cioè d = m/ V); l’unità di misura della densità è il kg/m³. Nell’uso comune si utilizza talvolta il kg/litro (kg/dm³), che corrisponde esattamente al g/cm³. Il materiale in esame può essere sia un liquido che un solido o un gas.
La densità di un materiale è il rapporto tra la sua massa ed il suo volume (cioè d = m/ V); l’unità di misura della densità è il kg/m³. Nell’uso comune si utilizza talvolta il kg/litro (kg/dm³), che corrisponde esattamente al g/cm³. Il materiale in esame può essere sia un liquido che un solido o un gas.
La concentrazione di un componente in una miscela è una grandezza che esprime invece il rapporto tra la quantità del componente rispetto alla quantità totale di tutti i componenti della miscela (compreso il suddetto componente). Nel caso specifico di una soluzione, la concentrazione di un determinato soluto nella soluzione esprime il rapporto tra la quantità del soluto rispetto alla quantità totale di soluzione, o, in alcuni modi di esprimerla, del solo solvente (ad esempio molalità).
La densità in soluzione pi indica il rapporto tra la massa del soluto mi rispetto al volume V dell’intera soluzione:
pi = mi / V
La densità in soluzione si esprime in kg/m3 (pari a g/L).
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
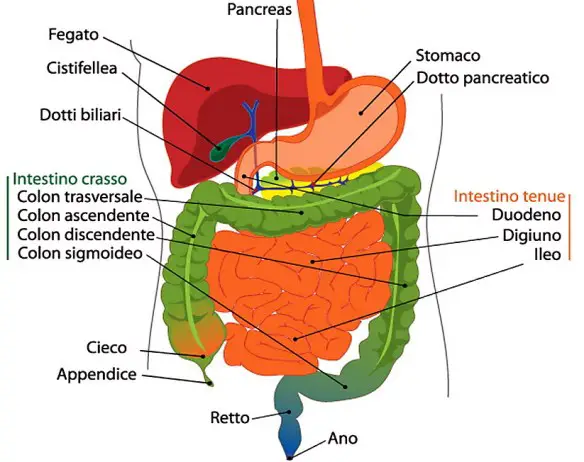 Con meteorismo viene indicato un disturbo gastrointestinale associato alla distensione addominale provocata da una eccessiva produzione e accumulo di gas nel tratto digestivo, usualmente nel tratto intestinale (Meteorismus intestinalis) o nello stomaco, più raramente nella cavità addominale. L’accumulo di gas che risale nel tratto gastro-intestinale e che non viene evacuato, ad esempio attraverso la flatulenza, può dar luogo a complicanze, una tra tutte il rigonfiamento dell’addome stesso.
Con meteorismo viene indicato un disturbo gastrointestinale associato alla distensione addominale provocata da una eccessiva produzione e accumulo di gas nel tratto digestivo, usualmente nel tratto intestinale (Meteorismus intestinalis) o nello stomaco, più raramente nella cavità addominale. L’accumulo di gas che risale nel tratto gastro-intestinale e che non viene evacuato, ad esempio attraverso la flatulenza, può dar luogo a complicanze, una tra tutte il rigonfiamento dell’addome stesso.
La quantità di gas all’interno dell’intestino è abbastanza costante, e non rappresenta che una piccola frazione del volume totale realmente prodotto. Il volume totale dei gas è soltanto da 100 a 200 mL. La quantità dei gas è regolata dal transito intestinale e dall’evacuazione del gas in eccesso. I gas entrano nell’organismo con la deglutizione, le reazioni biochimiche, la diffusione a partire dal sangue e dalla fermentazione batterica intestinale. I gas escono invece per assorbimento dalla parete intestinale, per escrezione respiratoria, per sintesi batterica e per evacuazione anale.
Questa è influenzata dalla ricchezza in fibre alimentari (soprattutto pectina, poco la cellulosa), la cui riduzione causa una netta diminuzione dei gas prodotti. Esso dipende anche dalla durata del transito: più è lento, più la produzione sarà importante (costipazione).
Leggi anche:
L’intestino, tramite la peristalsi, mette in movimento i gas prodotti in modo da evacuare la parte non riassorbita dall’intestino. In alcuni pazienti vi è un rallentamento della propulsione dei gas e formazione di sacche gassose. Anche lo sfintère anale ha un ruolo; normalmente il gas è evacuato mediante l’associazione di una leggera contrazione dei muscoli addominali con il rilasciamento dell’ano; talvolta non c’è tale coordinazione e lo sfintère non si rilascia. In conclusione, non è tanto l’eccesso dei gas, ma la distribuzione anormale di essi a essere responsabile del meteorismo addominale. È da notare che la ritenzione dei gas nell’intestino tenue dà una sintomatologia più marcata della ritenzione nel colon. Inoltre è stato notato che, per una stessa quantità di gas, certe persone si sentono gonfie e altre no, quindi vi è un fattore personale di sensibilità e di tolleranza a tale sintomo.
Il carbone vegetale riveste un ruolo di assoluta rilevanza come rimedio erboristico naturale, seguito da piante carminative come finocchio ed anice.
Si distinguono quattro categorie di carbone:
Il carbone, in generale, ha proprietà adsorbenti che lo rendono capace di trattenere i gas intestinali; inoltre, facilita l’eliminazione batterica che provoca la fermentazione. Per i soggetti che presentano solamente una forma di meteorismo causata da un’alimentazione scorretta, il carbone dev’essere assunto dopo i pasti. Solitamente, per i soggetti che seguono una cura farmacologica, il carbone dovrebbe essere evitato, perché potrebbe diminuire la biodisponibilità dei farmaci. Il carbone, inoltre, non dev’essere assunto dalle persone che presentano carenze vitaminiche e dai soggetti che manifestano problemi di assorbimento in generale: il carbone, infatti, va ad indebolire l’assorbimento dei principali nutrienti. Sarebbe buona regola assumere fermenti lattici in concomitanza al carbone per favorire il ripristino della flora intestinale, di conseguenza per combattere il meteorismo. Il consulto del medico è comunque indispensabile.
Leggi anche:
Tra rimedi naturali contro il meteorismo spiccano anche le tisane con estratti di piante carminative, che agiscono diminuendo il gonfiore a livello addominale: finocchio, anice, cumino, sono i più noti, ma anche melissa, mirto e camomillasono molto efficaci per contrastare il meteorismo.
Qui di seguito trovate una lista di prodotti di varie marche per il benessere del vostro apparato digerente, in grado di combattere stipsi, fecalomi, meteorismo, gonfiore addominale, acidità di stomaco, reflusso, cattiva digestione ed alitosi. Noi NON sponsorizziamo né siamo legati ad alcuna azienda produttrice: per ogni tipologia di prodotto, il nostro Staff seleziona solo il prodotto migliore, a prescindere dalla marca. Ogni prodotto viene inoltre periodicamente aggiornato ed è caratterizzato dal miglior rapporto qualità prezzo e dalla maggior efficacia possibile, oltre ad essere stato selezionato e testato ripetutamente dal nostro Staff di esperti:
Leggi anche:
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
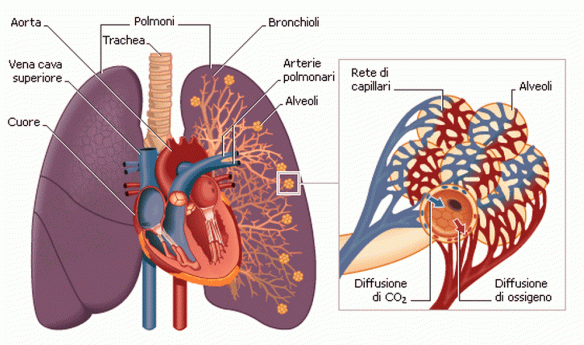 I polmoni destro e sinistro si trovano nella cavità toracica ai lati del mediastino. Ciascuno di essi è avvolto da una membrana sierosa a doppia parete, la pleura, che costituisce i sacchi pleurici, completamente chiusi. Nel sottile spazio tra i due foglietti pleurici di ciascun sacco vi è una pressione negativa che permette al polmone di espandersi nell’inspirazione e ricevere l’aria atmosferica. Il polmone destro è più voluminoso del sinistro La superficie esterna dei polmoni è percorsa da profonde scissure interlobari, che dividono il polmone destro in tre lobi e quello sinistro in due. L’ambiente del polmone è molto umido e quindi facilmente attaccabile da batteri. Molte malattie respiratorie sono proprio dovute ad un’infezione virale o batterica.
I polmoni destro e sinistro si trovano nella cavità toracica ai lati del mediastino. Ciascuno di essi è avvolto da una membrana sierosa a doppia parete, la pleura, che costituisce i sacchi pleurici, completamente chiusi. Nel sottile spazio tra i due foglietti pleurici di ciascun sacco vi è una pressione negativa che permette al polmone di espandersi nell’inspirazione e ricevere l’aria atmosferica. Il polmone destro è più voluminoso del sinistro La superficie esterna dei polmoni è percorsa da profonde scissure interlobari, che dividono il polmone destro in tre lobi e quello sinistro in due. L’ambiente del polmone è molto umido e quindi facilmente attaccabile da batteri. Molte malattie respiratorie sono proprio dovute ad un’infezione virale o batterica.
Leggi anche: Apparato respiratorio: anatomia in sintesi, struttura e funzioni
La principale (ma non esclusiva) funzione dei polmoni è quella di trasportare l’ossigeno atmosferico ai fluidi corporei come sangue o emolinfa, e di espellere anidride carbonica da essi all’atmosfera. Questo scambio di gas è compiuto in un mosaico di cellule specializzate che formano delle piccole sacche d’aria chiamate alveoli. Il 70% della respirazione è guidata dal diaframma il quale si trova in fondo al torace. La contrazione del diaframma espande verticalmente la cavità dove il polmone è semichiuso. Il rilassamento del muscolo ha l’effetto opposto. L’aria entra attraverso le cavità nasali o orali; essa passa attraverso la laringe e successivamente per la trachea, arrivando ai bronchi. I bronchi dividono i polmoni in parti sempre più piccole, chiamati bronchioli. I polmoni terminano con le sacche alveolari. Gli alveoli sono piccole sacche a contatto con il sangue capillare. Qui l’ossigeno viene diffuso nel sangue, trasportato dall’emoglobina fino al cuore attraverso le vene polmonari. Il sangue senza ossigeno dal cuore parte arrivando attraverso l’arteria polmonare fino ai polmoni per avviare il processo di ossigenazione.
Leggi anche: A che serve l’osso ioide e dove si trova? Cos’è il pomo d’Adamo?
Oltre alle funzioni di respirazione come lo scambio di gas e la regolazione dell’idrogeno, i polmoni:
Leggi anche: Differenza tra inspirazione e espirazione: l’atto respiratorio
All’ingresso nei polmoni, i bronchi principali si ramificano dando origine all’albero bronchiale. Il bronco principale destro dà origine a tre bronchi lobari, che si portano ai tre lobi del P. destro, il sinistro ne forma invece due. Il parenchima polmonare è formato dall’insieme dei lobuli polmonari. Ogni lobulo ha forma poliedrica e riceve un bronco lobulare accompagnato da un ramo dell’arteria polmonare. Il bronco lobulare emette una serie di ulteriori ramificazioni, i bronchi intralobulari che, ramificandosi ulteriormente, danno origine a 10-15 rami più piccoli, i bronchioli terminali. Ciascun bronchiolo terminale si biforca in due bronchioli respiratori la cui parete presenta, a intervalli, estroflessioni sacciformi che vengono circondate da una rete di capillari originati dai rami dell’arteria polmonare. Sono gli alveoli polmonari, sede degli scambi gassosi e strettamente contigui gli uni agli altri. L’unità elementare del parenchima polmonare è rappresentata dall’acino polmonare, definito come l’insieme delle ramificazioni, provviste di alveoli polmonari, che originano da un bronchiolo terminale. In ogni acino sono presenti da 500 a 2.000 alveoli polmonari.
Leggi anche:
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!