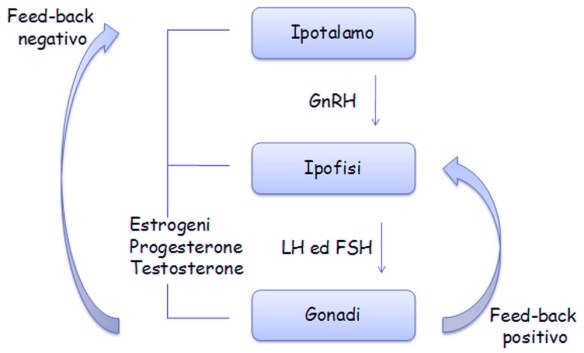
 L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.
L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.
La secrezione di GnRH da parte dell’ipotalamo inizia nella 4° settimana di gestazione; questo rilascio pian piano sollecita l’ipofisi a rilasciare LH ed FSH e la loro sintesi inizia verso la 10 – 12 settimana di gestazione; poco prima della nascita questi valori decadono per mantenersi basse durante la prima infanzia e la secrezione si mantiene bassa anche durante la seconda infanzia e anche nell’età peri-puberale, momento in cui l’asse inizia a svegliarsi. Durante l’infanzia la quantità di FSH circolante supera quella dell’LH, in effetti l’FSH ha effetti sull’attività maturativa dei gameti. Durante la pubertà vediamo che l’attività secretoria del GnRH diventa più consistente probabilmente perché ci sono fattori di tipo inibitorio che vengono rimossi anche se ci sono ancora molti studi in corso.
L’LH a livello gonadale inizia la sintesi degli steroidi gonadici, testosterone nel testicolo, estrogeni e progesterone nelle ovaie. Nella donna la secrezione di LH ed FSH è ciclica mentre nell’uomo questa ciclicità non c’è. Nella tarda età nella donna l’attività riproduttiva cessa, nella menopausa infatti la quantità di gameti femminili è stata consumata o comunque è andata incontro ad un processo degenerativo per cui la donna non è più in grado di concepire; l’uomo invece mantiene la sua attività maturativa anche al di là dei 60 anni.
Il GnRH è un decapeptide, una proteina di 10 aa. che tramite la circolazione portale ipofisaria raggiunge l’ipofisi dove induce sintesi e rilascio di LH ed FSH che sono due glicoproteine costituite da una sub unità alfa e una beta quindi sono etero dimeri e includono nella molecola anche residui carboidratici; la subunità alfa è costituita da uno stesso numero di aa. che sono sempre gli stessi e quindi questa subunità alfa è comune alla subunità alfa del TSH e della gonadotropina corionica CG, quella che cambia è la subunità beta che si differenzia sia per lunghezza in aa. che per sequenza.
Il GnRH induce a recettori specifici di membrana sulle cellule ipofisarie e la risposta che dà quando si lega è che va ad attivare il metabolismo dei fosfolipidi, in generale tutti i fattori di rilascio ipotalamici vanno ad attivare recettori di membrana connessi con l’attivazione dei fosfolipidi di membrana quindi formazione di DAG, attivazione proteina chinasi C e di IP3 ma anche attivazione dell’cAMP mentre LH ed FSH hanno recettori di membrana è il meccanismo di traduzione che attivano è quello dell’adenilato ciclasi con incremento di cAMP.
Leggi anche:
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Asse ipotalamo-ipofisi-surrene: funzionamento ed ormoni rilasciati
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Patologie di ipotalamo e ipofisi
- Virilizzazione (mascolinizzazione): tipi, cause, sintomi, diagnosi e terapie
- Irsutismo: cause, sintomi, diagnosi e trattamenti
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Ormone della crescita (GH) a che serve e da cosa è prodotto?
- Ormone della crescita (GH): body building e doping in palestra
- Ormone della crescita (GH): effetti avversi nel body building e nello sport
- Quando essere troppo alti è una malattia: il gigantismo
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso simpatico: funzioni
- Sistema nervoso parasimpatico: funzioni
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Cervello maschile e femminile: quali sono le differenze?
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Cos’è l’adrenalina ed a cosa serve?
- L’altezza media italiana nel 2017 di maschi e femmine
- L’altezza media italiana 2017 da 1 a 19 anni di maschi e femmine
- L’altezza media mondiale nel 2017 di maschi e femmine [TABELLA]
- Altezza: quando si può parlare di nanismo o gigantismo
- Differenza tra midollo osseo e spinale
- Differenza tra sistema nervoso centrale e periferico: anatomia e funzioni in sintesi
- A cosa serve il midollo osseo?
- Differenza tra midollo osseo e cellule staminali
- Differenza tra midollo spinale e allungato
- Differenza tra epifisi, diafisi, metafisi ed ipofisi
- Quanto è alto l’uomo più alto del mondo?
- Quanto è alto l’uomo più basso del mondo?
- Nanismo: sintomi, cura, cause, terapia, diagnosi e prevenzione
- Charlotte, la bambina più piccola del mondo
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!

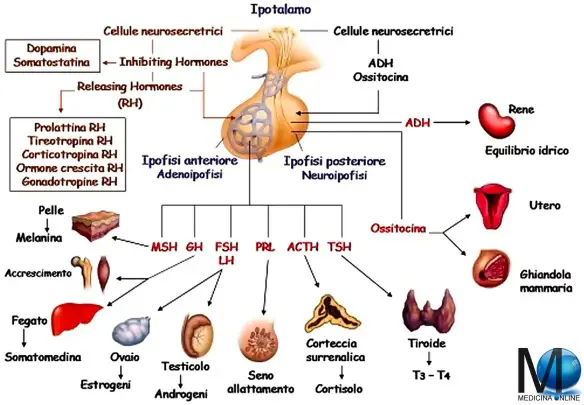
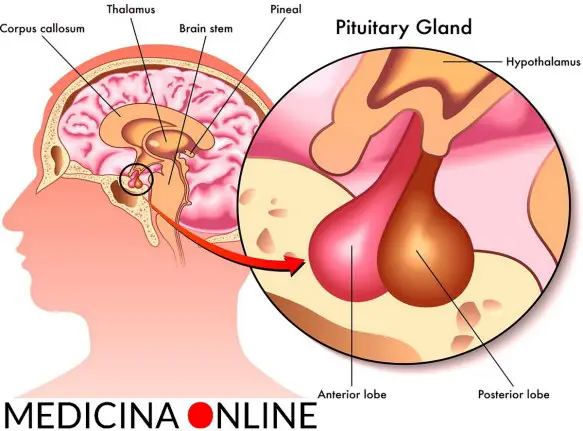 L’ipofisi (con l’accento sulla o), anche chiamata ghiandola pituitaria (hypophysis o pituitary gland in inglese), è una ghiandola endocrina situata alla base del cranio, nella fossa ipofisaria della sella turcica dell’osso sfenoide. Si può dividere in due lobi, diversi per sviluppo embrionale, struttura e funzioni, che controllano – attraverso la secrezione di numerosi ormoni – l’attività endocrina e metabolica di tutto l’organismo:
L’ipofisi (con l’accento sulla o), anche chiamata ghiandola pituitaria (hypophysis o pituitary gland in inglese), è una ghiandola endocrina situata alla base del cranio, nella fossa ipofisaria della sella turcica dell’osso sfenoide. Si può dividere in due lobi, diversi per sviluppo embrionale, struttura e funzioni, che controllano – attraverso la secrezione di numerosi ormoni – l’attività endocrina e metabolica di tutto l’organismo: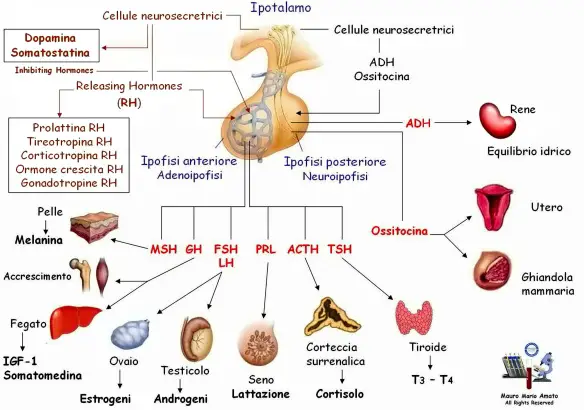
 Le patologie che possono colpire l’ipotalamo o l’ipofisi sono molte e differenti ma portano tutte alla medesima situazione : una iperfunzione o una ipofunzione del sistema ipotalamo-ipofisi.
Le patologie che possono colpire l’ipotalamo o l’ipofisi sono molte e differenti ma portano tutte alla medesima situazione : una iperfunzione o una ipofunzione del sistema ipotalamo-ipofisi.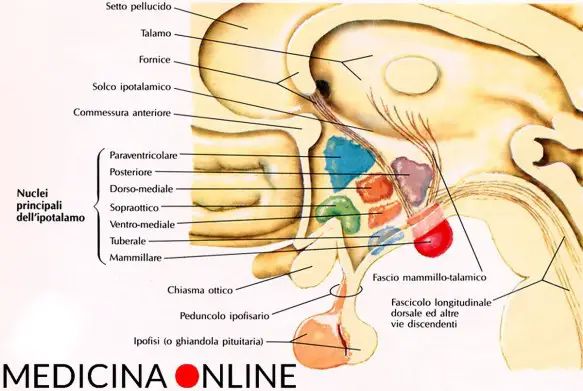 L’ipotalamo e l’ipofisi sono due strutture anatomiche, strettamente collegate fra loro, situate alla base del cranio. Si tratta di due strutture che rappresentano la più importante area di interconnessione fra il sistema nervoso e il sistema endocrino da cui partono gli impulsi e gli stimoli ormonali che governano l’intero sistema endocrino.
L’ipotalamo e l’ipofisi sono due strutture anatomiche, strettamente collegate fra loro, situate alla base del cranio. Si tratta di due strutture che rappresentano la più importante area di interconnessione fra il sistema nervoso e il sistema endocrino da cui partono gli impulsi e gli stimoli ormonali che governano l’intero sistema endocrino.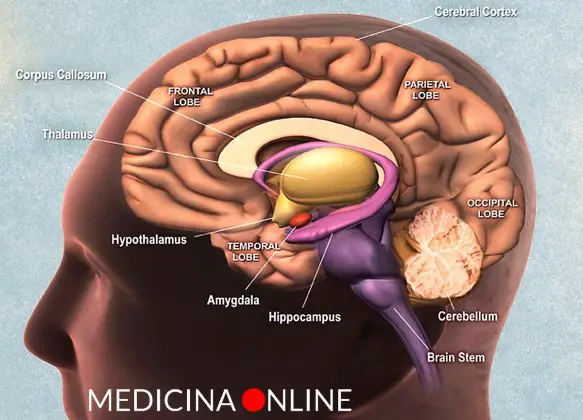 L’ipotalamo (hypothalamus in inglese) è una struttura del SNC (sistema nervoso centrale), situata nella zona centrale interna ai due emisferi cerebrali, e costituisce la parte ventrale del diencefalo. L’ipotalamo comprende molti nuclei che attivano, controllano e integrano i meccanismi autonomici periferici, l’attività endocrina e molte funzioni somatiche tra cui:
L’ipotalamo (hypothalamus in inglese) è una struttura del SNC (sistema nervoso centrale), situata nella zona centrale interna ai due emisferi cerebrali, e costituisce la parte ventrale del diencefalo. L’ipotalamo comprende molti nuclei che attivano, controllano e integrano i meccanismi autonomici periferici, l’attività endocrina e molte funzioni somatiche tra cui: A tutti sarà capitato di sentirsi annoiati di tanto intanto, di essere vittime della noia. Lo si inizia a sperimentare da subito, fin da bambini. Si tende a far derivare la noia dalla mancanza di stimoli, dall’ambiente circostante, o comunque da qualcosa di esterno a noi. Aimè purtroppo, la noia, spesso, non è dovuta ad una causa esterna, ma nasce dentro di noi.
A tutti sarà capitato di sentirsi annoiati di tanto intanto, di essere vittime della noia. Lo si inizia a sperimentare da subito, fin da bambini. Si tende a far derivare la noia dalla mancanza di stimoli, dall’ambiente circostante, o comunque da qualcosa di esterno a noi. Aimè purtroppo, la noia, spesso, non è dovuta ad una causa esterna, ma nasce dentro di noi. Prima di iniziare la lettura, ti consiglio di leggere prima questo articolo:
Prima di iniziare la lettura, ti consiglio di leggere prima questo articolo: 