 Quante volte, nella nostra vita, in un periodo triste abbiamo detto “sono depresso”? La realtà è che la depressione, nelle sue varie forme, è qualcosa di completamente diverso alla “semplice” tristezza: è il non provare più piacere, il sentirsi inutili, la fine di ogni speranza, il non vedere vie di uscita se non – a volte – addirittura il suicidio. Nel depresso non c’è bisogno che arrivi la sera per sentirsi avvolto dalle tenebre.
Quante volte, nella nostra vita, in un periodo triste abbiamo detto “sono depresso”? La realtà è che la depressione, nelle sue varie forme, è qualcosa di completamente diverso alla “semplice” tristezza: è il non provare più piacere, il sentirsi inutili, la fine di ogni speranza, il non vedere vie di uscita se non – a volte – addirittura il suicidio. Nel depresso non c’è bisogno che arrivi la sera per sentirsi avvolto dalle tenebre.
Cos’è la depressione maggiore?
La depressione maggiore (anche chiamata “depressione endogena” o “depressione unipolare” o “disturbo depressivo maggiore”) è un disturbo psichiatrico che appartiene al gruppo dei disturbi dell’umore, che colpisce ogni anno circa il 5% della popolazione, in particolare le donne tra i 30 ed i 40 anni, e può avere gravi conseguenze sulla qualità della vita di un individuo. Il disturbo depressivo maggiore si manifesta in prevalenza nel sesso femminile, con un rapporto di circa 2:1 rispetto al sesso maschile L’Organizzazione Mondiale della Sanità valuta la depressione maggiore come uno dei disturbi più invalidanti al mondo. Diversamente da una normale sensazione di tristezza o di un passeggero stato di cattivo umore, la depressione maggiore presenta caratteristiche di persistenza e può interferire pesantemente sul modo di pensare di un individuo, sul suo comportamento, sulle condizioni dell’umore, sull’attività ed il benessere fisico. Una considerevole parte (oltre la metà) di coloro che sono stati colpiti da un primo episodio di depressione potranno presentare altri episodi depressivi durante il resto della vita. Alcune persone sono colpite da più episodi durante l’anno; in questo caso si parla di depressione ricorrente. Qualora non vengano curati, gli episodi di depressione possono durare dai sei mesi a un anno. La Depressione Maggiore è solo una delle varie forme di disturbo depressivo. Altre forme di depressione sono la distimia (depressione minore), e la depressione bipolare (che è poi la fase depressiva del disturbo bipolare, anche chiamato disturbo maniaco-depressivo). Il disturbo depressivo maggiore è stato inserito nel 1980 all’interno del DSM-III, il Manuale statistico e diagnostico dei disturbi mentali. La depressione maggiore è inserita anche nella quinta e più recente edizione del DSM (il DSM-5).
Leggi anche:
Cos’è la depressione minore?
La depressione minore, o distimia o ancora disturbo distimico, è un disturbo cronico caratterizzato dalla presenza di umore depresso che persiste per la maggior parte del giorno ed è presente nella maggior parte dei giorni. Secondo la quarta e penultima edizione del Diagnostic and Statistical Manual of Mental Disorders (DSM-IV) le più caratteristiche manifestazioni del disturbo erano sentimenti di inadeguatezza, colpa, irritabilità e rabbia; ritiro sociale; perdita di interesse, inattività e mancanza di produttività. Il termine “distimia”, indicativo “di cattivo umore”, fu introdotto nel 1980 e modificato in disturbo distimico nel DSM-IV. Prima del 1980, la maggior parte dei pazienti ora classificati come affetti da disturbo distimico era classificata come affetta da nevrosi depressiva (detta anche depressione nevrotica). Il disturbo distimico è comune nella popolazione generale e colpisce il 3-5% di tutti gli individui. II disturbo distimico è più frequente tra le persone non sposate e giovani e in quelle a basso reddito. Inoltre, il disturbo distimico spesso coesiste con altri disturbi mentali, soprattutto il disturbo depressivo maggiore, i disturbi d’ansia (in particolare quello da attacchi di panico), l’abuso di sostanze e probabilmente il disturbo borderline di personalità.
I criteri diagnostici del DSM per il disturbo distimico richiedono la presenza di umore depresso per la maggior parte del tempo per almeno due anni. Perché i criteri diagnostici siano soddisfatti, il soggetto non dovrebbe presentare sintomi meglio classificabili come disturbo depressivo maggiore. Il paziente non dovrebbe aver mai avuto un episodio maniacale o ipomaniacale.
II disturbo distimico è un disturbo cronico caratterizzato non da episodi di malattia, ma piuttosto dalla costante presenza dei sintomi. Tuttavia, il paziente con disturbo distimico può presentare alcune variazioni temporali nella gravità dei sintomi. Gli stessi sintomi sono simili a quelli del disturbo depressivo maggiore e la presenza di umore depresso – cioè il sentirsi triste, giù di corda, il vedere tutto nero e la mancanza di interesse nelle abituali attività – è un aspetto centrale del disturbo. La gravità dei sintomi depressivi nel disturbo distimico è di solito minore che nel disturbo depressivo maggiore, ma è la mancanza di episodi discreti a far pesare la bilancia a favore della diagnosi di disturbo distimico.
I pazienti con disturbo distimico possono spesso essere sarcastici, nichilisti, meditabondi, esigenti e reclamanti; possono essere tesi e rigidi e resistenti nei confronti degli interventi terapeutici, pur presentandosi regolarmente agli appuntamenti. Come risultato, il medico può provare rabbia nei confronti del soggetto e persino trascurarne le lamentele. Per definizione le persone con disturbo distimico non hanno sintomi psicotici.
I sintomi associati comprendono alterazioni dell’appetito e del sonno, ridotta autostima, perdita di energia, rallentamento psicomotorio, ridotta pulsione sessuale e preoccupazione ossessiva per i problemi di salute.
Una difficoltà nei rapporti sociali è talora la ragione per cui i pazienti con disturbo distimico cercano una cura. In effetti divorzio, disoccupazione e problemi sociali sono comuni in questi pazienti. Essi possono lamentarsi di avere difficoltà di concentrazione e riferire che le loro prestazioni scolastiche o lavorative sono scadenti. Lamentandosi di essere malati fisicamente, i pazienti possono perdere giorni di lavoro e appuntamenti sociali. I soggetti con disturbo distimico possono avere problemi coniugali derivanti da disfunzioni sessuali (ad esempio impotenza) o dall’incapacità di mantenere l’intimità emotiva.
Depressione doppia: il 40% circa dei soggetti con disturbo depressivo maggiore soddisfa anche i criteri per disturbo distimico. Questa combinazione di disturbi viene spesso definita depressione doppia. I dati disponibili sostengono la conclusione che i pazienti con depressione doppia hanno una prognosi peggiore di quelli con solo disturbo depressivo maggiore. Il trattamento dei casi di depressione doppia dovrebbe essere diretto verso entrambi i disturbi, poiché la risoluzione dei sintomi di un disturbo depressivo maggiore in tali pazienti li lascia ancora con un significativo problema psichiatrico.
Leggi anche:
Differenze tra i vari tipi di depressione
Il disturbo depressivo minore è caratterizzato da episodi di sintomi depressivi meno gravi di quelli osservati nel disturbo depressivo maggiore. La differenza fra disturbo distimico e disturbo depressivo minore è legata principalmente alla natura episodica dei sintomi nel secondo. Fra un episodio e l’altro, i pazienti con disturbo depressivo minore hanno infatti umore eutimico, mentre quelli con disturbo distimico non hanno praticamente periodi eutimici.
Cause
Possibili cause di depressione maggiore e minore, sono:
1) Eventi della vita e stress ambientali. Un’osservazione clinica di vecchia data che è stata replicata è che eventi stressanti della vita molto più spesso precedono i primi episodi di disturbo dell’umore rispetto a episodi successivi. Questa associazione è stata riportata per pazienti sia con disturbo depressivo maggiore sia con disturbo bipolare I. Una teoria proposta per spiegare questa osservazione è che lo stress che accompagna il primo episodio determini alterazioni durature nella biologia del cervello. Tali alterazioni perduranti possono risultare in cambiamenti nello stato funzionale dei vari neurotrasmettitori e dei sistemi intraneuronali e possono anche includere la perdita di neuroni e una riduzione eccessiva nei contatti sinaptici. Il risultato netto di questi cambiamenti è che essi aumentano nella persona il rischio di manifestare episodi successivi di un disturbo dell’umore, anche in assenza di un evento stressante esterno. Da una prospettiva psicodinamica, il medico è sempre interessato al significato del fattore stressante. La ricerca ha dimostrato che il fattore stressante percepito dal paziente come maggiormente condizionante in modo negativo l’autostima più probabilmente produce depressione. Inoltre quello che può sembrare un fattore stressante relativamente lieve a persone esterne può essere devastante per il paziente a causa dei significati particolarmente idiosincrasici connessi all’evento. Alcuni medici sono assolutamente convinti che gli eventi della vita giochino un ruolo primario o principale nella depressione; altri suggeriscono che abbiano solo un ruolo limitato nell’esordio e nella cadenza degli episodi depressivi.
I dati più significativi mostrano che l’evento vitale più frequentemente associato al successivo sviluppo di depressine è la perdita di un genitore prima dell’età di 11 anni. Lo stress ambientale maggiormente associato all’esordio di un episodio depressivo è la perdita del coniuge.
2) Famiglia. Molti articoli teorici e molte segnalazioni aneddotiche riguardano la relazione fra il funzionamento della famiglia e l’inizio o il decorso di un disturbo dell’umore, in particolare il disturbo depressivo maggiore. Numerosi dati mostrano che la psicopatologia osservata nella famiglia durante il periodo in cui il paziente identificato è stato trattato tende a rimanere anche dopo che il soggetto si è rimesso. Inoltre, il grado di psicopatologia nella famiglia può condizionare il tasso di recupero, la ricomparsa dei sintomi e l’adattamento del paziente dopo il recupero. Dati clinici e aneddotici sostengono l’importanza di valutare la vita familiare di un individuo e di prendere in esame tutti gli eventi stressanti riconosciuti come correlati alla famiglia.
3) Fattori della personalità premorbosa. Nessun tratto singolo e nessun tipo di personalità predispone da solo un soggetto alla depressione; tutti gli esseri umani, con qualunque personalità, possono diventare e in effetti divengono depressi in circostanze appropriate. Tuttavia alcuni tipi di personalità – dipendenti, ossessivo-compulsivi e isterici – possono avere un maggiore rischio di depressione rispetto a tipi di personalità antisociale, paranoide o altri tipi che possono utilizzare la proiezione e altri meccanismi difensivi di estemalizzazione per proteggere se stessi dalla rabbia interna. Nessuna evidenza indica che un particolare disturbo di personalità sia associato allo sviluppo successivo di un disturbo bipolare I, ma quelli con disturbo distimico e ciclotimico hanno un rischio maggiore di sviluppare successivamente un disturbo bipolare I.
Sintomi
I sintomi principali della depressione maggiore e minore, sono:
- un persistente umore triste o irritabile;
- importanti variazioni nelle abitudini del dormire (insonnia e altri disturbi del sonno), dell’appetito e del movimento;
- difficoltà nel pensare, della concentrazione, e della memoria;
- mancanza di interesse o piacere nelle attività che invece prima interessavano;
- sentimenti di colpa, di inutilità, mancanza di speranze e senso di vuoto;
- pensieri ricorrenti di morte o di suicidio;
- sintomi fisici persistenti che non rispondono alle cure come mal di testa, problemi di digestione, dolori persistenti e generalizzati.
Non tutti questi sintomi possono essere presenti contemporaneamente.
Come si manifesta la depressione?
E’ raro che una persona depressa abbia contemporaneamente tutti i sintomi riportati precedentemente, ma se soffre quotidianamente dei primi due sintomi su descritti e di almeno altri tre è molto probabile che abbia un disturbo depressivo.
Spesso la depressione si associa ad altri disturbi, sia psicologici (frequentemente di ansia) sia medici. In questi casi la persona si deprime per il fatto di avere un disturbo psicologico o medico. 25 persone su 100 che soffrono di un disturbo organico, come il diabete, la cardiopatia, l’HIV, l’invalidità corporea fino ad arrivare ai casi di malattie terminali, si ammalano anche di depressione. Purtroppo la depressione può portare ad un aggravamento ulteriore, dato che quando si è depressi si ha difficoltà a collaborare nella cura, perché ci si sente affaticati, sfiduciati, impotenti e si ha una scarsa fiducia di migliorare. Inoltre, la depressione può complicare la cura anche per le conseguenze negative che può avere sul sistema immunitario e sulla qualità di vita già compromessa dalla malattia medica.
I sintomi depressivi possono alternarsi, e a volte presentarsi in contemporanea, a sintomi di eccitamento (euforia, irritazione, impulsività, loquacità, pensieri veloci che si accavallano e a cui è difficile stare dietro, sensazioni di grandiosità, infinita potenzialità personale o convinzioni di essere perseguitati). In questo caso si tratta di episodi depressivi o misti all’interno di un disturbo bipolare dell’umore.
Leggi anche:
Decorso e conseguenze della depressione
La depressione è un disturbo spesso ricorrente e cronico. Chi si ammala di depressione può facilmente soffrirne più volte nell’arco della vita. Mentre nei primi episodi l’evento scatenante è facilmente individuabile in un evento esterno che la persona valuta e sente come perdita importante e inaccettabile, nelle ricadute successive gli eventi scatenanti sono difficilmente individuabili perché spesso si tratta di eventi “interni” all’individuo come un normale abbassamento dell’umore, che per chi è stato depresso già diverse volte è preoccupante e segnale di ricaduta.
Il disturbo depressivo può portare a gravi compromissioni nella vita di chi ne soffre. Non si riesce più a lavorare o a studiare, a iniziare e mantenere relazioni sociali e affettive, a provare piacere e interesse nelle attività. 15 persone su 100 che soffrono di depressione clinica grave muoiono per suicidio. Più giovane è la persona colpita, più le compromissioni saranno gravide di conseguenze. Per esempio un adolescente depresso non riesce a studiare e ad avere relazioni, e quindi non riesce a costruire i mattoni su cui costruire il proprio futuro.
Diagnosi
Secondo la quanti a più recente edizione del Manuale statistico e diagnostico dei disturbi mentali (DSM-5), per poter stabilire una diagnosi di depressione maggiore, devono essere presenti almeno cinque dei seguenti sintomi:
- perdita di interesse e piacere nel fare qualsiasi cosa;
- agitazione psicomotoria o rallentamento psicomotorio;
- difficoltà nel pensare e restare concentrati, oppure patologica indecisione;
- stanchezza cronica;
- umore depresso (ad esempio sentire di non avere un futuro, essere tristi, vuoti, senza speranza);
- significativa perdita di peso o aumento di peso;
- sentimenti di indegnità o sensi di colpa eccessivi o inappropriati;
- ricorrenti pensieri di morte o di suicidio oppure reali tentativi di suicidio.
Per raggiungere una diagnosi, almeno uno dei sintomi sopra elencati deve essere umore depresso o perdita di interesse nel fare qualsiasi cosa.
Terapie
Come si cura la depressione? Esistono varie terapie disponibili. Le principali cure sono rappresentate da farmaci e psicoterapia, che agiscono in sinergia tra loro.
Psicoterapia Cognitivo-Comportamentale
La psicoterapia Cognitivo-Comportamentale (TCC): ha mostrato scientificamente una buona efficacia sia sui sintomi acuti che sulla ricorrenza. A volte è necessario associare la TCC ai farmaci antidepressivi o ai regolatori dell’umore, soprattutto nelle forme moderate-gravi. L’associazioni della Terapia Cognitivo-Comportamentale e i farmaci aumentano l’efficacia della cura. Nel corso della Psicoterapia Cognitivo-Comportamentale la persona viene aiutata a prendere consapevolezza dei circoli viziosi che mantengono e aggravano la malattia e a liberarsene gradualmente attraverso la riattivarsi del comportamento e l’acquisizione di modalità di pensiero e di comportamento più funzionali. Inoltre, dal momento che la depressione è un disturbo ricorrente, la TCC prevede una particolare attenzione alla cura della vulnerabilità alla ricaduta. Per far questo utilizza anche specifici protocolli, come la Schema-Therapy, il lavoro sul Benessere Psicologico e la Mindfulness.
Farmaci
I primi farmaci antidepressivi furono scoperti verso la metà degli anni Cinquanta. Da allora numerosi sono stati gli antidepressivi immessi nel mercato. Non tutti hanno avuto successo, alcuni hanno resistito all’arrivo dei nuovi farmaci, altri sono usciti dal commercio perché o poco efficaci di per sé o perché surclassati dai nuovi arrivati o perché gravati da maggiori effetti collaterali. Generalmente gli antidepressivi si suddividono in gruppi in funzione della struttura chimica o del/i neuromediatore/i su cui agiscono. Ecco alcuni farmaci usati in caso di depressione:
- gli inibitori delle monoaminoossidasi o I-MAO,
- gli antidepressivi triciclici o TCA,
- gli antidepressivi Atipici,
- inibitori selettivi del reuptake di uno o più neuromediatori:
- gli SSRI: serotonin selective reuptake inhibitors,
- i NaRI: noradrenalin reuptake inhibitors,
- gli SNRI: serotonin-noradrenalin reuptake inhibitors,
- i NaSSA: noradrenergic and specific serotonergic antidepressants, modulatori della trasmissione serotoninergica e noradrenergica.
Leggi anche:
Come può una sostanza chimica modificare emozioni e sentimenti?
Per comprendere come delle sostanze chimiche possano agire sulle emozioni e sui sentimenti è necessario fare una breve premessa sul funzionamento del cervello . Le cellule che consentono il funzionamento del cervello sono i neuroni, delle cellule specializzate nella trasmissione degli impulsi. I neuroni sono collegati tra loro a formare dei circuiti deputati prevalentemente a specifiche funzioni (sensazioni, movimento, emozioni/sentimenti, integrazione di esperienze diverse, funzioni vegetative, ecc.). Il sistema che si attiva quando il soggetto prova delle emozioni o agisce sotto la spinta delle emozioni è il sistema limbico. In condizioni di normale equilibrio, i neuroni di questo sistema controllano l’umore, l’iniziativa, la volontà, ecc. in risposta a stimoli provenienti dall’esterno e dall’interno del nostro organismo. Quando questo equilibrio si altera per qualsiasi ragione, interna o esterna, i neuroni non riescono più a comunicare tra loro in maniera efficiente perché i neuromediatori che consentono il passaggio dello stimolo tra i neuroni sono ridotti e/o è alterata la sensibilità dei rispettivi recettori. È così che compaiono i sintomi dei disturbi dell’umore. Nel caso si sviluppi la malattia, queste alterazioni tendono a stabilizzarsi e richiedono, perciò, un intervento terapeutico per essere riportate al normale funzionamento. Se è l’alterazione dei neuromediatori, ed in particolare di Noradrenalina, Serotonina e Dopamina, alla base dell’alterato funzionamento del sistema limbico e quindi del disturbo dell’umore, è ipotizzabile che normalizzando questi neuromediatori si possa ripristinare il funzionamento del sistema e riportare così l’umore al suo normale equilibrio.
Farmaci antidepressivi: quali i rischi?
Gli antidepressivi comportano – in varia misura – effetti indesiderati e rischi: in linea generale, la tollerabilità e la sicurezza di questi farmaci sono molto migliorate passando da quelli di prima generazione a quelli ad attività selettiva su specifici neuromediatori.
- Gli I-MAO comportano interazioni anche gravi se assunti assieme a determinati farmaci o alimenti; questo li rende farmaci da usare con molta cautela ed in pazienti che garantiscano (magari anche con l’aiuto dei familiari) il massimo rispetto delle regole alimentari e/o terapeutiche.
- I TCA sono farmaci gravati da numerosi effetti indesiderati, generalmente sgradevoli ma non pericolosi; gli elementi più critici, nel trattamento normale, sono rappresentati dal glaucoma ad angolo chiuso, dall’ipertrofia prostatica, dall’infarto miocardico recente e dai disturbi della conduzione cardiaca che possono aggravarsi provocando situazioni di rischio. I problemi maggiori sono legati all’overdose (accidentale o a scopo suicidario), che può risultare letale, ed all’associazione con gli I-MAO.
- Gli Antidepressivi Atipici si pongono, in generale, un gradino al di sopra rispetto ai TCA per tollerabilità e sicurezza (con le dovute eccezioni, danno meno effetti indesiderati e sono meno pericolosi anche nell’overdose (ma sono, forse, anche un po’ meno efficaci) e mantengono l’incompatibilità con gli I-MAO.
- Gli inibitori selettivi del reuptake sono molto più sicuri in caso di overdose, ma rimane la possibilità di effetti negativi, come la sindrome serotoninergica (una condizione tossica iperserotoninergica, la cui causa più comune è l’interazione tra agenti serotoninergici, come gli SSRI ed i TCA, e gli I-MAO).
- Degli SSRI (e di alcuni di essi in particolare) si è parlato, anche del tutto recentemente, come di farmaci potenzialmente capaci di indurre il suicidio in alcuni casi specifici. Generalmente, i principali effetti collaterali indotti dagli inibitori selettivi del riassorbimento della serotonina sono: nausea, diarrea, agitazione, ansia, insonnia e disfunzioni della sfera sessuale.
Test di autovalutazione della depressione
Per una valutazione iniziale, potete eseguire un test per valutare in modo autonomo la possibile presenza di una depressione, fermo restando che la diagnosi vera e propria spetta solo al medico. Per fare il test, scarica questo pdf e segui le istruzioni: test-di-autovalutazione-della-depressione-zung
Se hai spesso idee suicidarie, non riesci a trovare una “via d’uscita” ai tuoi problemi o credi di soffrire di depressione, prenota la tua visita e, grazie ad una serie di colloqui riservati, ti aiuterò a risolvere definitivamente il tuo problema.

Leggi anche:
- Combatti lo stress e ritrova il benessere psicofisico con il decalogo del buonumore
- Test di Rorschach: immagini, a cosa serve, interpretazione
- Disturbo post-traumatico da stress rivivere ogni giorno una esperienza drammatica
- Dismorfismo corporeo: i sintomi della percezione distorta del proprio corpo
- Disturbo dell’identità dell’integrità corporea: voler essere disabili
- Liberarsi dalla dipendenza affettiva e dalla paura dell’abbandono
- Dipendenza affettiva: riconoscerla, affrontarla e superarla
- Farmaci antidepressivi: cosa sono, a cosa servono e quali tipi esistono
- Sostanze naturali ad azione antidepressiva
- Farmaci Inibitori Selettivi della Ricaptazione della Serotonina (SSRI): cosa sono ed a che servono
- I peggiori modi per essere lasciati da qualcuno
- Mi sento così sola, perché non riesco a trovare l’amore?
- Ecco perché in amore “aspettare” è quasi sempre inutile
- Le migliori scuse per lasciare qualcuno, per lui e per lei
- In amore chi deve fare il primo passo, l’uomo o la donna?
- Come fare il primo passo con un ragazzo?
- Gli piaccio, ma lui non non si fa avanti: perché?
- Coppia: le cose per cui non vale MAI la pena litigare
- Primo appuntamento: ecco come fare colpo su di lui
- Ci siamo lasciati: adesso come si fa?
- Sono gelosa delle sue ex: come fare?
- Superare la fine di una storia, come riuscirci?
- Tutti i motivi per cancellare il tuo ex fidanzato da Facebook
- “Mi ha lasciato e non mi cerca”: cosa fare quando lui (o lei) ti lascia
- Perché si soffre così tanto per amore?
- Lui mi ha lasciata all’improvviso, senza una spiegazione: che fare?
- Cosa fare quando si soffre per amore
- Antidepressivi SSRI: meccanismo d’azione e farmacocinetica
- SSRI: efficacia in depressione, disturbo ossessivo compulsivo, ansia ed eiaculazione precoce
- SSRI: uso di antidepressivi in gravidanza ed allattamento
- SSRI: effetti collaterali, disfunzioni sessuali, sospensione e suicidio
- Disfunzione sessuale post-SSRI: sintomi, effetti a lungo termine e cure
- SSRI: effetti a breve e lungo termine
- SSRI in pazienti con diabete, iponatriemia, osteoporosi e prolungamento QT
- Inibitori della ricaptazione della serotonina-norepinefrina (SNRI)
- Disturbo ossessivo compulsivo: il trattamento con farmaci e terapia cognitivo-comportamentale è la migliore scelta
- Citalopram (Elopram): modalità d’assunzione e meccanismo d’azione
- Citalopram (Elopram): lista degli effetti collaterali del farmaco
- Citalopram (Elopram): interruzione, astinenza, diabete e prolungamento QT
- Citalopram (Elopram): uso in gravidanza ed allattamento
- Fluoxetina (Fluoxeren): meccanismo d’azione del farmaco
- Fluoxetina (Fluoxeren): lista degli effetti collaterali e diabete
- Fluoxetina (Fluoxeren): uso in gravidanza ed allattamento
- Antidepressivi triciclici: tipi, indicazioni e meccanismo di azione
- Antidepressivi triciclici: tipici effetti collaterali dei farmaci
- Antidepressivi triciclici: overdose, tossicità e trattamento
- Antipsicotici (neurolettici): classificazione, usi e meccanismo di azione
- Farmaci antipsicotici: differenza tra neurolettici tipici ed atipici
- Farmaci antipsicotici (neurolettici): lista degli effetti collaterali
- I difetti femminili che gli uomini odiano e che le donne sottovalutano spesso
- Perché la donna tradisce l’uomo? Nove donne raccontano senza censure il loro tradimento
- Un semplice test per misurare i tuoi livelli di autostima e migliorarli
- Aumenta la tua autostima ed impara ad amarti
- Il peggior nemico siamo noi stessi: i segnali che ci stiamo autosabotando
- Scopri come affronti la vita e le sue difficoltà, con il “Test del bosco”
- Impara a camminare da solo e non cadrai mai
- Le 5 cose che indicano che stai con qualcuno che ti farà sicuramente soffrire
- I 10 uomini da evitare accuratamente in una relazione
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn e su Pinterest, grazie!
Condividi questo articolo:
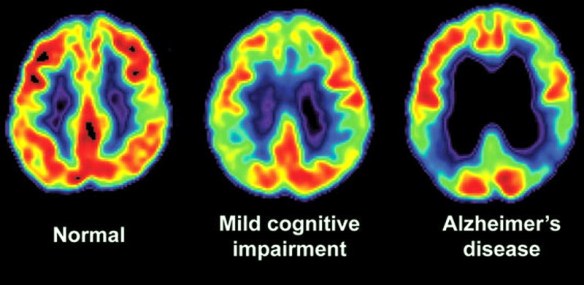 Diversi test di screening neuropsicologico vengono utilizzati per la diagnostica nei casi di Alzheimer. I test valutano diverse funzioni e competenze cognitive, come il saper copiare disegni simili a quelli mostrati nella foto, ricordare parole, leggere e sottrarre numeri in serie. Test neuropsicologici come il Mini Mental State Examination (MMSE), sono ampiamente utilizzati per valutare i disturbi cognitivi che vengono considerati per la formulazione della diagnosi. Una batteria di test più completa è necessaria per garantire la massima affidabilità dei risultati, in particolare nelle prime fasi della malattia. L’esame neurologico nelle prime fasi della malattia solitamente presenta risultati normali, fatta eccezione per evidenti deficit cognitivi che non differiscono però da quello derivanti da altre malattie di tipo demenziale.
Diversi test di screening neuropsicologico vengono utilizzati per la diagnostica nei casi di Alzheimer. I test valutano diverse funzioni e competenze cognitive, come il saper copiare disegni simili a quelli mostrati nella foto, ricordare parole, leggere e sottrarre numeri in serie. Test neuropsicologici come il Mini Mental State Examination (MMSE), sono ampiamente utilizzati per valutare i disturbi cognitivi che vengono considerati per la formulazione della diagnosi. Una batteria di test più completa è necessaria per garantire la massima affidabilità dei risultati, in particolare nelle prime fasi della malattia. L’esame neurologico nelle prime fasi della malattia solitamente presenta risultati normali, fatta eccezione per evidenti deficit cognitivi che non differiscono però da quello derivanti da altre malattie di tipo demenziale.
 Nel paziente con malattia di Alzheimer, oltre al trattamento farmacologico, esistono interventi comportamentali, di supporto psicosociale e di training cognitivo che possono aiutare il soggetto. Tali misure sono solitamente integrate in maniera complementare con il trattamento farmacologico, e hanno dimostrato una loro efficacia positiva nella gestione clinica complessiva del paziente.
Nel paziente con malattia di Alzheimer, oltre al trattamento farmacologico, esistono interventi comportamentali, di supporto psicosociale e di training cognitivo che possono aiutare il soggetto. Tali misure sono solitamente integrate in maniera complementare con il trattamento farmacologico, e hanno dimostrato una loro efficacia positiva nella gestione clinica complessiva del paziente. Anche se al momento non esiste una cura efficace, sono state proposte diverse strategie terapeutiche per tentare di influenzare clinicamente il decorso della malattia di Alzheimer; tali strategie puntano a modulare farmacologicamente alcuni dei meccanismi patologici che ne stanno alla base.
Anche se al momento non esiste una cura efficace, sono state proposte diverse strategie terapeutiche per tentare di influenzare clinicamente il decorso della malattia di Alzheimer; tali strategie puntano a modulare farmacologicamente alcuni dei meccanismi patologici che ne stanno alla base.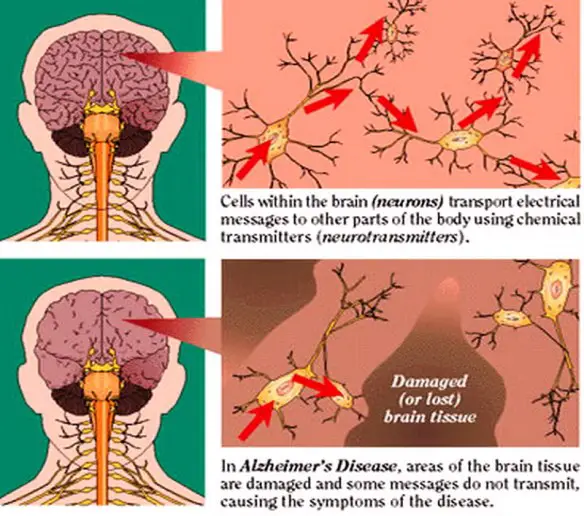 La causa per la maggior parte dei casi di Alzheimer è ancora in gran parte sconosciuta, ad eccezione che per casi dall’1% al 5% in cui sono state individuate le differenze genetiche esistenti.
La causa per la maggior parte dei casi di Alzheimer è ancora in gran parte sconosciuta, ad eccezione che per casi dall’1% al 5% in cui sono state individuate le differenze genetiche esistenti. Il decorso della malattia di Alzheimer è diviso in quattro fasi, contraddistinte da sintomi diversi:
Il decorso della malattia di Alzheimer è diviso in quattro fasi, contraddistinte da sintomi diversi: Quante volte, nella nostra vita, in un periodo triste abbiamo detto “sono depresso”? La realtà è che la depressione, nelle sue varie forme, è qualcosa di completamente diverso alla “semplice” tristezza: è il non provare più piacere, il sentirsi inutili, la fine di ogni speranza, il non vedere vie di uscita se non – a volte – addirittura il suicidio. Nel depresso non c’è bisogno che arrivi la sera per sentirsi avvolto dalle tenebre.
Quante volte, nella nostra vita, in un periodo triste abbiamo detto “sono depresso”? La realtà è che la depressione, nelle sue varie forme, è qualcosa di completamente diverso alla “semplice” tristezza: è il non provare più piacere, il sentirsi inutili, la fine di ogni speranza, il non vedere vie di uscita se non – a volte – addirittura il suicidio. Nel depresso non c’è bisogno che arrivi la sera per sentirsi avvolto dalle tenebre.
 La scienza medica ha identificato alcuni sintomi di autismo che possono rappresentare indicatori precoci della patologia a cui è bene prestare molta attenzione. Non sempre debbono essere presenti tutti gli indicatori di seguito elencati per procedere ad effettuare un approfondimento psicodiagnostico, allo stesso modo la presenza di un singolo sintomo non deve necessariamente condurre a diagnosi. Se sono presenti tutti o alcuni di questi sintomi si consiglia comunque di rivolgersi al più presto ad un medico.
La scienza medica ha identificato alcuni sintomi di autismo che possono rappresentare indicatori precoci della patologia a cui è bene prestare molta attenzione. Non sempre debbono essere presenti tutti gli indicatori di seguito elencati per procedere ad effettuare un approfondimento psicodiagnostico, allo stesso modo la presenza di un singolo sintomo non deve necessariamente condurre a diagnosi. Se sono presenti tutti o alcuni di questi sintomi si consiglia comunque di rivolgersi al più presto ad un medico. Vicino ad Amsterdam, nei Paesi Bassi, esiste una piccola città con 23 case, alcuni ristoranti, vari caffè, negozi, un salone di bellezza, un teatro e un cinema. Questa città si chiama Hogewey ed al suo interno ci vivono attualmente 152 persone, tutte anziane, e tutte affette da una grave demenza o da uno stadio avanzato di Alzheimer. Hogewey è letteralmente una casa di cura organizzata come un piccolo paese, così da permettere ai pazienti di condurre una vita quasi normale e di sentirsi a casa, e di ricevere nello stesso tempo le cure necessarie. Hogewey è stata fondata nel 2009 e da allora è diventata, specie per la sua particolare natura, un punto di riferimento importante a livello mondiale anche tra gli studiosi della demenza.
Vicino ad Amsterdam, nei Paesi Bassi, esiste una piccola città con 23 case, alcuni ristoranti, vari caffè, negozi, un salone di bellezza, un teatro e un cinema. Questa città si chiama Hogewey ed al suo interno ci vivono attualmente 152 persone, tutte anziane, e tutte affette da una grave demenza o da uno stadio avanzato di Alzheimer. Hogewey è letteralmente una casa di cura organizzata come un piccolo paese, così da permettere ai pazienti di condurre una vita quasi normale e di sentirsi a casa, e di ricevere nello stesso tempo le cure necessarie. Hogewey è stata fondata nel 2009 e da allora è diventata, specie per la sua particolare natura, un punto di riferimento importante a livello mondiale anche tra gli studiosi della demenza.