Cos’è l’anemia?
L’anemia è una condizione caratterizzata da calo di emoglobina nel sangue (l’emoglobina è la sostanza dei globuli rossi che trasporta ossigeno ai tessuti). Esistono moltissimi tipi diversi di anemia ed ognuna ha una causa specifica, ad esempio:
- l’anemia aplastica è dovuta ad un difetto del midollo osseo che non produce abbastanza globuli rossi;
- l’anemia megaloblastica è dovuta al fatto che il midollo produce sì globuli rossi, ma immaturi;
- l’anemia sideropenica è dovuta alla carenza di ferro nell’organismo (il ferro è uno dei principali ingredienti dell’emoglobina);
- l’anemia falciforme è dovuta ad un difetto di costruzione dell’emoglobina che fa assumere ai globuli rossi una forma di falce, la quale li fa “incastrare” e bloccare nel capillari.
L’anemia può anche essere causata da sanguinamento prolungato (come nel caso di chi soffre di emofilia) o da distruzione accelerata dei globuli rossi per difetti della milza e terapie farmacologiche.
Cos’è l’anemia mediterranea (talassemia)?
L’anemia mediterranea (anche chiamata “beta talassemia” in quanto si verifica una ridotta sintesi delle catene beta; denominata anche anemia di Cooley o semplicemente “talassemia”) è un tipo particolare di anemia, frequente nelle zone mediterranee, ed è una patologia a trasmissione ereditaria che si manifesta solo se si ricevono gli alleli mutati da entrambi i genitori. Chi presenta un solo allele mutato è microcitemico, non ha problemi di salute ma i suoi globuli rossi sono generalmente più piccoli della norma. La talassemia causa una riduzione della sintesi dell’emoglobina, con conseguente anemia ipocromica, cioè con globuli rossi poco colorati. Ci sono due varianti della talassemia; quella meno grave può essere asintomatica o solo lievemente sintomatica e non richiede alcuna cura, quella più grave può richiedere trasfusioni di sangue, somministrazione di emoglobina sintetica, rimozione chirurgica della milza e trapianto di cellule staminali ematopoietiche (cioè creatrici di globuli rossi).
Leggi anche:
- Emocromo: guida completa a tutti i valori del sangue normali e patologici
- Emocromo: valori di riferimento e significato clinico [SCHEMA]
- Ematocrito (HCT): basso, alto, in gravidanza, valori normali e interpretazione
- Differenza tra anemia e microcitemia
- Differenza tra anemia megaloblastica e perniciosa
- Differenza tra anemia mediterranea e falciforme
- Differenza tra emoglobina e mioglobina
- Differenza tra emoglobina fetale ed adulta
- Differenza tra emoglobina, ferro, ferritina e transferrina
- Differenza tra emoglobina e globuli rossi
- Differenza tra emocromo ed ematocrito
- Indici corpuscolari MCV, MCH, MCHC, RDW: cosa sono ed a che servono
- Volume corpuscolare medio (MCV): alto, basso, valori normali e significato
- MCH alto, basso, valori normali ed interpretazione
- MCHC alto, basso, valori normali ed interpretazione
- RDW alto, basso, valori normali ed interpretazione
- Ormoni tiroidei: differenza T3 e T4, valori normali e patologici
- TSH alto, basso e valori normali: qual è il significato clinico?
- Tireoglobulina alta, bassa, valori normali ed interpretazione
- Globuli rossi (eritrociti) alti, bassi, valori normali e interpretazione
- Globuli bianchi (leucociti) alti, bassi, valori normali ed interpretazione
- Eosinofili alti, bassi, valori normali ed interpretazione
- Neutrofili alti, bassi, valori normali ed interpretazione
- Basofili alti, bassi, valori normali ed interpretazione
- Emoglobina bassa, alta, cause e valori normali
- Emoglobina nelle urine (emoglobinuria): cause, sintomi e terapia
- Differenza tra anemia e leucemia
- Perché la mononucleosi è chiamata anche “malattia del bacio”?
- Leucemia: sintomi, cause, cure e le diverse forme
- Leucemia mieloide acuta: cause, sintomi, diagnosi e cura
- Mieloma multiplo: cause, sintomi, diagnosi e cura
- Microcitemia (talassemia) : cause, sintomi, diagnosi e cura
- Testosterone basso, alto, valori normali ed interpretazione
- Ormone follicolo stimolante (FSH) alto, basso, valori normali e significato
- Anemia da carenza di ferro: cause, sintomi e cure
- Diagnosi di laboratorio di anemia da carenza di ferro
- Aumentare il ferro in modo naturale, specie in gravidanza
- Emocromo completo con formula leucocitaria: valori, interpretazione e significato
- Differenza tra globuli rossi, bianchi e piastrine
- VES alta o bassa: cause, sintomi e valori normali della velocità di eritrosedimentazione
- Esame delle urine completo con urinocoltura: come fare e capire i risultati
- Scura o chiara, liquida o schiumosa: la tua urina rivela la tua salute
- Glicemia alta o bassa: valori normali, che patologie indica e come si controlla nei diabetici
- Azotemia (Urea) alta o bassa: valori, cause, sintomi e cosa fare
- Insulina alta: cause, diabete, prediabete, valori normali e cure
- Differenze tra il diabete di tipo 1 e 2 (insulino dipendente e resistente)
- Emoglobina glicata alta, valori normali, IFCC e diabete
- Clearance della creatinina: alta o bassa, valori, calcolo e sintomi
- Colesterolo: cos’è ed a cosa serve?
- Colesterolo e uova: si o no? Tutta la verità scientifica
- Colesterolo: gli italiani non lo misurano e non fanno prevenzione
- Colesterolo e trigliceridi: valori normali, alti, bassi ed interpretazione
- Dieta per abbassare il colesterolo: cibi consigliati e da evitare
- Differenza tra colesterolo HDL “buono” e LDL “cattivo”
- Eccesso di colesterolo (ipercolesterolemia): perché è pericoloso?
- Fattore reumatoide alto o basso? Valori normali e Reuma test
- Tiroide: dove si trova, com’è fatta e quali funzioni svolge?
- Patologie della tiroide: possono far veramente ingrassare?
- Le tue feci dicono se sei in salute: con la Scala di Bristol impara ad interpretarle
- Parassiti e vermi nelle feci: sintomi e come eliminarli con farmaci e rimedi naturali
- Coprocoltura e antibiogramma: procedura e perché si eseguono
- Esame e raccolta delle feci: come si fa nel modo corretto ed a che serve
- Feci con sangue, muco, cibo: quando preoccuparsi?
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Assumi abbastanza vitamina D? I sintomi che indicano la sua carenza e i cibi che ne contengono in abbondanza
- Differenza tra tumore benigno, maligno, neoplasia, cancro e metastasi
- Cos’è un tumore? Perché viene il cancro? Quali sono le cause?
- Acido folico (vitamina B9): a cosa serve, in quali alimenti trovarlo e perché è importante prima e durante la gravidanza
- Beta carotene: cos’è, a cosa serve e in quali cibi lo trovo?
- Ecco come il nostro corpo ci segnala la carenza di vitamine
- Hai voglia di un cibo in particolare? E’ il tuo corpo che ti rivela le carenze nutrizionali che hai
- Di cosa è composto il sangue e quali sono le sue funzioni?
- Plasma e cellule (elementi corpuscolati) che compongono il sangue
- Plasma e suoi derivati (plasmaderivati)
- Gruppi sanguigni: cosa sono e quali sono compatibili tra loro
- Differenza tra sangue, plasma e siero
- Come si ottiene il plasma?
- Plasmaferesi e donazione di sangue
- Plasma: a cosa serve e quali sono le sue funzioni?
- Differenza tra plasma liquido e secco
- Differenza tra siero e plasma
- Il plasma contiene fibrinogeno? Ed il siero?
- Come si separa il siero dal sangue?
- Qual è il volume totale del sangue (volemia) nel corpo umano?
- Da cosa viene prodotto il sangue nel corpo umano?
- Quanti litri di sangue abbiamo nel corpo?
- Quanto sangue si può donare in una sola volta?
- Ogni quanto tempo si può donare il sangue
- Quanto tempo serve per reintegrare il sangue dopo una donazione?
- Donare sangue: come fare con mestruazioni, pillola o gravidanza
- Condizioni e preparazione per donare il sangue: tutte le informazioni
- Quanto sangue possiamo perdere prima di morire dissanguati?
- Fibrinogeno: cos’è, a che serve, quali sono i suoi valori normali?
- Fibrinogeno alto o basso: valori normali ed interpretazione
- Fibrinogeno alto o basso in gravidanza: quando preoccuparsi?
- Proteggere la pelle dal freddo e prevenirne l’invecchiamento: l’importanza degli integratori di vitamine
- Hai dolori mestruali insopportabili? ti consiglio 10 formidabili rimedi naturali per alleviarli
- Dismenorrea: quando le mestruazioni sono dolorose
- Il ciclo influenza le prestazioni in palestra: il periodo migliore per allenarsi e gli esercizi da fare durante le mestruazioni
- Come alleviare i sintomi della Sindrome pre-mestruale?
- Farmaci per curare le mestruazioni dolorose e terapia non farmacologica
- Perché viene la diarrea prima e durante il ciclo mestruale e cure
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Assumi abbastanza vitamina D? I sintomi che indicano la sua carenza e i cibi che ne contengono in abbondanza
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Reddit, su Tumblr e su Pinterest, grazie!

 Il pacemaker è uno strumento elettronico capace di monitorare il battito del nostro cuore e di erogare un impulso elettrico se rileva una frequenza bassa o molto bassa. In pratica serve per risolvere quei blocchi cardiaci che causano una bradicardia patologica (ritmo cardiaco molto lento, causa di vertigini o svenimenti). Il pacemaker viene inserito attraverso un’incisione sotto la clavicola.
Il pacemaker è uno strumento elettronico capace di monitorare il battito del nostro cuore e di erogare un impulso elettrico se rileva una frequenza bassa o molto bassa. In pratica serve per risolvere quei blocchi cardiaci che causano una bradicardia patologica (ritmo cardiaco molto lento, causa di vertigini o svenimenti). Il pacemaker viene inserito attraverso un’incisione sotto la clavicola.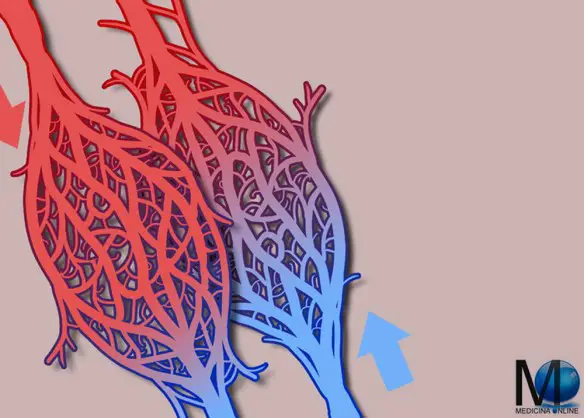 La rete mirabile è una rete di capillari sanguigni interposta tra due tronchi arteriosi (rete mirabile arteriosa) o tra due tronchi venosi (rete mirabile venosa). La rete dipende dal flusso sanguigno controcorrente (il sangue scorre all’interno dei vasi della rete in direzioni opposte) e scambia calore, ioni e gas tra le pareti dei vasi sanguigni. In questo modo si mantiene un gradiente di temperatura o di concentrazione dei gas o dei soluti tra i flussi sanguigni arteriosi e venosi. L’efficacia delle reti è determinata principalmente da quanto velocemente vengono scambiati calore, ioni o gas. Inoltre, per una data lunghezza, l’efficacia della rete decresce andando dagli scambi di calore e gas, ai piccoli ioni e alle altre sostanze.
La rete mirabile è una rete di capillari sanguigni interposta tra due tronchi arteriosi (rete mirabile arteriosa) o tra due tronchi venosi (rete mirabile venosa). La rete dipende dal flusso sanguigno controcorrente (il sangue scorre all’interno dei vasi della rete in direzioni opposte) e scambia calore, ioni e gas tra le pareti dei vasi sanguigni. In questo modo si mantiene un gradiente di temperatura o di concentrazione dei gas o dei soluti tra i flussi sanguigni arteriosi e venosi. L’efficacia delle reti è determinata principalmente da quanto velocemente vengono scambiati calore, ioni o gas. Inoltre, per una data lunghezza, l’efficacia della rete decresce andando dagli scambi di calore e gas, ai piccoli ioni e alle altre sostanze.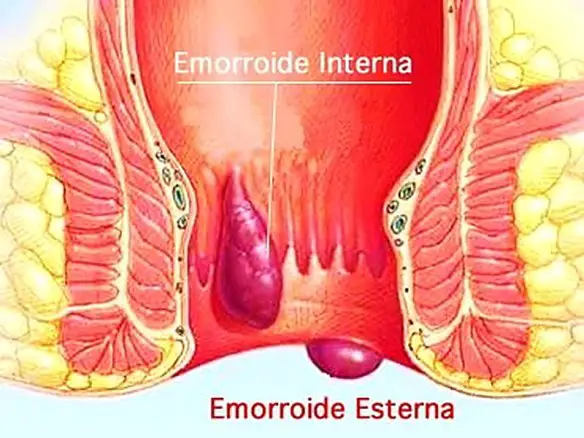 La rettorragia o proctorragia è un particolare tipo di emorragia che interessa l’ano, definita come perdita di grandi quantità di
La rettorragia o proctorragia è un particolare tipo di emorragia che interessa l’ano, definita come perdita di grandi quantità di  Il fibrinogeno è il nome con il quale si indica una proteina che fa parte del plasma. È conosciuta anche come Fattore I, fibrinogeno attivo e antigene del fibrinogeno. Il nome significa letteralmente “produttore di fibrina”. Infatti, per permettere la coagulazione del sangue, la trombina si trasforma il fibrinogeno in fibrina, dando inizio al processo di coagulazione.
Il fibrinogeno è il nome con il quale si indica una proteina che fa parte del plasma. È conosciuta anche come Fattore I, fibrinogeno attivo e antigene del fibrinogeno. Il nome significa letteralmente “produttore di fibrina”. Infatti, per permettere la coagulazione del sangue, la trombina si trasforma il fibrinogeno in fibrina, dando inizio al processo di coagulazione. Il sangue è comporto da due parti:
Il sangue è comporto da due parti: Se avete cronicamente la pressione bassa, ecco alcuni consigli che valgono soprattutto nei mesi caldi in cui la pressione tende ad abbassarsi ulteriormente:
Se avete cronicamente la pressione bassa, ecco alcuni consigli che valgono soprattutto nei mesi caldi in cui la pressione tende ad abbassarsi ulteriormente: La leucemia mieloide acuta (LMA) è una malattia che si sviluppa a partire dal midollo osseo (mieloide) e che progredisce velocemente (acuta). Le cellule del sangue sono presenti nel midollo osseo sotto forma di “precursori” e, attraverso un percorso di maturazione, si possono differenziare in globuli bianchi (tra cui i linfociti), globuli rossi, o piastrine. Se in questo percorso che li porta a diventare “adulti” i precursori” (tranne quelli dei linfociti) vanno incontro a una trasformazione in senso tumorale, si arriva alla LMA.
La leucemia mieloide acuta (LMA) è una malattia che si sviluppa a partire dal midollo osseo (mieloide) e che progredisce velocemente (acuta). Le cellule del sangue sono presenti nel midollo osseo sotto forma di “precursori” e, attraverso un percorso di maturazione, si possono differenziare in globuli bianchi (tra cui i linfociti), globuli rossi, o piastrine. Se in questo percorso che li porta a diventare “adulti” i precursori” (tranne quelli dei linfociti) vanno incontro a una trasformazione in senso tumorale, si arriva alla LMA.