 Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
I recettori possono essere suddivisi in due grandi categorie, a seconda della loro localizzazione cellulare:
- recettori transmembrana (o più semplicemente “recettori di membrana“): sono recettori che possiedono domini extracellulari, transmembrana ed intracellulari;
- recettori intracellulari: sono localizzati all’interno della cellula, distinti in recettori citosolici o nucleari, in base alla loro localizzazione rispettivamente nel citosol o nel nucleo della cellula.
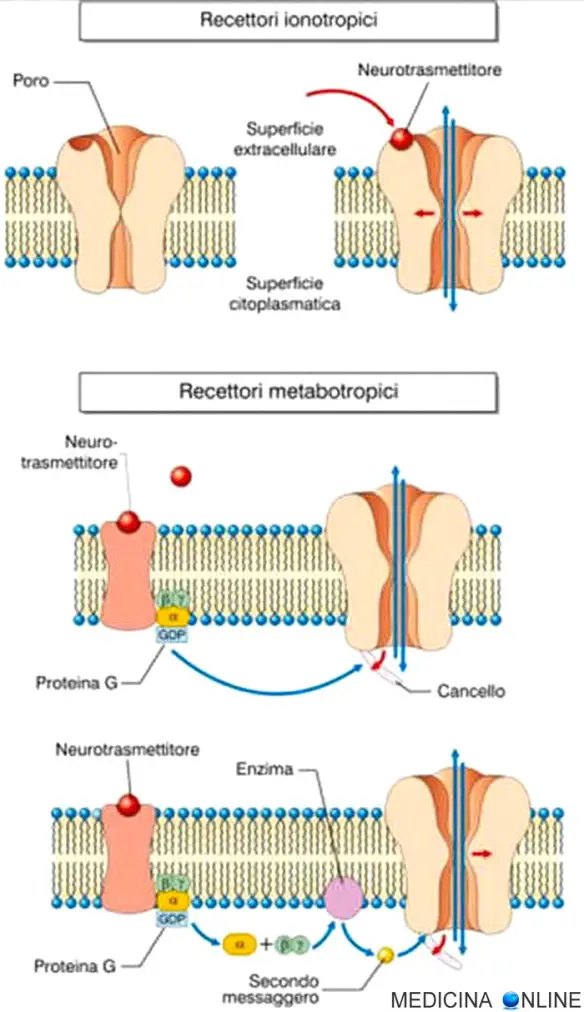
I recettori transmembrana sono suddivisibili in due differenti classi: ionotropi e metabotropici. I recettori ionotropi, definiti anche recettori-canale, sono recettori la cui apertura causa il flusso di ioni. Esistono sei tipi principali di recettori ionotropi:
- recettore colinergico nicotinico, che lega il neurotrasmettitore acetilcolina
- recettori sigma (δ)
- recettore della glicina
- recettore del GABA di tipo A e C
- recettore del glutammato
- recettore AMPA
- recettore NMDA
- recettori serotoninergici del tipo 5-HT3
I recettori metabotropici sono una classe di recettori che, in seguito all’interazione con lo specifico ligando, inducono una cascata di reazioni cellulari. Sono riconducibili a quattro tipologie recettoriali principali:
- recettori accoppiati a proteine G: strutture recettoriali transmembrana costituiti da sette domini transmembrana (TM) la cui risposta è modulata da una proteina G. Tra tali tipi di recettore possiamo trovare:
- recettore colinergico muscarinico, che lega il neurotrasmettitore acetilcolina
- recettori adrenergici, che lega le catecolammine (adrenalina e noradrenalina)
- recettore del GABA di tipo B
- recettore dell’angiotensina
- recettore dei cannabinoidi
- recettore della colecistochinina
- recettori della dopamina
- recettore dei leucotrieni
- recettori oppioidi
- recettore della rodopsina
- recettore della somatostatina
- recettori attivati da proteasi PAR
- probabilmente molti altri ancora non definiti
- recettori tirosin chinasici, tra cui:
- recettore dell’EGF (fattore di crescita epidermico)
- recettore dell’eritropoietina
- recettore dell’IGF-1
- recettori per le citochine, definiti anche recettori accoppiati a chinasi: sono recettori la cui struttura ed il meccanismo d’azione è simile a quello dei recettori tirosin chinasici. Al contrario di questi, i recettori per le citochine non hanno attività tirosin chinasica intrinseca, ma l’attività è mediata da una chinasi cellulare.
- recettori guanilil-ciclasi: sono recettori ad attività guailato-ciclasica, poco rappresentati negli organismi superiori. Si possono ricordare:
- recettore del peptide natriuretico
- recettore della guanilina
Differenza tra recettori ionotropi e metabotropi
Da quanto detto appare chiaro che i recettori ionotropici ed i recettori metabotropici hanno punti in comune ma anche differenze. Entrambi sono localizzati a livello della membrana citoplasmatica (e non nel nucleo o nel citosol) e sono perciò entrambi recettori transmembrana.
Nei recettori ionotropici il legame con il ligando causa l’apertura del canale racchiuso dal recettore stesso, invece il recettore metabotropico, al contrario del recettore ionotropico, una volta legato il ligando, avvia una serie di reazioni a cascata intracellulari mediata da un secondo messaggero ed alla base della trasduzione del segnale. Inoltre mentre il recettore ionotropo è un canale ionico, invece il recettore metabotropico non è un canale.
Leggi anche:
- Differenza tra recettori citosolici e nucleari
- Differenza tra recettori adrenergici e colinergici
- Differenza tra recettori alfa e beta adrenergici
- Differenza tra recettori muscarinici e nicotinici
- Mitocondri: definizione, dimensioni e funzioni
- Citoscheletro: funzioni e struttura
- Ribosomi e reticolo endoplasmatico: cosa sono e che funzioni svolgono?
- Nucleo cellulare: funzioni, dimensioni e membrane nucleari
- Lisosomi: cosa sono? Significato e dimensioni
- Perossisomi: definizione e funzioni
- Membrana plasmatica: definizione e funzioni
- Apparato del Golgi: spiegazione semplice e funzioni
- Citosol: definizione e funzioni
- Ipotalamo: anatomia, struttura e funzioni
- Differenze tra ipotalamo, ipofisi, neuroipofisi e adenoipofisi
- Differenza tra enzima e coenzima
- Differenza tra enzimi e catalizzatori
- Differenza tra enzimi ed ormoni
- Patologie di ipotalamo e ipofisi
- Ipofisi (ghiandola pituitaria): anatomia, funzioni e ormoni secreti
- Asse ipotalamo-ipofisario: fisiologia e ormoni rilasciati
- Ciclo di Krebs e respirazione cellulare: spiegazione facile e schema
- Quanti muscoli abbiamo nel nostro corpo?
- Differenza tra muscoli volontari, involontari, scheletrici e viscerali
- Differenza tra organismi aerobi obbligati e facoltativi con esempi
- Differenza tra organismi anaerobi obbligati, facoltativi, microaerofili ed aerotolleranti
- Differenze mitosi e meiosi in sintesi [SCHEMA]
- Differenza tra cellule eucariote e procariote
- Virus e virioni: cosa sono, come sono fatti, come funzionano e come si riproducono
- Differenza tra cellula aploide e diploide con esempi
- Riproduzione cellulare e ciclo cellulare
- Meiosi: spiegazione di tutte tappe
- Mitosi: spiegazione delle quattro fasi
- Differenza tra ipertrofia ed iperplasia con esempi
- Differenza tra ipertrofia muscolare sarcolplasmatica e miofibrillare
- Ipertrofia muscolare: cosa significa e come si raggiunge
- Differenza tra iperplasia e neoplasia
- Differenza tra atrofia, distrofia ed aplasia con esempi
- Come nasce un cancro? Cosa sono i cancerogeni e come avviene la cancerogenesi?
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

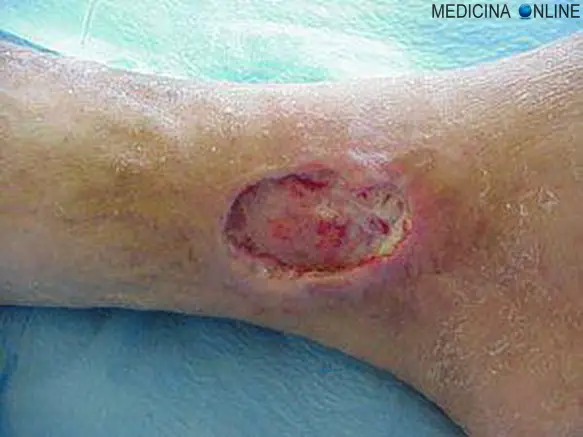 Quando nel corpo si verifica una ferita, l’organismo se possibile mette in atto un complesso processo biologico finalizzato al riempimento della soluzione di continuo rappresentata dalla ferita, con una struttura definitiva di natura connettivale chiamata “cicatrice”. Pur se generalmente il tessuto cicatriziale, che sia di epidermide o di altro tipo, ricalchi il più possibile il tessuto originario, sicuramente non possiede le medesime caratteristiche sia nell’ambito delle funzioni che della elasticità. Il tessuto cicatriziale generalmente perde in parte o totalmente le funzionalità possedute dal tessuto originario e tende ad essere meno elastico di quest’ultimo, pur essendo generalmente molto robusto e resistente. Anche se di solito il termine “cicatrice” è riferito alle ferite cutanee, in realtà può essere riferito alle ferite di tutti i tessuti biologici.
Quando nel corpo si verifica una ferita, l’organismo se possibile mette in atto un complesso processo biologico finalizzato al riempimento della soluzione di continuo rappresentata dalla ferita, con una struttura definitiva di natura connettivale chiamata “cicatrice”. Pur se generalmente il tessuto cicatriziale, che sia di epidermide o di altro tipo, ricalchi il più possibile il tessuto originario, sicuramente non possiede le medesime caratteristiche sia nell’ambito delle funzioni che della elasticità. Il tessuto cicatriziale generalmente perde in parte o totalmente le funzionalità possedute dal tessuto originario e tende ad essere meno elastico di quest’ultimo, pur essendo generalmente molto robusto e resistente. Anche se di solito il termine “cicatrice” è riferito alle ferite cutanee, in realtà può essere riferito alle ferite di tutti i tessuti biologici.
 Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco. Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco. Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.
Con “recettore” in biochimica si intende una proteina che ha la capacità di legarsi con una molecola specifica, definita “ligando”. Il legame di un recettore col proprio ligando, causa nel recettore una variazione conformazionale in seguito alla quale si ha una cascata di reazioni (trasduzione del segnale) che portano all’insorgenza di una risposta cellulare o un effetto biologico specifici. Il farmacologia il recettore è una molecola che rappresenta il bersaglio specifico di un dato farmaco: la definizione di recettore assume quindi – in ambito farmacologico – un significato più ampio rispetto al campo biochimico, essendo definito “recettore” qualsiasi struttura biologica (proteine, enzimi, lipidi, acidi nucleici…) che diviene bersaglio del farmaco.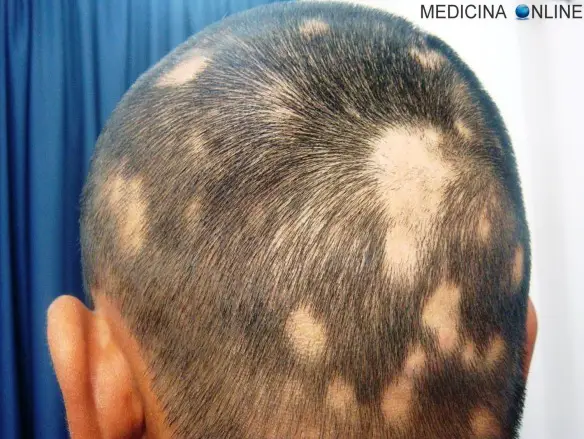 Alcuni ricercatori della Indiana University School of Medicine (USA), diretti dal dott. Karl Koehler hanno, hanno coltivato il primo tessuto cutaneo sviluppato in laboratorio completo di follicoli piliferi. Una sorta di cuoio capelluto a tutti gli effetti, sviluppato utilizzando le cellule staminali di topo, che potrà rivelarsi utile per testare farmaci, comprendere quelli per favorire la crescita dei capelli, riducendo la pratica dei test sugli animali.
Alcuni ricercatori della Indiana University School of Medicine (USA), diretti dal dott. Karl Koehler hanno, hanno coltivato il primo tessuto cutaneo sviluppato in laboratorio completo di follicoli piliferi. Una sorta di cuoio capelluto a tutti gli effetti, sviluppato utilizzando le cellule staminali di topo, che potrà rivelarsi utile per testare farmaci, comprendere quelli per favorire la crescita dei capelli, riducendo la pratica dei test sugli animali. Per capire bene i concetti di “cancro” e di “leucemia” è di fondamentale importanza comprendere il significato del termine “tumore”. Un tumore (anche chiamato “neoplasia“) è una massa di tessuto anormale che origina da una singola cellula mutata nel suo DNA e che cresce in eccesso ed in modo incontrollato rispetto ai tessuti normali. Un tumore, al contrario dei tessuti sani, ha potenzialmente la caratteristica di invadere i tessuti e gli organi circostanti, per continuità o tramite il sistema circolatorio o quello linfatico, grazie alle metastasi.
Per capire bene i concetti di “cancro” e di “leucemia” è di fondamentale importanza comprendere il significato del termine “tumore”. Un tumore (anche chiamato “neoplasia“) è una massa di tessuto anormale che origina da una singola cellula mutata nel suo DNA e che cresce in eccesso ed in modo incontrollato rispetto ai tessuti normali. Un tumore, al contrario dei tessuti sani, ha potenzialmente la caratteristica di invadere i tessuti e gli organi circostanti, per continuità o tramite il sistema circolatorio o quello linfatico, grazie alle metastasi.