 Gli antidepressivi sono una classe di farmaci, appartenenti alla categoria degli psicofarmaci, utilizzati nel trattamento di diverse patologie psichiatriche. Nonostante il loro nome, gli antidepressivi si sono dimostrati efficaci non soltanto nella cura della depressione, ma anche nella cura di altre condizioni quali i disturbi dell’ansia (ansia generalizzata ed attacchi di panico), il disturbo ossessivo compulsivo, i disturbi dell’alimentazione, disturbo post traumatico da stress, alcuni disturbi della sfera sessuale (come l’eiaculazione precoce o le parafilie patologiche) e alcuni disturbi mediati dagli ormoni (come la dismenorrea, vampate post-menopausa o il disturbo disforico premestruale). Da soli o assieme agli anticonvulsivanti (per esempio, la carbamazepina o il valproato), alcuni di questi farmaci possono essere usati per il trattamento del deficit di attenzione e iperattività (ADHD) e l’abuso di sostanze stupefacenti. Gli antidepressivi sono talvolta utilizzati per il trattamento di altre condizioni non prettamente psichiatriche come le emicranie, il dolore cronico, l’enuresi notturna, fibromialgia, disturbi del sonno o della roncopatia.
Gli antidepressivi sono una classe di farmaci, appartenenti alla categoria degli psicofarmaci, utilizzati nel trattamento di diverse patologie psichiatriche. Nonostante il loro nome, gli antidepressivi si sono dimostrati efficaci non soltanto nella cura della depressione, ma anche nella cura di altre condizioni quali i disturbi dell’ansia (ansia generalizzata ed attacchi di panico), il disturbo ossessivo compulsivo, i disturbi dell’alimentazione, disturbo post traumatico da stress, alcuni disturbi della sfera sessuale (come l’eiaculazione precoce o le parafilie patologiche) e alcuni disturbi mediati dagli ormoni (come la dismenorrea, vampate post-menopausa o il disturbo disforico premestruale). Da soli o assieme agli anticonvulsivanti (per esempio, la carbamazepina o il valproato), alcuni di questi farmaci possono essere usati per il trattamento del deficit di attenzione e iperattività (ADHD) e l’abuso di sostanze stupefacenti. Gli antidepressivi sono talvolta utilizzati per il trattamento di altre condizioni non prettamente psichiatriche come le emicranie, il dolore cronico, l’enuresi notturna, fibromialgia, disturbi del sonno o della roncopatia.
I farmaci più comunemente associati a questa classe sono gli inibitori della monoamino ossidasi (MAOIs), gli antidepressivi triciclici (TCAs), gli inibitori selettivi della ricaptazione della serotonina (SSRIs) e della serotonina-noradrenalina (SNRIs), gli antidepressivi atipici (o di seconda generazione). La loro efficacia, meccanismo di azione ed effetti collaterali sono continuo oggetto di approfondimento e ne fanno una delle classi di farmaci maggiormente studiate.
Leggi anche:
- Sostanze naturali ad azione antidepressiva
- Disturbo ossessivo compulsivo: il trattamento con farmaci e terapia cognitivo-comportamentale è la migliore scelta
Tipi di antidepressivi
Esistono molti composti approvati per il trattamento della depressione che possono essere classificati in base al loro meccanismo d’azione fondamentale, principalmente in inibitori del reuptake delle monoammine (che bloccano i processi di recupero di questi neurotrasmettitori), inibitori degli enzimi degradativi (come gli IMAO) e agonisti/antagonisti recettoriali (cioè dei farmaci in grado di attivare o disattivare particolari “interruttori” biologici).
Anche altri farmaci formalmente approvati per altri disturbi e che non rientrano nella categoria degli antidepressivi hanno un effetto antidepressivo ma i limiti del loro utilizzo (dovuti ad esempio ad uno scarso profilo di effetti collaterali, al potenziale d’abuso, alla scarsa tollerabilità nel lungo termine) hanno causato controversie circa il loro utilizzo per tale scopo ed inoltre la prescrizione per condizioni altre da quelle ufficialmente approvate rappresenta sempre un rischio, nonostante la possibile efficacia superiore. Ad esempio gli antipsicotici a basso dosaggio e le benzodiazepine possono essere utilizzati per la gestione della depressione (anche in aggiunta ad un antidepressivo), sebbene l’uso di benzodiazepine possa causare dipendenza e quello di antipsicotici altri effetti collaterali. Gli oppioidi sono stati utilizzati per trattare la depressione maggiore fino alla fine degli anni cinquanta e le anfetamine fino alla metà degli anni sessanta. Sia gli oppioidi che le anfetamine inducono una risposta terapeutica molto veloce, mostrando risultati entro ventiquattro o quarantotto ore e i loro indici terapeutici sono maggiori di quelli degli antidepressivi triciclici. In un piccolo studio pubblicato nel 1995, l’oppioide buprenorfina si è mostrato essere un buon candidato per il trattamento della depressione grave, resistente al trattamento. Recentemente altre sostanze d’abuso come la ketamina o la psilocibina, opportunamente utilizzate, hanno mostrato degli spiccati e rapidi effetti antidepressivi e i loro derivati saranno probabilmente alla base di una futura generazione di farmaci.
Anche alcuni estratti di origine naturale, spesso classificati come integratore alimentare, mostrano un effetto antidepressivo (anche se la portata del loro effetto è stata a volte messa in discussione): ad esempio l’estratto dell’erba di San Giovanni è comunemente utilizzato come antidepressivo specialmente in Europa; alcuni probiotici hanno mostrato di migliorare sintomi di ansia e depressione in trial clinici e modelli animali, mettendo in luce il collegamento tra salute intestinale e mentale; L’Acetil l-Carnitina ha mostrato in uno studio rapido effetto nel trattamento della distimia; l’inositolo in uno studio ha mostrato in uno studio un effetto ansiolitico paragonabile a quello della fluoxetina; l’Adenosil Metionina (SAMe) è ampiamente pubblicizzato come alterativa naturale agli antidepressivi; la nicotinaagisce come antidepressivo, tramite la stimolazione del rilascio di Dopamina e Norepinefrina e la desensibilizzazione dei recettori della nicotina a seguito della tolleranza.
Principali farmaci antidepressivi
Nella sequente tabella elenchiamo le principali classi di antidepressivi con i rispettivi principi attivi:
- TCA (antidepressivi triciclici)
- Imipramina, Amitriptilina, Clomipramina, Doxepina, Dosulepina, Trimipramina, Nortriptilina,
- IMAO ( inibitori delle monoamino ossidasi)
- Tranilcipromina, Fenelzina, Isocarboxazide, Moclobemide
- SSRI (inibitori selettivi della ricaptazione della serotonina)
- Citalopram, Escitalopram, Paroxetina, Fluoxetina, Fluvoxamina, Sertralina
- NaRI (Inibitori della Ricaptazione della NorAdrenalina)
- Reboxetina
- SNRI (inibitori della ricaptazione della serotonina-norepinefrina)
- Venlafaxina, Duloxetina
- NDRI (inibitori della ricaptazione della noradrenalina e della dopamina)
- Bupropione
- Altri
- Mirtazapina, Trazodone, Agomelatina, Tianeptina, Sulpiride\Amilsupride, Mianserina
Criteri di prescrizione di un farmaco antidepressivo
Attualmente non è possibile stabilire quale particolare alterazione del funzionamento cerebrale sia la causa di un disturbo depressivo in un dato paziente, per cui non è possibile prevedere quale sarà il farmaco più efficace per il trattamento della patologia. I diversi farmaci antidepressivi hanno mostrato una capacità all’incirca comparabile nel determinare una riduzione dei sintomi (nel caso di disturbo grave e persistente) e prevenire le ricadute depressive (rispetto al placebo) mostrando differenze significative essenzialmente nel profilo degli effetti collaterali e secondari (attivazione, sedazione, ansiolisi etc.). Sulla base di ciò la scelta dell’antidepressivo si basa principalmente sulla valutazione del suo profilo di effetti collaterali e della tollerabilità per un dato paziente, per questo la scelta ricade di norma su un SSRI\SNRI.
A tal proposito nel 2003 la SOPSI (Società italiana di psicopatologia) ha effettuato un’indagine conoscitiva su un campione di 750 Psichiatri italiani, a cui sono state somministrate 28 domande a risposta multipla che esploravano l’area della diagnosi e quella del trattamento farmacologico dei disturbi depressivi.
Tra i vari aspetti esplorati dall’indagine, un aspetto particolare valutato è stato quello dei criteri di scelta tra un SSRI ed un farmaco ad azione sulla Noradrenalina. Secondo i risultati la prescrizione di un antidepressivo SSRI sarebbe preferibile nei quadri caratterizzati da una spiccata componente ansiosa e di agitazione, mentre i farmaci noradrenergici sarebbero più indicati nei quadri melanconici e nelle personalità premorbose evitanti e passive.
Il trattamento viene di norma protratto per alcune settimane prima di poterne valutare l’efficacia (che si instaura e aumenta nel corso delle prime settimane di trattamento) e nel caso non dovessero esserci sostanziali miglioramenti, si può optare per un aggiustamento terapeutico (variazione del dosaggio o passaggio ad altro farmaco) seguendo il metodo del “trial and error”. Un protocollo terapeutico utilizzabile può essere quello suggerito dai risultati dello STAR*D Trial (Sequenced Treatment Alternatives to Relieve Depression) uno dei maggiori studi condotti sul tema. Alcuni autori ed istituzioni criticano l’uso degli SSRI\SNRI come trattamento di prima linea per la depressione a causa dello scarso rapporto tra efficacia ed effetti collaterali.
Inibitori selettivi della ricaptazione della serotonina (SSRI)
Gli inibitori selettivi della ricaptazione della serotonina (In inglese: selective serotonin reuptake inhibitor “SSRI”) sono una classe di antidepressivi considerati lo standard corrente per la terapia farmacologica della depressione perché caratterizzati da un favorevole profilo di effetti collaterali e da bassa tossicità. Una possibile causa (o concausa) della depressione è il quantitativo inadeguato di serotonina, un neurotrasmettitore utilizzato nel cervello anche per trasmettere segnali tra i neuroni. Si ritiene che gli SSRI funzionino aumentando la concentrazione di serotonina nelle sinapsi prevenendone la ricaptazione (un processo biologico di recupero e riciclo dei neurotrasmettitori). I primi a scoprire una SSRI, la fluoxetina, sono stati Klaus Schmiegel e Bryan Molloy della Eli Lilly. Questa classe di farmaci include:
- Citalopram (Elopram, Seropram in Italia; Celexa in USA)
- Escitalopram (Cipralex, Entact in Italia; Lexapro in USA)
- Fluoxetina (Fluoxeren, Fluoxetina generica in Italia; Prozac in Italia e USA)
- Fluvoxamina (Dumirox, Fevarin, Maveral, Fluvoxamina generica in Italia; Luvox in USA)
- Paroxetina (Daparox, Eutimil, Sereupin, Seroxat, Stiliden, Paroxetina generica in Italia; Paxil in USA)
- Sertralina (Tatig, Sertralina generica in Italia; Zoloft in Italia e USA)
Tipicamente questi antidepressivi hanno meno effetti avversi rispetto ai triciclici, oppure gli inibitori della monoaminossidasi, anche se si possono verificare effetti collaterali come la sonnolenza, la bocca secca, irritabilità, ansietà, insonnia, diminuzione dell’appetito, e diminuzione della pulsione e capacità sessuale. Alcuni effetti collaterali possono diminuire quando una persona si abitua al farmaco, ma altri effetti collaterali possono essere persistenti. Anche se più sicuri rispetto alla prima generazione di antidepressivi, gli SSRI potrebbero non funzionare per molti pazienti, con una efficacia minore rispetto alle precedenti classi di antidepressivi.
Un lavoro di due ricercatori ha messo in discussione il legame tra carenza di serotonina e sintomi della depressione, evidenziando che l’efficacia del trattamento a base di SSRI non prova tale legame. La ricerca indica che questi farmaci possono interagire con i fattori di trascrizione conosciuti come “clock genes”, che possono avere un ruolo nelle proprietà di dipendenza dei farmaci (abuso di farmaci) e probabilmente nell’obesità.
Per approfondire:
- Farmaci Inibitori Selettivi della Ricaptazione della Serotonina (SSRI): cosa sono ed a che servono
- Antidepressivi SSRI: meccanismo d’azione e farmacocinetica
- SSRI: efficacia in depressione, disturbo ossessivo compulsivo, ansia ed eiaculazione precoce
- SSRI: uso di antidepressivi in gravidanza ed allattamento
- SSRI: effetti collaterali, disfunzioni sessuali, sospensione e suicidio
- Disfunzione sessuale post-SSRI: sintomi, effetti a lungo termine e cure
- SSRI: effetti a breve e lungo termine
- SSRI in pazienti con diabete, iponatriemia, osteoporosi e prolungamento QT
Inibitori della ricaptazione della serotonina e della norepinefrina (SNRI)
Gli inibitori della ricaptazione della serotonina-noradrenalina (in inglese: serotonin-norepinephrine reuptake inhibitor “SNRI”) sono antidepressivi che agiscono sia sul circuito della noradrenalina che sulla serotonina, avendo perciò un meccanismo d’azione simile a quello dei triciclici ma con meno effetti collaterali. Questi tipicamente hanno effetti collaterali ed efficacia simili a quelli degli SSRI e come questi quando interrotti possono presentare una sindrome da sospensione (withdrawal syndrome) per cui si raccomanda la lenta diminuzione del dosaggio (“wash-out” del farmaco). Questi includono:
- Desvenlafaxina (Pristiq)
- Duloxetina (Cymbalta, Xeristar in Italia e USA)
- Milnacipram (Ixel)
- Venlafaxina (Efexor, Zarelis)
Questi farmaci inibiscono il riassorbimento della serotonina e della noradrenalina dalle sinapsi bloccando l’attività dei rispettivi “trasportatori” (delle proteine in grado di raccoglierli dallo spazio sinaptico e trasportarli all’interno del neurone). L’inibizione del processo di ricaptazione prolunga l’effetto del neurotrasmettirore sul neurone postsinaptico, per questo è anche il motivo per cui questo tipo di farmaci è chiamato inibitore duale della ricaptazione.
Per approfondire: Inibitori della ricaptazione della serotonina-norepinefrina (SNRI)
Inibitori della ricaptazione della noradrenalina (NaRI)
Gli inibitori della ricaptazione della noradrenalina NaRI oppure NRIs (dall’inglese Norepinephrine (noradrenaline) reuptake inhibitors) agiscono incrementando la trasmissione noradrenergica mediante il blocco del trasportatore (e quindi del reuptake) della noradrenalina (nota anche come norepinefrina). Alcuni studi indicano che gli NRI abbiano effetti positivi sulla capacità di concentrazione mentale e in particolare sulla motivazione. Questa classe include:
- Atomoxetina (Strattera)
- Mazindolo (Mazanor, Sanorex)
- Reboxetina (Davedax, Edronax)
- Viloxazina (Vivalan)
Alcuni di questi (come l’atomoxetina) sono specificatamente approvati per il trattamento dei deficit di attenzione; la reboxetina è utilizzata anche per il trattamento del dolore neuropatico mentre la viloxazina mostra risultati promettenti nel trattamento dell’enuresi notturna e della narcolessia. La loro efficacia nel trattamento della depressione (rispetto ad altre classi di antidepressivi) è stata però oggetto di critiche.
Leggi anche:
- Citalopram (Elopram): modalità d’assunzione e meccanismo d’azione
- Citalopram (Elopram): lista degli effetti collaterali del farmaco
- Citalopram (Elopram): interruzione, astinenza, diabete e prolungamento QT
- Citalopram (Elopram): uso in gravidanza ed allattamento
Antidepressivi atipici
Inibitori del reuptake della nor-epinefrina e della dopamina (NDRI)
Gli inibitori della ricaptazione della noradrenalina e della dopamina (sigla NDRI, dall’inglese: norepinephrine-dopamine reuptake inhibitor) diminuiscono la ricaptazione neuronale della dopamina e della noradrenalina (o norepinefrina). Questi includono:
- Bupropione (Elontril, Wellbutrin, Zyban)
- Metilfenidato (Ritalin)
Il metilfenidato è approvato per il trattamento del deficit di attenzione ed iperattività. Sono preferiti nelle forme depressive caratterizzate da astenia ed ipersonnia, rallentamento cognitivo e quando gli effetti collaterali di altre classi di antidepressivi, come ad esempio di aumento di peso e disfunzioni sessuali, risultano intollerabili.
Farmaci che aumentano selettivamente la ricaptazione della serotonina\meccanismo vario (SSREs)
Hanno un meccanismo d’azione complesso e multifattoriale
- Tianeptina (Stablon, Coaxil, Tatinol)
Agonisti melatonergici
Agiscano attivando i recettori della melatonina e, in misura minore, agiscono su altri target neuronali
- Agomelatina (Valdoxan, Melitor, Thymanax)
Antagonisti serotoninergici
Bloccano l’azione della serotonina su particolari sotto classi recettoriali
- Nefazodone (Serzone)
Antidepressivi specifici noradrenergici e serotonergici (NaSSA)
Gli antidepressivi specifici noradrenergici e serotoninergici o NaSSA (dall’inglese noradrenergic and specific serotonergic antidepressant) costituiscono una classe di antidepressivi che si crede diano luogo ad un aumento della neurotrasmissione noradrenergica (noradrenalina) e serotoninergica (serotonina) grazie al blocco dei recettori adrenergici presinaptici alfa-2 ed al contemporaneo blocco di alcuni recettori della serotonina. Possono presentare effetti collaterali come sonnolenza, aumento dell’appetito e di peso; questi includono:
- Mianserina (Lantanon in Italia, Tolvon in USA)
- Mirtazapina (Remeron, Avanza, Zispin)
Antidepressivi ad azione serotoninergica mista (SARI)
Agiscono come potenziatori dell’attività serotoninergica (attraverso il blocco del reuptake) ma bloccando o attivando contemporaneamente alcuni sottotipi recettoriali
- Vortioxetina (Brintellix)
- Trazodone (Trittico)
- Vilazodone (Viibryd)
Antidepressivi che potenziano l’attività dopaminergica
- Agonisti dopaminergici, non sono specificatamente approvati per il trattamento della depressione ma hanno mostrato potenziale antidepressivo in diversi studi.
Alcuni antipsicotici a basse dosi potenziano l’attività dopaminergica invece di inibirla, risultando in un’attività antidepressiva ed ansiolitica.
- Amisulpride (Deniban)
- Sulpiride (Dobren).
Leggi anche:
- Fluoxetina (Fluoxeren): meccanismo d’azione del farmaco
- Fluoxetina (Fluoxeren): lista degli effetti collaterali e diabete
- Fluoxetina (Fluoxeren): uso in gravidanza ed allattamento
Inibitori della ricaptazione della dopamina
Aumentano le concentrazioni sinaptiche di dopamina bloccandone il processo di ricaptazione
- Amineptina (Survector)
Antidepressivi triciclici (TCA)
Gli antidepressivi triciclici o TCA (dall’inglese: Tricyclic antidepressant) sono la classe più vecchia di farmaci antidepressivi, dopo gli IMAO che, storicamente, furono i primi in assoluto. I triciclici bloccano la ricaptazione di alcuni neurotrasmettitori come la noradrenalina (norepinefrina) e la serotonina. Attualmente vengono usati meno comunemente a causa dello sviluppo di farmaci più selettivi e con meno effetti collaterali. Molti di questi farmaci, inoltre, interagiscono con recettori neurotrasmettitoriali, tra cui i recettori colinergici muscarinici, i recettori serotoninergici e i recettori istaminici.
Inibitori delle mono-amino-ossidasi (IMAO)
Gli inibitori delle monoamino ossidasi IMAO oppure MAOI (dall’inglese monoamine oxidase inhibitors) sono stati tra i primi antidepressivi ad essere scoperti. Pur mostrando una elevata efficacia terapeutica, spesso sono utilizzati solo come trattamento di seconda linea quando altri farmaci antidepressivi si rivelano inefficaci dal momento che esistono interazioni potenzialmente anche gravi tra questa classe di medicamenti e alcuni cibi o farmaci (cioè quelli contenenti amine simpaticomimetiche come la tiramina, contenuta particolarmente nei cibi stagionati come alcuni formaggi, vino rosso). Comunque, queste precauzioni non si applicano a una nuova formulazione in cerotto transdermico di selegilina, che grazie al fatto di bypassare il metabolismo epatico non è mai stato correlato all’induzione di tachicardia e di crisi ipertensive. Inoltre non si applicano agli IMAO di nuova generazione detti reversibili inibitore reversibile della monoaminoossidasi A (RIMA) di cui fanno parte moclobemide (Aurorix o Manerix) e tolaxotone.
Il gruppo di farmaci MAOI include:
- Isocarboxazide (Marplan)
- Moclobemide (Aurorix, Manerix)
- Fenelzina (Nardil)
- Selegilina (Eldepryl, Emsam)
- Tranilcipromina (Parnate).
Leggi anche:
- Antidepressivi triciclici: tipi, indicazioni e meccanismo di azione
- Antidepressivi triciclici: tipici effetti collaterali dei farmaci
- Antidepressivi triciclici: overdose, tossicità e trattamento
- Antipsicotici (neurolettici): classificazione, usi e meccanismo di azione
- Farmaci antipsicotici: differenza tra neurolettici tipici ed atipici
- Farmaci antipsicotici (neurolettici): lista degli effetti collaterali
Farmaci potenzianti l’effetto antidepressivo
L’effetto terapeutico di alcuni antidepressivi può essere amplificato dall’aggiunta di altri farmaci. Il loro effetto è sinergico, cioè queste associazioni generano un effetto terapeutico maggiore di quello ottenibile dalla somma degli effetti dei singoli farmaci.
Di questi “potenziatori” si trovano:
- Antidepressivi
- Ansiolitici
- Ormoni tiroidei
- Antipsicotici
- Anticonvulsivanti
- Stimolanti
Gli ansiolitici possono venire prescritti in associazione agli antidepressivi per migliorarne l’efficacia o trattare altri aspetti della patologia. In particolare i sedativi, come le benzodiazepine, vengono prescritti per attenuare gli stati d’ansia e favorire il sonno; a volte vengono prescritte per nelle prime settimane di trattamento con gli SSRI\SNRI per mitigarne alcuni effetti collaterali. A causa dell’alto rischio di dipendenza, questi medicinali sono pensati per agire solamente a breve termine o per uso occasionale. L’aggiunta di buspirone, un ansiolitico atipico, ad un trattamento con antidepressivo SSRI ha dimostrato di incrementarne gli effetti terapeutici senza sortire particolari effetti collaterali aggiuntivi. Gli antipsicotici di seconda generazione come il risperidone, l’olanzapina e la quetiapina possono essere prescritti in aggiunta ad un trattamento antidepressivo nei casi di depressione resistente al trattamento nel caso il solo farmaco antidepressivo abbia fallito nel generare sufficienti effetti terapeutici. Possono inoltre essere sfruttati per aumentare la concentrazione plasmatica di un altro farmaco, per alleviare i sintomi psicotici e paranoidi, ansiosi e di irritabilità che spesso accompagnano il disturbo depressivo. Tali farmaci comunque, in particolare ad alti dosaggi, possono causare effetti collaterali importanti come offuscamento della vista, spasmi muscolari, irrequietezza, discinesia tardiva e aumento di peso. Farmaci più nuovi, come l’aripiprazolo, possono perciò essere preferiti anche se la sicurezza di queste combinazioni dovrà essere ancora approfonditamente studiata. Per questo motivo tali combinazioni sono considerati degli approcci di seconda linea. Comuni sono le combinazioni tra diversi antidepressivi per potenziarne sinergicamente l’efficacia. A volte piccole dosi di un altro antidepressivo possono essere aggiunte per incrementare la concentrazione plasmatica (e quindi la potenza) di un altro utilizzato a dosaggio pieno, o per sfruttarne alcuni effetti collaterali (come ad esempio quelli sedativi). A questo scopo, ad esempio, il trazodone viene a volte utilizzato come adiuvante del sonno per i suoi effetti sedativi o nell’ambito di una terapia combinata per potenziare l’effetto degli antidepressivi SSRI\SNRI. Anche il nefazodone viene a volte aggiunto ad un SSRI per potenziarne l’efficacia. Altri antidepressivi che vengono comunemente combinati sono il buproprione con un SSRI, al fine di ottenere un maggiore effetto terapeutico ed anche per contrastare alcuni effetti collaterali degli SSRI come quelli sulla sfera sessuale e la sedazione; la mirtazapina con venlafaxina, una combinazione usata particolarmente in Canada per i casi di depressione resistente al trattamento, prende il nome colloquiale di “california rocket fuel”. Psicostimolanti sono aggiunti a volte alla cura antidepressiva se il paziente soffre di anedonia, ipersonnia e/o eccessiva alimentazione e scarsa motivazione. Tali sintomi sono comuni in depressioni atipiche e possono essere risolti aggiungendo alla cura dosi moderate di anfetamine (Adderall), metilfenidato (Ritalin) oppure modafinil (Provigil, Alertec) poiché queste sostanze possono migliorare il grado di motivazione personale e il comportamento, sopprimendo l’eccessivo appetito e sonno. In particolare il Modafinil è unico per effetti sul sonno: aumenta infatti l’attenzione e riduce la sonnolenza quando il paziente è nello stato attivo, senza inibire il normale sonno. Questi accorgimenti medici possono ristabilire il desiderio sessuale, sebbene questo sia solamente un effetto collaterale e non costituisca la ragione di prescrizione di tali psicostimolanti. Farmaci di tale natura devono essere somministrati con estrema cautela in alcuni tipi di pazienti: gli stimolanti infatti possono indurre episodi maniaco-depressivi in persone affette da disordine bipolare.
Il litio è uno stabilizzante dell’umore ed è il trattamento elettivo per il disturbo bipolare, spesso è usato insieme ad altri medicinali per il trattamento di episodi maniacali o della depressione. Alcuni anticonvulsivanti, come la carbamazepina (Tegretol), valproato di sodio (Epilim) e lamotrigina (Lamictal) sono utilizzati come stabilizzatori dell’umore, particolarmente nel disturbo bipolare, spesso in associazione a degli atnidepressivi. Sia il litio che la lamotrigina sono stati studiati e utilizzati per aumentare gli effetti antidepressivi nella depressione unipolare resistente. Diversi ormoni sono stati sperimentati in combinazione con un farmaco antidepressivo per potenziarne gli effetti. In particolare la tireoiodina, un ormone tiroideo, può essere somministrato in pazienti con depressione refrattaria ad altri trattamenti, in aggiunta ad un farmaco antidepressivo, anche se la funzionalità tiroidea è nella norma. Alcune evidenze ci sono per il potenziamento con alcune sostanze di derivazione naturale come acidi grassi Omega-3, SAMe, acido folico, inositolo, minerali come zinco e magnesio, vitamine soprattutto del gruppo B ad alte dosi.
Leggi anche:
- Depressione maggiore e minore, suicidio, diagnosi e cura: fai il test e scopri se sei a rischio
- Serotonina e triptofano: cosa sono ed in quali cibi trovarli
- Xanax (alprazolan) 0,25mg 0,50mg 1mg compresse, 0,75mg gocce, foglietto illustrativo
- Tavor (lorazepam) 2mg/ml gocce orali, foglietto illustrativo
- Che cos’è il Disturbo ossessivo-compulsivo di personalità, come si riconosce, come si cura e come si distingue dal Disturbo ossessivo-compulsivo
- Schizofrenia: sintomi iniziali, violenza, test, cause e terapie
- Disturbo ossessivo-compulsivo: ripetere, ripetere e ripetere ancora all’infinito un gesto. Differenze col disturbo di personalità ossessivo-compulsivo
- Perché mi capita di piangere senza motivo? Come affrontare il problema?
- Depressione post coitale: perché le donne piangono dopo aver fatto l’amore? Cause e cura
- La Sindrome da abbandono: cos’è e come si supera
- Ho paura di fare l’amore: tutte le fobie del sesso
- Fobie: quando un ragno o un ascensore ci mettono nel panico
- Indifferenza ed anaffettività: ecco come si manifesta il disturbo schizoide di personalità
- Schizofrenia: cause familiari, genetica, ambiente, stupefacenti e gravidanza
- Cause della schizofrenia: fattori psicologici e neurologici
- Come si diventa schizofrenici
- Come riconoscere uno schizofrenico: primi sintomi di schizofrenia
- Comportamento schizofrenico: come fare diagnosi di schizofrenia
- Schizofrenia: come si cura
- Test per la diagnosi di schizofrenia
- Disturbo schizofreniforme ed evoluzione verso la schizofrenia
- Amare uno schizofrenico: come comportarsi con uno schizofrenico?
- Schizofrenia: cosa fare in caso di crisi? A chi chiedere aiuto?
- Emicrania con aura: cause, sintomi, diagnosi e trattamenti
- Emicrania senza aura: cause, sintomi, diagnosi e trattamenti
- Differenza tra emicrania con aura ed emicrania senza aura
- Cos’è l’aura emicranica?
- Cefalea coitale ed orgasmica: il mal di testa durante il sesso e l’orgasmo
- Com’è fatto il cervello, a che serve e come funziona la memoria?
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Sistema nervoso autonomo simpatico e parasimpatico: anatomia e funzioni
- Depressione post parto: come riconoscere i primi sintomi e superarla
- Liberarsi dalla dipendenza affettiva e dalla paura dell’abbandono
- Dipendenza affettiva: riconoscerla, affrontarla e superarla
- Scopri come affronti la vita e le sue difficoltà, con il “Test del bosco”
- I dieci comportamenti che comunicano agli altri che sei una persona introversa
- Perché si piange? Per quale motivo si piange di gioia, di dolore e dal ridere?
- Disturbo da attacchi di panico: sensazione di morte imminente e angoscia
- Perché le donne piangono dopo aver fatto l’amore? Le cause della depressione post coitale e come superarla
- Diminuire ansia e stress per essere sereni ogni giorno della tua vita
- Differenza tra paura, fobia, ansia, panico e terrore
- Vi insegno le 12 regole d’oro per battere l’insonnia ed avere un sonno perfetto
- Depressione post parto: come riconoscere i primi sintomi e superarla
- Lacrime: di che sono fatte, a che servono e cosa le produce?
- Lacrime: di che sono fatte, a che servono e cosa le produce?
- Le lacrime femminili riducono l’eccitazione sessuale maschile
- Differente approccio di psicologo, psicoterapeuta e psichiatra
- Che significa somministrazione di un farmaco PER OS o PO?
- Via di somministrazione orale, per os: vantaggi e svantaggi
- Differenze tra le varie scuole di psicoterapia: quale la più efficace?
- Scuola psicoanalitica (psicodinamica): l’efficacia della psicoanalisi
- Psicoterapia adleriana (o individualpsicologica)
- Psicoterapia cognitivo-comportamentale: lo schema comportamentale diventa sintomo
- Psicoterapia sistemico-relazionale: la famiglia converge sul paziente
- Psicoterapia psicosintetica: l’allontanamento dal Sé transpersonale
- Psicoterapia funzionale: le alterazioni dei meccanismi psicofisiologici
- Psicoterapia ericksoniana: l’ipnoterapia
- Neurotrasmettitori: cosa sono ed a che servono
- Acetilcolina: cos’è ed a cosa serve?
- Dopammina: cos’è ed a che serve?
- Giunzione neuromuscolare (placca motrice) cos’è ed a che serve?
- Sinapsi chimica ed elettrica: cosa sono ed a che servono?
- Cos’è l’adrenalina ed a cosa serve?
- Dopammina: biosintesi, rilascio nello spazio sinaptico e degradazione
- Cos’è una ghiandola endocrina? A che servono gli ormoni ed il sistema endocrino?
- Quali sono le funzioni della Dopammina?
- Sistema dopamminergico: i circuti nervosi della dopammina
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!

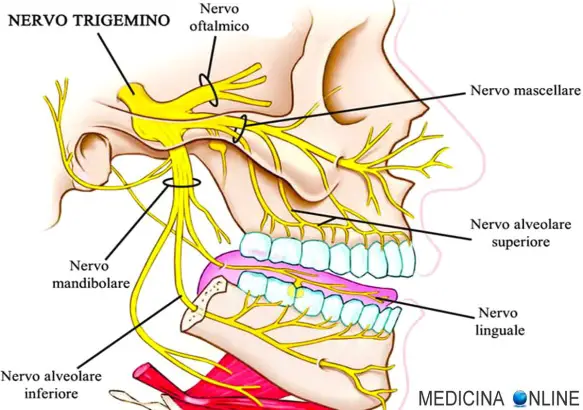 Il nervo trigemino è il V paio di nervi cranici. È un nervo misto somatico costituito prevalentemente da fibre sensitive somatiche e da un piccolo contingente di fibre motorie. Questi due componenti emergono direttamente dal nevrasse come due radici distinte: la radice sensitiva, più voluminosa, laterale rispetto a quella motrice ed appiattita in senso anteroposteriore, mette capo al ganglio semilunare del Gasser; la radice motrice, più piccola, mediale rispetto a quella sensitiva, passa al di sotto del ganglio medesimo e si unisce alla terza branca trigeminale.
Il nervo trigemino è il V paio di nervi cranici. È un nervo misto somatico costituito prevalentemente da fibre sensitive somatiche e da un piccolo contingente di fibre motorie. Questi due componenti emergono direttamente dal nevrasse come due radici distinte: la radice sensitiva, più voluminosa, laterale rispetto a quella motrice ed appiattita in senso anteroposteriore, mette capo al ganglio semilunare del Gasser; la radice motrice, più piccola, mediale rispetto a quella sensitiva, passa al di sotto del ganglio medesimo e si unisce alla terza branca trigeminale. Cosa studia l’ecocolordoppler?
Cosa studia l’ecocolordoppler? La paura è un’emozione primaria, comune sia al genere umano sia al genere animale. Il Galimberti così la definisce:
La paura è un’emozione primaria, comune sia al genere umano sia al genere animale. Il Galimberti così la definisce: In linguistica, l’ipotesi di Sapir-Whorf (in inglese “hypothesis of linguistic relativity” o “Whorfianism” o “Sapir-Whorf hypothesis“, da cui l’acronimo SWH), conosciuta anche come “ipotesi della relatività linguistica” o semplicemente “relatività linguistica“, afferma che
In linguistica, l’ipotesi di Sapir-Whorf (in inglese “hypothesis of linguistic relativity” o “Whorfianism” o “Sapir-Whorf hypothesis“, da cui l’acronimo SWH), conosciuta anche come “ipotesi della relatività linguistica” o semplicemente “relatività linguistica“, afferma che  La lipotimia è una sensazione di improvvisa debolezza che non comporta la completa perdita della coscienza. Tuttavia esistono altre definizioni di lipotimia come breve e parziale perdita dello stato di coscienza con o senza sintomi neurovegetativi. Inoltre in letteratura è possibile trovare un altro termine “pre-lipotimia” per indicare i sintomi prodromi non seguiti dalla perdita dello stato di coscienza. Per questo motivo le recenti linee guida della Società Italiana di Cardiologia suggeriscono di evitare l’utilizzo di questi due termini, sebbene presente ancora in svariati testi di semeiotica, e di uniformarsi alla terminologia internazionale che distingue la sincope dalla presincope. Per pre-sincope o prodromo sincopale si intende l’insieme dei sintomi prodromi a cui può seguire la sincope ovvero la perdita transitoria dello stato di coscienza dovuta ad una ipoperfusione cerebrale acuta. La sincope può anche non essere preceduta dalla presincope.
La lipotimia è una sensazione di improvvisa debolezza che non comporta la completa perdita della coscienza. Tuttavia esistono altre definizioni di lipotimia come breve e parziale perdita dello stato di coscienza con o senza sintomi neurovegetativi. Inoltre in letteratura è possibile trovare un altro termine “pre-lipotimia” per indicare i sintomi prodromi non seguiti dalla perdita dello stato di coscienza. Per questo motivo le recenti linee guida della Società Italiana di Cardiologia suggeriscono di evitare l’utilizzo di questi due termini, sebbene presente ancora in svariati testi di semeiotica, e di uniformarsi alla terminologia internazionale che distingue la sincope dalla presincope. Per pre-sincope o prodromo sincopale si intende l’insieme dei sintomi prodromi a cui può seguire la sincope ovvero la perdita transitoria dello stato di coscienza dovuta ad una ipoperfusione cerebrale acuta. La sincope può anche non essere preceduta dalla presincope. La neuropatia diabetica (detta “polineuropatia diabetica” quando vengono colpiti più nervi) è una complicanza frequente del diabete che può interessare sia il sistema nervoso periferico, sia il sistema nervoso autonomo. In generale si distinguono due tipologie: neuropatia periferica e neuropatia autonoma. La neuropatia periferica colpisce le fibre nervose che vanno dalla periferia al midollo spinale, mentre quella autonoma coinvolge i funicoli nervosi che controllano le funzioni autonome del corpo, come il cuore e la circolazione, la digestione, gli ormoni, i reni il fegato. Nel caso di neuropatia periferica, generalmente si tratta di una polineuropatia polidistrettuale, di solito simmetrica, distale e più frequentemente interessa gli arti inferiori, più raramente è prossimale. La neuropatia autonomica invece presenta sintomi del tutto diversi.
La neuropatia diabetica (detta “polineuropatia diabetica” quando vengono colpiti più nervi) è una complicanza frequente del diabete che può interessare sia il sistema nervoso periferico, sia il sistema nervoso autonomo. In generale si distinguono due tipologie: neuropatia periferica e neuropatia autonoma. La neuropatia periferica colpisce le fibre nervose che vanno dalla periferia al midollo spinale, mentre quella autonoma coinvolge i funicoli nervosi che controllano le funzioni autonome del corpo, come il cuore e la circolazione, la digestione, gli ormoni, i reni il fegato. Nel caso di neuropatia periferica, generalmente si tratta di una polineuropatia polidistrettuale, di solito simmetrica, distale e più frequentemente interessa gli arti inferiori, più raramente è prossimale. La neuropatia autonomica invece presenta sintomi del tutto diversi. Tra gli elementi della natura l’acqua, insieme al fuoco, è uno dei più potenti. Alcune persone hanno paura dell’acqua da sempre e non hanno mai imparato a nuotare. Per altri la paura dell’acqua potrebbe essere arrivata a seguito di un trauma. Con molta calma si può provare a superare la paura dell’acqua e ad imparare a nuotare in modo graduale.
Tra gli elementi della natura l’acqua, insieme al fuoco, è uno dei più potenti. Alcune persone hanno paura dell’acqua da sempre e non hanno mai imparato a nuotare. Per altri la paura dell’acqua potrebbe essere arrivata a seguito di un trauma. Con molta calma si può provare a superare la paura dell’acqua e ad imparare a nuotare in modo graduale.