 La colomba, tipico dolce pasquale, possiede circa da 350 a 380 calorie ogni 100 grammi di prodotto; per quanto riguarda i carboidrati si aggirano intorno ai 55 grammi, mentre i grassi sono 12 grammi e le proteine 3 grammi. Questi valori possono variare molto in base alla marca ed alla eventuale farcitura aggiuntiva.
La colomba, tipico dolce pasquale, possiede circa da 350 a 380 calorie ogni 100 grammi di prodotto; per quanto riguarda i carboidrati si aggirano intorno ai 55 grammi, mentre i grassi sono 12 grammi e le proteine 3 grammi. Questi valori possono variare molto in base alla marca ed alla eventuale farcitura aggiuntiva.
La colomba è un alimento sconsigliato al diabetico, tuttavia può essere saltuariamente assunto dal paziente, in dosi moderate, preferibilmente lontano dai pasti principali e dopo parere positivo del medico. Sarebbe comunque preferibile sostituirlo con altri dolci meno calorici e con meno carboidrati.
Il problema vero della colomba è che spesso viene servito in tavola alla fine dei pasti pasquali che già da soli non sono ipercalorici e ricchi di carboidrati e vanno così ad aggiungersi a un menu già fin troppo abbondante. Per evitare un eccessivo apporto calorico e di carboidrati, un trucco potrebbe essere quello di ridurre le calorie durante la cena, diminuendo le porzioni ad esempio di pasta. Altro trucco è – se prevedete un pranzo abbondante – quello di limitare le calorie a cena o, comunque, nei giorni precedenti e successivi al periodo pasquale. Altro trucco è, ovviamente, quello di limitare le porzioni e di aumentare l’attività fisica prima, durante e dopo le feste.
Importante: in caso di dubbio, il paziente diabetico può – sotto controllo medico – monitorare la propria risposta glicemica all’assunzione di certi alimenti, annotando i valori su un taccuino e raffrontando le relative glicemie.
Leggi anche:
- Il diabetico può mangiare il gelato?
- Diabete: il diabetico può mangiare cioccolato? Quale preferire?
- I diabetici possono mangiare i dolci?
- Cosa può e non può mangiare il diabetico: cibi per controllare la glicemia
- Il diabetico può mangiare la pizza? Quale preferire?
- Torrone al cioccolato e nocciole fatto in casa: ricetta facile e golosa
- Torrone bianco morbido: ricetta facile e deliziosa
- Diabete e dolci di Natale: il diabetico può mangiare il pandoro?
- Pandoro e dieta: calorie, carboidrati e valori nutrizionali
- Diabete e dolci di Natale: il diabetico può mangiare il panettone?
- Panettone e dieta: calorie, carboidrati e valori nutrizionali
- Diabete e dolci di Natale: il diabetico può mangiare il torrone?
- Torrone e dieta: calorie, carboidrati e valori nutrizionali
- Colomba e dieta: calorie, carboidrati e valori nutrizionali
- Il pandoro fa bene o fa male al colesterolo? Fa ingrassare?
- Il pandoro fa male ai cani? Ed il panettone o il torrone?
- Differenza tra torrone e torroncino
- Differenza tra torrone morbido e duro
- Torrone, tutti i tipi e la storia del più buono tra i dolci di Natale
- Differenza tra torrone e mandorlato
- Differenza tra cubbaita e torrone
- Differenza tra pandoro e panettone
- Panettone o pandoro: quale fa ingrassare di più?
- Pandoro, panettone o torrone: quale mangiare per non ingrassare?
- Panettone e pandoro: quale dei due contiene più burro?
- Pandoro o panettone: quale scegliere nella dieta?
- Quante calorie hanno pandoro, panettone e torrone?
- Differenza tra panettone e colomba: forma, ingredienti e calorie
- Ingrassa di più pandoro, panettone, torrone o colomba?
- Consigli per scegliere il panettone più buono e salutare
- Quanti tipi di panettone esistono?
- Differenza tra pandoro e offella
- Differenza tra panettone e veneziana
- Panettone fatto in casa: ingredienti e ricetta facile, veloce e gustosa
- Panettone con lievito di birra: ricetta facile, veloce e gustosa
- Panettone: la ricetta più facile e veloce rispetto a quella tradizionale
- Panettone light: ricetta facile, gustosa e leggera
- Pandoro: ricetta con lievito di birra, facile e gustosa
- Pandoro: ricetta con lievito madre, facile e gustosa
- Pandoro light: ricetta facile, leggera e gustosa
- Il diabetico può bere caffè?
- Diabete: con cosa posso sostituire lo zucchero?
- Il diabetico può mangiare le uova?
- Il diabetico può bere vino?
- I diabetici possono mangiare lo yogurt?
- Il diabetico può mangiare arance, limoni, mandarini, cedro e bergamotto?
- Il diabetico può mangiare lo zucchero di canna? Quanti carboidrati e calorie ha?
- Diabete: le sostituzioni di alcuni alimenti di uso comune
- I 10 cibi che ti aiutano a combattere lo stress del periodo natalizio
- Lo stress da shopping natalizio ci rende aggressivi e scatena istinti primordiali di sopravvivenza
- Christmas Blues: a Natale sei triste perché sei obbligato ad essere felice. I consigli per stare bene durante le feste
- La calorie dei dolci di Natale
- Diabete a Natale: le 10 regole da seguire per tenere sotto controllo la glicemia
- Tutto quello che voglio per Natale, sei tu!
- Troppi dolci a Natale? Dite addio alla memoria
- Il segreto per evitare l’abbuffata natalizia? E’ un colore
- Chi ha paura di Babbo Natale?
- Starnuti natalizi? Forse sei allergico all’albero di Natale
- Natale: le dieci regole per non ingrassare durante le feste
- La dieta preventiva per non ingrassare a Natale
- Dieta disintossicante dopo il periodo natalizio: le sei regole per recuperare il peso forma dopo le abbuffate delle feste
- Le 5 migliori tisane per affrontare freddo e cambio di stagione
- I 6 cibi migliori per combattere la stanchezza autunnale
- Geloni alle mani e ai piedi: sintomi e rimedi naturali
- Perché quando cambia il tempo fanno male ossa, cicatrici e testa
- Quando inizia e finisce l’estate?
- Quando inizia e finisce l’inverno?
- L’alimentazione ideale per sopravvivere al freddo inverno
- Raffreddore: rimedi naturali e farmacologici
- Labbra screpolate e gonfie: cause e rimedi in bambini ed adulti
- Perché il freddo e l’ansia riducono le dimensioni del pene?
- Differenza tra prosciutto di Parma e San Daniele
- Differenza tra prosciutto e culatello
- Differenza tra prosciutto crudo e speck
- Differenza tra prosciutto cotto, crudo ed affumicato
- Differenza tra culatello e coppa
- Differenze tra merluzzo, nasello, baccalà o stoccafisso
- Differenza tra vino rosso, bianco e rosato
- Differenze tra noci ed arachidi: calorie ed idee in cucina
- Differenza tra pepe nero e peperoncino: proprietà, calorie ed idee in cucina
- Differenza tra pizza e piadina: calorie ed idee in cucina
- Differenza tre Parmigiano Reggiano e Pecorino Romano: calorie ed idee in cucina
- Differenze tra parmigiano e grana: colesterolo, valori nutrizionali e dieta
- Differenza tra grassi animali e vegetali
- Differenza tra proteine animali e vegetali: quali sono le migliori?
- Differenza tra grassi ed oli con esempi
- Differenza grassi saturi, monoinsaturi e polinsaturi
- Differenza tra omega 3, omega 6 ed omega 9: quale integratore scegliere?
- Perché ho sempre le mani ed i piedi freddi? Cosa fare e cosa NON fare per scaldarli
- La dieta anti-freddo per rafforzare il tuo sistema immunitario: mai più raffreddore!
- E’ arrivato il freddo: ecco i consigli per difendersi dalle labbra secche
- Perché ci viene la febbre e perché non dobbiamo aver paura di lei
- Proteggi la pelle del viso dal freddo con la maschera alla soia
- Col freddo diminuisce il desiderio sessuale? Non è vero
- Quasi 70 gradi sotto zero: il villaggio più freddo al mondo
- Perché viene la tosse e come faccio a farla passare?
- Avete sempre freddo? Ecco la dieta che vi riscalda!
- Come fare un aerosol spiegato in modo semplice [GUIDA]
- Le regole per proteggere la nostra salute dagli sbalzi di temperatura
- Freddo e mani ruvide: crema emolliente (e non idratante), guanti, saponi non aggressivi ed altri consigli
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

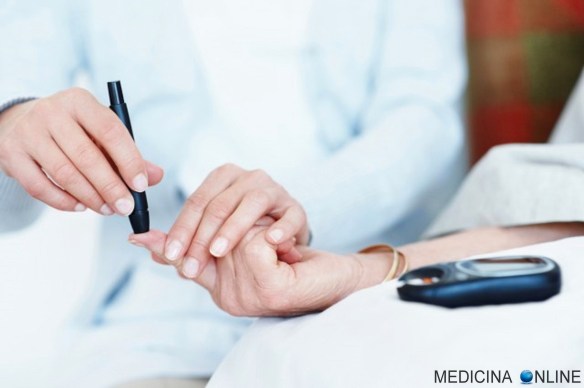 Il diabete mellito abbreviato DM è una forma di diabete ovvero un gruppo di disturbi metabolici accomunati dal fatto di presentare una persistente instabilità del livello glicemico del sangue, passando da condizioni di iperglicemia, più frequente, a condizioni di ipoglicemia.
Il diabete mellito abbreviato DM è una forma di diabete ovvero un gruppo di disturbi metabolici accomunati dal fatto di presentare una persistente instabilità del livello glicemico del sangue, passando da condizioni di iperglicemia, più frequente, a condizioni di ipoglicemia. Perché è importante prestare attenzione all’indice glicemico degli alimenti, specie per il paziente con diabete mellito?
Perché è importante prestare attenzione all’indice glicemico degli alimenti, specie per il paziente con diabete mellito?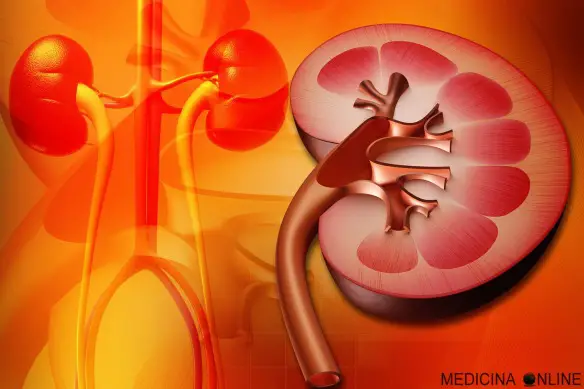 La vasopressina (o ADH, acronimo dall’inglese antidiuretic hormone) è un peptide di nove aminoacidi con funzioni di ormone, neurotrasmettitore e modulatore della trasmissione nervosa. È nota anche come ormone antidiuretico, adiuretina o arginina-vasopressina (AVP). La maggior parte della vasopressina viene sintetizzata dai nuclei sopraottico e paraventricolare dell’ipotalamo, una importante struttura del sistema nervoso centrale.
La vasopressina (o ADH, acronimo dall’inglese antidiuretic hormone) è un peptide di nove aminoacidi con funzioni di ormone, neurotrasmettitore e modulatore della trasmissione nervosa. È nota anche come ormone antidiuretico, adiuretina o arginina-vasopressina (AVP). La maggior parte della vasopressina viene sintetizzata dai nuclei sopraottico e paraventricolare dell’ipotalamo, una importante struttura del sistema nervoso centrale.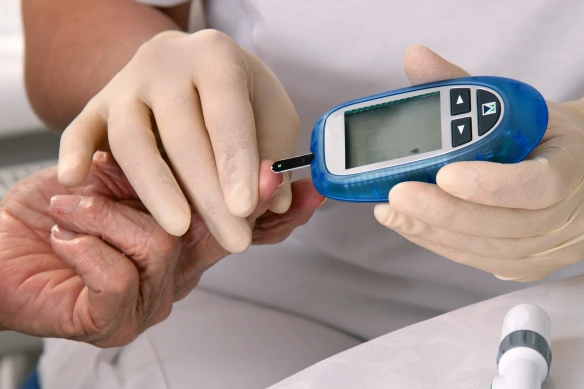 La glicemia indica il valore della concentrazione di glucosio nel sangue al momento del prelievo di sangue, l’emoglobina glicata indica invece, essendo proporzionale alla concentrazione di glucosio registrata nel sangue in un certo arco di tempo, quelli che possono essere stati i livelli medi di glicemia negli ultimi 3 mesi. In un certo senso la glicemia “fa una foto“ della situazione, mentre l’emoglobina glicata “fa un video” degli ultimi mesi.
La glicemia indica il valore della concentrazione di glucosio nel sangue al momento del prelievo di sangue, l’emoglobina glicata indica invece, essendo proporzionale alla concentrazione di glucosio registrata nel sangue in un certo arco di tempo, quelli che possono essere stati i livelli medi di glicemia negli ultimi 3 mesi. In un certo senso la glicemia “fa una foto“ della situazione, mentre l’emoglobina glicata “fa un video” degli ultimi mesi.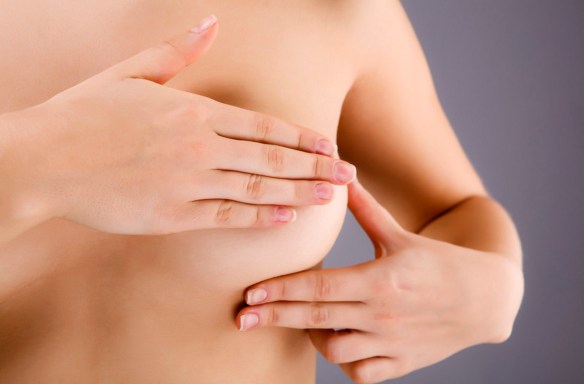 Le donne con carcinoma della mammella positivo per i recettori degli estrogeni devono evitare di ricorrere ai fitoestrogeni nel tentativo di ridurre gli effetti da deprivazione ormonale causati dalla ormonoterapia in atto. Il 70% circa dei carcinomi della mammella esprime recettori per gli estrogeni. Questo dato è alla base della terapia adiuvante con farmaci che riducono la stimolazione di questi recettori quali il tamoxifene e derivati e gli inibitori delle aromatasi. L’ormonoterapia di per sé causa però numerosi effetti collaterali da deprivazione ormonale. I sintomi meno tollerati sono la secchezza delle mucose e la sindrome vasomotoria (le cosiddette vampate), oltre alle manifestazioni legate al lungo trattamento (artralgie, tipicamente causate dagli inibitori delle aromatasi, osteoporosi, ipertensione, alterazioni del metabolismo lipidico).
Le donne con carcinoma della mammella positivo per i recettori degli estrogeni devono evitare di ricorrere ai fitoestrogeni nel tentativo di ridurre gli effetti da deprivazione ormonale causati dalla ormonoterapia in atto. Il 70% circa dei carcinomi della mammella esprime recettori per gli estrogeni. Questo dato è alla base della terapia adiuvante con farmaci che riducono la stimolazione di questi recettori quali il tamoxifene e derivati e gli inibitori delle aromatasi. L’ormonoterapia di per sé causa però numerosi effetti collaterali da deprivazione ormonale. I sintomi meno tollerati sono la secchezza delle mucose e la sindrome vasomotoria (le cosiddette vampate), oltre alle manifestazioni legate al lungo trattamento (artralgie, tipicamente causate dagli inibitori delle aromatasi, osteoporosi, ipertensione, alterazioni del metabolismo lipidico).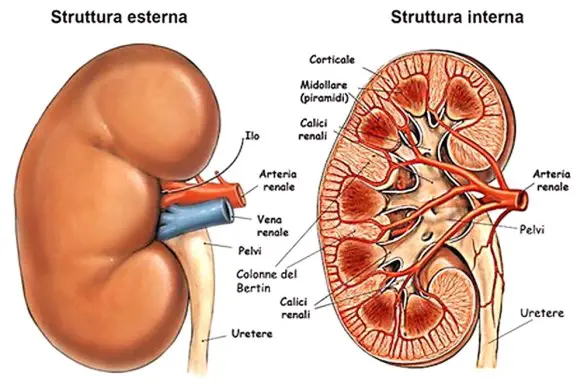 Il diabete insipido, o DIN, è una malattia caratterizzata da poliuria e da diminuita capacità del rene di concentrare le urine, che si traduce in urine abbondanti e molto diluite. Nonostante il nome, la malattia presenta meccanismi fisiopatologici molto diversi rispetto al diabete mellito, infatti in caso di DIN non si riscontrano alterazioni nella concentrazione di glucosio nel sangue e nelle urine, che dagli esami risultano quindi nella norma.
Il diabete insipido, o DIN, è una malattia caratterizzata da poliuria e da diminuita capacità del rene di concentrare le urine, che si traduce in urine abbondanti e molto diluite. Nonostante il nome, la malattia presenta meccanismi fisiopatologici molto diversi rispetto al diabete mellito, infatti in caso di DIN non si riscontrano alterazioni nella concentrazione di glucosio nel sangue e nelle urine, che dagli esami risultano quindi nella norma.