 Asportazione chirurgica delle metastasi
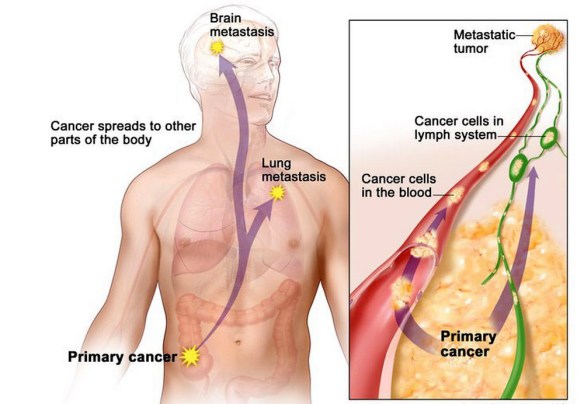
Asportazione chirurgica delle metastasi
Nel paziente metastatico, in casi selezionati, la chirurgia può ancora essere utilizzata a scopo curativo: ad esempio, se le metastasi sono in numero limitato e di ridotte dimensioni, possono essere asportabili chirurgicamente. Tuttavia bisogna chiarire che solo una piccola percentuale di pazienti con metastasi da tumore del colon retto può essere sottoposta a rimozione chirurgica delle metastasi, a causa di alcuni fattori che possono rendere l’intervento di esecuzione difficile o troppo rischiosa.
Tali fattori sono:
- condizioni generali del paziente;
- dimensioni delle metastasi;
- quantità delle metastasi;
- localizzazione delle metastasi.
Per facilitare la rimozione chirurgica delle metastasi, si ricorre ai così detti trattamenti neoadiuvanti. Essi hanno lo scopo di ridurre le dimensioni delle masse tumorali per rendere più facile la loro asportazione chirurgica.
Il termine “trattamento di conversione” indica invece un trattamento che rende (converte in) operabile una metastasi non sarebbe operabile. I trattamenti di conversione consistono spesso in una combinazione di chemioterapia a farmaci biologici.
Leggi anche:
Metastasi sincrone e metacrone
Se al momento della diagnosi di tumore del colon retto, il tumore primitivo ha già dato origine a metastasi queste ultime si definiscono metastasi sincrone. Se i medici che hanno in cura il soggetto esprimono una valutazione favorevole sia dal punto di vista medico che chirurgico, si può procedere all’asportazione del tumore primitivo e delle metastasi, scegliendo tra due possibili approcci:
- effettuare un unico intervento;
- procedere a più interventi chirurgici, eventualmente preceduti e/o seguiti da altri trattamenti che verranno descritti nei paragrafi successivi.
Anche in caso di diagnosi di metastasi metacrone, vale a dire sviluppatesi dopo la rimozione del tumore primitivo, si deciderà se procedere con la rimozione delle metastasi stesse e quali ulteriori trattamenti adottare. Gli specialisti coinvolti valuteranno tutte le informazioni e i dati disponibili poiché la chirurgia delle metastasi, in alcuni casi selezionati, può rappresentare la cura definitiva del tumore del colon retto metastatico.
Leggi anche: Le tue feci dicono se sei in salute: con la Scala di Bristol impara ad interpretarle
Chemioterapia
Nei pazienti in fase metastatica in cui sia praticabile la rimozione chirurgica delle metastasi, la chemioterapia può eventualmente precedere l’intervento chirurgico per ridurre le dimensioni delle metastasi e consentire di effettuare un intervento meno esteso e aggressivo (chemioterapia neoadiuvante). Si pratica una chemioterapia di conversione quando le metastasi non sono operabili al momento della diagnosi, ma lo possono eventualmente diventare a fronte di adeguata riduzione delle dimensioni. In questi casi di solito la chemioterapia si associa farmaci biologici. Quando invece la malattia metastatica è in uno stadio così avanzato da non essere più operabile, la chemioterapia diventa una soluzione obbligata. In questo caso si parla di chemioterapia palliativa, che ha la importante finalità di rallentare la progressione della malattia, alleviare i sintomi e migliorare la qualità della vita.
I regimi chemioterapici più comunemente utilizzati nel trattamento del tumore del colon retto metastatico sono combinazioni di più farmaci che prevedono sostanzialmente l’utilizzo di irinotecan od oxaliplatino in associazione al 5-fluorouracile o suoi derivati. I nomi dei regimi più comuni sono FOLFIRI (e la sua variante XELIRI) e FOLFOX (e la sua variante XELOX). Tuttavia esistono anche trattamenti più semplici, a base di un solo chemioterapico (ad esempio il 5-fluorouracile o la capecitabina utilizzati singolarmente), così come esistono regimi ancora più complessi, che associano contemporaneamente al 5-fluorouracile sia irinotecan che oxaliplatino, quale il regime FOLFOXIRI.
Negli studi clinici le combinazioni di più chemioterapici hanno dimostrato di essere più efficaci rispetto agli stessi farmaci utilizzati singolarmente. Analogamente, ulteriori studi clinici hanno provato che nel cancro del colon retto l’aggiunta di terapie biologiche alla chemioterapia consente di ottenere migliori risultati rispetto alla chemioterapia sola. Tuttavia, non tutti i farmaci sono adatti per tutti i pazienti e, il compito di scegliere la miglior cura per ciascun paziente, spetta agli specialisti che l’hanno in trattamento.
Ricordiamo infine che la chemioterapia utilizza farmaci citotossici, ovvero tossici per le cellule. In genere il loro effetto è quello di bloccare la divisione delle cellule in rapida replicazione, senza però distinguere tra cellule sane e cellule malate. Infatti, una delle caratteristiche meglio conosciute delle cellule tumorali è la loro capacità di dividersi (e quindi di moltiplicarsi) più rapidamente rispetto alla maggior parte delle cellule sane, la qual cosa rende le cellule tumorali altamente sensibili ai farmaci chemioterapici che bloccano la divisione cellulare. Tuttavia, hanno la capacità di dividersi molto rapidamente anche alcune cellule sane che fanno parte di tessuti che devono continuamente rinnovarsi. E’ il caso delle cellule del midollo osseo che formano i globuli rossi e i globuli bianchi e le cellule dette delle membrane (“epiteli”) che rivestono le superfici interne di organi che entrano in contatto con “materiali” provenienti dall’ambiente esterno all’organismo, come le vie aeree e il tubo digerente.
La maggior parte dei chemioterapici, interferendo con la divisione cellulare, uccide le cellule tumorali e qualche cellula sana che si divide rapidamente: per questo motivo molti farmaci chemioterapici danno come effetto collaterale, ad esempio, anemia e ulcere nella bocca e in gola.
Le moderne terapie biologiche vengono oggi sempre più associate alla chemioterapia per aumentarne l’efficacia e ridurne gli effetti collaterali.
Leggi anche:
Le terapie biologiche
La “nuova frontiera” della terapia nel tumore del colon retto, come in molti altri tipi di tumore solido, è rappresentata dai farmaci biologici (detti anche farmaci intelligenti, farmaci “mirati”, o biotecnologici), già utilizzati con successo in alcune altre patologie (ad es. tumore del polmone e della mammella). Sono molecole create in laboratorio per interagire con una precisa funzione della cellula cancerosa e non hanno effetti, o hanno effetti minimi, sulle cellule normali.
L’efficacia delle terapie biologiche non dipende dalla velocità della divisione cellulare: alcune modalità con cui le cellule tumorali del colon retto differiscono dalle sane, sono state scoperte negli ultimi anni, e questo ha permesso agli scienziati di mettere a punto farmaci che agiscono in maniera selettiva. Sono stati scoperti anche alcuni processi importanti per la sopravvivenza del tumore, e si è potuto sviluppare farmaci che li contrastano.
Gli effetti indesiderati più di frequente associati alla chemioterapia non sono presenti con i farmaci biologici, che risultano meglio tollerati, ma è bene specificare che i farmaci biologici, pur essendo mirati contro un preciso bersaglio caratteristico delle cellule tumorali, non sono del tutto privi di effetti collaterali.
I farmaci mirati attualmente impiegati nella pratica clinica per la terapia del tumore del colon retto appartengono alla categoria degli anticorpi monoclonali alla quale accenniamo brevemente qui, e per approfondimenti rimandiamo alla scheda ad essi dedicata.
Gli anticorpi monoclonali sono proteine, simili a quelle che produce l’organismo umano, in grado di interferire con meccanismi chiave della proliferazione cellulare importanti per la sopravvivenza del tumore.
- Per esempio, gli anticorpi monoclonali rivolti contro il fattore di crescita epidermico (anti-EGFR) sono in grado di agire in modo mirato sui meccanismi che regolano la crescita del tumore. La loro efficacia in associazione alla chemioterapia standard nei tumori in fase avanzata è ormai dimostrata, e il loro uso si sta diffondendo nella comune pratica clinica (cetuximab e panitumumab).
- Oltre agli anti-EGFR, altre terapie sono già comunemente in uso con successo nel trattamento di diversi tipi di tumore, quali gli inibitori di VEGF (VEGF: fattore di crescita dell’endotelio vascolare) (bevacizumab), ed esistono anche alcune ulteriori opzioni ancora in fase sperimentale.
Al momento, gli anticorpi monoclonali non sono ancora un’alternativa completa alla chemioterapia, ma un complemento da utilizzarsi preferibilmente in combinazione ad essa.
Leggi anche:
- Tumore del colon retto: trattamento chirurgico, radioterapia e chemioterapia
- Tumore del colon retto: terapia personalizzata col test RAS
- Anticorpi monoclonali contro il tumore del colon retto metastatico
- Differenza tra tumore benigno, maligno, neoplasia, cancro e metastasi
- Cos’è un tumore? Perché viene il cancro? Quali sono le cause?
- Differenza tra tumore e tessuto normale con esempi
- Differenze tra ileo meccanico ed ileo paralitico: cause, sintomi e trattamenti
- Esame e raccolta delle feci: come si fa nel modo corretto ed a che serve
- Feci gialle, giallo oro, giallastre: cause ed interpretazione clinica
- Quanto peso perdiamo ogni volta che andiamo in bagno?
- Feci con sangue, muco, cibo: quando preoccuparsi?
- Parassiti e vermi nelle feci: sintomi e come eliminarli con farmaci e rimedi naturali
- Che significa malattia cronica? Esempi di malattia cronica
- Come nasce un cancro? Cosa sono i cancerogeni e come avviene la cancerogenesi?
- Quanto tempo mi rimane da vivere?
- Differenza tra prevenzione primaria, secondaria e terziaria con esempi
- Capire se si ha un tumore: come viene diagnosticato un cancro
- Cure palliative: cosa sono ed a che servono?
- Dolore: cos’è, da cosa è causato, quanti tipi di dolore esistono?
- Differenza tra sintomo e segno con esempi
- Differenza tra malattia, sindrome e disturbo con esempi
- Differenza tra malattia acuta e cronica con esempi
- Come prevenire i tumori ed il cancro? I 10 cambiamenti consigliati
- Differenza tra ipertrofia ed iperplasia con esempi
- Differenza tra iperplasia e neoplasia
- Differenze tra ileostomia, colostomia e urostomia
- Poliposi gastrointestinale giovanile: cause, sintomi, diagnosi, terapia
- Poliposi infantile e giovanile: cause, sintomi, diagnosi, terapia
- Poliposi adenomatosa familiare: cause, sintomi, diagnosi, terapia
- Sindrome di Peutz-Jeghers: cause, sintomi, diagnosi, terapia
- Sindrome di Bannayan-Riley-Ruvalcaba: cause, sintomi, diagnosi, terapia
- Polipi intestinali: tipi, cause, fattori di rischio, fattori protettivi
- Polipi intestinali: sintomi, segni, esami, diagnosi, screening
- Polipi intestinali: terapia, chirurgia, colectomia, farmaci, prevenzione
- Differenza tra atrofia, distrofia ed aplasia con esempi
- È vero che i campi elettromagnetici causano tumore e cancro?
- E’ vero che cucinare i cibi al microonde fa male alla salute?
- Stadiazione e classificazione TNM: cancro curabile o terminale?
- Differenza tra adenocarcinoma e carcinoma con esempi
- Differenza tra cancro e carcinoma con esempi
- Stomie: cosa sono, a che servono, quanti tipi esistono?
- Differenza tra ipertrofia muscolare sarcolplasmatica e miofibrillare
- Ipertrofia muscolare: cosa significa e come si raggiunge
- Esofago di Barrett: sintomi iniziali, diagnosi, terapia, dieta e chirurgia
- Differenza tra metaplasia, displasia e neoplasia con esempi
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!
Condividi questo articolo:
 Tempo fa un paziente mi ha fatto questa domanda:
Tempo fa un paziente mi ha fatto questa domanda:
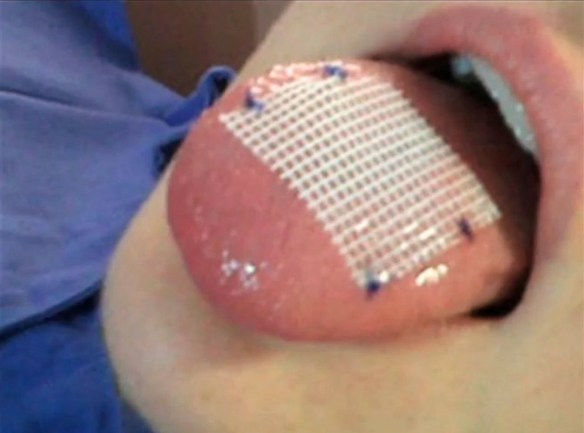 In medicina l’amputazione totale o parziale della lingua può avvenire principalmente per traumi severi (ad esempio in caso di incidenti stradali) o in caso di tumore maligno della lingua, patologia che si riscontra specie in pazienti fumatori.
In medicina l’amputazione totale o parziale della lingua può avvenire principalmente per traumi severi (ad esempio in caso di incidenti stradali) o in caso di tumore maligno della lingua, patologia che si riscontra specie in pazienti fumatori.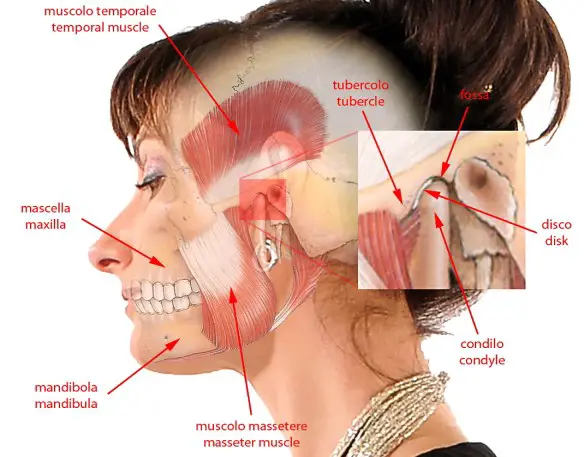
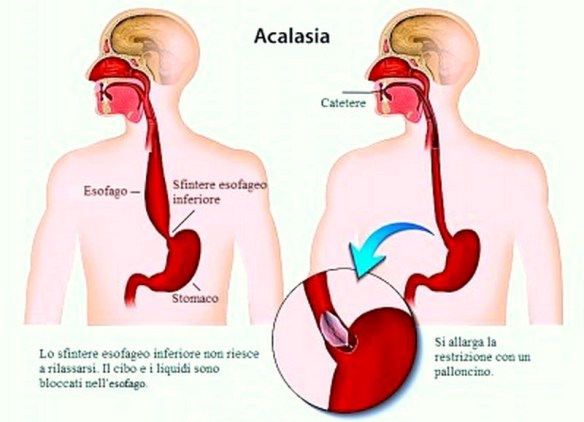 L’acalasia esofagea è una rara patologia dell’esofago a eziologia non nota caratterizzata da un disturbo della motilità esofagea che si esprime con un ipertono dello sfintere esofageo inferiore (che si rilascia incompletamente e in modo non coordinato con passaggio del cibo) e con l’assenza della peristalsi fisiologica a livello del corpo esofageo. Ne derivano disfagia (difficoltà a deglutire), rigurgito, scialorrea, calo ponderale e dolore toracico; inoltre la condizione determina generalmente la comparsa di una dilatazione dell’esofago che può assumere una forma cosiddetta “sigmoidea” caratterizzata da curvature nel tratto sovradiaframmatico, con possibili lesioni al tratto terminale.
L’acalasia esofagea è una rara patologia dell’esofago a eziologia non nota caratterizzata da un disturbo della motilità esofagea che si esprime con un ipertono dello sfintere esofageo inferiore (che si rilascia incompletamente e in modo non coordinato con passaggio del cibo) e con l’assenza della peristalsi fisiologica a livello del corpo esofageo. Ne derivano disfagia (difficoltà a deglutire), rigurgito, scialorrea, calo ponderale e dolore toracico; inoltre la condizione determina generalmente la comparsa di una dilatazione dell’esofago che può assumere una forma cosiddetta “sigmoidea” caratterizzata da curvature nel tratto sovradiaframmatico, con possibili lesioni al tratto terminale.
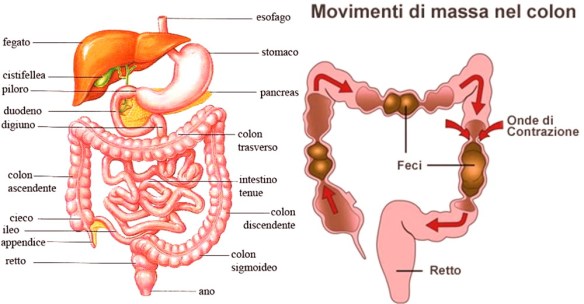
 I muscoli e i nervi che controllano la digestione possono essere influenzati dalla malattia, con conseguente costipazione e gastroparesi (il cibo rimane nello stomaco per un periodo di tempo più lungo del normale). Una alimentazione equilibrata, sulla base di periodiche valutazioni nutrizionali, è consigliata e deve essere finalizzata ad evitare la perdita o il guadagno di peso e a ridurre al minimo le conseguenze delle disfunzioni gastrointestinali.
I muscoli e i nervi che controllano la digestione possono essere influenzati dalla malattia, con conseguente costipazione e gastroparesi (il cibo rimane nello stomaco per un periodo di tempo più lungo del normale). Una alimentazione equilibrata, sulla base di periodiche valutazioni nutrizionali, è consigliata e deve essere finalizzata ad evitare la perdita o il guadagno di peso e a ridurre al minimo le conseguenze delle disfunzioni gastrointestinali.
 Asportazione chirurgica delle metastasi
Asportazione chirurgica delle metastasi