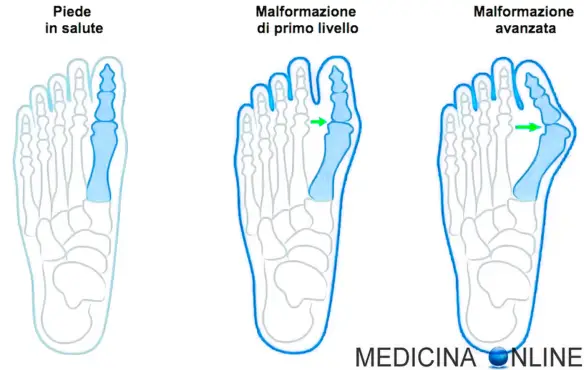
 L’alluce valgo è una patologia del piede molto comune, caratterizzata dallo spostamento verso l’esterno della base dell’alluce e dallo spostamento della punta dell’alluce stesso che devia lateralmente in direzione delle altre dita. Tale deformazione comporta anche una sporgenza del primo osso del metatarso, che si accompagna a un’infiammazione, che può essere ripetuta nel tempo o costante, della cosiddetta borsa mucosa, situata alla base dell’impianto del dito. È un disturbo che interessa molto più frequentemente le donne degli uomini, specie oltre i 30 anni di età.
L’alluce valgo è una patologia del piede molto comune, caratterizzata dallo spostamento verso l’esterno della base dell’alluce e dallo spostamento della punta dell’alluce stesso che devia lateralmente in direzione delle altre dita. Tale deformazione comporta anche una sporgenza del primo osso del metatarso, che si accompagna a un’infiammazione, che può essere ripetuta nel tempo o costante, della cosiddetta borsa mucosa, situata alla base dell’impianto del dito. È un disturbo che interessa molto più frequentemente le donne degli uomini, specie oltre i 30 anni di età.
Conseguenze dell’alluce valgo: l’accavallamento dell’alluce
Nei casi più gravi la deviazione dell’alluce può portare all’accavallamento dell’alluce stesso con il secondo dito del piede. La pelle che ricopre l’articolazione interessata da questo disturbo può apparire arrossata e dolente. Il progredire della patologia può provocare:
- dolore inizialmente intermittente, poi persistente e sempre più intenso;
- una limitata capacità di movimento dell’alluce fino alla totale immobilità;
- deformazioni più o meno invalidanti;
- difficoltà nell’indossare le scarpe;
- difficoltà nella deambulazione.
Quali sono le cause dell’alluce valgo?
Diverse sono le cause alla base dell’insorgenza dell’alluce valgo. La deformazione può essere dovuta a:
- lesioni a carico del piede;
- problemi di peso, di postura o di tono muscolare;
- predisposizione genetica;
- malformazioni congenite;
- utilizzo di calzature inadatte (pianta stretta, punta stretta e tacco alto);
- alcuni tipi di artrite.
Quali sono i soggetti a rischio di alluce valgo?
I soggetti più a rischio sono donne, oltre i 30 anni, in sovrappeso od obese, con artrite, che indossano scarpe di bassa qualità e con casi in famiglia di alluce valgo.
Quali sono i sintomi dell’alluce valgo?
La sintomatologia può variare da persona a persona: alcuni pazienti lamentano dolore al secondo dito, piuttosto che all’alluce, mentre altri riferiscono di provare un violento dolore, pur senza avere deformità notevoli. In generale, comunque, l’alluce valgo è caratterizzato dalla presenza di diversi sintomi, alcuni aspecifici, altri caratteristici.
Sintomi iniziali (malformazione di primo livello):
- la presenza di un lieve rigonfiamento alla base dell’alluce;
- lieve gonfiore e/o arrossamento intorno all’alluce;
- dolore intermittente intorno all’alluce;
- diminuzione della capacità dei movimenti dell’alluce;
- iniziale deviazione dell’alluce.
Sintomi tardivi (malformazione di primo livello):
- la presenza di un rigonfiamento evidente alla base dell’alluce;
- severo gonfiore e/o arrossamento intorno all’alluce;
- ispessimento della pelle alla base dell’alluce;
- dolore persistente intorno all’alluce;
- deficit elevato nei movimenti dell’alluce fino ad arrivare all’impossibilità totale di movimento;
- deviazione grave dell’alluce con accavallamento dell’alluce stesso con il secondo dito del piede;
- difficoltà nell’indossare le scarpe;
- difficoltà nella deambulazione.
Si può prevenire l’alluce valgo? Quale scarpa scegliere?
In parte si. Per prevenire l’insorgenza dell’alluce valgo (o almeno per non peggiorarlo) si consiglia di indossare scarpe comode e di qualità e di evitare calzature con pianta stretta, punta stretta e tacco alto, perché costringono il piede in una posizione innaturale, così come le suole troppo piatte, che non consentono alle dita un corretto appoggio a terra. Inoltre non bisogna mai massaggiare il gonfiore esterno – chiamato anche borsite o, più comunemente, “cipolla” – per evitare di infiammare ulteriormente l’area. Utile sarà cercare di ripetere movimenti naturali per il piede, imparando a riconoscere i propri punti d’appoggio. A questo scopo, si può utilizzare una pallina morbida da far scorrere dolcemente sotto la pianta del piede: aiuterà a capire quali articolazioni, muscoli e tendini sono coinvolti in ogni fase della camminata.
Leggi anche:
Diagnosi di alluce valgo
La diagnosi di alluce valgo spetta al medico, al quale sarà sufficiente alcune domande specifiche (anamnesi) ed un accurato esame obiettivo per effettuare la diagnosi di alluce valgo: durante la visita lo specialista effettuerà alcune manovre atte a valutare la capacità di movimento dell’alluce. In caso di dubbio, una semplice radiografia del piede può risultare utile per la diagnosi ed anche per identificare la causa e la gravità del disturbo.
Cura dell’alluce valgo
Diversi sono i trattamenti a disposizione per l’alluce valgo. La scelta dipende dalla gravità del disturbo e dalla quantità di dolore che provoca.
Trattamenti non chirurgici, detti anche “conservativi”:
- Indossare scarpe ampie e comode che offrano molto spazio per le dita dei piedi.
- Applicazione di un bendaggio che mantenga il piede in posizione normale, riducendo lo stress sull’alluce e alleviando il dolore.
- Uso di farmaci antidolorifici.
- Iniezioni di cortisone per ridurre il gonfiore.
- Utilizzo di cuscinetti separa dita e plantari correttivi per distribuire uniformemente il peso del corpo e la pressione quando si muovono i piedi (aiutano a prevenire o correggere anche altre patologie dell’avampiede o del retropiede associate all’alluce valgo).
- Applicazione di ghiaccio sulla zona interessata dal disturbo e di pomate antinfiammatorie: soprattutto dopo che si è stati a lungo in piedi, questo semplice rimedio può aiutare a lenire il dolore e l’infiammazione.
Le opzioni chirurgiche:
Se il trattamento conservativo non fornisce alcun sollievo potrebbe essere necessario un intervento chirurgico.
- Approccio chirurgico classico: lo scopo della chirurgia è alleviare il disagio dovuto a questa condizione restituendo all’alluce la giusta posizione. Attraverso l’apertura chirurgica della cute e dei tessuti sottostanti (procedura “a cielo aperto”) la correzione della deformità viene effettuata mediante l’asportazione di parte di osso e l’inserimento di supporti volti a riportare l’alluce nella corretta posizione.
- Approccio chirurgico percutaneo: consente di ottenere i medesimi risultati dell’approccio chirurgico classico ma in modo meno invasivo e con tempi di recupero post-operatori molto più brevi. La procedura percutanea – mediante appositi strumenti e sotto la guida di immagini radioscopiche – permette di operare direttamente sull’osso attraverso forellini effettuati nella cute.
Esercizi per prevenzione e cura dell’alluce valgo
Così come già accennato, la diagnosi e il trattamento dell’alluce valgo spettano sempre al medico che, con l’aiuto di un fisioterapista, potrà definire la serie di esercizi più idonea per il singolo caso: il disturbo varia infatti da persona a persona, quindi è importante non improvvisare terapie “improbabili” bensì seguire le istruzioni dei professionisti. Chiarito ciò, vi presentiamo una lista di esercizi genericamente usati per correggere l’alluce valgo:
- camminata: un esercizio potenzialmente ottimo per l’alluce valgo è quello di camminare a piedi nudi in casa o, qualora vi fosse la possibilità, su una distesa di sabbia come in spiaggia. Dopo circa dieci passi, effettuati mantenendo il piede dritto e non sporgente verso l’esterno, ci si fermi. Piegando lievemente il ginocchio, al contatto con il suolo dovranno rimanere solo le dita. Scoperto il proprio punto d’appoggio, si mantenga la posizione per 5 secondi e si riprenda a camminare;
- rotazione: seduti con le gambe distese, si cerchi di muovere l’alluce seguendo un’immaginaria forma circolare, a piacere in senso orario o antiorario. Dopo circa 10 secondi, cercare di estendere lateralmente il pollice, mantenendo la posizione per un paio di secondi. Si tratta di movimenti che possono risultare complessi per chi soffrisse di una deformazione grave, per questo ci si dovrà fermare qualora si provasse del dolore, anche di media intensità;
- pallina: il primo esercizio è lo stesso che si esegue in fase di prevenzione, poiché indicato per evitare il peggioramento dei sintomi. In posizione eretta, si pone una pallina abbastanza morbida – delle dimensioni di una da golf – sotto la pianta del piede. Quindi si muove dolcemente l’arto, senza effettuare un’eccessiva pressione, partendo dall’arco plantare fino alle dita e poi in direzione opposta fino al tallone. A ogni passaggio – falangi, arco e tallone – bisognerà mantenere la posizione per qualche secondo;
- guida: sempre da seduti con le gambe distese, aiutandosi con le mani si muova dolcemente l’alluce, senza pressioni o forzarne il piegamento. Lo si abbassi lievemente e quindi lo si sollevi, cercando di mantenere il suo asse;
- muro: questo esercizio si esegue da sdraiati, le gambe piegate e i piedi poggiati su un muro. Questi andranno sollevati gradualmente partendo dal tallone, quindi si stimola l’area d’appoggio con una lievissima pressione prima su falangi, poi su arco e talloni. A ogni passaggio si dovrà mantenere la posizione per circa 5 secondi.
Non si dimentichi, infine, come un buon aiuto all’alluce valgo provenga dai plantari. Il consiglio più indicato è quello di rivolgersi a un podologo, per la realizzazione di plantari su misura.
I migliori prodotti per la cura dei piedi
Qui di seguito trovate una lista di prodotti di varie marche per la cura ed il benessere dei tuoi piedi, tra cui anche correttori e plantari che possono essere utili per prevenire e curare l’alluce valgo. Noi NON sponsorizziamo né siamo legati ad alcuna azienda produttrice: per ogni tipologia di prodotto, il nostro Staff seleziona solo il prodotto migliore, a prescindere dalla marca ed è caratterizzato dal miglior rapporto qualità prezzo e dalla maggior efficacia possibile:
Leggi anche:
- Piede piatto: cos’è e perché può diventare pericoloso per la salute
- Artrite reumatoide: sintomi iniziali, cause, cure e mortalità
- Malattie reumatiche: cosa sono, come si curano, sono pericolose?
- Differenze tra artrite ed artrosi: sintomi comuni e diversi
- Lupus eritematoso sistemico (LES): cause, sintomi e terapie
- Glucosamina e condroitina: dose, efficacia e controindicazioni
- Differenza tra artrite ed artrosi: come riconoscerle
- Articolazioni: cosa sono, come sono fatte e come funzionano
- Dolori alle articolazioni: cosa fare? Cause e rimedi
- Dolori alle articolazioni: consigli per la prevenzione e cura
- Gotta: sintomi, cause, dieta e rimedi per la malattia
- Differenza tra gotta ed artrite reumatoide
- Dolore che interessa una singola articolazione: cause e terapia
- Dolore che interessa varie articolazioni (poliarticolare): cause e rimedi
- Lussazione della spalla: cause, tipi, sintomi e cosa fare per guarire
- Sclerodermia: cause, sintomi e cura
- Sindrome di Sjögren: sintomi, invalidità, terapia e mortalità
- Fibromialgia: sintomi, cause, cura e tender points
- Fibromialgia: dove si trovano i tender points che provocano dolore alla palpazione?
- Dita ippocratiche congenite e secondarie: cause, sintomi e terapie
- Fenomeno di Raynaud: cause, sintomi e trattamento
- Differenza tra legamento ed articolazione con esempi
- Differenza tra legamento e tendine con esempi
- Legamenti: cosa sono, dove si trovano ed a che servono?
- Articolazioni mobili, semimobili, sinoviali e fisse: struttura e funzioni
- Articolazione del ginocchio: com’è fatta, quali sono le patologie, i sintomi e gli esami da fare?
- Quante ossa ha il piede e come si chiamano?
- Quanto pesano scheletro ed ossa?
- Femore rotto: tipi di frattura, sintomi, intervento, riabilitazione e conseguenze
- Osso omero: anatomia e funzioni in sintesi
- Scapola: dove si trova ed a che serve?
- Terapia con Infrarossi per il dolore
- Come viene effettuata una ecografia articolare (muscolo tendinea) ed a cosa serve?
- Differenza tra distorsione, lussazione, sublussazione e strappo muscolare
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Condividi questo articolo:







 Un malformazione piuttosto particolare si è verificata in uno sfortunato neonato dell’Azerbaigian, che è nato con due organi genitali maschili: il primo pene è posizionato nella sua sede fisiologica, mentre il secondo pene sulla schiena. I medici dell’Istituto di Ricerca Scientifica di Pediatria di Baku, dapprima stupiti della cosa hanno poi stabilito che si trattava in una parte del corpo di un gemello del neonato che non si è sviluppato.
Un malformazione piuttosto particolare si è verificata in uno sfortunato neonato dell’Azerbaigian, che è nato con due organi genitali maschili: il primo pene è posizionato nella sua sede fisiologica, mentre il secondo pene sulla schiena. I medici dell’Istituto di Ricerca Scientifica di Pediatria di Baku, dapprima stupiti della cosa hanno poi stabilito che si trattava in una parte del corpo di un gemello del neonato che non si è sviluppato. L’alluce valgo è una patologia del piede molto comune, caratterizzata dallo spostamento verso l’esterno della base dell’alluce e dallo spostamento della punta dell’alluce stesso che devia lateralmente in direzione delle altre dita. Tale deformazione comporta anche una sporgenza del primo osso del metatarso, che si accompagna a un’infiammazione, che può essere ripetuta nel tempo o costante, della cosiddetta borsa mucosa, situata alla base dell’impianto del dito. È un disturbo che interessa molto più frequentemente le donne degli uomini, specie oltre i 30 anni di età.
L’alluce valgo è una patologia del piede molto comune, caratterizzata dallo spostamento verso l’esterno della base dell’alluce e dallo spostamento della punta dell’alluce stesso che devia lateralmente in direzione delle altre dita. Tale deformazione comporta anche una sporgenza del primo osso del metatarso, che si accompagna a un’infiammazione, che può essere ripetuta nel tempo o costante, della cosiddetta borsa mucosa, situata alla base dell’impianto del dito. È un disturbo che interessa molto più frequentemente le donne degli uomini, specie oltre i 30 anni di età.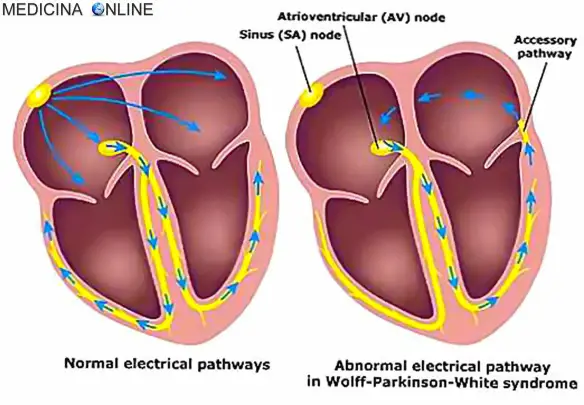 La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti. I pazienti con sindrome di WPW spesso hanno più di una via accessoria, ed in alcuni possono essere anche più di otto; questo è stato dimostrato in soggetti affetti dall’anomalia di Ebstein. La sindrome di WPW è talora associata alla neuropatia ottica ereditaria di Leber (LHON),una forma di malattia mitocondriale.
La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti. I pazienti con sindrome di WPW spesso hanno più di una via accessoria, ed in alcuni possono essere anche più di otto; questo è stato dimostrato in soggetti affetti dall’anomalia di Ebstein. La sindrome di WPW è talora associata alla neuropatia ottica ereditaria di Leber (LHON),una forma di malattia mitocondriale.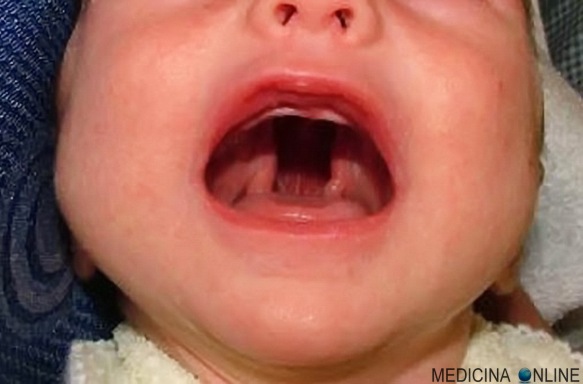 La palatoschisi è una malformazione del palato, che si presenta come una fenditura più o meno estesa della parte anteriore del palato duro. Qualora la fenditura prosegua coinvolgendo anche il labbro superiore (labbro leporino o cheiloschisi) si parla di cheilognatopalatoschisi o labiopalatoschisi.
La palatoschisi è una malformazione del palato, che si presenta come una fenditura più o meno estesa della parte anteriore del palato duro. Qualora la fenditura prosegua coinvolgendo anche il labbro superiore (labbro leporino o cheiloschisi) si parla di cheilognatopalatoschisi o labiopalatoschisi.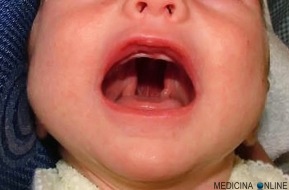 La palatoschisi è una malformazione del palato, che si presenta come una fenditura più o meno estesa della parte anteriore del palato duro.
La palatoschisi è una malformazione del palato, che si presenta come una fenditura più o meno estesa della parte anteriore del palato duro.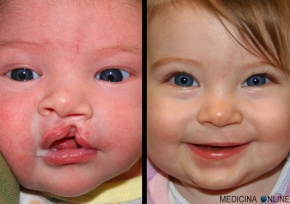 La labioschisi, o cheiloschisi comunemente chiamata “labbro leporino”, è invece una malformazione del labbro superiore. Nella foto vediamo un bimbo con labioschisi, prima e dopo l’intervento chirurgico correttivo.
La labioschisi, o cheiloschisi comunemente chiamata “labbro leporino”, è invece una malformazione del labbro superiore. Nella foto vediamo un bimbo con labioschisi, prima e dopo l’intervento chirurgico correttivo.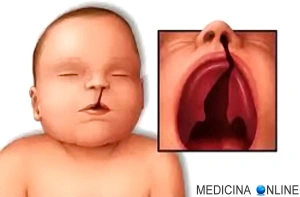 Quando la fenditura tipica di una palatoschisi prosegue coinvolgendo anche il labbro superiore si parla di cheilognatopalatoschisi o labiopalatoschisi.
Quando la fenditura tipica di una palatoschisi prosegue coinvolgendo anche il labbro superiore si parla di cheilognatopalatoschisi o labiopalatoschisi.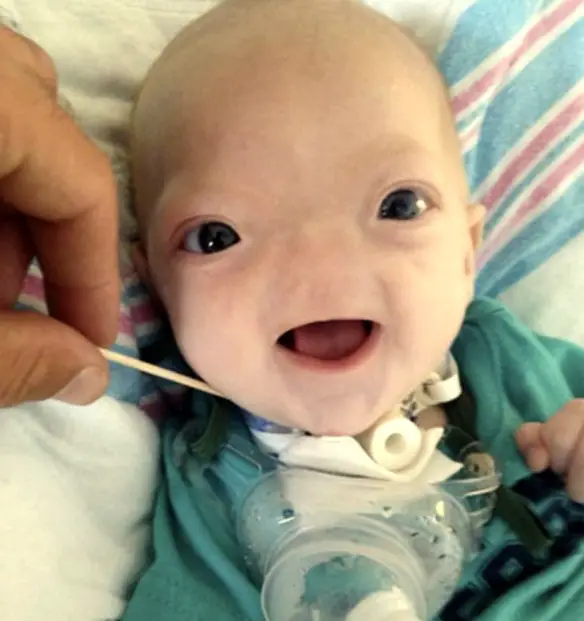 L’arinia è una patologia caratterizzata dalla mancanza congenita del naso, spesso associata con altre malformazioni del cranio e dell’encefalo (aprosopia, ecc.). E’ una condizione rarissima: in letteratura si contano soltanto 29 casi. L’arinia congenita può essere parziale, qualora interessi soltanto le strutture nasali esterne, o totale, se coinvolge l’apparato olfattivo in toto (compresi nervi e bulbi olfattivi). Le cause possono essere molteplici: sono stati descritti casi associati ad inversione e trisomia del cromosoma 9, diabete materno, polidramnios. E’ molto difficile da trattare.
L’arinia è una patologia caratterizzata dalla mancanza congenita del naso, spesso associata con altre malformazioni del cranio e dell’encefalo (aprosopia, ecc.). E’ una condizione rarissima: in letteratura si contano soltanto 29 casi. L’arinia congenita può essere parziale, qualora interessi soltanto le strutture nasali esterne, o totale, se coinvolge l’apparato olfattivo in toto (compresi nervi e bulbi olfattivi). Le cause possono essere molteplici: sono stati descritti casi associati ad inversione e trisomia del cromosoma 9, diabete materno, polidramnios. E’ molto difficile da trattare.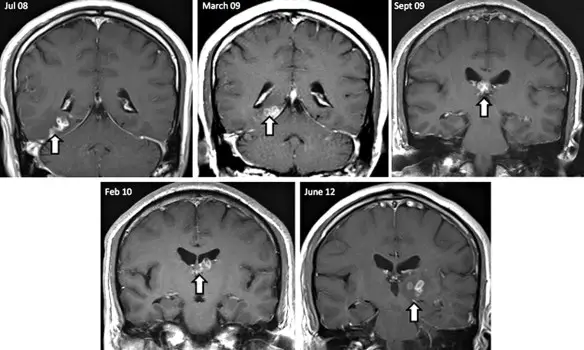 Per meglio comprendere l’argomento, leggi prima:
Per meglio comprendere l’argomento, leggi prima: