 Quando si scopre un cancro, è fondamentale intervenire rapidamente asportando chirurgicamente quanto più tessuto maligno sia possibile, anche a costo di amputare parti del corpo importanti, demolendo ad esempio parzialmente o totalmente tiroide, fegato, pancreas, polmone, mammella e retto. Diagnosticare e rimuovere un cancro al più presto è importante perché permette di evitare che il tessuto tumorale diventi troppo grande e che le sue cellule arrivino a colonizzare altri organi tramite la diffusione metastatica. I tumori maligni, infatti, non sono formazioni statiche, bensì dinamiche, che cambiano nel tempo.
Quando si scopre un cancro, è fondamentale intervenire rapidamente asportando chirurgicamente quanto più tessuto maligno sia possibile, anche a costo di amputare parti del corpo importanti, demolendo ad esempio parzialmente o totalmente tiroide, fegato, pancreas, polmone, mammella e retto. Diagnosticare e rimuovere un cancro al più presto è importante perché permette di evitare che il tessuto tumorale diventi troppo grande e che le sue cellule arrivino a colonizzare altri organi tramite la diffusione metastatica. I tumori maligni, infatti, non sono formazioni statiche, bensì dinamiche, che cambiano nel tempo.
Il tumore progredisce
Nelle fasi iniziali un cancro è generalmente di dimensioni più ridotte, è più localizzato, non ha ancora colonizzato altri organi; nelle fasi successive esso si ingrandisce e colonizza gli organi vicini: intervenire nelle fasi iniziali o nelle fasi tardive della progressione cancerosa, può letteralmente fare la differenza tra la vita e la morte del paziente. Per questo, quando viene diagnosticato un cancro, diventa per il medico molto importante il capire in quale fase della malattia si trova il tumore maligno. Ciò avviene soprattutto alla diagnostica per immagini: una RX, una TAC, una risonanza magnetica, permettono di capire lo stadio della malattia; leggi anche: Differenze tra risonanza magnetica, TAC, PET, MOC, radiografia, ecografia ed endoscopia
La classificazione TNM
Tutte le indagini volte a capire in quale stadio si trova il tumore, convergono nella “classificazione TNM“, cioè un sistema di classificazione dei tumori internazionale, a partire dal quale si può velocemente intuire “a che punto” della sua progressione si trova la neoplasia. Ogni tumore viene classificato attraverso questa sigla, che ne riassume le caratteristiche principali, contribuendo a determinare la stadiazione, da cui deriveranno, insieme con altri fattori, le scelte terapeutiche (farmaci, chirurgia, terapie palliative) e la prognosi (probabilità di guarigione o morte) associata. A partire dalla conoscenza dei parametri della classificazione TNM, si può ricavare lo stadio in cui si trova il tumore maligno, cioè l’estensione della malattia e quindi la sua gravità.
Leggi anche:
I parametri della classificazione TNM
Per qualsiasi tipo di tumore esistono quattro stadi, a cui va aggiunto lo stadio 0 in cui si ha un carcinoma in situ, cioè un tumore non invasivo che non ha infiltrato altri organi ed è quindi di solito facilmente curabile).
I quattro stadi sono indicati con numeri da 1 a 4, in ordine crescente di gravità; tale divisione, a partire dalla classificazione TNM, varia a seconda della sede del tumore primario (ad esempio il T2N0M0 fa parte del secondo stadio nel tumore al seno e del primo nel tumore polmonare), ma in genere le differenze non sono molto significative.
- Il parametro T può essere 1, 2, 3, 4 a seconda della grandezza del tumore (1 piccola, 4 grande). Può inoltre essere “is” ovvero “in situ”. Il T4 in genere è tale non solo per la dimensione, ma anche per l’infiltrazione di organi vitali adiacenti (pericardio, esofago, trachea, ecc.).
- Il parametro N indica lo stato dei linfonodi vicini al tumore, se è 0 sono del tutto indenni, altrimenti può valere 1, 2, 3 con gravità via via crescente. Il coinvolgimento linfonodale è molto importante per capire la gravità del tumore.
- Il parametro M indica la presenza di metastasi a distanza, esso può valere solo 0 (nessuna metastasi) o 1 (presenza di metastasi). La presenza di metastasi è un fattore prognostico molto importante per capire la gravità del tumore.
- Un parametro rappresentato da una “x” (ad esempio, T2N1Mx) indica che non si conosce l’esatta estensione a distanza della malattia per il quale sono necessari ulteriori esami di approfondimento (ad esempio: PET, TAC, RMN, scintigrafia ossea, ecografia, radiografie…).
Leggi anche:
Valutazione del grading
In alcune neoplasie (per esempio nei sarcomi dei tessuti molli) nella stadiazione rientra anche la valutazione del grading. Il grado di aggressività del tumore o grado di differenziazione cellulare della neoplasia (grading) è indicato con (G), che va da 1 a 4. (Va tenuto presente che le cellule “sane” sono quelle completamente differenziate ossia quelle che si sono sviluppate fino ad arrivare ad avere le caratteristiche per svolgere perfettamente le funzioni per le quali sono state destinate.
- Il grado 1 (G1, tumore ben differenziato) si riferisce a neoplasie con cellule tumorali che hanno, all’esame microscopico, aspetto lievemente differente rispetto alle cellule normali dello stesso tessuto;
- Il grado 2 (G2, tumore moderatamente differenziato) è quello intermedio.
- Il grado 3 (G3, tumore scarsamente differenziato) si riferisce a cellule tumorali con aspetto altamente difforme da quelle dello stesso tessuto normale;
- Il grado 4 (G4, indifferenziato) si riferisce a cellule che hanno perso totalmente le caratteristiche del tessuto d’origine (anaplasia).
Il grading considera parametri ora citologici, ora istologici, ora entrambi a seconda dell’istogenesi del tumore. Esistono svariati sistemi di grading più o meno complessi, anche se per questioni di riproducibilità e standardizzazione, si sta cercando di adottare sistemi a classi dicotomiche (alto/basso), annullando così classi intermedie che sono fonte di variabilità e soggettività.
Esempio di classificazione
Ecco la classificazione in stadi nel caso del tumore polmonare maligno di tipo non-microcitoma:
| Stadio |
TNM |
| Stadio 0 |
Tis N0 M0
(tumore in situ) |
| Stadio I |
T1-2 N0 M0 |
| Stadio II |
T1-2 N1 M0
T3 N0 M0 |
| Stadio III |
T1-2 N2-3 M0
T3 N1-3 M0
T4 N0-3 M0 |
| Stadio IV |
T1-4 N0-3 M1
(qualunque caso in cui si abbiano metastasi a distanza) |
Stadio della malattia e prognosi
Abbiamo quindi capito quanto la conoscenza dello stadio della malattia sia importante per fornire al paziente delle cure il più possibile appropriate, oltre che per formulare una prognosi. Nello stadio 0 le percentuali di guarigione sono praticamente del 100%; gli stadi I e II sono considerati iniziali e la prognosi è, nella maggioranza dei casi, favorevole (soprattutto se non vi è coinvolgimento linfonodale); Nello stadio III è in genere utile associare alla chirurgia una terapia sistemica “adiuvante”; lo stadio IV viene considerato come malattia avanzata e la prognosi è spesso infausta in quanto guaribile solo in pochi tipi di neoplasia. In presenza di un tumore avanzato, soprattutto se metastatico, la terapia (tranne pochi tipi tumorali) non può avere l’ambizione dei guarire il paziente, ed è quindi palliativa, finalizzata cioè a prolungare la durata della vita, a mantenere o migliorare la qualità della vita, a limitare i sintomi (prevalentemente il dolore) nel paziente. Bisogna però tenere presente che queste sono solo indicazioni generali di massima, e che le cose variano da tumore a tumore. Ad esempio, le percentuali di guarigione di un cancro al testicolo avanzato sono superiori a quelle di un cancro al pancreas in fase iniziale: ogni tumore ha, in virtù di posizione, vascolarizzazione, citologia ed una moltitudine di altri fattori, capacità ed aggressività diverse dagli altri tumori.
Leggi anche:
L’importanza della prevenzione e dello screening
Molti tumori maligni non danno sintomi se non nelle fasi terminali e vengono purtroppo scoperti solo quando sono talmente estesi che nessuna cura potrà impedire la morte del paziente, è il caso ad esempio di alcuni tipi di tumore del pancreas che, dopo la diagnosi, determinano spesso la morte in pochi mesi. Per questo motivo è importante prevenire i tumori (con dieta adeguata, attività fisica, eliminazione di fumo di sigaretta…) ma è anche vitale lo screening nei soggetti a rischio. Il termine “screening” indica una strategia di indagini diagnostiche in soggetti che, pur non avendo alcun sintomo, né segno clinico di malattia, hanno un’alta probabilità di averla. Per esempio una donna di 40 anni, con una madre che ha sofferto di cancro al seno, dovrebbe periodicamente effettuare palpazione al seno, unita ad ecografia mammaria e mammografia, anche se non ha alcun sintomo di tumore. In questo modo, un eventuale neoplasia, sarà scoperta nelle sue fasi più precoci, con stadiazione meno grave e – come avete intuito dalla lettura di questo articolo – più facilmente curabile. Ricordate: scoprire al più presto un tumore maligno, equivale ad avere molte più chance di sopravvivenza.
Leggi anche:
- Differenza tra tumore e tessuto normale con esempi di tumori benigni e maligni
- Significato di lesione neoplastica, lesione eteroformativa, eteroplasia e lesione eteroplastica
- Tumore primitivo, lesione eteroplastica primitiva e lesione eteroformativa primitiva: cosa significano?
- L’ecografia mammaria: un esame innocuo ed indolore che ti può salvare vita
- Chemioterapia: durata, in pastiglie, come funziona, fa male, perché farla?
- Radioterapia: cos’è, come si fa, come funziona e durata del trattamento
- Chemioterapia: gli effetti collaterali più e meno comuni
- Radioterapia: rischi, dolore, fastidio ed effetti collaterali
- Radioterapia in gravidanza: può far male al bambino?
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Condividi questo articolo:
 Salsiccia fresca ritirata a causa del rischio salmonella. Il ministero della Salute ha pubblicato il richiamo di un lotto di salsicce fresche in filze prodotta da Bevanati Claudio e Figli, un’azienda di Foligno (Perugia), per la presenza di salmonella.
Salsiccia fresca ritirata a causa del rischio salmonella. Il ministero della Salute ha pubblicato il richiamo di un lotto di salsicce fresche in filze prodotta da Bevanati Claudio e Figli, un’azienda di Foligno (Perugia), per la presenza di salmonella.
 La salmonella nei bambini si comporta diversamente rispetto agli adulti. Il bambino con meno di cinque anni ha in media un periodo di escrezione del germe con le feci più lungo rispetto ai bambini più grandi o agli adulti. In pratica, circa il 45% degli infetti sotto i cinque anni elimina ancora il germe dopo tre mesi e circa l’1% lo fa ancora dopo un anno. La definizione di portatore sano si applica già ai primi giorni dopo la malattia: siccome tutti i malati, quando guariscono clinicamente (cioè non hanno più sintomi), continuano comunque ad eliminare germi per un po’, tutti sono per un certo periodo portatori sani.
La salmonella nei bambini si comporta diversamente rispetto agli adulti. Il bambino con meno di cinque anni ha in media un periodo di escrezione del germe con le feci più lungo rispetto ai bambini più grandi o agli adulti. In pratica, circa il 45% degli infetti sotto i cinque anni elimina ancora il germe dopo tre mesi e circa l’1% lo fa ancora dopo un anno. La definizione di portatore sano si applica già ai primi giorni dopo la malattia: siccome tutti i malati, quando guariscono clinicamente (cioè non hanno più sintomi), continuano comunque ad eliminare germi per un po’, tutti sono per un certo periodo portatori sani. Con “ittero” in medicina si intende un segno caratterizzato da colorazione giallastra della pelle, delle sclere e delle mucose causata dall’eccessivo innalzamento dei livelli di bilirubinemia, cioè della bilirubina nel sangue. Affinché l’ittero sia visibile il livello di bilirubina deve superare 2,5 mg/dL. Un ittero lieve (sub-ittero), osservabile esaminando le sclere alla luce naturale, è di solito evidenziabile quando i valori della bilirubina sierica sono compresi tra 1,5 – 2,5 mg/dl. L’ittero è una condizione parafisiologica nel neonato, mentre è frequentemente segno di patologia nell’adulto. La bilirubina deriva dal catabolismo dell’eme (molecola contenuta nell’emoglobina), ed è presente nel corpo umano in due forme: forma indiretta, che si trova normalmente in circolo ed è veicolata dall’albumina plasmatica; forma diretta, in cui la bilirubina è coniugata con l’acido glucuronico, indice che è stata glucoronoconiugata dal fegato e resa idrofila, adatta ad essere eliminata con la bile. L’identificazione di quale delle due forme di bilirubina è presente in eccesso dà un’indicazione sulle cause dell’ittero.
Con “ittero” in medicina si intende un segno caratterizzato da colorazione giallastra della pelle, delle sclere e delle mucose causata dall’eccessivo innalzamento dei livelli di bilirubinemia, cioè della bilirubina nel sangue. Affinché l’ittero sia visibile il livello di bilirubina deve superare 2,5 mg/dL. Un ittero lieve (sub-ittero), osservabile esaminando le sclere alla luce naturale, è di solito evidenziabile quando i valori della bilirubina sierica sono compresi tra 1,5 – 2,5 mg/dl. L’ittero è una condizione parafisiologica nel neonato, mentre è frequentemente segno di patologia nell’adulto. La bilirubina deriva dal catabolismo dell’eme (molecola contenuta nell’emoglobina), ed è presente nel corpo umano in due forme: forma indiretta, che si trova normalmente in circolo ed è veicolata dall’albumina plasmatica; forma diretta, in cui la bilirubina è coniugata con l’acido glucuronico, indice che è stata glucoronoconiugata dal fegato e resa idrofila, adatta ad essere eliminata con la bile. L’identificazione di quale delle due forme di bilirubina è presente in eccesso dà un’indicazione sulle cause dell’ittero. Prima di iniziare la lettura, per meglio comprendere l’argomento trattato, ti consiglio di leggere:
Prima di iniziare la lettura, per meglio comprendere l’argomento trattato, ti consiglio di leggere:  Quando si scopre un cancro, è fondamentale intervenire rapidamente asportando chirurgicamente quanto più tessuto maligno sia possibile, anche a costo di amputare parti del corpo importanti, demolendo ad esempio parzialmente o totalmente tiroide, fegato, pancreas, polmone, mammella e retto. Diagnosticare e rimuovere un cancro al più presto è importante perché permette di evitare che il tessuto tumorale diventi troppo grande e che le sue cellule arrivino a colonizzare altri organi tramite la diffusione metastatica. I tumori maligni, infatti, non sono formazioni statiche, bensì dinamiche, che cambiano nel tempo.
Quando si scopre un cancro, è fondamentale intervenire rapidamente asportando chirurgicamente quanto più tessuto maligno sia possibile, anche a costo di amputare parti del corpo importanti, demolendo ad esempio parzialmente o totalmente tiroide, fegato, pancreas, polmone, mammella e retto. Diagnosticare e rimuovere un cancro al più presto è importante perché permette di evitare che il tessuto tumorale diventi troppo grande e che le sue cellule arrivino a colonizzare altri organi tramite la diffusione metastatica. I tumori maligni, infatti, non sono formazioni statiche, bensì dinamiche, che cambiano nel tempo. I polisaccaridi sono macromolecole formate dall’unione di numerose molecole di monosi (uguali o diversi) uniti da legame covalente ed hanno peso molecolare variabile in base al numero di costituenti. Sono poco solubili o insolubili in acqua (dato l’elevato numero di legami che contemporaneamente dovrebbero spezzarsi), privi di sapore dolce e vengono scomposti nei rispettivi monomeri mediante idrolisi in soluzione acida ed in presenza di enzimi. I polisaccaridi sono i glucidi più rappresentati in natura, in particolare nei vegetali, dove svolgono funzioni di riserva, di sostegno e di protezione.
I polisaccaridi sono macromolecole formate dall’unione di numerose molecole di monosi (uguali o diversi) uniti da legame covalente ed hanno peso molecolare variabile in base al numero di costituenti. Sono poco solubili o insolubili in acqua (dato l’elevato numero di legami che contemporaneamente dovrebbero spezzarsi), privi di sapore dolce e vengono scomposti nei rispettivi monomeri mediante idrolisi in soluzione acida ed in presenza di enzimi. I polisaccaridi sono i glucidi più rappresentati in natura, in particolare nei vegetali, dove svolgono funzioni di riserva, di sostegno e di protezione.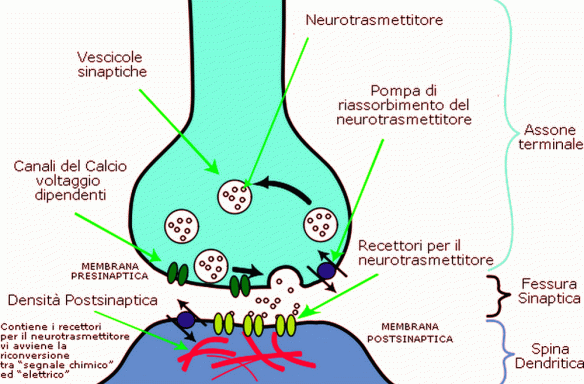 L’acetilcolina (in inglese “acetylcholine”, abbreviato “ACh”) è un neurotrasmettitore, cioè una sostanza che veicola le informazioni fra le cellule componenti il sistema nervoso, i neuroni, attraverso la trasmissione sinaptica; a tal proposito leggi anche:
L’acetilcolina (in inglese “acetylcholine”, abbreviato “ACh”) è un neurotrasmettitore, cioè una sostanza che veicola le informazioni fra le cellule componenti il sistema nervoso, i neuroni, attraverso la trasmissione sinaptica; a tal proposito leggi anche:  I valori normali di fibrinogeno dovrebbero aggirarsi tra i 200 e 400 mg/dl, anche se si tratta di valori che non tengono conto, ovviamente, dei cambiamenti che avvengono nel nostro corpo durante la nostra gestazione. Durante la gravidanza sono infatti ritenuti normali valori fino a 700 mg/dl, con il valore minimo che si sposta anch’esso verso l’alto e si attesta intorno ai 400 mg/dl. È dunque più che normale avere valori elevati di fibrinogeno durante la gravidanza e questo, almeno finché si rimane nella forbice sopra indicata, non deve essere assolutamente motivo di preoccupazione.
I valori normali di fibrinogeno dovrebbero aggirarsi tra i 200 e 400 mg/dl, anche se si tratta di valori che non tengono conto, ovviamente, dei cambiamenti che avvengono nel nostro corpo durante la nostra gestazione. Durante la gravidanza sono infatti ritenuti normali valori fino a 700 mg/dl, con il valore minimo che si sposta anch’esso verso l’alto e si attesta intorno ai 400 mg/dl. È dunque più che normale avere valori elevati di fibrinogeno durante la gravidanza e questo, almeno finché si rimane nella forbice sopra indicata, non deve essere assolutamente motivo di preoccupazione.