 La leucemia è un tumore che si sviluppa nelle cellule del sangue; vengono comunemente distinte in acute e croniche, sulla base della velocità di progressione della malattia:
La leucemia è un tumore che si sviluppa nelle cellule del sangue; vengono comunemente distinte in acute e croniche, sulla base della velocità di progressione della malattia:
- nella forma acuta il numero di cellule tumorali aumenta rapidamente e con essa i sintomi,
- nella forma cronica invece le cellule maligne tendono a proliferare più lentamente e la malattia più rimanere più a lungo senza manifestare sintomi.
Considerando l’insieme delle diverse forme il tumore colpisce molto più spesso i bambini che gli adulti, per esempio le leucemie acute sono il tumore più diffuso in età infantile. Le forme croniche sono invece più diffuse in età adulta.
I sintomi iniziali dipendono dalla forma che si manifesta, in molti casi purtroppo possono essere asintomatiche o manifestarsi disturbi molto vaghi come stanchezza che non accenna a passare.
In Italia vengono diagnosticati circa 15 nuovi casi ogni 100.000 persone all’anno. La sopravvivenza a 5 anni è di poco inferiore al 50%, ma molto dipende dalla forma sviluppata, ad esempio arriva al 90% nei bambini colpiti da leucemie linfoidi, e supera il 65% nella forma mieloide acuta.
Ad oggi non è possibile indicare come prevenire l’insorgere della malattia, perchè non se conoscono ancora le cause scatenanti.
Leucemia fulminante
Il termine abbastanza improprio di leucemia fulminante fa riferimento a casi acuti con decorso particolarmente rapido; si tratta per esempio della forma promielocitica acuta, che rappresenta la variante più aggressiva dei tumori del sangue e, se non diagnosticata rapidamente, porta a decesso in pochi giorni. I sintomi iniziali sono spesso
- emorragie cutanee (sangue dal naso, dalle gengive, dall’apparato digerente, …),
- stanchezza,
- malessere generale.
Leggi anche:
Cause
Quando si riceve una diagnosi di tumore è naturale chiedersi quali siano le cause della malattia. Le cause della leucemia non sono note, i medici riescono solo in rari casi a capire perché alcuni soggetti si ammalino mentre altri rimangano perfettamente sani, tuttavia le ricerche dimostrano che determinati fattori di rischio fanno aumentare il rischio di ammalarsi di leucemia.
I fattori di rischio, con ogni probabilità, sono diversi per ciascuno dei tipi di leucemia:
- Esposizione alle radiazioni. Le persone esposte a dosi massicce di radiazioni hanno maggiori probabilità di ammalarsi di leucemia mieloide acuta, leucemia mieloide cronica o leucemia linfocitica acuta.
- Esplosioni atomiche. Dosi massicce di radiazioni sono state provocate dalle esplosioni atomiche, ad esempio quelle avvenute in Giappone durante la Seconda Guerra Mondiale. I sopravvissuti alle esplosioni, e soprattutto i bambini, corrono un rischio maggiore di ammalarsi di leucemia.
- Radioterapia. Un’altra fonte di esposizione a dosi massicce di radiazioni è la radioterapia contro il tumore e altre malattie. La radioterapia fa aumentare il rischio di ammalarsi di leucemia.
- Radiografie. Le radiografie dentali o di altri tipi (ad esempio la TAC) espongono il paziente a dosi di radiazioni estremamente basse. Non è tuttora chiaro se queste quantità minime di radiazioni siano collegate ai casi di leucemia nei bambini e negli adulti. I ricercatori stanno studiando se le radiografie ripetute e se le TAC effettuate durante l’infanzia siano in grado di aumentare il rischio di leucemia.
- Fumo. Il fumo di sigaretta fa aumentare il rischio di leucemia mieloide acuta.
- Benzene. L’esposizione al benzene sul posto di lavoro può provocare la leucemia mieloide, la leucemia mieloide cronica oppure la leucemia linfocitica acuta. Il benzene è una sostanza molto usata nell’industria chimica, ma si può trovare anche nel fumo di sigaretta e nel gasolio.
- Chemioterapia. In alcuni casi i pazienti affetti da tumore e curati con determinati farmaci chemioterapici possono ammalarsi in un secondo momento di leucemia mieloide acuta o di leucemia linfocitica acuta. Ad esempio, la cura con gli agenti alchilanti o con gli inibitori della topoisomerasi è associata a una scarsa probabilità di soffrire di leucemia acuta in una fase successiva.
- Sindrome di Down e altre malattie ereditarie. La sindrome di Down e alcune altre malattie ereditarie fanno aumentare il rischio di soffrire di leucemia.
- Mielodisplasia e altre malattie del sangue. chi è affetto da determinate malattie del sangue corre un maggior rischio di soffrire di leucemia mieloide acuta.
- Virus dei linfociti T dell’uomo di tipo 1 (HTLV-I). Chi è affetto dal virus HTLV di tipo 1 corre un rischio maggiore di ammalarsi di una forma rara di leucemia nota come leucemia a cellule T. Anche se questa malattia rara è provocata dal virus HTLV-I, la leucemia a cellule T dell’adulto non è contagiosa, come tutti gli altri tipi di leucemia.
- Precedenti famigliari di leucemia. È raro che diversi membri di una famiglia si ammalino di leucemia. Se dovesse succedere, è probabile che si tratti di leucemia linfocitica cronica. Tuttavia solo una piccola percentuale di pazienti affetti da leucemia linfocitica cronica ha un genitore, un fratello o un figlio affetto dalla stessa malattia.
Avere uno o più fattori di rischio non significa che ci si ammalerà necessariamente di leucemia. La maggior parte delle persone che presentano fattori di rischio non si ammalerà mai.
Le cellule del sangue
La maggior parte delle cellule del sangue si forma a partire dalle cellule staminali che si trovano nel midollo osseo, cioè nel tessuto spugnoso presente al centro di quasi tutte le ossa.
Le cellule staminali, maturando, si trasformano in diversi tipi di cellule del sangue ed ogni tipo ha la propria funzione:
- I globuli bianchi (leucociti) aiutano a combattere le infezioni. Ne esistono di diversi tipi.
- I globuli rossi trasportano l’ossigeno verso i tessuti dell’organismo.
- Le piastrine contribuiscono a far coagulare il sangue arrestando il sanguinamento.
I globuli bianchi, i globuli rossi e le piastrine sono fabbricati a partire dalle cellule staminali man mano che l’organismo ne ha bisogno. Quando le cellule invecchiano o subiscono danni, muoiono e vengono sostituite da cellule nuove. Le cellule staminali si trasformano in diversi tipi di globuli bianchi. La singola cellula staminale può trasformarsi in cellula della linea mieloide o in cellula della linea linfoide:
- La cellula della linea mieloide si trasforma in mieloblasto. Il mieloblasto può evolversi in globulo rosso, piastrina o in uno dei diversi tipi di globulo bianco.
- La cellula linfoide si evolve in linfoblasto, che a sua volta può formare i diversi tipi di globulo bianco, ad esempio i linfociti B o i linfociti T.
I globuli bianchi che si formano dai mieloblasti sono diversi da quelli che si formano a partire dai linfoblasti. La maggior parte delle cellule del sangue maturano nel midollo osseo, per poi spostarsi nei vasi sanguigni. Il sangue che scorre nei vasi sanguigni e nel cuore forma il cosiddetto sangue periferico.
Le cellule tumorali
Nei pazienti affetti da leucemia il midollo osseo produce globuli bianchi anomali, cioè cellule tumorali. Diversamente dai globuli bianchi normali le cellule tumorali non muoiono ma vanno ad aggiungersi ai globuli bianchi, ai globuli rossi e alle piastrine normali. In questo modo il lavoro delle cellule normali diventa più difficile.
Tipi di leucemia
I diversi tipi di leucemia possono essere classificati in base alla velocità di sviluppo e di peggioramento della malattia. La leucemia può essere cronica (a decorso lento) o acuta (a decorso veloce):
- Leucemia cronica: Nelle prime fasi della malattia le cellule tumorali riescono ancora a svolgere in parte il lavoro dei globuli bianchi normali. In un primo tempo i pazienti possono non presentare sintomi ed i medici spesso diagnosticano la leucemia cronica durante una normale visita di controllo, prima che i sintomi si presentino. La leucemia cronica peggiora lentamente, con l’aumento delle cellule tumorali nel sangue iniziano i sintomi, ad esempio il gonfiore dei linfonodi o le infezioni. Se compaiono, i sintomi all’inizio sono lievi e peggiorano gradualmente.
- Leucemia acuta: Le cellule tumorali non possono svolgere il lavoro dei globuli bianchi normali. Si moltiplicano rapidamente e quindi la leucemia acuta di solito peggiora molto in fretta.
I vari tipi di leucemia possono anche essere classificati in base al tipo di globulo bianco colpito. La leucemia può svilupparsi nelle cellule linfoidi o in quelle mieloidi, il primo tipo è detto leucemia linfoide, linfocitica o linfoblastica; invece la leucemia che colpisce le cellule mieloidi è detta leucemia mieloide, mielogena o mieloblastica.
Esistono quattro forme di leucemia frequenti:
- Leucemia linfocitica cronica (o leucemia linfatica cronica, LLC). Colpisce le cellule linfoidi e di solito si sviluppa molto lentamente. Negli Stati Uniti, è causa di più di 15.000 nuovi casi di leucemia ogni anno. Nella maggior parte dei casi i pazienti a cui è diagnosticata hanno più di 55 anni. Non colpisce quasi mai i bambini.
- Leucemia mieloide cronica (LMC). Colpisce le cellule mieloidi e di solito in una prima fase si sviluppa molto lentamente. Negli Stati Uniti causa circa 5.000 casi di leucemia all’anno. Colpisce soprattutto gli adulti.
- Leucemia linfocitica (linfoblastica) acuta (LLA). Colpisce le cellule linfoidi e si sviluppa molto rapidamente. Negli Stati Uniti provoca più di 5.000 casi di leucemia ogni anno. È la forma di leucemia più frequente tra i bambini, ma può colpire anche gli adulti.
- Leucemia mieloide acuta (LMA o LAM). Questo tipo di leucemia si sviluppa nelle cellule mieloidi e ha un decorso molto rapido. Negli Stati Uniti provoca più di 13.000 nuovi casi all’anno. Colpisce sia gli adulti sia i bambini.
La leucemia a tricoleucociti è una forma rara di leucemia cronica. In questo articolo non parleremo né di questo tipo di leucemia né delle leucemie rare che, nel complesso, fanno registrare meno di 6.000 casi ogni anno negli USA.
Sintomi
Le cellule tumorali si spostano all’interno dell’organismo come le normali cellule del sangue. I sintomi della leucemia dipendono dal numero di cellule tumorali e dal luogo dell’organismo in cui si accumulano.
Chi è affetto da leucemia cronica può non manifestare alcun sintomo, i medici normalmente diagnosticano la malattia a seguito di una normale visita di controllo. Chi invece è affetto da leucemia acuta di solito va dal medico perché non si sente bene. Se a essere colpito è il cervello, si può soffrire di:
- mal di testa,
- vomito,
- confusione,
- perdita di controllo muscolare,
- convulsioni.
La leucemia può anche colpire altre parti del corpo, ad esempio
- l’apparato digerente,
- i reni,
- i polmoni,
- il cuore,
- i testicoli.
Tra i sintomi frequenti della leucemia cronica o acuta possiamo annoverare:
- gonfiore non doloroso dei linfonodi (soprattutto quelli del collo o delle ascelle),
- febbre o sudorazione notturna,
- infezioni frequenti,
- debolezza o stanchezza,
- sanguinamento o lividi anomali (gengive che sanguinano, lividi sulla pelle, macchioline rosse sottopelle),
- gonfiore o problemi addominali (milza o fegato gonfi),
- dimagrimento inspiegabile,
- dolore alle ossa o alle articolazioni.
Nella maggior parte dei casi questi sintomi non sono da imputare al tumore, infatti possono essere provocati da un’infezione o da altri problemi di salute. Solo il medico potrà effettuare una diagnosi certa. Chiunque soffra di questi sintomi dovrebbe recarsi dal proprio medico, in modo che i problemi possano essere diagnosticati e curati il prima possibile.
Leggi anche:
Diagnosi
Spesso i medici diagnosticano la leucemia dopo un normale esame del sangue. Se soffrite di sintomi che possono far pensare alla leucemia, il medico cercherà di scoprire quali sono le cause e probabilmente vi chiederà di quali problemi di salute voi e i vostri famigliari avete sofferto in passato.
Probabilmente vi dovrete sottoporre a uno o più dei seguenti esami:
- Visita. Il medico controllerà se i linfonodi, la milza o il fegato sono gonfi.
- Esami del sangue. Le analisi complete controllano il numero di globuli bianchi, di globuli rossi e di piastrine. La leucemia causa un aumento dei globuli bianchi, una diminuzione delle piastrine e dell’emoglobina, una sostanza presente nei globuli rossi.
- Biopsia. La biopsia è un prelievo di tessuto effettuato per individuare eventuali cellule tumorali. La biopsia è l’unico metodo sicuro per sapere se nel midollo osseo ci sono cellule tumorali. Prima del prelievo vi verrà somministrata l’anestesia locale, che vi aiuterà a non avvertire dolore. Il chirurgo preleverà un campione di midollo osseo dal femore o da un’altra delle ossa principali. Il patologo, usando il microscopio, controllerà se nel tessuto ci sono cellule tumorali. Il midollo osseo può essere prelevato in due modi diversi. Alcuni pazienti devono sottoporsi a entrambi gli interventi seguenti contemporaneamente:
- Ago aspirato. Il medico usa una specie di grande ago, internamente cavo, per prelevare il campione di midollo osseo.
- Biopsia. Il medico usa un grande ago internamente cavo per prelevare un minuscolo campione di osso e di midollo osseo.
Altri esami
Gli altri esami che il medico vi prescriverà dipendono dai sintomi e dal tipo di leucemia di cui soffrite. Tra di essi ricordiamo:
- Analisi citogenetica. In laboratorio si esaminano i cromosomi ricavati dalle cellule del sangue, del midollo osseo o dei linfonodi. Se si evidenziano cromosomi anomali l’analisi può stabilire il tipo di leucemia che provoca il problema; ad esempio i pazienti affetti da leucemia mieloide cronica hanno un cromosoma anomalo detto cromosoma Philadelphia, dalla città in cui fu scoperto.
- Puntura lombare. Il medico può prelevare un campione di liquor cefalorachidiano (il liquido che riempie gli spazi intorno al cervello e alla colonna vertebrale). Il prelievo viene effettuato nella zona lombare, mediante un ago lungo e sottile. L’intervento richiede circa mezz’ora e viene effettuato in anestesia locale. È necessario rimanere distesi per alcune ore dopo il prelievo, per evitare il mal di testa. Il campione sarà esaminato in laboratorio, alla ricerca di cellule tumorali o altri segni di problemi in atto.
- Radiografia toracica. La radiografia può evidenziare linfonodi gonfi o altri sintomi a livello del torace.
Cura e terapia
I pazienti affetti da leucemia hanno di fronte a sé diverse possibilità, tra le quali ricordiamo:
- l’attesa vigile,
- la chemioterapia,
- la terapia mirata,
- la terapia biologica,
- la radioterapia,
- il trapianto di cellule staminali.
Se la milza è eccessivamente dilatata il medico può consigliarvi l’intervento chirurgico per asportarla. In alcuni casi invece può essere necessario ricorrere a una combinazione di diverse terapie.
La scelta della terapia dipende principalmente da:
- Tipo di leucemia (acuta o cronica),
- Età del paziente,
- Eventuale presenza di cellule tumorali all’interno del liquido cefalorachidiano.
La scelta della terapia, inoltre, può dipendere da determinate caratteristiche delle cellule tumorali; il medico prenderà anche in considerazione i sintomi e il vostro stato di salute generale.
Chi è affetto da leucemia acuta deve farsi curare immediatamente, lo scopo della terapia è distruggere le cellule tumorali presenti nell’organismo e di far così scomparire i sintomi (remissione). Quando la remissione è iniziata può essere somministrata un’ulteriore terapia che prevenga le recidive: questo tipo di terapia è detto di consolidamento o di mantenimento. La maggior parte dei pazienti affetti da leucemia acuta può essere curata.
Se invece soffrite di leucemia cronica, senza sintomi apparenti, può darsi che non dobbiate ricorrere immediatamente alla terapia. Il vostro medico terrà sotto controllo il vostro stato di salute e la terapia inizierà solo quando avvertirete i primi sintomi. Rinviare l’inizio della terapia e ricorrere a controlli periodici in attesa che i sintomi si manifestino è una modalità terapeutica detta attesa vigile.
Se necessaria per la leucemia cronica, la terapia spesso può tenere sotto controllo la malattia e i suoi sintomi. I pazienti possono ricevere una terapia di mantenimento che contribuisca a mantenere il tumore in stato di remissione, ma solo in rari casi la leucemia cronica può essere curata con la chemioterapia. Per alcune persone affette da leucemia cronica la miglior possibilità di cura rimane infine il trapianto di cellule staminali.
Il medico può descrivervi le opportunità terapeutiche, i risultati attesi e gli eventuali effetti collaterali: potete lavorare insieme a lui per creare un piano terapeutico che venga incontro alle vostre necessità.
Il medico di base può indirizzarvi presso uno specialista, oppure potete essere voi stessi a richiedergli un consiglio riguardo lo specialista da consultare. Tra gli specialisti in grado di curare la leucemia ricordiamo:
- l’ematologo,
- l’oncologo,
- il radiologo.
Gli oncologi e gli ematologi pediatrici curano la leucemia nei bambini.
Prima dell’inizio della terapia, è consigliabile informarsi sugli effetti collaterali e sulle ricadute della terapia sulle normali attività quotidiane. In molti casi la terapia contro il tumore danneggia anche le cellule e i tessuti sani, quindi gli effetti collaterali sono frequenti. Gli effetti collaterali possono essere diversi da paziente a paziente e possono cambiare anche da una sessione alla successiva.
Terapia di supporto
La leucemia e la terapia possono causare altri problemi di salute, probabilmente dovrete sottoporvi a una terapia di supporto prima, durante o dopo quella contro il tumore.
La terapia di supporto è in grado di prevenire o combattere le infezioni, di tenere sotto controllo il dolore e gli altri sintomi, di alleviare gli effetti collaterali della terapia antitumorale e di aiutarvi ad affrontare le ricadute psicologiche della diagnosi di tumore. Potete sottoporvi a una terapia di supporto per prevenire o affrontare questi problemi, in modo da migliorare la qualità della vita durante la terapia contro il tumore.
- Infezioni. I pazienti affetti da leucemia sono estremamente vulnerabili alle infezioni, quindi devono essere curati con antibiotici e farmaci di altro tipo. Alcuni si fanno vaccinare contro l’influenza e la polmonite. L’équipe che vi segue può consigliarvi di evitare i luoghi affollati e le persone affette da raffreddore e da altri disturbi contagiosi. Se l’infezione vi colpisce può essere molto grave e dovrebbe essere curata il prima possibile. Può essere necessario il ricovero in ospedale.
- Anemia e sanguinamento. L’anemia e il sanguinamento sono gli altri due problemi per cui spesso si rivela necessaria la terapia di supporto. È probabile che il paziente si debba sottoporre a una trasfusione di globuli rossi o di piastrine. Le trasfusioni sono utili per curare l’anemia e fanno diminuire il rischio di emorragie gravi.
- Problemi dentali. La leucemia e la chemioterapia possono aumentare la sensibilità della bocca, favorire le infezioni e il sanguinamento nel cavo orale. I medici spesso consigliano ai pazienti di fare una visita dentistica completa e, se possibile, di curare i problemi ai denti prima dell’inizio della chemioterapia. Il dentista vi insegnerà le pratiche di igiene dentale necessarie durante la terapia.
Alimentazione e attività fisica
È fondamentale prendersi cura di se stessi seguendo un’alimentazione sana e cercando di mantenersi il più attivi possibile.
Per mantenere un peso corretto è necessario assumere la giusta quantità di calorie, è anche importante assumere proteine a sufficienza per salvaguardare la propria forza. Mangiare bene vi aiuterà a sentirvi meglio e ad avere maggiori energie.
In alcuni casi, soprattutto durante la terapia o nelle fasi immediatamente successive, potreste non aver voglia di mangiare, perché vi sentite stanchi o avete la nausea. Probabilmente avrete la sensazione che gli alimenti abbiano un gusto diverso dal solito ed inoltre gli effetti collaterali della terapia (ad esempio la mancanza di appetito, la nausea, il vomito o le ulcere in bocca) potranno impedirvi di mangiare bene. Il medico, il dietologo o altri componenti dell’équipe che vi segue possono suggerirvi i modi migliori per affrontare questi problemi.
Molte persone affermano di sentirsi meglio se riescono a mantenersi attive. Camminare, fare yoga, nuotare o fare altre attività vi aiuteranno a salvaguardare la forza e ad aumentare le energie. Con l’esercizio fisico si può diminuire la nausea e il dolore e si può sopportare meglio la terapia e lo stress. Prima di iniziare una qualsiasi attività fisica ricordatevi di chiedere il parere del medico; inoltre, se l’attività causa dolore o altri problemi, informate immediatamente il medico o l’infermiere.
Per approfondire, leggi:
- Leucemia acuta e cronica: cause, tipi, sopravvivenza e cura
- Leucemia linfoblastica acuta: sopravvivenza, guarigione, aspettativa di vita
- Leucemia linfoblastica acuta a cellule B: cause, diagnosi, sopravvivenza
- Leucemia indifferenziata acuta: cause, diagnosi, cure, sopravvivenza
- Leucemia mieloide acuta: sopravvivenza, guarigione, aspettativa di vita
- Leucemia promielocitica acuta: recidiva, diagnosi, ad alto rischio, cura
- Leucemia linfatica cronica: sintomi, sopravvivenza, guarigione
- Leucemia mieloide cronica: sintomi, emocromo, terapia, sopravvivenza
- Leucemia aleucemica (pseudoleucemia) mieloide e linfatica
- Leucemia a cellule capellute: sopravvivenza, guarigione, cure
Leggi anche:
- Emocromo: guida completa a tutti i valori del sangue normali e patologici
- Emocromo: valori di riferimento e significato clinico [SCHEMA]
- Ematocrito (HCT): basso, alto, in gravidanza, valori normali e interpretazione
- Indici corpuscolari MCV, MCH, MCHC, RDW: cosa sono ed a che servono
- Volume corpuscolare medio (MCV): alto, basso, valori normali e significato
- MCH alto, basso, valori normali ed interpretazione
- MCHC alto, basso, valori normali ed interpretazione
- RDW alto, basso, valori normali ed interpretazione
- Ormoni tiroidei: differenza T3 e T4, valori normali e patologici
- TSH alto, basso e valori normali: qual è il significato clinico?
- Tireoglobulina alta, bassa, valori normali ed interpretazione
- Globuli rossi (eritrociti) alti, bassi, valori normali e interpretazione
- Emoglobina bassa, alta, cause e valori normali
- Emoglobina nelle urine (emoglobinuria): cause, sintomi e terapia
- Differenza tra anemia ed anemia mediterranea (talassemia)
- Differenza tra anemia e leucemia
- Perché la mononucleosi è chiamata anche “malattia del bacio”?
- Differenza tra emoglobina fetale ed adulta
- Differenza tra emoglobina, ferro, ferritina e transferrina
- Differenza tra emoglobina e globuli rossi
- Differenza tra emocromo ed ematocrito
- Testosterone basso, alto, valori normali ed interpretazione
- Ormone follicolo stimolante (FSH) alto, basso, valori normali e significato
- Anemia da carenza di ferro: cause, sintomi e cure
- Diagnosi di laboratorio di anemia da carenza di ferro
- Aumentare il ferro in modo naturale, specie in gravidanza
- Emocromo completo con formula leucocitaria: valori, interpretazione e significato
- Differenza tra globuli rossi, bianchi e piastrine
- VES alta o bassa: cause, sintomi e valori normali della velocità di eritrosedimentazione
- Esame delle urine completo con urinocoltura: come fare e capire i risultati
- Scura o chiara, liquida o schiumosa: la tua urina rivela la tua salute
- Glicemia alta o bassa: valori normali, che patologie indica e come si controlla nei diabetici
- Azotemia (Urea) alta o bassa: valori, cause, sintomi e cosa fare
- Insulina alta: cause, diabete, prediabete, valori normali e cure
- Differenze tra il diabete di tipo 1 e 2 (insulino dipendente e resistente)
- Emoglobina glicata alta, valori normali, IFCC e diabete
- Clearance della creatinina: alta o bassa, valori, calcolo e sintomi
- Colesterolo: cos’è ed a cosa serve?
- Colesterolo e uova: si o no? Tutta la verità scientifica
- Colesterolo: gli italiani non lo misurano e non fanno prevenzione
- Colesterolo e trigliceridi: valori normali, alti, bassi ed interpretazione
- Dieta per abbassare il colesterolo: cibi consigliati e da evitare
- Differenza tra colesterolo HDL “buono” e LDL “cattivo”
- Eccesso di colesterolo (ipercolesterolemia): perché è pericoloso?
- Fattore reumatoide alto o basso? Valori normali e Reuma test
- Tiroide: dove si trova, com’è fatta e quali funzioni svolge?
- Patologie della tiroide: possono far veramente ingrassare?
- Le tue feci dicono se sei in salute: con la Scala di Bristol impara ad interpretarle
- Parassiti e vermi nelle feci: sintomi e come eliminarli con farmaci e rimedi naturali
- Coprocoltura e antibiogramma: procedura e perché si eseguono
- Esame e raccolta delle feci: come si fa nel modo corretto ed a che serve
- Feci con sangue, muco, cibo: quando preoccuparsi?
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Assumi abbastanza vitamina D? I sintomi che indicano la sua carenza e i cibi che ne contengono in abbondanza
- Differenza tra tumore benigno, maligno, neoplasia, cancro e metastasi
- Cos’è un tumore? Perché viene il cancro? Quali sono le cause?
- Acido folico (vitamina B9): a cosa serve, in quali alimenti trovarlo e perché è importante prima e durante la gravidanza
- Beta carotene: cos’è, a cosa serve e in quali cibi lo trovo?
- Ecco come il nostro corpo ci segnala la carenza di vitamine
- Hai voglia di un cibo in particolare? E’ il tuo corpo che ti rivela le carenze nutrizionali che hai
- Di cosa è composto il sangue e quali sono le sue funzioni?
- Plasma e cellule (elementi corpuscolati) che compongono il sangue
- Plasma e suoi derivati (plasmaderivati)
- Gruppi sanguigni: cosa sono e quali sono compatibili tra loro
- Differenza tra sangue, plasma e siero
- Come si ottiene il plasma?
- Plasmaferesi e donazione di sangue
- Plasma: a cosa serve e quali sono le sue funzioni?
- Differenza tra plasma liquido e secco
- Differenza tra siero e plasma
- Il plasma contiene fibrinogeno? Ed il siero?
- Come si separa il siero dal sangue?
- Qual è il volume totale del sangue (volemia) nel corpo umano?
- Da cosa viene prodotto il sangue nel corpo umano?
- Quanti litri di sangue abbiamo nel corpo?
- Quanto sangue si può donare in una sola volta?
- Ogni quanto tempo si può donare il sangue
- Quanto tempo serve per reintegrare il sangue dopo una donazione?
- Donare sangue: come fare con mestruazioni, pillola o gravidanza
- Condizioni e preparazione per donare il sangue: tutte le informazioni
- Quanto sangue possiamo perdere prima di morire dissanguati?
- Fibrinogeno: cos’è, a che serve, quali sono i suoi valori normali?
- Fibrinogeno alto o basso: valori normali ed interpretazione
- Fibrinogeno alto o basso in gravidanza: quando preoccuparsi?
- Proteggere la pelle dal freddo e prevenirne l’invecchiamento: l’importanza degli integratori di vitamine
- Hai dolori mestruali insopportabili? ti consiglio 10 formidabili rimedi naturali per alleviarli
- Dismenorrea: quando le mestruazioni sono dolorose
- Il ciclo influenza le prestazioni in palestra: il periodo migliore per allenarsi e gli esercizi da fare durante le mestruazioni
- Come alleviare i sintomi della Sindrome pre-mestruale?
- Farmaci per curare le mestruazioni dolorose e terapia non farmacologica
- Perché viene la diarrea prima e durante il ciclo mestruale e cure
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Assumi abbastanza vitamina D? I sintomi che indicano la sua carenza e i cibi che ne contengono in abbondanza
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Condividi questo articolo:
 L’epitopo (o determinante antigenico) è quella piccola parte di antigene che lega l’anticorpo specifico. La singola molecola di antigene può contenere diversi epitopi riconosciuti da anticorpi differenti.
L’epitopo (o determinante antigenico) è quella piccola parte di antigene che lega l’anticorpo specifico. La singola molecola di antigene può contenere diversi epitopi riconosciuti da anticorpi differenti.
 La leucemia è un tumore che si sviluppa nelle cellule del sangue; vengono comunemente distinte in acute e croniche, sulla base della velocità di progressione della malattia:
La leucemia è un tumore che si sviluppa nelle cellule del sangue; vengono comunemente distinte in acute e croniche, sulla base della velocità di progressione della malattia:
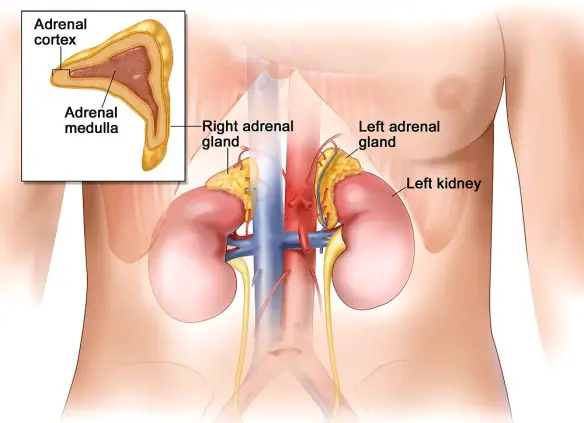 Il cortisolo è un ormone prodotto dalle ghiandole surrenali, più precisamente dalla zona fascicolata della loro porzione corticale. È un ormone di tipo steroideo, derivante cioè dal colesterolo, ed in particolare appartiene alla categoria dei glucocorticoidi, di cui fa parte anche il corticosterone (meno attivo).
Il cortisolo è un ormone prodotto dalle ghiandole surrenali, più precisamente dalla zona fascicolata della loro porzione corticale. È un ormone di tipo steroideo, derivante cioè dal colesterolo, ed in particolare appartiene alla categoria dei glucocorticoidi, di cui fa parte anche il corticosterone (meno attivo).
 In sintesi: anfotero si riferisce ad acidi e basi, anfipatico all’essere polare o apolare. Un esempio di molecola anfipatica è quella del sapone o dei fosfolipidi, mentre una molecola anfotera è quella dello ione bicarbonato.
In sintesi: anfotero si riferisce ad acidi e basi, anfipatico all’essere polare o apolare. Un esempio di molecola anfipatica è quella del sapone o dei fosfolipidi, mentre una molecola anfotera è quella dello ione bicarbonato. Il mieloma multiplo è un tumore che colpisce le plasmacellule, una componente molto importante del sistema immunitario. In particolare le plasmacellule sono il risultato della maturazione dei linfociti B che, assieme ai linfociti T, rappresentano le due principali tipologie cellulari coinvolte nella risposta immunitaria. Il ruolo delle plasmacellule, che si trovano soprattutto nel midollo osseo, è quello di produrre e liberare anticorpi per combattere le infezioni, ma in alcuni casi la loro crescita procede in maniera incontrollata dando origine al tumore.
Il mieloma multiplo è un tumore che colpisce le plasmacellule, una componente molto importante del sistema immunitario. In particolare le plasmacellule sono il risultato della maturazione dei linfociti B che, assieme ai linfociti T, rappresentano le due principali tipologie cellulari coinvolte nella risposta immunitaria. Il ruolo delle plasmacellule, che si trovano soprattutto nel midollo osseo, è quello di produrre e liberare anticorpi per combattere le infezioni, ma in alcuni casi la loro crescita procede in maniera incontrollata dando origine al tumore.