 L’elettrone è una particella subatomica con carica elettrica negativa che si ritiene essere una particella elementare; ruota attorno al nucleo dell’atomo costituito da protoni e neutroni. Gli elettroni, insieme ai protoni e ai neutroni, sono componenti degli atomi e, sebbene contribuiscano alla massa totale dell’atomo per meno dello 0,06%, ne caratterizzano sensibilmente la natura e ne determinano le proprietà chimiche: il legame chimico covalente si forma in seguito alla condivisione di elettroni tra due o più atomi. L’elettrone, come altre particelle di materia, è dotato di massa e carica elettrica, ha una velocità v (rispetto ad un sistema di riferimento) che non raggiunge mai la velocità della luce e possiede energia e quantità di moto (calcolabili a basse velocità per mezzo delle relazioni della fisica classica e ad alte velocità mediante la fisica relativistica).
L’elettrone è una particella subatomica con carica elettrica negativa che si ritiene essere una particella elementare; ruota attorno al nucleo dell’atomo costituito da protoni e neutroni. Gli elettroni, insieme ai protoni e ai neutroni, sono componenti degli atomi e, sebbene contribuiscano alla massa totale dell’atomo per meno dello 0,06%, ne caratterizzano sensibilmente la natura e ne determinano le proprietà chimiche: il legame chimico covalente si forma in seguito alla condivisione di elettroni tra due o più atomi. L’elettrone, come altre particelle di materia, è dotato di massa e carica elettrica, ha una velocità v (rispetto ad un sistema di riferimento) che non raggiunge mai la velocità della luce e possiede energia e quantità di moto (calcolabili a basse velocità per mezzo delle relazioni della fisica classica e ad alte velocità mediante la fisica relativistica).
Il fotone o quanto di energia, è una particella che che costituisce un’onda elettromagnetica ed al contrario dell’elettrone non possiede massa né carica elettrica, si muove in qualsiasi sistema di riferimento a velocità c, possiede energia e quantità di moto.
Il protone è una particella subatomica composta dotata di carica elettrica positiva, formata da due quark up e un quark down che sono detti di valenza, in quanto ne determinano quasi tutte le caratteristiche fisiche. Costituisce il nucleo assieme al neutrone, con il quale si trasforma continuamente mediante l’emissione e l’assorbimento di pioni.
Lo ione è un’entità molecolare elettricamente carica: si forma quando un atomo (o una molecola o un gruppo di atomi legati tra loro) cede o acquista uno o più elettroni si trasforma in uno ione, positivo (se ha perso l’elettrone) o negativo (se ne ha acquisito uno)
Leggi anche:
- Differenza tra orbita ed orbitale (in chimica ed astronomia)
- Differenza tra livello energetico ed orbitale
- Un atomo si può dividere? Cosa succede se si divide?
- Differenza tra atomo e molecola con esempi
- Differenza tra atomi e ioni e regola dell’ottetto
- Differenza tra atomo e elemento
- Differenza tra atomo e nucleo
- Differenza tra anfipatica ed anfotera
- Differenze tra H2O e H2S in chimica
- Cos’è la densità in chimica? Densità di acqua ed aria a varie temperature
- Massa e peso di un corpo sulla Luna rispetto alla Terra
- Differenza tra densità e concentrazione
- Differenze e punti in comune tra chimica e fisica
- Differenza tra fisica classica e quantistica
- Differenza tra fisica classica e meccanica quantistica
- Differenza tra microscopio ottico ed elettronico
- Differenza tra microscopio elettronico a scansione e a trasmissione
- Differenza tra raggi x e gamma
- Differenza tra stella, pianeta e satellite con esempi
- Differenza tra satellite naturale ed artificiale con esempi
- Differenza tra satellite artificiale scientifico ed applicativo
- Differenza tra pianeta e pianeta nano con esempi
- Differenza tra pianeta gioviano e terrestre con esempi
- Qual è la differenza fra meteoroide, meteora e meteorite?
- Differenza tra stella cadente e meteora
- In quali giorni dell’anno si possono vedere molte stelle cadenti?
- Differenza tra orbita e traiettoria
- Cos’è un anno luce ed a quanti km corrisponde?
- Differenza tra meteorite, asteroide e cometa con esempi
- Le distanze dell’universo, ovvero: bagliori di luce da una stella ormai scomparsa
- Un giorno sul pianeta Marte: quanto dura un Sol in astronomia?
- Samantha Cristoforetti e il vero simbolo del degrado italiano
- Andremo tutti a vivere su Kepler, il pianeta simile alla terra
- I 5 migliori libri da regalare ad un nerd
- Pale Blue Dot: la Terra vista dallo spazio è un granello nell’universo
- Teoria del Tempo Fantasma: 297 anni di storia non sono mai esistiti, ora siamo nel 1717
- Differenza tra raggi infrarossi, ultravioletti e visibili
- Quanto è grande il sole e quante volte è più grande di terra e luna?
- Come moriremmo se un mega asteroide colpisse la Terra?
- L’astronauta Luca Parmitano è stato proposto per tornare nello spazio nel 2019
- Samantha Cristoforetti astronauta da record mondiale: è la donna con la più grande permanenza consecutiva nello spazio!
- Entro dieci anni scopriremo forme di vita extraterrestri
- Cos’è la radiazione solare? Cosa sono i raggi ultravioletti? Che danni possono provocare alla nostra pelle?
- Prendere il sole fa bene alla salute del cuore: la vitamina D riduce il rischio di coronaropatia
- Differenza tra eclissi solare e lunare (spiegazione semplice)
- Differenza tra eclissi totale, parziale, anulare e penombrale
- Com’è fatta la tuta degli astronauti?
- Cos’è una galassia? Di cosa è fatta?
- L’iraniana Mirzakhani è la prima donna al mondo a ricevere il “Nobel” per la matematica
- Cos’è e dove si trova la Stella Polare? Come individuarla?
- Cos’è una eclissi lunare? Come e quando si verifica?
- Perché la notte di San Lorenzo cadono le stelle? Cos’è una stella cadente?
- Quante volte l’uomo è stato sulla Luna?
- Perché si verificano le maree?
- Perché la luna ci rivolge sempre la stessa faccia? Com’è il lato oscuro?
- Cos’è una eclissi solare? Come e quando si verifica?
- Quando inizia e finisce la primavera?
- Quando inizia e finisce l’estate?
- Quando inizia e finisce l’autunno?
- Quando inizia e finisce l’inverno?
- Vi spiego come far entrare sette miliardi di persone nello spazio di una palla da tennis
- Lorenzo il Magnifico: l’amore per la natura, gli animali e la prima giraffa in Italia
- Ciao Margherita!
- L’esperimento di Standford: la pazzia che colpisce chi indossa una divisa
- Donne italiane di cui andare orgogliosi
- Il mio professore era Albert Einstein
- Quante persone vivono a Roma, in Italia, in Europa e nel mondo?
- Differenza tra massa e peso in fisica ed in medicina
- La persona più intelligente al mondo mai esistita nella storia dell’uomo
- Jon Brower Minnoch: quanto è arrivato a pesare l’uomo più grasso del mondo?
- Il cardiochirurgo stremato dopo un trapianto cardiaco durato 23 ore
- Le 20 droghe più potenti e pericolose al mondo
- Il mio mito è invece Michel Petrucciani
- Il mio mito è invece Django Reinhardt
- Il mio mito è invece Albert Bruce Sabin
- Il mio mito è invece Giuseppe Moscati
- Il mio mito è invece Ignác Fülöp Semmelweis
- Il mio mito è invece Frederick Treves
- Differenza tra tuono, lampo, fulmine e saetta
- Calcolare la distanza di un temporale con il tempo tra lampo e tuono
- Differenza tra neve, grandine, ghiaccio, nevischio e pioggia
- Differenza tra temporale, pioggia, rovescio e tempesta
- Differenza tra neve artificiale e naturale: qual è la migliore per sciare?
- Differenze tra i vari tipi di neve
- Differenza tra tornado, tromba d’aria, uragano, ciclone e tifone
- Neve: cos’è, come si forma, come si verifica la neve sopra i 2 °C
- Tempesta: come si forma, tipi e classificazione
- Pioggia: come si forma, perché cade e quanti tipi esistono?
- Da cosa sono formate le nuvole e come si creano? Perché piove? Cos’è la grandine e come si forma?
- Quasi 70 gradi sotto zero: il villaggio più freddo al mondo
- Il profumo della pioggia e della natura
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

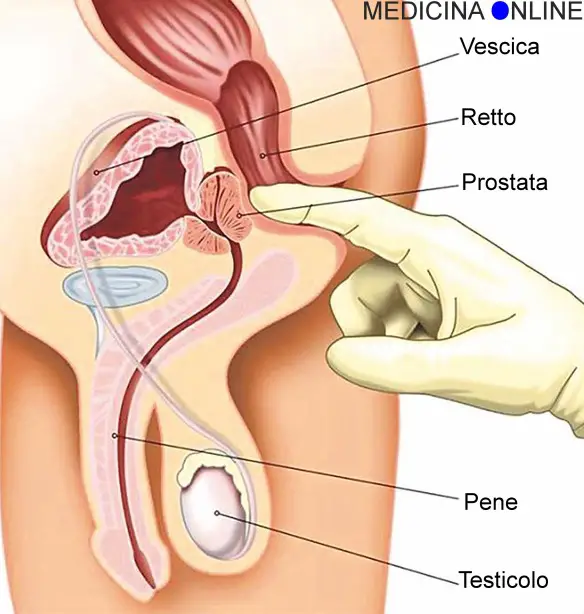 C’è un’idea abbastanza diffusa (perché istintiva): più controllo la mia salute, più sarò al sicuro da malattie. Quest’idea, semplice e banale, si è diffusa dovunque, soprattutto negli strati della popolazione più attenti alla propria salute ed ovviamente, dove c’è una richiesta, si crea subito un’offerta. I servizi di controllo delle malattie sono aumentati, ambulatori e centri privati, esami del sangue e di altro tipo che controllano tutti gli organi, test che si possono fare anche a casa. Sembra così evidente che mettere in discussione una cosa del genere crea imbarazzo.
C’è un’idea abbastanza diffusa (perché istintiva): più controllo la mia salute, più sarò al sicuro da malattie. Quest’idea, semplice e banale, si è diffusa dovunque, soprattutto negli strati della popolazione più attenti alla propria salute ed ovviamente, dove c’è una richiesta, si crea subito un’offerta. I servizi di controllo delle malattie sono aumentati, ambulatori e centri privati, esami del sangue e di altro tipo che controllano tutti gli organi, test che si possono fare anche a casa. Sembra così evidente che mettere in discussione una cosa del genere crea imbarazzo.
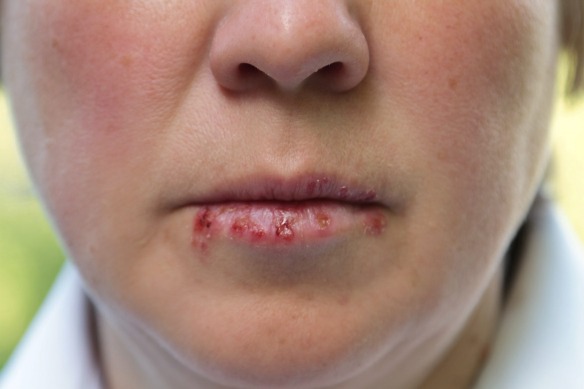 Oltre ad essere pruriginoso e doloroso, l’herpes labiale (più comunemente conosciuto come “febbre delle labbra”) può procurare disagio. Alcuni trattamenti, se impiegati alle prime avvisaglie di un focolaio, contribuiscono a ridurre la durata dell’infezione. Altri, invece, possono alleviare i sintomi. Nel corso dell’articolo, spiegheremo come riconoscere un focolaio di herpes labiale, come prevenirne la comparsa e in che modo curare questa spiacevole infezione.
Oltre ad essere pruriginoso e doloroso, l’herpes labiale (più comunemente conosciuto come “febbre delle labbra”) può procurare disagio. Alcuni trattamenti, se impiegati alle prime avvisaglie di un focolaio, contribuiscono a ridurre la durata dell’infezione. Altri, invece, possono alleviare i sintomi. Nel corso dell’articolo, spiegheremo come riconoscere un focolaio di herpes labiale, come prevenirne la comparsa e in che modo curare questa spiacevole infezione. Per capire a fondo quello di cui stiamo parlando, ti consiglio di leggere prima questo mio articolo:
Per capire a fondo quello di cui stiamo parlando, ti consiglio di leggere prima questo mio articolo:  Per comprendere appieno quello di cui stiamo parlando, vi consiglio di leggere prima questo mio articolo:
Per comprendere appieno quello di cui stiamo parlando, vi consiglio di leggere prima questo mio articolo: 
 Per comprendere meglio quello di cui stiamo parlando, ti consiglio di leggere prima questo mio articolo:
Per comprendere meglio quello di cui stiamo parlando, ti consiglio di leggere prima questo mio articolo: