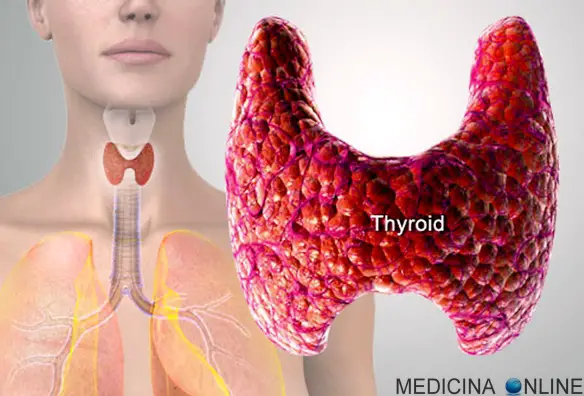
 L’ipotiroidismo è una patologia causata dalla mancata capacità della tiroide di sintetizzare una adeguata quantità di ormoni. Più raramente, può sussistere una resistenza all’azione dei suddetti ormoni a livello tissutale. L’ipotiroidismo può presentarsi sin dalla nascita (cretinismo) o comparire in età adulta, specie nelle donne ultracinquantenni. Può essere primario (congenito o acquisito), secondario o terziario. Da un punto di vista clinico-laboratoristico si possono distinguere:
L’ipotiroidismo è una patologia causata dalla mancata capacità della tiroide di sintetizzare una adeguata quantità di ormoni. Più raramente, può sussistere una resistenza all’azione dei suddetti ormoni a livello tissutale. L’ipotiroidismo può presentarsi sin dalla nascita (cretinismo) o comparire in età adulta, specie nelle donne ultracinquantenni. Può essere primario (congenito o acquisito), secondario o terziario. Da un punto di vista clinico-laboratoristico si possono distinguere:
- ipotiroidismo subclinico: caratterizzato da un’elevata concentrazione sierica di TSH in presenza di normali valori di FT3 e FT4 con sfumati o assenti segni e sintomi di ipotiroidismo;
- ipotiroidismo conclamato: caratterizzato da un’elevata concentrazione sierica di TSH in presenza di bassi livelli di FT3 e FT4 con chiari segni e sintomi di ipotiroidismo.
Leggi anche: Differenza tra Eutirox e Ibsa nella cura dell’ipotiroidismo
Epidemiologia
Si calcola che l’ipotiroidismo colpisca in media lo 0,5-1% della popolazione, con una netta prevalenza nel sesso femminile.
Cause di ipotiroidismo
Varie e numerose sono le cause in grado di determinare questo quadro morboso. L’ipotiroidismo può essere determinato – ad esempio – dall’assenza congenita della tiroide o da un suo sviluppo incompleto, per alterazioni anatomiche, per una sua asportazione chirurgica, per l’assunzione di farmaci antitiroidei o di iodio radioattivo. Come già accennato, le varie forme di ipotiroidismo vengono classificate in primarie (o primitive), secondarie e terziarie. Nel primo gruppo rientrano tutte quelle malattie dipendenti dalla ridotta funzionalità del tessuto tiroideo, mentre si parla di ipotiroidismo secondario e terziario quando le patologie sono a carico, rispettivamente, di ipofisi ed ipotalamo. Alcuni degli ormoni secreti da queste due strutture sono infatti capaci di regolare pesantemente l’attività della tiroide. Nella maggior parte dei casi, l’ipotiroidismo primario è associato a malattie autoimmunitarie della tiroide (la più comune delle quali è la tiroidite cronica di Hashimoto), oppure a gravi carenze di iodio nella dieta o a cause iatrogene (uso – abuso di determinati farmaci).
Ipotiroidismo dovuto a bassi livelli di iodio
Lo iodio è un minerale essenziale per la normale funzionalità della tiroide; se manca lo iodio la ghiandola non può sintetizzare i suoi ormoni ed insorge ipotiroidismo. Fortunatamente l’organismo possiede buone riserve sia di iodio che di ormoni tiroidei, sufficienti per circa 60-90 giorni, ed il semplice consumo di sale iodato basta per allontanare il rischio di carenze specifiche. Esistono tuttavia alcune aree del Pianeta in cui la carenza cronica di iodio nell’alimentazione provoca ipotiroidismo. A causa delle basse concentrazioni plasmatiche di ormoni tiroidei, la sintesi dell’ormone stimolante la tiroide o TSH viene sensibilmente accelerata. Questa ipersecrezione ha lo scopo di stimolare al massimo la ghiandola che, tuttavia, non riesce a sintetizzare i suoi ormoni perché non dispone di adeguate quantità di iodio. Si entra così in un circolo vizioso in cui l’iperstimolazione determina un vistoso ingrossamento della tiroide (gozzo).
Leggi anche: Il sale iodato è importante per prevenire le malattie della tiroide: in quali alimenti trovarlo?
Sintomi e segni dell’ipotiroidismo
Le conseguenze dell’ipotiroidismo variano in base allo stadio evolutivo durante il quale insorgono. Nella vita fetale si verificano gravi ed irreversibili alterazioni dello sviluppo corporeo e cerebrale. Anche nel bambino si possono verificare permanenti alterazioni dello sviluppo somatico ed intellettivo (gli ormoni tiroidei sono essenziali per la completa espressione dell’ormone della crescita). Si osserva inoltre un ritardo nello sviluppo sessuale.
Quando insorge in età adulta, l’ipotiroidismo si manifesta attraverso alcuni sintomi caratteristici:
1) Cute secca e capelli radi, sottili, affaticamento fisico e debolezza muscolare cronica (l’ipotiroidismo determina una riduzione della sintesi proteica).
2) L’espressione del viso, caratterizzata da zone palpebrali gonfie e rime ristrette, capelli e sopracciglia scarsi, bocca semiaperta che lascia intravedere una lingua ingrossata, conferisce al volto del paziente l’aspetto inconfondibile e poco intelligente della “facies mixedematosa“; anche i tessuti sottocutanei sono caratterizzati dal cosiddetto mixedema, su cui la pressione delle dita non lascia il segno della fovea. L’ipotiroidismo determina infatti un accumulo cutaneo di mucopolisaccaridi che richiamano acqua determinando questo tipico aspetto.
3) Cute fredda e intolleranza alle basse temperature: una diminuzione degli ormoni tiroidei rallenta il metabolismo e il consumo di ossigeno; viene meno anche la loro attività termogenica.
4) Sonnolenza (letargia) che può arrivare fino al coma, depressione, rallentamento dei processi ideativi e sensazione di stanchezza; questi sintomi insorgono a causa delle alterazioni nervose indotte dall’ipotiroidismo.
5) Altri sintomi: costipazione, aumento del peso corporeo, pallore e anemia, raucedine ed abbassamento del tono della voce, diminuzione dell’udito e della memoria, diminuzione della fertilità, flussi mestruali abbondanti (menorragia), crampi, bradicardia e riduzione della forza contrattile del cuore, vasocostrizione, aumento dei livelli di lipoproteine a bassa densità (LDL) e trigliceridi nel siero, con conseguente e sensibile aumento del rischio di malattia coronarica.
C’è spesso ipercarotenemia, particolarmente evidente alle mani ed alle piante dei piedi, a causa del deposito di carotene negli strati epidermici ricchi di lipidi. Il deposito di sostanze proteinacee nella lingua può produrre macroglossia. La riduzione sia degli ormoni tiroidei sia della stimolazione adrenergica provoca bradicardia. Il cuore può essere ingrandito, in parte a causa di dilatazione, ma principalmente per l’accumulo di un versamento sieroso ad alto contenuto proteico nel sacco pericardico. Si possono rilevare versamenti pleurici o peritoneali. I versamenti pleurici e pericardici si sviluppano lentamente e solo raramente provocano difficoltà respiratorie o emodinamiche. I pazienti generalmente accusano stipsi, che può essere grave. Sono comuni le parestesie delle mani e dei piedi, spesso dovute alla sindrome del tunnel carpale-tarsale causata dal deposito di una sostanza amorfa proteinacea nei legamenti intorno al polso e alla caviglia, con conseguente compressione dei nervi. I riflessi possono essere di grande aiuto dal punto di vista diagnostico, a causa della vivacità di contrazione e della lentezza dei tempi di rilassamento. Le donne con ipotiroidismo manifestano spesso menorragia, in contrasto con l’ipomenorrea dell’ipertiroidismo. Si osserva frequentemente ipotermia. Spesso è presente anemia, di solito normocromica normocitica e a eziologia sconosciuta, ma essa può essere ipocromica a causa della menorragia e talvolta macrocitica a causa dell’associata anemia perniciosa o del ridotto assorbimento di acido folico. In genere, l’anemia è raramente grave (Hb > 9 g/dl). Essa recede con la correzione dello stato ipometabolico, richiedendo talvolta da 6 a 9 mesi. Quando è primitivo, dovuto cioè a malattie della tiroide, l’ipotiroidismo nell’adulto è caratterizzato da un esordio lento e molto graduale che può pertanto sfuggire a lungo agli occhi del medico e dello stesso paziente.
Leggi anche: Nodulo Tiroideo: sintomi e cure
Diagnosi di ipotiroidismo
La conferma di ipotiroidismo avviene generalmente attraverso un semplice esame del sangue, tramite il quale si andranno a valutare vari parametri tra cui i livelli ormonali del paziente. È importante distinguere l’ipotiroidismo secondario da quello primitivo; anche se l’ipotiroidismo secondario non è frequente, spesso coinvolge altri organi endocrini sotto il controllo dell’asse ipotalamo-ipofisario. In una donna con ipotiroidismo, gli indizi che orientano verso l’ipotiroidismo secondario sono una storia di amenorrea piuttosto che di menorragia e alcune differenze indicative all’esame obiettivo. Nell’ipotiroidismo secondario la cute e i capelli sono secchi, ma non altrettanto ruvidi; spesso si osserva depigmentazione cutanea; la macroglossia non è così pronunciata; le mammelle sono atrofiche; il cuore è piccolo, senza accumulo di versamenti sierosi nel sacco pericardico; la PA è bassa e spesso si rileva ipoglicemia a causa della concomitante insufficienza corticosurrenalica o del deficit di ormone della crescita.
Le indagini di laboratorio dimostrano nell’ipotiroidismo secondario la presenza di un basso livello di TSH circolante (benché il TSH sierico possa essere normale alla misurazione con tecniche immunologiche, ma abbia ridotta attività biologica), mentre nell’ipotiroidismo primario (o primitivo) manca la retroinibizione sull’ipofisi normale e i livelli sierici di TSH sono elevati. Il dosaggio del TSH sierico è l’esame più semplice e più sensibile per la diagnosi di ipotiroidismo primitivo. In quest’ultimo il colesterolo sierico è generalmente elevato, mentre lo è meno in quello secondario. Altri ormoni ipofisari e i corrispondenti ormoni dei loro tessuti bersaglio possono essere diminuiti nell’ipotiroidismo secondario.
Il test al TRH può essere utile ai fini della distinzione tra ipotiroidismo secondario a un’insufficienza ipofisaria e ipotiroidismo dovuto a insufficienza ipotalamica. In quest’ultimo, viene rilasciato TSH in risposta al TRH.
La determinazione dei livelli sierici totali di T3 nell’ipotiroidismo merita una menzione. Oltre all’ipotiroidismo primitivo e a quello secondario, altre condizioni sono caratterizzate dalla riduzione dei livelli circolanti di T3 totale; esse comprendono la riduzione della TBG sierica, gli effetti di alcuni farmaci e della euthyroid sick syndrome dovuta a patologie acute e croniche, l’inanizione e le diete povere di carboidrati. Nell’ipotiroidismo di gravità maggiore, sono diminuiti i livelli sierici sia di T3 sia di T4. Tuttavia, molti pazienti con ipotiroidismo primitivo (elevato TSH sierico, basso livello sierico di T4) possono avere normali livelli circolanti di T3, probabilmente a causa della prolungata stimolazione da parte del TSH sulla tiroide insufficiente, che determina la sintesi e la secrezione preferenziale dell’ormone biologicamente attivo T3.
Per approfondire i vari strumenti usati nella diagnosi, leggi anche:
- Ormoni tiroidei: differenza T3 e T4, valori normali e patologici
- TSH alto, basso e valori normali: qual è il significato clinico?
- Tireoglobulina alta, bassa, valori normali ed interpretazione
- Esame obiettivo del collo: palpazione della tiroide, video e spiegazione
- Ecografia della tiroide: a cosa serve, come si svolge e come ci si prepara all’esame
- Scintigrafia tiroidea: risultati, captazione, noduli, costo
- Agoaspirato tiroideo: esito, complicanze, dolore, referto, prezzo
Terapie
La terapia dell’ipotiroidismo si basa sul recupero e sul mantenimento della funzionalità tiroidea, che avviene tramite la somministrazione sostitutiva di tiroxina (T4) per via orale. E’ inoltre necessaria una modificazione dietetica per evitare la costipazione. In caso di accertato ipotiroidismo è buona regola seguire un immediato percorso terapeutico; anche nell’evenienza di patologia presunta, è consigliabile richiedere un consulto medico, per evitare che i sintomi peggiorino nel tempo. L’ipotiroidismo, rispetto alla patologia opposta (l’ipertiroidismo) è assai più semplice da curare e controllare, grazie all’ausilio di farmaci di sintesi appropriati, la cui posologia dev’essere sempre stabilita dal medico, ed eventualmente modulata durante il corso della malattia.
Utile è trattare anche i sintomi secondari derivati dall’ipotiroidismo, come ad esempio l’anemia. La correzione delle abitudini alimentari non solo è utile per affrontare meglio la terapia, ma è necessaria per evitare stipsi, che spesso accompagna chi è affetto da ipotiroidismo.
Nell’evenienza di ipotiroidismo neonatale, è doveroso intervenire prontamente per indurre uno sviluppo fisiologico; sembra determinante la somministrazione di ormoni T3 e T4 già dai primissimi stadi di sviluppo dell’embrione. Il futuro bambino dovrà assumere per tutta la vita ormoni tiroidei, prestando particolare attenzione anche agli alimenti. Da qui di comprende come sia imprescindibile la terapia sostitutiva nelle donne in gravidanza affette da ipotiroidismo.
Leggi anche: Vuoi bruciare più calorie? Fai esplodere il tuo metabolismo!
Farmaci per trattare l’ipotiroidismo
Levotiroxina sodica (es. Eutirox, Syntroxine, Tiracrin, Tirosint): questo farmaco è largamente impiegato in terapia per l’ipotiroidismo, oltre a rappresentare il farmaco d’elezione per la cura della tiroidite di Hashimoto. La posologia, sempre accuratamente stabilita dal medico curante, può essere modificata da paziente a paziente, in base ai livelli di ormoni tiroidei nel sangue, al livello di TSH e alla risposta del paziente alla terapia. Indicativamente, il farmaco dev’essere somministrato per bocca alla posologia di 12,5-50 mcg/dì. È possibile incrementare la dose fino a 12,5-50 mcg al dì, ogni 1-2 settimane, nel pieno rispetto delle indicazioni stabilite dal medico. Nei bambini e negli anziani, la dose viene generalmente modificata dopo un intervallo di tempo maggiore (ogni 3-6 settimane). Non superare i 200 mcg. Qualora fosse necessaria un’assunzione parenterale (diversa dalla via orale), la dose del farmaco scende del 50-75% rispetto alla somministrazione del farmaco per os. Alcuni farmaci/alimenti possono incidere pesantemente sull’assorbimento di tale sostanza: sucralfato, integratori di calcio (es. Calcio Carbonato), integratori di ferro, CCColestiramina (es. Questran), idrossido di alluminio.
Per approfondire, leggi anche:
Liotironina sodica (es. Liotir, Titre): si tratta di un farmaco molto simile al precedente, dal punto di vista terapeutico, ma la molecola tende ad essere metabolizzata più velocemente dall’organismo: l’effetto terapeutico, pertanto, si manifesta dopo alcune ore ma svanisce entro 1-2 gg dal termine del trattamento. Si raccomanda di iniziare la somministrazione del farmaco alla posologia di 25 mcg, da assumere per via orale una volta ogni 24 ore. La dose può essere aumentata di 25 mcg ogni 7-14 gg, sotto la supervisione del medico. La dose di mantenimento generalmente varia da 25 a 75 mcg al dì. Non interrompere la terapia, anche in assenza dei tipici sintomi dell’ipotiroidismo.
Coma mixedematoso: sintomi, diagnosi e trattamento
Il coma mixedematoso è una complicanza dell’ipotiroidismo potenzialmente letale. Le sue caratteristiche comprendono un ipotiroidismo di fondo di lunga durata, uno stato di coma con ipotermia estrema (temperature da 24 a 32,2°C [da 75,2 a 90°F]), areflessia, convulsioni, ritenzione di CO2 e depressione respiratoria. L’ipotermia grave può non essere riconosciuta, a meno che non vengano impiegati termometri speciali con scala di lettura per le basse temperature. È imperativo porre la diagnosi rapidamente basandosi sul giudizio clinico, sull’anamnesi e sull’esame obiettivo, perché c’è la probabilità di un decesso precoce. I fattori precipitanti comprendono l’esposizione al freddo, le malattie, le infezioni, i traumi e i farmaci che deprimono il SNC. Il coma mixedematoso viene trattato con un’alta dose iniziale di T4 (da 200 a 500 mg EV) o di T3 (40 mg EV). La dose di mantenimento per la T4 va da 50 a 100 mg/die EV, e per la T3 da 10 a 20 mg/ die EV, fino a quando non si può somministrare T4 per via orale. Vengono somministrati anche corticosteroidi, perché inizialmente non può essere esclusa la possibilità di un ipotiroidismo di natura centrale. Il paziente non deve essere riscaldato rapidamente, per evitare il pericolo di aritmie cardiache. L’ipossiemia è comune, perciò all’inizio del trattamento deve essere misurata la Pao2. Se la ventilazione alveolare è compromessa, è necessaria l’assistenza ventilatoria meccanica immediata. La malattia precipitante deve essere prontamente e appropriatamente trattata, e la reintegrazione idrica condotta con prudenza, perché i pazienti ipotiroidei non eliminano l’acqua in maniera adeguata. Infine, tutti i farmaci devono essere somministrati con cautela poiché, vengono metabolizzati più lentamente di quanto avviene nelle persone normali.
Consigli dietetici
Ecco alcuni consigli per il paziente ipotiroideo:
- preferire cibi ricchi di iodio: pesce marino, molluschi, alghe brune, latte vaccino, uova;
- insaporire gli alimenti con sale iodato;
- seguire una dieta equilibrata in fibre, utile per contrastare la stipsi che spesso accompagna l’ipotiroidismo;
- l’assunzione di broccoli, cavolfiori, semi di lino, rape e ravanelli sembra incrementare il fabbisogno di iodio, pertanto il consumo di questi alimenti, nel contesto di ipotiroidismo accertato o presunto, dev’essere moderato.
Leggi anche:
- Differenza tra ipotiroidismo, ipertiroidismo, eutiroidismo e distiroidismo
- Differenza tra ipotiroidismo primario, secondario e terziario
- Tiroide e obesità: qual è il vero legame?
- Tiroide: anatomia, funzioni e patologie in sintesi
- Non mangio eppure ingrasso, e se fosse ipotiroidismo?
- Dimagrire scientificamente: scopri i fattori che aumentano o rallentano il tuo metabolismo
- Differenza tra ipotiroidismo e tiroidite
- Differenza tra ipotiroidismo e tiroidite di Hashimoto
- Differenza tra ipotiroidismo clinico e subclinico
- Tiroide, tumori in crescita a causa dell’inquinamento
- Ipertiroidismo: cause, cura, valori diagnosi, sintomi iniziali, conseguenze
- Ipertiroidismo nell’uomo: sintomi, conseguenze sulla libido, cure
- Morbo di Basedow: alimentazione, cura, occhi, si guarisce, rimedi
- Gozzo tiroideo: semplice, tossico, endemico, rimedi, intervento, immagini
- Gozzo tossico nodulare e multinodulare: sintomi, diagnosi e cura
- Alimenti gozzigeni (antitiroidei) vietati nelle alterazioni tiroidee
- Morbo di Plummer (adenoma tossico): sintomi, diagnosi e terapia
- Adenoma tiroideo: sintomi, diagnosi e trattamento
- Tireotossicosi autoimmune, iatrogena, factitia, valori, cura
- Tiroidite acuta, cronica, autoimmune: sintomi e conseguenze
- Tiroidite di Hashimoto: esami, cura, conseguenze, dieta, guarire
- Tiroidite di De Quervain (subacuta): sintomi, dieta, si guarisce, è contagiosa?
- Tiroidite post partum: sintomi, fasi, diagnosi, cura e rischi
- Devo sottopormi ad una tiroidectomia: perchè farla, cosa mi succederà in sala operatoria e come mi sentirò dopo l’intervento?
- Terapia radiometabolica dell’ipertiroidismo con radioiodio: indicazioni ed effetti collaterali
- Differenza tra tiroide e paratiroide
- Paratiroidectomia: intervento, convalescenza e conseguenze
- Aloe Vera per riattivare il metabolismo, dimagrire e combattere la cellulite
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Condividi questo articolo:
 Gli energy drink potrebbero portare al diabete: è quanto è risultato da uno studio dell’Università di Calgary presentato al Congresso Mondiale sul diabete. Secondo i ricercatori, le bevande a base di caffeina alzano i livelli di insulina e glucosio nel sangue del 30%. La combinazione di zucchero e caffeina alza l’insulina e il glucosio nel sangue ed è difficile riportarli a livelli normali; la caffeina rimane in circolo per 4-6 ore dopo l’assunzione.
Gli energy drink potrebbero portare al diabete: è quanto è risultato da uno studio dell’Università di Calgary presentato al Congresso Mondiale sul diabete. Secondo i ricercatori, le bevande a base di caffeina alzano i livelli di insulina e glucosio nel sangue del 30%. La combinazione di zucchero e caffeina alza l’insulina e il glucosio nel sangue ed è difficile riportarli a livelli normali; la caffeina rimane in circolo per 4-6 ore dopo l’assunzione.
 Mettersi a dieta non è roba per uomini, stando almeno ad alcuni ricercatori danesi, secondo i quali il sesso forte corre di più il rischio di morire di diabete perché si ritene ‘troppo macho‘ per seguire un regime alimentare. Alle donne, invece, meno restie a tagliare le calorie, andrebbe meglio. Lo studio, condotto da un gruppo di ricercatori e riportato dal ‘Daily Mail’, ha evidenziato che le donne che invece seguono una dieta e fanno esercizio fisico sono meno propense ad ammalarsi di malattie legate al diabete.
Mettersi a dieta non è roba per uomini, stando almeno ad alcuni ricercatori danesi, secondo i quali il sesso forte corre di più il rischio di morire di diabete perché si ritene ‘troppo macho‘ per seguire un regime alimentare. Alle donne, invece, meno restie a tagliare le calorie, andrebbe meglio. Lo studio, condotto da un gruppo di ricercatori e riportato dal ‘Daily Mail’, ha evidenziato che le donne che invece seguono una dieta e fanno esercizio fisico sono meno propense ad ammalarsi di malattie legate al diabete. Il dott. Michele Carruba, del Centro studi e ricerche sull’obesità dell’università degli studi di Milano, oggi all’Expo, ha dichiarato: “In Italia abbiamo il triste primato di avere i bambini più grassi d’Europa, con il 24% sovrappeso e il 12% obeso (e siamo secondi al mondo dopo gli Stati Uniti). Questo perché stiamo perdendo la nostra tradizione alimentare mediterranea. Con l’industrializzazione e la tecnologia le persone continuano a mangiare la stessa quantità di cibo da un punto di vista quantitativo, ma non si muovono più e quindi non bruciano energia”. In Italia è obeso il 10% della popolazione, cui si deve aggiungere un altro 46% di persone in sovrappeso. L’obesità è un importante fattore di rischio per il diabete e le malattie cardiavascolari, principali causa di morte nei Paesi occidentali.
Il dott. Michele Carruba, del Centro studi e ricerche sull’obesità dell’università degli studi di Milano, oggi all’Expo, ha dichiarato: “In Italia abbiamo il triste primato di avere i bambini più grassi d’Europa, con il 24% sovrappeso e il 12% obeso (e siamo secondi al mondo dopo gli Stati Uniti). Questo perché stiamo perdendo la nostra tradizione alimentare mediterranea. Con l’industrializzazione e la tecnologia le persone continuano a mangiare la stessa quantità di cibo da un punto di vista quantitativo, ma non si muovono più e quindi non bruciano energia”. In Italia è obeso il 10% della popolazione, cui si deve aggiungere un altro 46% di persone in sovrappeso. L’obesità è un importante fattore di rischio per il diabete e le malattie cardiavascolari, principali causa di morte nei Paesi occidentali. Concedersi un pisolino troppo lungo può aumentare moltiplicare il rischio di diabete di tipo 2. E’ ciò che si desume da uno studio presentato al Congresso dell’Associazione europea per lo studio di diabete (Easd), Stoccolma. Se il pisolino supera la durata di un’ora il pericolo di ammalarsi aumenta del 46%. La cosa migliore è dormire al massimo 40 minuti: solo superando questa soglia il pericolo di diabete cresce. La ricerca è stata condotta dal giapponese Tomohide Yamada dell’università di Tokyo ed è in realtà una meta-analisi di oltre 680 studi sul tema pubblicati fino al novembre 2014 e inseriti nei database di Medline, Cochrane Library e Web of Sciences condotti tra Europa, Asia e Usa, coinvolgevano complessivamente più di 260 mila persone. Le ragioni di questo legame sono ancora sconosciute.
Concedersi un pisolino troppo lungo può aumentare moltiplicare il rischio di diabete di tipo 2. E’ ciò che si desume da uno studio presentato al Congresso dell’Associazione europea per lo studio di diabete (Easd), Stoccolma. Se il pisolino supera la durata di un’ora il pericolo di ammalarsi aumenta del 46%. La cosa migliore è dormire al massimo 40 minuti: solo superando questa soglia il pericolo di diabete cresce. La ricerca è stata condotta dal giapponese Tomohide Yamada dell’università di Tokyo ed è in realtà una meta-analisi di oltre 680 studi sul tema pubblicati fino al novembre 2014 e inseriti nei database di Medline, Cochrane Library e Web of Sciences condotti tra Europa, Asia e Usa, coinvolgevano complessivamente più di 260 mila persone. Le ragioni di questo legame sono ancora sconosciute.
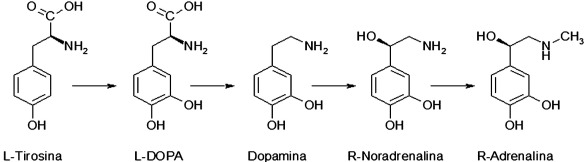
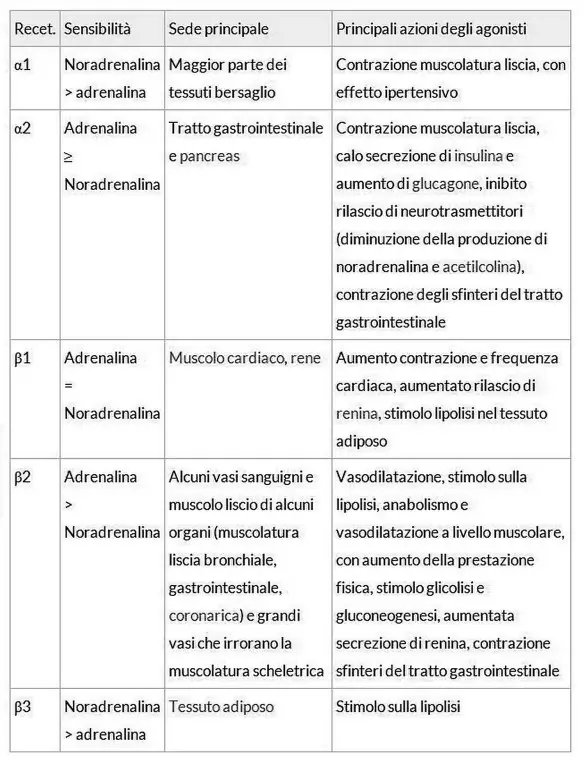
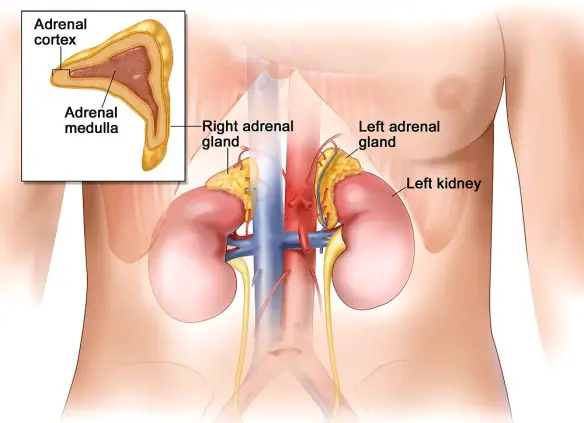 Quante volte l’avete sentita nominare nei telefilm a tema ospedaliero o anche in film come Pulp Fiction o Mission Impossible? Tantissime, sto parlando dell’adrenalina (o epinefrina, se amate Grey’s Anatomy come il sottoscritto!). Ma sapete esattamente cosa sia l’adrenalina? E sapete quali sono le sue funzioni? Facciamo un po’ di chiarezza.
Quante volte l’avete sentita nominare nei telefilm a tema ospedaliero o anche in film come Pulp Fiction o Mission Impossible? Tantissime, sto parlando dell’adrenalina (o epinefrina, se amate Grey’s Anatomy come il sottoscritto!). Ma sapete esattamente cosa sia l’adrenalina? E sapete quali sono le sue funzioni? Facciamo un po’ di chiarezza.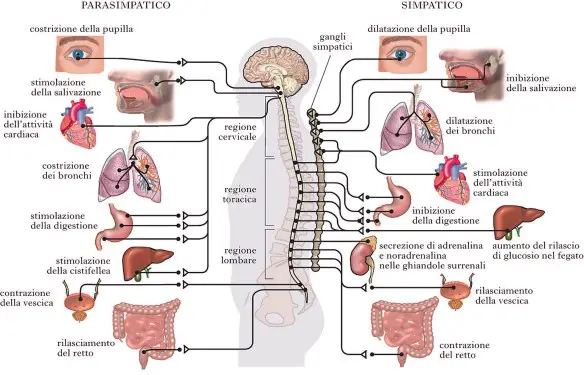
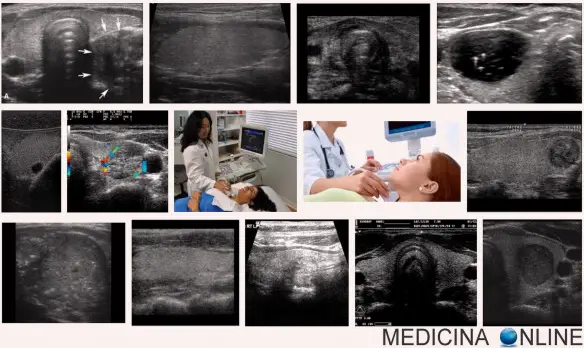 L’ecografia della tiroide è senza alcun dubbio l’esame diagnostico più importante per lo studio della morfologia della ghiandola tiroidea. Come tutte le tecniche ecografiche, si basa sulla differente capacità dei tessuti di riflettere gli ultrasuoni emessi da una sonda. L’apparecchio è in grado di registrare l’intensità delle onde riflesse, convertendole sullo schermo in segnali luminosi che ricostruiscono in tempo reale l’aspetto anatomico della tiroide.
L’ecografia della tiroide è senza alcun dubbio l’esame diagnostico più importante per lo studio della morfologia della ghiandola tiroidea. Come tutte le tecniche ecografiche, si basa sulla differente capacità dei tessuti di riflettere gli ultrasuoni emessi da una sonda. L’apparecchio è in grado di registrare l’intensità delle onde riflesse, convertendole sullo schermo in segnali luminosi che ricostruiscono in tempo reale l’aspetto anatomico della tiroide. L’ipotiroidismo è una patologia causata dalla mancata capacità della tiroide di sintetizzare una adeguata quantità di ormoni. Più raramente, può sussistere una resistenza all’azione dei suddetti ormoni a livello tissutale. L’ipotiroidismo può presentarsi sin dalla nascita (cretinismo) o comparire in età adulta, specie nelle donne ultracinquantenni. Può essere primario (congenito o acquisito), secondario o terziario. Da un punto di vista clinico-laboratoristico si possono distinguere:
L’ipotiroidismo è una patologia causata dalla mancata capacità della tiroide di sintetizzare una adeguata quantità di ormoni. Più raramente, può sussistere una resistenza all’azione dei suddetti ormoni a livello tissutale. L’ipotiroidismo può presentarsi sin dalla nascita (cretinismo) o comparire in età adulta, specie nelle donne ultracinquantenni. Può essere primario (congenito o acquisito), secondario o terziario. Da un punto di vista clinico-laboratoristico si possono distinguere: