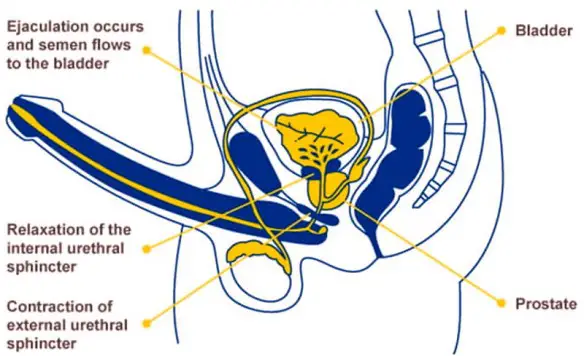
 L’eiaculazione retrograda (retrograde ejaculation in inglese) è una patologia in cui lo sperma, durante l’orgasmo maschile, viene eiaculato totalmente o in parte nella vescica urinaria anziché fuoriuscire dal meato uretrale (l’apertura all’apice del glande del pene) tramite l’uretra peniena. L’eiaculazione viene definita “retrograda” proprio perché l’emissione del liquido seminale avviene in direzione contraria a quella fisiologica, non verso l’esterno ma verso la vescica. L’eiaculazione “fisiologica”, invece, viene invece definita “anterograda”, appunto perché il liquido seminale viene espulso verso l’esterno.
L’eiaculazione retrograda (retrograde ejaculation in inglese) è una patologia in cui lo sperma, durante l’orgasmo maschile, viene eiaculato totalmente o in parte nella vescica urinaria anziché fuoriuscire dal meato uretrale (l’apertura all’apice del glande del pene) tramite l’uretra peniena. L’eiaculazione viene definita “retrograda” proprio perché l’emissione del liquido seminale avviene in direzione contraria a quella fisiologica, non verso l’esterno ma verso la vescica. L’eiaculazione “fisiologica”, invece, viene invece definita “anterograda”, appunto perché il liquido seminale viene espulso verso l’esterno.
Differenza tra eiaculazione retrograda e aneiaculazione
L’aneiaculazione è un disturbo diverso dall’eiaculazione retrograda, per approfondire le differenze tra le due patologie, segui questo link: Differenza tra eiaculazione retrograda e aneiaculazione
Leggi anche:
- Differenza tra spermatorrea, eiaculazione, polluzione
- Spermatorrea: la perdita involontaria di sperma senza eccitazione sessuale
- Polluzione notturna maschile e femminile: cos’è e perché avviene
Sintomi e segni
Il paziente prova un orgasmo con le tipiche contrazioni, non dissimile da un orgasmo di un paziente sano, con la differenza che lo sperma non viene emesso all’esterno, oppure fuoriesce dal pene in quantità ridotta rispetto alle quantità medie emesse da un maschio adulto sano (da 2 a 5 ml di sperma). L’eiaculazione retrograda non provoca alcun dolore al paziente.
Cosa accade allo sperma rimasto all’interno del corpo?
Lo sperma, rimasto intrappolato all’interno della vescica, viene espulso insieme all’urina durante le minzioni immediatamente successive alla mancata eiaculazione.
Leggi anche:
- Erezione debole o assente da cause psicologiche: cura e rimedi
- Il punto G femminile: come trovarlo e stimolarlo e quali sono le posizioni sessuali che più lo eccitano
Cause e fattori di rischio
In condizioni di normalità, durante l’emissione di sperma, una serie di meccanismi automatici impedisce al liquido seminale di raggiungere la vescica. L’eiaculazione retrograda è dovuta nella maggioranza dei casi all’impossibilità da parte dell’imbocco della vescica di chiudersi durante l’atto eiaculatorio, e ciò permette il flusso spermatico retrogrado.
La mancata chiusura dell’imbocco della vescica è causata, a sua volta, da traumi fisici a livello vescicale, da patologie o da deficit neurologici, congeniti od acquisiti.
L’eiaculazione retrograda rappresenta un problema che riguarda molti pazienti con diabete: la neuropatia diabetica sembra infatti la maggior responsabile del danneggiamento a carico della connessione nervosa alla vescica.
Tra gli altri fattori causali direttamente implicati nell’eiaculazione retrograda, spiccano anche l’assunzione di alcuni farmaci, le disfunzioni della prostata, deficit del sistema nervoso autonomo, complicanze chirurgiche che interessano prostata e collo vescicale, e l’intervento TURP (acronimo di resezione endoscopica trans uretrale prostatica, il più noto intervento volto al trattamento dell’ipertrofia prostatica).
L’eiaculazione retrograda è stata diagnosticata anche dopo interventi chirurgici mirati, quali elettroresezione endoscopica di adenomi prostatici di natura benigna, adenomiectomia prostatica, chirurgia spinale e degli organi pelvici, chirurgia del retro peritoneo. Le cause più comuni di eiaculazione retrograda sono sinteticamente:
- diabete;
- disfunzioni del sistema nervoso autonomo;
- disfunzioni della prostata;
- complicazioni di operazioni chirurgiche a carico della prostata compiute attraversando l’uretra o di una linfoadenectomia retroperitoneale;
- farmaci, principalmente antipertensivi, antidepressivi e neurolettici, in particolare, i farmaci neurolettici ed antipertensivi aumentano la probabilità di generare questo disturbo.
Diagnosi
Nella maggior parte dei casi, la diagnosi viene confermata se si riscontra un elevato numero di spermatozoi in un campione di urina dopo l’eiaculazione. L’eiaculazione retrograda è indistinguibile dall’aneiaculazione, specie nella sua variante orgasmica, senza un esame delle urine che constati la presenza di spermatozoi nell’urina. E’ importante però ricordare che, in un paziente affetto da azoospermia (nello sperma non sono presenti spermatozoi), l’assenza di spermatozoi nelle urine non esclude con certezza l’eiaculazione retrograda: in simili frangenti, è consigliata la ricerca del fruttosio nell’urina.
Tra le altre strategie diagnostiche, anche l’ecografia prostatica trans rettale potrebbe rappresentare un valido aiuto per l’indagine di eventuali anomalie morfologico-strutturali delle vescicole seminali.
Leggi anche:
- Come fare per avere un’eiaculazione più abbondante e migliorare sapore, odore, colore e densità dello sperma?
- Come avviene l’eiaculazione maschile [VIDEO] Attenzione: immagini sessualmente esplicite
Trattamento e complicanze fisiche e psicologiche
L’eiaculazione retrograda, come facilmente intuibile, può risultare in un’evidente causa di sterilità, oltre a determinare danni psicologici non indifferenti nel paziente. Per approfondire continua la lettura con questo articolo: Eiaculazione retrograda: cure e complicanze fisiche e psicologiche
Integratori alimentari efficaci nel migliorare quantità di sperma, erezione e libido maschile e femminile
Qui di seguito trovate una lista completa di integratori alimentari acquistabili senza ricetta, potenzialmente in grado di migliorare la prestazione sessuale sia maschile che femminile a qualsiasi età e trarre maggiore soddisfazione dai rapporti sessuali:
- Integratore completo per aumentare la potenza sessuale: https://amzn.to/3x6fF5m
- Maca peruviana: https://amzn.to/3QKmCCP
- Ossido nitrico: https://amzn.to/3dLQnV3
- Arginina: https://amzn.to/2xbksro
- Ornitina: https://amzn.to/2sjpXj8
- Citrullina: https://amzn.to/3T3nDYd
- ZMA (Zinco/Magnesio/Vitamina B6): https://amzn.to/3zp7W3P
- Damiana: https://amzn.to/3MCflSH
- Catuaba: https://amzn.to/3A6T1wi
- Ginkgo Biloba: https://amzn.to/35gKZBQ
- Ginseng: https://amzn.to/2kkzKRA
- Guaranà: https://amzn.to/2GGOuTH
- Zinco: https://amzn.to/3pzXN0E
- Tribulus Terrestris: http://amzn.to/2nu4kt9
- Muira Puama: https://amzn.to/35pgiuh
- Fieno greco: https://amzn.to/3QAFmVg
- Cordyceps Sinensis: http://amzn.to/2B6TTVK
- Carnitina: https://amzn.to/2x4e5Gy
- Taurina: https://amzn.to/2Tw5R5t
- Vitamine e sali minerali: https://amzn.to/2JdCyNB
- Acido folico: https://amzn.to/2RQSzAa
- Allicina: https://amzn.to/3zp7SRD
- Saw Palmetto: https://amzn.to/2RVEOAm
- Calcio, vitamina D3 e vitamina K : http://amzn.to/2BDGeBE
- Omega 3: http://amzn.to/2AdJXtx
Leggi anche:
- Come avere la più potente erezione della tua vita senza farmaci
- Come cambia lo sperma negli anni? Quantità, consistenza ed altre caratteristiche
- Come cambiano i testicoli e lo scroto con l’età?
- Un uomo può avere un orgasmo senza eiaculare sperma?
- Il pene si accorcia o no con l’età? Come le misure cambiano negli anni
- Sesso ad alta quota: fantasia o realtà?
- Sbagliata l’operazione al pene: 17enne denuncia il chirurgo
- Si fascia i genitali per sembrare donna: pene amputato
- Erezione di pene con protesi peniena [VIDEO] Attenzione: immagini sessualmente esplicite
- Un mese senza guardare porno, ecco com’è andata e cosa ho imparato
- Quali sono le forme di pene più comuni ed in cosa sono facilitate nel rapporto?
- Quali sono le paure sessuali più diffuse tra le donne?
- Quali sono le paure sessuali più diffuse tra gli uomini?
- L’uomo nato con due peni
- Prostata ingrossata ed infiammata: ecco cosa fare per mantenerla in salute
- Erezione: come allenare i muscoli di pene e clitoride con gli esercizi di Kegel
- Se odi i gay, sei omosessuale: gli omofobi sono attratti dai gay
- Julio Iglesias dedica un brano al suo pene: “è il mio alleato, il mio amico fedele”
- Si spoglia, si taglia il pene ed inveisce contro i passanti
- L’auto grande è davvero il prolungamento di un pene piccolo?
- I 10 motivi per cui è stressante avere il pene, che le donne non possono capire
- Muore perché voleva avere un pene più grande
- Da oggi puoi usare la foto del tuo pene come password
- Alla guida con un pene di gomma e urina sintetica
- Sindrome del pene piccolo: quando si può parlare di patologia?
- Lunghezza media pene a 15 anni: quando il pene raggiunge la massima lunghezza possibile?
- Cosa NON devi assolutamente fare prima di un rapporto sessuale
- Com’è fatto uno spermatozoo e quanto è piccolo rispetto al gamete femminile?
- Ipoposia: quando lo sperma è troppo poco. Cause e terapie per aumentare la quantità di eiaculato
- Mappa delle zone erogene femminili: scopri i punti che la fanno impazzire
- Zone erogene femminili: scopri i punti insospettabili che le danno piacere
- Testicoli piccoli: quali sono le cause e le dimensioni normali?
- Testicolo gonfio e dolorante: cause, diagnosi e terapie
- Astenospermia: spermiogramma, spermatozoi deboli e fattori che influenzano la loro motilità
- Storia e psicologia della masturbazione
- Cattivi odori del pene: cause e consigli per neutralizzarli
- Da cosa dipende l’odore dello sperma ed a che serve?
- Le dimensioni del pene contano o no? Le confessioni senza censura delle mie pazienti ed i loro consigli per avere un pene più bello
- L’uomo con il pene più grande del mondo:”Faccio sesso orale da solo e da morto donerò il mio pene a…”
- Esercizi per allungamento del pene (massaggio Jelqing): funzionano? Tecnica e rischi
- Quali sono le differenze tra orgasmo vaginale e clitorideo?
- Anorgasmia: quando manca l’orgasmo, cause e rimedi
- Si può essere allergici allo sperma?
- Cosa contiene lo sperma?
- Quante calorie contiene lo sperma?
- Ragazza di 15 anni rimane incinta dopo sesso orale
- Lo sperma ingoiato fa bene alla salute
- Vagina: anatomia, funzioni e patologie in sintesi
- Differenza tra vagina e vulva
- Utero: anatomia, funzioni, patologie e sintomi in sintesi
- Apparato genitale femminile: anatomia, funzioni e patologie in sintesi
- La vagina è uguale in tutte le donne?
- Quanto è profonda una vagina?
- Masturbazione maschile: 10 cose che le donne non sanno
- Dieci ragazze raccontano le loro tecniche di masturbazione
- Tecniche di masturbazione femminile: 5 errori da non fare
- “Se ti tocchi diventi cieco”: tutti i falsi miti sulla masturbazione
- Maggio è il mese della masturbazione: tutto sull’orgasmo
- Masturbazione: ecco i 10 effetti sulla salute della donna
- Come bloccare sul nascere il desiderio di masturbarti in 10 passi
- Masturbazione maschile: suggerimenti per raggiungere orgasmi incredibili
- La masturbazione secondo la Bibbia è un peccato?
- USA: in arrivo la prima legge contro la masturbazione
- 13 ragioni per cui ogni donna dovrebbe masturbarsi regolarmente
- Crisi di mezza età maschile: sintomi, quanto dura, depressione
- Crisi di mezza età maschile: come superarla?
- Differenza tra la crisi di mezza età maschile e femminile
- Come confortare vostro marito durante la crisi di mezza età
- Crisi di mezza età maschile: come influisce sul matrimonio e come superarla?
- Differenze tra menopausa ed andropausa: come cambia la sessualità nell’uomo e nella donna
- Andropausa (menopausa maschile): cos’è, a che età, sintomi e cura
- Andropausa precoce: quali sono i sintomi ed i rimedi
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!

 Che differenza c’è tra Carabinieri e Polizia di Stato? La maggior parte delle persone tende a fare confusione quando si tratta delle forze dell’ordine, confondendo le caratteristiche e le funzioni che svolge ognuna di loro. L’Arma dei carabinieri e la Polizia di Stato si differenziano tra loro per storia, organizzazione e funzioni che svolgono. Vediamo insieme che differenza c’è tra Carabinieri e Polizia. La prima diversità è che, mentre la Polizia è un’arma civile che dipende direttamente dal Ministero dell’Interno, l’Arma dei carabinieri è una forza armata che dipende dal Ministero della Difesa e, oltre a esercitare funzioni civili, può compiere operazioni nei paesi esteri insieme all’esercito.
Che differenza c’è tra Carabinieri e Polizia di Stato? La maggior parte delle persone tende a fare confusione quando si tratta delle forze dell’ordine, confondendo le caratteristiche e le funzioni che svolge ognuna di loro. L’Arma dei carabinieri e la Polizia di Stato si differenziano tra loro per storia, organizzazione e funzioni che svolgono. Vediamo insieme che differenza c’è tra Carabinieri e Polizia. La prima diversità è che, mentre la Polizia è un’arma civile che dipende direttamente dal Ministero dell’Interno, l’Arma dei carabinieri è una forza armata che dipende dal Ministero della Difesa e, oltre a esercitare funzioni civili, può compiere operazioni nei paesi esteri insieme all’esercito. Se sei stato lasciato almeno una volta nella vita e sei caduto in un profondo buco nero, ti sarai già posto la domanda: si può soffrire così tanto per amore?
Se sei stato lasciato almeno una volta nella vita e sei caduto in un profondo buco nero, ti sarai già posto la domanda: si può soffrire così tanto per amore?
 In alcuni luoghi della terra avviene circa due volte al giorno, in altri succede in particolari momenti della giornata, in altri ancora non avviene mai. Stiamo parlando della marea, il fenomeno periodico che provoca l’innalzamento o all’abbassamento di mari, laghi e oceani sparsi nel mondo.
In alcuni luoghi della terra avviene circa due volte al giorno, in altri succede in particolari momenti della giornata, in altri ancora non avviene mai. Stiamo parlando della marea, il fenomeno periodico che provoca l’innalzamento o all’abbassamento di mari, laghi e oceani sparsi nel mondo.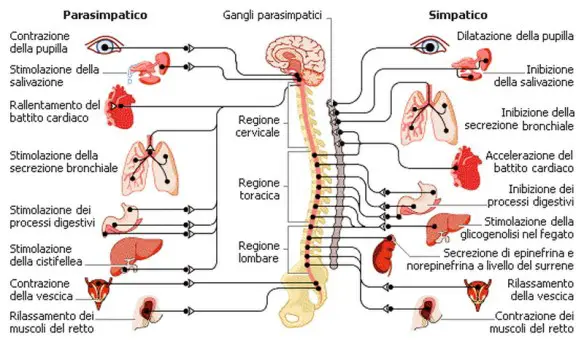 Le funzioni del sistema parasimpatico sono numerose, il nervo vago, il X paio di nervi cranici, ne costituisce l’asse portante.
Le funzioni del sistema parasimpatico sono numerose, il nervo vago, il X paio di nervi cranici, ne costituisce l’asse portante.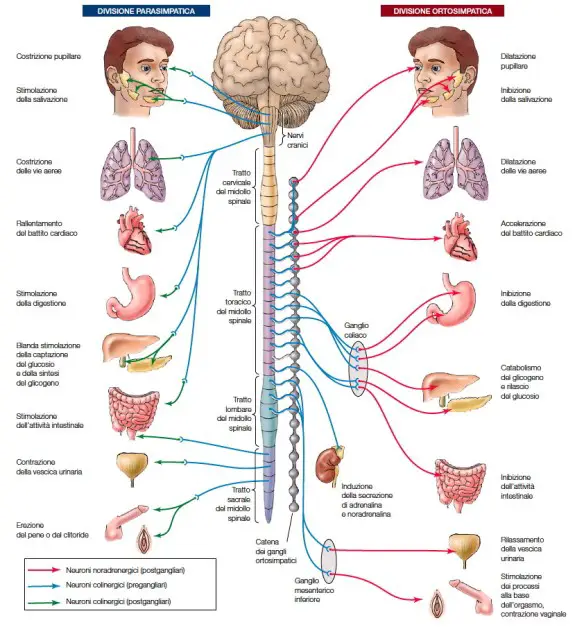 Con “sistema nervoso autonomo” (da cui l’acronimo “SNA“), conosciuto anche come “sistema nervoso vegetativo” o “sistema nervoso viscerale“, in medicina si identifica l’insieme di cellule e fibre che innervano gli organi interni e le ghiandole, controllando le “funzioni vegetative”, ossia quelle funzioni che generalmente sono al di fuori del controllo volontario: per tale modivo viene anche definito “sistema autonomo involontario“. Il SNA è parte del “sistema nervoso periferico” (SNP) ed ha la funzione di regolare l’omeostasi dell’organismo ed è un sistema neuromotorio non influenzabile dalla volontà che opera con meccanismi appunto autonomi, relativi a riflessi periferici sottoposti al controllo centrale.
Con “sistema nervoso autonomo” (da cui l’acronimo “SNA“), conosciuto anche come “sistema nervoso vegetativo” o “sistema nervoso viscerale“, in medicina si identifica l’insieme di cellule e fibre che innervano gli organi interni e le ghiandole, controllando le “funzioni vegetative”, ossia quelle funzioni che generalmente sono al di fuori del controllo volontario: per tale modivo viene anche definito “sistema autonomo involontario“. Il SNA è parte del “sistema nervoso periferico” (SNP) ed ha la funzione di regolare l’omeostasi dell’organismo ed è un sistema neuromotorio non influenzabile dalla volontà che opera con meccanismi appunto autonomi, relativi a riflessi periferici sottoposti al controllo centrale.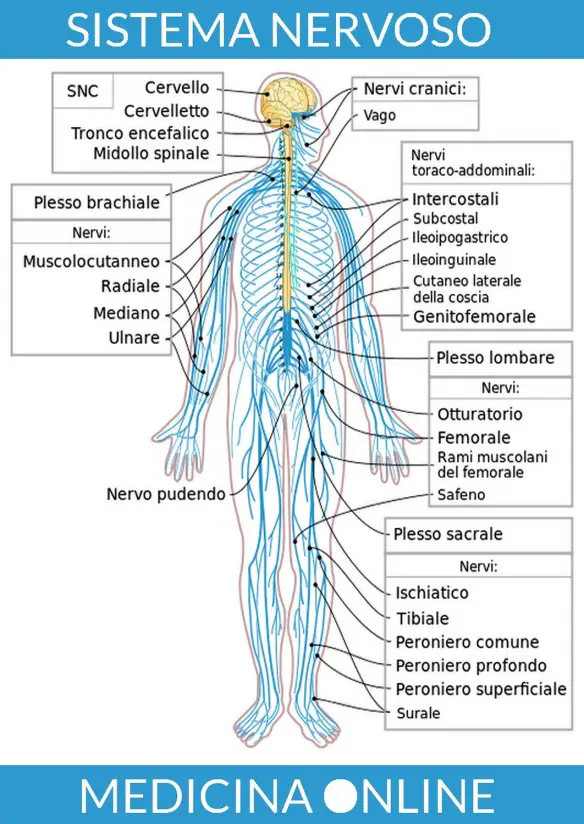 Il sistema nervoso negli esseri umani può essere anatomicamente suddiviso in
Il sistema nervoso negli esseri umani può essere anatomicamente suddiviso in