 La BPCO, acronimo di “broncopneumopatia cronica ostruttiva” (in inglese “COPD” acronimo di Chronic obstructive pulmonary disease) è una malattia infiammatoria cronica dell’apparato respiratorio caratterizzata da un’ostruzione irreversibile delle vie aeree, di entità variabile a seconda della gravità. La BPCO è solitamente progressiva ed è associata a uno stato di infiammazione cronica del tessuto polmonare. La conseguenza a lungo termine è un vero e proprio rimodellamento dei bronchi, che provoca una riduzione consistente della capacità respiratoria. La malattia provoca disabilità, riduce la qualità della vita e – nei casi più gravi – è potenzialmente mortale.
La BPCO, acronimo di “broncopneumopatia cronica ostruttiva” (in inglese “COPD” acronimo di Chronic obstructive pulmonary disease) è una malattia infiammatoria cronica dell’apparato respiratorio caratterizzata da un’ostruzione irreversibile delle vie aeree, di entità variabile a seconda della gravità. La BPCO è solitamente progressiva ed è associata a uno stato di infiammazione cronica del tessuto polmonare. La conseguenza a lungo termine è un vero e proprio rimodellamento dei bronchi, che provoca una riduzione consistente della capacità respiratoria. La malattia provoca disabilità, riduce la qualità della vita e – nei casi più gravi – è potenzialmente mortale.
Ad aggravare questo quadro clinico è l’aumento della predisposizione alle infezioni respiratorie di origine virale, batterica o fungina. Non esiste al momento una cura efficace, ma sono disponibili diversi trattamenti per controllare i sintomi, rallentare la progressione della malattia e per evitare pericolose complicanze. Fondamentale è invece la prevenzione, per ridurre al minimo i fattori di rischio, principalmente rappresentati dal fumo di sigaretta. Tra le prime descrizioni di probabili casidi BPCO ricordiamo quelle del grande medico ed anatomista italiano Giovanni Battista Morgagni nel 1769, che annota polmoni “turgidi in particolare nell’inspirio”.
Leggi anche: Asma bronchiale in bambini e adulti: cause, sintomi e cura
Cause
La causa principale di una BPCO è il processo infiammatorio cronico relativo alle vie respiratorie, che dura anni: ciò comporta una graduale perdita della funzionalità dei polmoni con una disfunzione non completamente reversibile anche se viene trattata. Il processo infiammatorio è promosso, nella maggioranza dei casi, dal fumo di sigaretta, ed in misura minore da esposizione professionale a sostanze irritanti e l’inquinamento ambientale. In genere, queste esposizioni avvengono diversi decenni prima che i sintomi si manifestino.
Fattori di rischio
Esistono diversi fattori di rischio, alcuni individuali, altri di origine ambientale. Tra i fattori individuali, ci sono molti geni che si ritiene possano essere associati all’insorgenza della BPCO. Al momento, i dati più significativi in proposito sono quelli relativi al deficit di alfa1-antitripsina, una condizione ereditaria piuttosto rara caratterizzata dalla carenza di questa proteina epatica che normalmente protegge i polmoni. Ci sono poi alcune patologie respiratorie complesse che possono contribuire allo sviluppo della malattia, in particolare l’asma e l’ipersensibilità bronchiale.
Tra i fattori ambientali, numerosi studi indicano che il principale fattore di rischio per lo sviluppo della BPCO è il fumo di tabacco, in particolare quello di sigaretta (meno quello di sigaro e pipa), che accelera e accentua il decadimento naturale della funzione respiratoria. Anche il fumo passivo e terziario può contribuire parzialmente allo sviluppo della malattia, in quanto favorisce l’inalazione di gas e particolato. Gioca un ruolo determinante anche l’esposizione a polveri, sostanze chimiche, vapori o fumi irritanti all’interno dell’ambiente di lavoro (per esempio silice o cadmio).
Altri fattori di rischio, seppure meno influenti, associati allo sviluppo della BPCO sono l’inquinamento dell’aria: non solo quello atmosferico causato da smog e polveri sottili, ma anche quello presente all’interno degli ambienti chiusi (provocato dalle emissioni di stufe, apparecchi elettrici, impianti di aria condizionata ecc.). Infezioni respiratorie come bronchiti, polmoniti e pleuriti possono predisporre infine al deterioramento dei bronchi. Altri possibili fattori di rischio sono: la povertà, la malnutrizione per difetto, un peso alla nascita inferiore alla media, alcune malattie infettive come quelle da HIV e la tubercolosi.
Sintomi e segni
Prima della diagnosi, i due sintomi e segni principali della BPCO sono la tosse e la dispnea, qualche volta accompagnati da respiro sibilante. Spesso la tosse è cronica, più intensa al mattino e caratterizzata dalla produzione di muco. La dispnea compare gradualmente nell’arco di diversi anni e nei casi più gravi può arrivare a limitare le normali attività quotidiane. In genere, queste persone sono soggette a infezioni croniche dell’apparato respiratorio, che occasionalmente provocano ricadute accompagnate da una sintomatologia aggravata. Con il progredire della malattia questi episodi tendono a divenire sempre più frequenti.
Leggi anche: Tumore al polmone in chi non fuma: da cosa viene causato?
Diagnosi
Gli esami utili alla diagnosi ed a determinare gravità e prognosi, sono:
- Spirometria;
- Saturazione arteriosa; se inferiore al 94% è utile eseguire:
- Emogasanalisi
- 6 Minutes Walking Test
- Calcolo dell’indice di massa corporea (BMI)
- Calcolo del grado di dispnea
Per la diagnosi differenziale potrebbero essere usati vari strumenti, tra cui esami di diagnostica per immagini (radiografia, TC, broncoscopia…) e/o indagini di laboratorio (tampone faringeo, esame del sangue venoso…). I segni caratteristici alla radiografia del torace sono polmoni iper-espansi, diaframma appiattito, aumento dello spazio aereo retrosternale e la presenza di bolle. La presenza di tali segni può aiutare a escludere altre malattie polmonari, come la polmonite, l’edema polmonare o uno pneumotorace. Nella TC del torace si possono notare le localizzazioni dell’enfisema nei polmoni e ciò può essere utile per escludere altre malattie polmonari, tuttavia, se non è previsto l’intervento chirurgico, tale segno raramente può influenzare il trattamento. Un’analisi del sangue arterioso (emogasanalisi) viene richiesta per determinare l’eventuale necessità di ossigeno supplementare. Questo esame è consigliato in coloro che presentano una FEV1 inferiore al 35% del normale, in coloro che presentano una saturazione arteriosa periferica inferiore al 92% e in coloro che hanno sintomi di insufficienza cardiaca congestizia. Nelle zone del mondo in cui è comune il deficit di alfa 1-antitripsina, si consiglia di effettuare questo esame a chi soffre di BPCO (in particolare in coloro con una età inferiore ai 45 anni e con un enfisema che interessa le porzioni inferiori dei polmoni). La misurazione del picco di flusso espiratorio, comunemente utilizzata nell’asma, non è sufficiente per la diagnosi di BPCO. Il principale strumento diagnostico per la BPCO rimane comunque la spirometria, che permette di misurare la capacità polmonare residua.
Spirometria
Le valutazioni spirometriche vengono effettuate allo scopo di stimare il grado di ostruzione delle vie aeree; generalmente seguono l’assunzione di un broncodilatatore. Per raggiungere una diagnosi vengono indagate due componenti principali: il volume espiratorio forzato in un secondo (VEMS o FEV1), che è il massimo volume di aria emesso nel primo secondo di un’espirazione forzata, e la capacità vitale forzata (FVC), il massimo volume d’aria che può essere emesso con un unico grande respiro. Normalmente, nel primo secondo si espira tra il 75% e l’80% della FVC; in un individuo che presenta sintomi di BPCO, un rapporto FEV1/FVC (chiamato “indice di Tiffeneau”) inferiore al 70% è indice di malattia. Sulla base di questi soli parametri, però, nei soggetti anziani la spirometria porterebbe a un eccesso di diagnosi di BPCO. La misurazione spirometrica viene ripetuta, dopo la somministrazione di 400 µg di β2 agonista (un broncodilatatore), a distanza di 40 minuti.
- Se non migliorano i risultati, ma solo la sintomatologia, è possibile la diagnosi di BPCO: indice di Tiffeneau (FEV1/FVC) ridotto.
- Un incremento di FEV1 di 200 ml o del 12%, rispetto al valore pre-broncodilatatore, è considerato un indice prognostico favorevole.
- Se il valore di FEV1 torna nella norma, si esclude diagnosi di BPCO: è verosimile una diagnosi di asma.
Non vi è una evidenza certa che consigli di utilizzare la spirometria, nel tentativo di diagnosticare la malattia, in coloro che non presentano sintomi; pertanto tale pratica non è raccomandata. Per approfondire, leggi: Spirometria diretta ed indiretta: come si esegue ed a cosa serve
Diagnosi differenziale
La diagnosi differenziale si pone principalmente nei confronti di asma, di insufficienza cardiaca, di tubercolosi, di embolia polmonare di polmonite e di pneumotorace.
Gravità
La BPCO è stata classificata in quattro diversi livelli di gravità:
- stadio 0: soggetto a rischio, che presenta tosse cronica e produzione di espettorato. La funzionalità respiratoria risulta ancora normale alla spirometria
- stadio I: malattia lieve, caratterizzata da una leggera riduzione della capacità respiratoria
- stadio II: malattia moderata, caratterizzata da una riduzione più consistente della capacità respiratoria e da dispnea in caso di sforzo
- stadio III: malattia severa caratterizzata da una forte riduzione della capacità respiratoria oppure dai segni clinici di insufficienza respiratoria o cardiaca.
Leggi anche: Broncoscopia polmonare con biopsia: a cosa serve, fa male, è pericolosa?
Terapia
Non esiste una cura efficace per la BPCO che consenta di ripristinare la funzionalità respiratoria perduta. Esistono comunque tutta una serie di trattamenti per gestire la malattia e consentire di raggiungere i seguenti obiettivi:
- prevenire la progressione della malattia;
- ridurre i sintomi;
- migliorare la capacità sotto sforzo;
- migliorare lo stato di salute generale;
- prevenire e trattare le complicanze;
- prevenire e trattare l’aggravarsi della malattia;
- ridurre la mortalità.
Leggi anche: Differenza tra BPCO ed asma: terapia e sintomi comuni e diversi
Terapia farmacologica
I farmaci più indicati per la BPCO sono i broncodilatatori, somministrati per via inalatoria, che sono in grado di dilatare le vie aeree e garantire così il maggior flusso possibile di aria. In caso di forme gravi o acute, si possono usare antinfiammatori potenti come cortisone e suoi derivati, evitandone però l’uso prolungato a causa dei pesanti effetti collaterali. Esistono due tipologie principali di broncodilatatori: gli agonisti β2 e gli anticolinergici; entrambi esistono sia in forma a lunga durata sia a breve durata d’azione. Il loro utilizzo riduce la mancanza di respiro, limita il respiro sibilante e rende più facile compiere attività, migliorando conseguentemente la qualità della vita. Non è chiaro se vi sia anche un cambiamento nel decorso della malattia di base. In quelli che presentano una malattia lieve, farmaci a breve durata d’azione sono raccomandati in base alle necessità. In quelli con una condizione più grave si raccomandano invece agenti a lunga durata. Se i broncodilatatori a lunga durata appaiono insufficienti, vengono aggiunti anche corticosteroidi sempre per via inalatoria. Per quanto riguarda gli agenti a lunga durata d’azione non è chiaro se il tiotropio (un anticolinergico a lunga azione) o i beta-agonisti a lunga azione (LABA) portino a risultati migliori, e può essere indicato provarli entrambi per capire quelli che funzionano meglio. Entrambi gli agenti sembrano ridurre il rischio di riacutizzazioni del 15-25%. Vi sono diversi β2 agonisti a breve azione disponibili, tra cui il salbutamolo (Ventolin) e la terbutalina. Essi forniscono un sollievo dai sintomi per 4-6 ore. β2 agonisti a lunga durata, come il salmeterolo e il formoterolo, sono spesso usati come terapia di mantenimento. Alcuni ritengono che i benefici dal loro utilizzo siano limitati, mentre altri sostengono il contrario. L’uso a lungo termine appare sicuro nella BPCO, gli effetti collaterali includono tremori e palpitazioni. Quando vengono utilizzati insieme a steroidi inalatori aumentano il rischio di polmonite. Sebbene gli steroidi e i LABA possano lavorare meglio insieme, non è chiaro se questo leggero vantaggio superi i maggiori rischi. Ci sono due anticolinergici principali utilizzati nella BPCO, l’ipratropio e il tiotropio. L’ipratropio è un agente a breve durata d’azione, mentre il tiotropio a lunga. Il tiotropio è associato a una diminuzione delle riacutizzazioni e una migliore qualità della vita. Non sembra tuttavia influenzare la mortalità il tasso di ospedalizzazione. Gli anticolinergici possono causare secchezza alla bocca e sintomi del tratto urinario. Essi sono anche associati a un aumentato del rischio di malattie cardiache e ictus.
Altre terapie e consigli
Accanto ai farmaci, esistono altre possibilità di gestione della malattia, come per esempio l’ossigenoterapia, ovvero la somministrazione di ossigeno puro, e la ventilazione meccanica, che supplisce all’insufficiente attività respiratoria. Ai pazienti si raccomanda di vaccinarsi regolarmente contro malattie come l’influenza o la polmonite da pneumococchi, che potrebbero aggravare una funzionalità polmonare già fortemente compromessa. Un consiglio utile è quello di praticare giornalmente una serie di esercizi specifici per tenere in attività i muscoli del respiro. Non ci sarebbe neanche bisogno di specificarlo: il paziente deve smettere di fumare e dovrebbe evitare l’esposizione a smog, inquinanti ambientali e sostanze chimiche irritanti. Importante controllare il peso corporeo, per non affaticare ulteriormente il sistema respiratorio: il paziente sovrappeso od obeso dovrebbe seguire una dieta ipocalorica e svolgere regolarmente attività fisica adeguata. In ogni caso viene consigliato al paziente di seguire un’alimentazione equilibrata e ricca di vitamine e sali minerali, ad esempio ricca di frutta e verdura di stagione. Utile è anche assumere ogni giorno un integratore multivitaminico multiminerale completo, come questo: https://amzn.to/3Xz3PNY
Ossigenoterapia
La somministrazione di ossigeno supplementare è raccomandato nei soggetti con bassi livelli di ossigeno a riposo (pressione parziale di ossigeno inferiore a 50-55 mmHg o saturazione arteriosa inferiore all’88%). In questo gruppo di persone diminuisce il rischio di insufficienza cardiaca e di morte, se utilizzato per 15 ore al giorno. In persone con livelli normali o lievemente bassi di ossigeno, può essere necessario valutare il livello di saturazione sotto sforzo, ad esempio con il test del cammino 6 minuti, in tal caso la supplementazione di ossigeno può migliorare la dispnea e migliorare la capacità di esercizio. Vi è il rischio di incendi e di scarsi benefici in coloro che continuano a fumare nonostante la condizione. In questa situazione spesso si sconsiglia l’ossigeno. Durante le riacutizzazioni, è importante non somministrare alte concentrazioni di ossigeno senza tenere conto dei valori di saturazione sanguigna, ciò può portare a un aumento dei livelli di anidride carbonica, peggiorando la prognosi. In coloro che sono ad alto rischio di livelli di biossido di carbonio, una saturazione di ossigeno tra l’88% e il 92% è raccomandata, mentre per coloro senza questo rischio, i livelli corretti dovrebbero essere tra il 94% e il 98%.
Chirurgia
In coloro che presentano una condizione estremamente grave, è possibile prendere in considerazione la chirurgia e questa può includere un trapianto polmonare o la riduzione del volume polmonare. La chirurgia di riduzione del volume polmonare consiste nel rimuovere le parti del polmone più danneggiate da enfisema permettendo alla porzione restante di espandersi relativamente meglio. Il trapianto polmonare è talvolta eseguita per casi di BPCO molto severa e soprattutto negli individui più giovani.
Prognosi e mortalità
La BPCO solitamente peggiora nel tempo, e in ultima analisi, può portare alla morte. Si stima che il 3% di tutte le disabilità siano legate alla BPCO. La sopravvivenza a 10 anni dall’insorgenza è del 40%. La percentuale di invalidità da BPCO a livello mondiale è diminuita tra il 1990 e il 2010, grazie al miglioramento della qualità dell’aria all’interno delle abitazioni. La velocità con cui la condizione peggiora varia a seconda della presenza di fattori negativi, quali una grave ostruzione del flusso d’aria, la scarsa capacità di compiere sforzi, la mancanza di respiro, un significativo sottopeso o sovrappeso (una importante perdita di peso è un indice molto negativo), la presenza di insufficienza cardiaca congestizia, il continuare a fumare e il verificarsi di frequenti riacutizzazioni. Gli esiti a lungo termine nella BPCO possono essere stimati utilizzando l’indice BODE (o BODE index), che fornisce un punteggio da 0 a 10 a seconda dei valori di FEV1, dell’indice di massa corporea, della distanza percorsa in sei minuti e tramite la scala di dispnea mMRC. I risultati della spirometria possono essere un buon indice predittivo per la prognosi della malattia, ma mai quanto l’indice BODE.
Prevenzione
Eliminare il fumo di sigaretta, gli inquinanti ambientali e l’esposizione a sostanze chimiche irritanti, prevengono la BPCO e rallentano la sua progressione. Le vaccinazioni antinfluenzali annuali in coloro che soffrono di BPCO riducono le probabilità delle riacutizzazioni, di incorrere in ospedalizzazioni e di decesso.
I migliori prodotti per il fumatore che vuole smettere di fumare
Qui di seguito trovate una lista di prodotti di varie marche, pensati per il fumatore che vuole smettere di fumare o che ha smesso da poco:
- Libro “È facile smettere di fumare se sai come farlo”: http://amzn.to/2yMgBMZ
- Capsule per alleviare la sindrome d’astinenza: http://amzn.to/2jaLsxs
- Gomme senza nicotina sostitutive del tabacco: http://amzn.to/2AKPGTW
- Sigarette finte per mantenere la gestualità: http://amzn.to/2yLNFom
- Sigaretta elettronica di alta qualità: https://amzn.to/3YPPldM
- Collutorio zero alcol: http://amzn.to/2ANPxD6
- Gomma da masticare per alito fresco: http://amzn.to/2BoB4x3
- Gomme contro l’alito cattivo: https://amzn.to/3PZ6JJk
- Collutorio alla menta per rinfrescare l’alito e combattere l’alito cattivo: http://amzn.to/2AOdeLC
- Spray per rinfrescare l’alito: https://amzn.to/3YOs3VH
- Carbone attivo in polvere per sbiancare i denti e rimuovere macchie: https://amzn.to/3YQmiXH
- Spray purificante per eliminare la puzza di fumo: http://amzn.to/2CJq4bl
Leggi anche:
- Tutti gli articoli sullo smettere di fumare
- Enfisema polmonare: sintomi, tipi, cause, diagnosi e terapia
- Alveoli polmonari: cosa sono e che funzioni svolgono?
- Enfisema polmonare: cure, complicazioni, quando chiamare il medico
- Apparato respiratorio: anatomia in sintesi, struttura e funzioni
- Differenza tra inspirazione e espirazione: l’atto respiratorio
- Differenza tra ventilazione polmonare e alveolare: spazio morto anatomico e fisiologico
- Asma bronchiale: spirometria e diagnosi differenziale
- Che significa malattia autoimmune? Spiegazione ed esempi
- Parametri della spirometria: capacità, volumi, rapporti e flussi
- Polmoni: anatomia e funzioni in sintesi
- Differenza tra laringe, faringe e trachea
- Pneumotorace spontaneo primario, secondario ed iperteso: cause, sintomi, terapie
- Sangue dal naso (epistassi) in bambini e adulti: cause, rimedi naturali, cosa fare e cosa NON fare
- Bronchi polmonari: anatomia, posizione e funzioni in sintesi
- Bronchioli e ramificazioni dell’albero bronchiale: anatomia e funzioni
- Bronchioli terminali: anatomia, posizione e funzioni in sintesi
- Polmoni: differenza tra funzioni respiratorie e non respiratorie
- Surfattante, compliance polmonare, alveoli, composizione e funzioni
- Differenza tra vie aeree superiori ed inferiori
- Differenza tra pneumociti di tipo I e di tipo II
- Diramazioni delle vie aeree inferiori: spiegazione e schema
- Bronchiolite in neonati e bambini: sintomi, cause, è pericolosa?
- Bronchiolite nei bimbi: mortalità, pericoli, complicazioni e durata
- Bronchiolite nei bambini: quando chiamare il medico?
- Bronchiolite nei bambini: qual è la migliore terapia?
- Drenaggio toracico (toracostomia): a che serve, quando si rimuove
- Valvola di Heimlich: com’è fatta, a che serve e come funziona
- Versamento pleurico, scompenso cardiaco, neoplastico, conseguenze
- Chilotorace: cause, sintomi e trattamento
- Empiema pleurico, subdurale, della colecisti: cause e cure
- Differenza tra empiema ed ascesso
- Emotorace (sangue nella cavità pleurica): sintomi, cause e cura
- Idrotorace: cause, patologie, sintomi, diagnosi e cure
- Embolia polmonare: massiva, diagnosi, da tumore, terapia
- Polmoniti nosocomiali: cause, terapie e linee guida ATS
- Polmonite interstiziale, atipica, senza febbre: sintomi e cure in bimbi ed adulti
- Polmonite in bimbi ed adulti: quando chiamare subito il medico
- Polmonite in bimbi ed adulti: quando diventa davvero pericolosa
- Differenza tra dispnea, apnea e tachipnea
- Differenza apnea statica, dinamica e profonda
- Differenza tra ipossiemia, ipossia ed anossia
- Differenza tra ipossiemia e ipercapnia
- Differenza tra insufficienza respiratoria di tipo 1 e 2
- Crisi respiratoria acuta e rischio di morte: cosa fare?
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su Tumblr e su Pinterest, grazie!

 Le forme farmaceutiche più frequentemente adoperate in omeopatia sono i globuli ed i granuli. In entrambi i casi si tratta di sferette di saccarosio, ricoperte di lattosio, sulle quali si fanno cadere – utilizzando particolari macchinari – gocce della singola sostanza, opportunamente diluita (i globuli sono 10 volte più piccoli dei granuli).
Le forme farmaceutiche più frequentemente adoperate in omeopatia sono i globuli ed i granuli. In entrambi i casi si tratta di sferette di saccarosio, ricoperte di lattosio, sulle quali si fanno cadere – utilizzando particolari macchinari – gocce della singola sostanza, opportunamente diluita (i globuli sono 10 volte più piccoli dei granuli). Il placebo (dal latino placere, letteralmente “io piacerò”) è una una sostanza priva di principi attivi specifici, ma che sono amministrate come se avessero veramente proprietà curative o farmacologiche. Lo stato di salute del paziente che ha accesso a tale trattamento in teoria non dovrebbe migliorare grazie ad un placebo, dal momento che non contiene alcun principio attivo farmacologico, cioè nessuna sostanza che possiede una attività biologica terapeutica. Nonostante ciò, la salute di un paziente può realmente migliorare grazie ad un placebo, ma solo a condizione che il paziente riponga fiducia in tale sostanza o terapia. Questo miglioramento indotto dalle aspettative positive del paziente è detto “effetto placebo”.
Il placebo (dal latino placere, letteralmente “io piacerò”) è una una sostanza priva di principi attivi specifici, ma che sono amministrate come se avessero veramente proprietà curative o farmacologiche. Lo stato di salute del paziente che ha accesso a tale trattamento in teoria non dovrebbe migliorare grazie ad un placebo, dal momento che non contiene alcun principio attivo farmacologico, cioè nessuna sostanza che possiede una attività biologica terapeutica. Nonostante ciò, la salute di un paziente può realmente migliorare grazie ad un placebo, ma solo a condizione che il paziente riponga fiducia in tale sostanza o terapia. Questo miglioramento indotto dalle aspettative positive del paziente è detto “effetto placebo”. Numerosi farmaci interferiscono con il desiderio, l’erezione e l’eiaculazione. Alcuni utilizzati per la cura della depressione come gli antidepressivi triciclici, a fronte di una elevata efficacia rispetto ai sintomi depressivi , determinano deficit erettile, riduzione della libido e dell’eiaculazione.
Numerosi farmaci interferiscono con il desiderio, l’erezione e l’eiaculazione. Alcuni utilizzati per la cura della depressione come gli antidepressivi triciclici, a fronte di una elevata efficacia rispetto ai sintomi depressivi , determinano deficit erettile, riduzione della libido e dell’eiaculazione.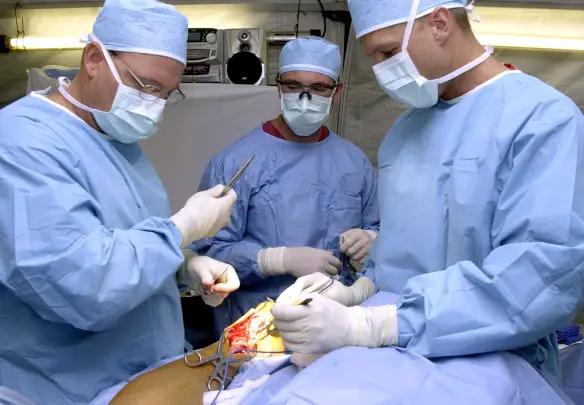 Prima di iniziare la lettura vi consiglio di leggere questo articolo:
Prima di iniziare la lettura vi consiglio di leggere questo articolo: 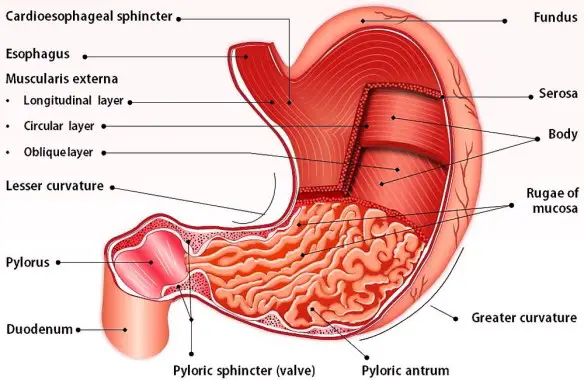 Un “antiacido” è un composto chimico, genericamente uno o più sali basici, che neutralizza l’acidità. I farmaci antiacidi sono una categoria di farmaci che comprende tutti quelli impiegati per contrastare l’acidità gastrica e i suoi effetti negativi.
Un “antiacido” è un composto chimico, genericamente uno o più sali basici, che neutralizza l’acidità. I farmaci antiacidi sono una categoria di farmaci che comprende tutti quelli impiegati per contrastare l’acidità gastrica e i suoi effetti negativi.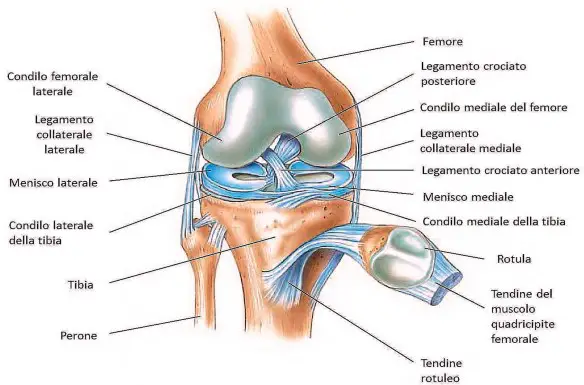 La tendinite del rotuleo è una patologia del ginocchio molto frequente che consiste nell’infiammazione del tendine rotuleo e che colpisce il tendine rotuleo maggiormente nel punto dove inizia, ovvero nella sezione inferiore della rotula. Il tendine rotuleo rientra nell’apparato estensore del ginocchio e quando il muscolo quadricipite si contrae, lo traziona insieme alla tibia e alla rotula, e il ginocchio si estende. Questa patologia è molto frequente fra gli sportivi che praticano il basket, la pallavolo, il calcio, l’atletica leggera ed il sollevamento pesi. Sono tutti sport che necessitano uno sforzo ripetitivo del muscolo quadricipite che sollecita continuamente il tendine rotuleo fino a procurargli una lesione.
La tendinite del rotuleo è una patologia del ginocchio molto frequente che consiste nell’infiammazione del tendine rotuleo e che colpisce il tendine rotuleo maggiormente nel punto dove inizia, ovvero nella sezione inferiore della rotula. Il tendine rotuleo rientra nell’apparato estensore del ginocchio e quando il muscolo quadricipite si contrae, lo traziona insieme alla tibia e alla rotula, e il ginocchio si estende. Questa patologia è molto frequente fra gli sportivi che praticano il basket, la pallavolo, il calcio, l’atletica leggera ed il sollevamento pesi. Sono tutti sport che necessitano uno sforzo ripetitivo del muscolo quadricipite che sollecita continuamente il tendine rotuleo fino a procurargli una lesione. I farmaci usati nel trattamento della stipsi sono diversi: antrachinoni, lassativi di volume, emollienti/lubrificanti, anticolinesterasici (o para-simpaticomimetici), lassativi salini.
I farmaci usati nel trattamento della stipsi sono diversi: antrachinoni, lassativi di volume, emollienti/lubrificanti, anticolinesterasici (o para-simpaticomimetici), lassativi salini.