 Il testosterone è il più importante un ormone steroideo androgeno ed è responsabile nell’uomo dello sviluppo degli organi genitali e dei caratteri sessuali secondari (barba, peli, timbro della voce, muscolatura), mentre nella donna funge da precursore per la sintesi di un importante ormone femminile (estrogeno). In entrambi i sessi ha poi effetto anabolizzante (stimolazione della sintesi di nuove proteine con conseguente aumento della massa muscolare) e profonde influenze sul comportamento (anche, ma non solo, sul desiderio sessuale).
Il testosterone è il più importante un ormone steroideo androgeno ed è responsabile nell’uomo dello sviluppo degli organi genitali e dei caratteri sessuali secondari (barba, peli, timbro della voce, muscolatura), mentre nella donna funge da precursore per la sintesi di un importante ormone femminile (estrogeno). In entrambi i sessi ha poi effetto anabolizzante (stimolazione della sintesi di nuove proteine con conseguente aumento della massa muscolare) e profonde influenze sul comportamento (anche, ma non solo, sul desiderio sessuale).
Nell’uomo viene prodotto principalmente dalle cellule di Leydig, presenti nei testicoli, mentre nelle donne la produzione avviene nelle ovaie (soprattutto in età fertile); la produzione viene stimolata e controllata dall’ormone luteinizzante (LH), sintetizzato dall’ipofisi, all’aumentare dell’LH diminuisce la produzione di testosterone. L’esame misura la concentrazione di quest’ormone in un campione di sangue.
Il testosterone circola nel sangue libero (1-4%) e legato (98% circa). Quest’ultimo può essere in parte legato all’albumina (38%), la principale proteina del plasma, oppure a una proteina legante specifica, e cioè la SHBG, la globulina legante gli ormoni sessuali (60%), anche detta SSBG, cioè globulina legante gli steroidi sessuali. Il legame tra l’ormone e l’albumina non è molto forte e può essere facilmente spezzato, quindi l’espressione testosterone biodisponibile (BAT) è riferita alla somma del testosterone libero e di quello legato all’albumina. Si ritiene che la frazione biodisponibile rappresenti la parte dell’ormone circolante che entra con maggior facilità nelle cellule e rispecchi meglio la bioattività rispetto alla misura pura della quantità totale.
Ricordiamo poi che la variazione dei livelli dell’SHBG può causare inesattezze nella misurazione della concentrazione biodisponibile. La diminuzione del livello di SHBG può essere riscontrata in caso di obesità, ipotiroidismo, durante l’uso degli androgeni e nella sindrome nefrosica. L’SHBG aumenta in caso di cirrosi, ipertiroidismo e uso di estrogeni. In queste situazioni può essere più indicativa la misura del testosterone libero. In molti casi la misura della quantità totale dà al medico tutte le informazioni che gli servono tuttavia, in certi casi (ad esempio se c’è un’anomalia del livello dell’SHBG), può essere eseguito l’esame del testosterone biodisponibile che può diagnosticare con maggior precisione un’eventuale patologia.
Nell’uomo adulto i livelli di testosterone rivestono un ruolo di fondamentale importanza relativamente a
- sessualità e fertilità (regola il desiderio sessuale e permette la maturazione degli spermatozoi),
- apparato muscolo scheletrico (previene l’osteroporosi),
- salute cardiovascolare (rappresenta un fattore protettivo verso diverse malattie metaboliche, come pressione alta e diabete).
Viene utilizzato anche come farmaco, sia negli uomini che nelle donne, in caso di carenza.
Leggi anche:
- Virilizzazione (mascolinizzazione): tipi, cause, sintomi, diagnosi e terapie
- Irsutismo: cause, sintomi, diagnosi e trattamenti
- Atletica, respinto il ricorso della Semenya: è iperandrogena e non può gareggiare
- Iperandrogenismo femminile: significato, cause, sintomi e terapie
- Iperandrogenismo nell’uomo: significato, cause, sintomi e terapie
Valori normali del testosterone
Totale
- Uomini
- 0 – 5 mesi: 75 – 400 ng/dl
- 6 mesi – 9 anni: 7 – 20 ng/dl
- 10 – 11 anni: 7 – 130 ng/dl
- 12 – 13 anni: 7 – 800 ng/dl
- 14 anni: 7 – 1,200 ng/dl
- 15 – 16 anni: 100 – 1,200 ng/dl
- 17 – 18 anni: 300 – 1,200 ng/dl
- Adulti: 240 – 950 ng/dl
- Donne
- 0 – 5 mesi: 20 – 80 ng/dl
- 6 mesi – 9 anni: 7 – 20 ng/dl
- 10 – 11 anni: 7 – 44 ng/dl
- 12 – 16 anni: 7 – 75 ng/dl
- 17 – 18 anni: 20 – 75 ng/dl
- Adulti: 8 – 60 ng/dl
Libero
- Uomini: 9 – 30 ng/dl
- Donne: 0.3 – 1.9 ng/dl
Biodisponibile
- Uomini
- 20 – 29 anni: 83 – 257 ng/dl
- 30 – 39 anni: 72 – 235 ng/dl
- 40 – 49 anni: 61 – 213 ng/dl
- 50 – 59 anni: 50 – 190 ng/dl
- 60 – 69 anni: 40 – 168 ng/dl
(Attenzione, gli intervalli di riferimento possono differire da un laboratorio all’altro, fare quindi riferimento a quelli presenti sul referto in caso di esami del sangue ed urina.)
Integrazione
Se interessati all’aumento dei livelli di testosterone in grado di migliorare la prestazione sessuale a qualsiasi età, qui di seguito trovate una lista di altri integratori alimentari acquistabili senza ricetta, potenzialmente in grado di aumentare la quantità di sperma disponibile, potenziare l’erezione e procurare un aumento di libido sia nell’uomo che nella donna. Ogni prodotto viene periodicamente aggiornato ed è caratterizzato dal miglior rapporto qualità prezzo e dalla maggior efficacia possibile, oltre ad essere stato selezionato e testato ripetutamente dal nostro Staff di esperti:
Interpretazione
Uomini
Durante l’infanzia un’eccessiva produzione di testosterone può causare l’inizio di una pubertà precoce.
Nell’uomo adulto un lieve aumento è in genere asintomatico (senza sintomi); aumenti più importanti possono essere segno di tumore e come tale il risultato andrà approfondito.
In caso di valori inferiori alla normalità si è in genere in presenza di ipogonadismo, che può manifestarsi con alterazione delle caratteristiche sessuali (per esempio impotenza) e riduzione della fertilità. Si parla in questi casi di:
- ipogonadismo primario, quando associato a un aumento dei livelli di LH e FSH, legato a cause:
- genetiche (per esempio la sindrome di Klinefelter),
- dello sviluppo (testicolo ritenuto),
- traumi,
- ischemia (blocco del flusso di sangue dovuto per esempio a torsione testicolare),
- infezioni (in passato per esempio un grosso rischio era rappresentato dagli orecchioni),
- malattie autoimmuni,
- malattie metaboliche (per esempio insufficienza epatica),
- orchiectomia (asportazione testicoli);
- ipogonadismo secondario/terziario, associato a livelli di LH/FSH normali:
- problemi ipotalamici,
- problemi ipofisari,
- iperprolattinemia,
- malnutrizione,
- eccesso di esercizio fisico,
- alcune sostanze d’abuso come la cannabis.
Donne
Durante l’infanzia un’eccessiva produzione di testosterone può causare una mascolinizzazione nelle bambine.
In età adulta può invece manifestarsi sotto forma di
- comparsa di peli (irsutismo),
- acne,
- irregolarità mestruali,
- problemi di fertilità.
Questa condizione è spesso parte di un quando più generale di sindrome dell’ovaio policistico, più comune nelle donne in sovrappeso; può inoltre essere causata da
- tumore delle ovaie o alle ghiandole surrenali,
- iperplasia adenocorticale congenita.
Una diminuzione delle concentrazioni rispetto ai valori di riferimento causa invece sintomi più sfumati, come un calo del desiderio sessuale e alterazioni del tono dell’umore; può essere dovuta a insufficienza ovarica.
Valori Bassi
- AIDS
- Cirrosi
- Criptorchidismo bilaterale
- Distrofia miotonica
- Insufficienza renale
- Iperplasia surrenalica congenita
- Ipogonadismo
- Pubertà tardiva
- Sindrome di Down
- Sindrome di Klinefelter
Valori Alti
- Celiachia
- Gravidanza molare
- Ipertiroidismo
- Obesità femminile
- Ovaio policistico
- Pubertà precoce
- Sindrome di Cushing
- Sindrome di Reifenstein
- Tumore secernente androgeni
- Tumore surrene
- Tumori ovarici
(Attenzione, elenco non esaustivo. Si sottolinea inoltre che spesso piccole variazioni dagli intervalli di riferimento possono non avere significato clinico.)
Fattori che influenzano l’esame
- Negli uomini giovani il livello misurato nelle prime ore del mattino in media è superiore del 50% rispetto alla misurazione nelle ore serali.
- Il livello può variare considerevolmente a seconda del giorno in cui viene misurato, e a volte varia addirittura più rapidamente. La valutazione dei livelli degli androgeni dovrebbe essere quindi basata su diverse misurazioni.
- Un aumento eccessivo può essere legato all’uso di steroidi anabolizzanti.
- Negli uomini i valori possono diminuire in caso di alcolismo e malattie epatiche. Anche alcuni tipi di farmaci, come gli androgeni e gli steroidi, possono far diminuire i livelli degli androgeni.
- Il tumore alla prostata reagisce agli androgeni, quindi molti uomini con tumori alla prostata in stadio avanzato ricevono una terapia con farmaci che fanno diminuire il livello del testosterone.
- I farmaci come gli anticonvulsivanti, i barbiturici e il clomifene (Clomid®) possono far aumentare la concentrazione dell’ormone. Le donne in terapia con gli estrogeni possono avere valori più alti del normale.
- Aumenta dopo l’esercizio fisico e diminuisce con l’età (superati i 40 anni tende a diminuire annualmente dell’1%).
Quando viene richiesto l’esame
Quest’esame in molti casi viene prescritto insieme a quelli dell’FSH e dell’LH ai ragazzi in cui lo sviluppo si presenta tardi o non progredisce. Non tutti i ragazzi iniziano a svilupparsi nello stesso momento, ma di solito lo sviluppo inizia prima dei 10 anni. Tra i sintomi del ritardo della pubertà ricordiamo:
- ritardo nello sviluppo della massa muscolare,
- voce che non si abbassa e peli che non crescono,
- pene e testicoli che non si sviluppano o si sviluppano troppo lentamente.
L’esame può anche essere prescritto in caso di pubertà precoce, con uno sviluppo troppo rapido dei caratteri sessuali secondari (barba, peli, voce adulta, …). Tra le cause della pubertà precoce ricordiamo diversi tipi di tumore e l’iperplasia surrenale congenita.
Negli uomini l’esame può essere prescritto
- se si sospetta l’infertilità,
- se il desiderio sessuale diminuisce,
- osteoporosi,
- in caso di disfunzione erettile.
Tra gli altri campanelli d’allarme ricordiamo: la mancanza di barba e di peli, la diminuzione della massa muscolare e la ginecomastia (cioè lo sviluppo del seno). La carenza di testosterone totale e biodisponibile è stata inoltre connessa alla maggior presenza di tessuto adiposo viscerale (grasso viscerale o grasso intra-addominale) e all’aumento del rischio di coronaropatie.
Nelle donne l’esame può essere prescritto in caso di irregolarità mestruali o amenorrea (assenza delle mestruazioni), problemi a rimanere incinta o caratteri sessuali maschili, come l’eccesso di peli, calvizie, acne, e/o abbassamento della voce. Il livello può aumentare a causa di tumori che si sviluppano nelle ovaie o nelle ghiandole surrenali, oppure per altre malattie, come la PCOS (sindrome dell’ovaio policistico).
Preparazione richiesta
Non viene richiesta alcuna preparazione.
Altre informazioni
Terapia con il testosterone
L’ormone raggiunge il picco durante l’adolescenza e le prime fasi dell’età adulta. Invecchiando, la quantità diminuisce gradualmente, di solito dell’1% annuo circa dopo i 30 anni. Negli uomini anziani è importante capire se la carenza di testosterone è causata dall’invecchiamento oppure da una malattia (ipogonadismo).
La terapia con il testosterone (con cerotti o iniezioni) è in grado di far aumentare la quantità dell’ormone nell’organismo. Può essere utile per alleviare alcuni sintomi e/o prevenire la perdita di tessuto muscolare e osseo che accompagna l’invecchiamento. I benefici della terapia, tuttavia, non sono ancora stati provati definitivamente. Gli esperti, infatti, temono che la terapia ormonale sostitutiva possa aggravare il tumore alla prostata, ma nessuna ricerca ha finora dimostrato che tale terapia possa provocare il cancro. Chi soffre di disfunzione erettile può avere una carenza di ormone, ma in molti casi la somministrazione di testosterone non migliora i sintomi perché ci sono altre patologie a monte.
La terapia sostituiva offre molte possibilità affascinanti:
- può aumentare la massa muscolare,
- migliorare la memoria e la concentrazione,
- migliorare la libido,
- far aumentare l’energia.
ma i benefici per la salute offerti dalla terapia sostitutiva non sono però così chiari.
Quali sono i rischi?
La terapia con il testosterone presenta diversi rischi, ad esempio può:
- far aumentare il rischio di apnea nel sonno, un disturbo del sonno potenzialmente grave in cui il respiro si arresta e riprende più volte nel corso del sonno,
- far produrre all’organismo troppi globuli rossi (policitemia), aumentando il rischio di malattie cardiache,
- causare l’acne o altre reazioni cutanee,
- causare l’iperplasia prostatica benigna (un aumento benigno delle dimensioni della prostata) e forse anche la crescita dei tumori alla prostata,
- aumentare le dimensioni del seno,
- limitare la produzione di spermatozoi o far contrarre i testicoli.
Se pensate che la terapia sostitutiva faccia al caso vostro, chiedete al medico quali sono i rischi e quali i benefici. La terapia può essere necessaria se c’è una patologia che fa diminuire la concentrazione di ormone circolante, ma attualmente non è consigliabile curare i normali problemi connessi all’invecchiamento con il testosterone.
La quantità di peli è direttamente proporzionale a quella del testosterone?
Le ricerche hanno dimostrato che c’è una proporzionalità tra la quantità di ormone e quella dei peli, ma la crescita è diversa nelle varie parti del corpo; ad esempio in alcuni uomini l’ormone fa crescere i peli sull’addome e sulla schiena, ma non sul cuoio capelluto, causando la calvizie. I fattori genetici sono i principali responsabili dell’’espressione dell’enzima 5-alfa reduttasi, che converte il testosterone nel diidrotestosterone, causando la predisposizione famigliare alla calvizie. Il finasteride (Propecia®) è un farmaco che inibisce l’azione della 5-alfa reduttasi e può risolvere la tendenza alla calvizie in alcuni uomini.
Leggi anche:
- Ormone follicolo stimolante (FSH) alto, basso, valori normali e significato
- Anemia da carenza di ferro: cause, sintomi e cure
- Diagnosi di laboratorio di anemia da carenza di ferro
- Aumentare il ferro in modo naturale, specie in gravidanza
- Emocromo completo con formula leucocitaria: valori, interpretazione e significato
- Differenza tra globuli rossi, bianchi e piastrine
- VES alta o bassa: cause, sintomi e valori normali della velocità di eritrosedimentazione
- Esame delle urine completo con urinocoltura: come fare e capire i risultati
- Scura o chiara, liquida o schiumosa: la tua urina rivela la tua salute
- Glicemia alta o bassa: valori normali, che patologie indica e come si controlla nei diabetici
- Emocromo: guida completa a tutti i valori del sangue normali e patologici
- Emocromo: valori di riferimento e significato clinico [SCHEMA]
- Ematocrito (HCT): basso, alto, in gravidanza, valori normali e interpretazione
- Indici corpuscolari MCV, MCH, MCHC, RDW: cosa sono ed a che servono
- Volume corpuscolare medio (MCV): alto, basso, valori normali e significato
- MCH alto, basso, valori normali ed interpretazione
- MCHC alto, basso, valori normali ed interpretazione
- RDW alto, basso, valori normali ed interpretazione
- Ormoni tiroidei: differenza T3 e T4, valori normali e patologici
- TSH alto, basso e valori normali: qual è il significato clinico?
- Tireoglobulina alta, bassa, valori normali ed interpretazione
- Globuli rossi (eritrociti) alti, bassi, valori normali e interpretazione
- Globuli bianchi (leucociti) alti, bassi, valori normali ed interpretazione
- Eosinofili alti, bassi, valori normali ed interpretazione
- Neutrofili alti, bassi, valori normali ed interpretazione
- Basofili alti, bassi, valori normali ed interpretazione
- Emoglobina bassa, alta, cause e valori normali
- Emoglobina nelle urine (emoglobinuria): cause, sintomi e terapia
- Differenza tra anemia ed anemia mediterranea (talassemia)
- Differenza tra anemia e leucemia
- Perché la mononucleosi è chiamata anche “malattia del bacio”?
- Leucemia: sintomi, cause, cure e le diverse forme
- Leucemia mieloide acuta: cause, sintomi, diagnosi e cura
- Mieloma multiplo: cause, sintomi, diagnosi e cura
- Microcitemia (talassemia) : cause, sintomi, diagnosi e cura
- Differenza tra anemia e microcitemia
- Differenza tra anemia megaloblastica e perniciosa
- Differenza tra anemia mediterranea e falciforme
- Differenza tra emoglobina e mioglobina
- Differenza tra emoglobina fetale ed adulta
- Differenza tra emoglobina, ferro, ferritina e transferrina
- Differenza tra emoglobina e globuli rossi
- Differenza tra emocromo ed ematocrito
- Azotemia (Urea) alta o bassa: valori, cause, sintomi e cosa fare
- Insulina alta: cause, diabete, prediabete, valori normali e cure
- Differenze tra il diabete di tipo 1 e 2 (insulino dipendente e resistente)
- Emoglobina glicata alta, valori normali, IFCC e diabete
- Clearance della creatinina: alta o bassa, valori, calcolo e sintomi
- Colesterolo: cos’è ed a cosa serve?
- Colesterolo e uova: si o no? Tutta la verità scientifica
- Colesterolo: gli italiani non lo misurano e non fanno prevenzione
- Colesterolo e trigliceridi: valori normali, alti, bassi ed interpretazione
- Dieta per abbassare il colesterolo: cibi consigliati e da evitare
- Differenza tra colesterolo HDL “buono” e LDL “cattivo”
- Eccesso di colesterolo (ipercolesterolemia): perché è pericoloso?
- Fattore reumatoide alto o basso? Valori normali e Reuma test
- Tiroide: dove si trova, com’è fatta e quali funzioni svolge?
- Patologie della tiroide: possono far veramente ingrassare?
- Le tue feci dicono se sei in salute: con la Scala di Bristol impara ad interpretarle
- Parassiti e vermi nelle feci: sintomi e come eliminarli con farmaci e rimedi naturali
- Coprocoltura e antibiogramma: procedura e perché si eseguono
- Esame e raccolta delle feci: come si fa nel modo corretto ed a che serve
- Feci con sangue, muco, cibo: quando preoccuparsi?
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Assumi abbastanza vitamina D? I sintomi che indicano la sua carenza e i cibi che ne contengono in abbondanza
- Differenza tra tumore benigno, maligno, neoplasia, cancro e metastasi
- Cos’è un tumore? Perché viene il cancro? Quali sono le cause?
- Acido folico (vitamina B9): a cosa serve, in quali alimenti trovarlo e perché è importante prima e durante la gravidanza
- Beta carotene: cos’è, a cosa serve e in quali cibi lo trovo?
- Ecco come il nostro corpo ci segnala la carenza di vitamine
- Hai voglia di un cibo in particolare? E’ il tuo corpo che ti rivela le carenze nutrizionali che hai
- Di cosa è composto il sangue e quali sono le sue funzioni?
- Plasma e cellule (elementi corpuscolati) che compongono il sangue
- Plasma e suoi derivati (plasmaderivati)
- Gruppi sanguigni: cosa sono e quali sono compatibili tra loro
- Differenza tra sangue, plasma e siero
- Come si ottiene il plasma?
- Plasmaferesi e donazione di sangue
- Plasma: a cosa serve e quali sono le sue funzioni?
- Differenza tra plasma liquido e secco
- Differenza tra siero e plasma
- Il plasma contiene fibrinogeno? Ed il siero?
- Come si separa il siero dal sangue?
- Qual è il volume totale del sangue (volemia) nel corpo umano?
- Da cosa viene prodotto il sangue nel corpo umano?
- Quanti litri di sangue abbiamo nel corpo?
- Quanto sangue si può donare in una sola volta?
- Ogni quanto tempo si può donare il sangue
- Quanto tempo serve per reintegrare il sangue dopo una donazione?
- Donare sangue: come fare con mestruazioni, pillola o gravidanza
- Condizioni e preparazione per donare il sangue: tutte le informazioni
- Quanto sangue possiamo perdere prima di morire dissanguati?
- Fibrinogeno: cos’è, a che serve, quali sono i suoi valori normali?
- Fibrinogeno alto o basso: valori normali ed interpretazione
- Fibrinogeno alto o basso in gravidanza: quando preoccuparsi?
- Proteggere la pelle dal freddo e prevenirne l’invecchiamento: l’importanza degli integratori di vitamine
- Hai dolori mestruali insopportabili? ti consiglio 10 formidabili rimedi naturali per alleviarli
- Dismenorrea: quando le mestruazioni sono dolorose
- Il ciclo influenza le prestazioni in palestra: il periodo migliore per allenarsi e gli esercizi da fare durante le mestruazioni
- Come alleviare i sintomi della Sindrome pre-mestruale?
- Farmaci per curare le mestruazioni dolorose e terapia non farmacologica
- Perché viene la diarrea prima e durante il ciclo mestruale e cure
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Assumi abbastanza vitamina D? I sintomi che indicano la sua carenza e i cibi che ne contengono in abbondanza
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Condividi questo articolo:
 Descrizione
Descrizione
 Il testosterone è il più importante un ormone steroideo androgeno ed è responsabile nell’uomo dello sviluppo degli organi genitali e dei caratteri sessuali secondari (barba, peli, timbro della voce, muscolatura), mentre nella donna funge da precursore per la sintesi di un importante ormone femminile (estrogeno). In entrambi i sessi ha poi effetto anabolizzante (stimolazione della sintesi di nuove proteine con conseguente aumento della massa muscolare) e profonde influenze sul comportamento (anche, ma non solo, sul desiderio sessuale).
Il testosterone è il più importante un ormone steroideo androgeno ed è responsabile nell’uomo dello sviluppo degli organi genitali e dei caratteri sessuali secondari (barba, peli, timbro della voce, muscolatura), mentre nella donna funge da precursore per la sintesi di un importante ormone femminile (estrogeno). In entrambi i sessi ha poi effetto anabolizzante (stimolazione della sintesi di nuove proteine con conseguente aumento della massa muscolare) e profonde influenze sul comportamento (anche, ma non solo, sul desiderio sessuale).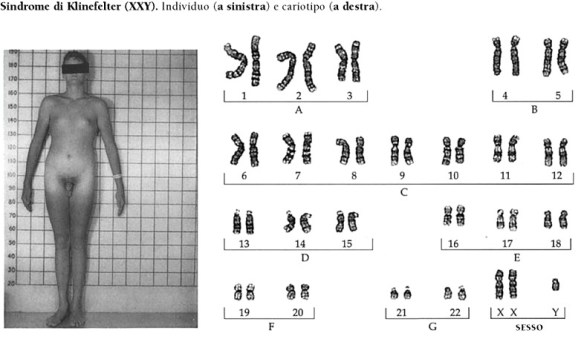 La sindrome di Klinefelter è una condizione caratterizzata dalla presenza di un cromosoma sessuale X in più nei soggetti di sesso maschile (47,XXY). Questa condizione prende il nome dal medico statunitense Harry Klinefelter, del Massachusetts General Hospital di Boston, che nel 1942 pubblicò i risultati delle sue ricerche su nove uomini che manifestavano testicoli ipotrofici, aumento del volume delle mammelle e diminuzione/mancanza di peli sulla superficie corporea. L’assetto cromosomico dei soggetti aventi tali caratteristiche fisiche fu identificato negli anni Cinquanta; negli anni Settanta, l’istituto statunitense National Institute of Child Health and Human Development avviò uno screening su larga scala per determinare il tipo di cromosomi sessuali presenti in 40.000 neonati, e la frequenza della condizione XXY. Attualmente, sembra che l’incidenza di XXY sia relativamente alta (circa uno su 1000 neonati maschi); in realtà, solo una bassa percentuale di questi individui sviluppano una vera e propria sindrome, cioè un insieme di disturbi correlati al loro particolare assetto cromosomico. Per questo motivo, molti autori hanno preferito abbandonare la vecchia denominazione di sindrome di Klinefelter, e indicano i soggetti in questione semplicemente come “maschi-XXY”.
La sindrome di Klinefelter è una condizione caratterizzata dalla presenza di un cromosoma sessuale X in più nei soggetti di sesso maschile (47,XXY). Questa condizione prende il nome dal medico statunitense Harry Klinefelter, del Massachusetts General Hospital di Boston, che nel 1942 pubblicò i risultati delle sue ricerche su nove uomini che manifestavano testicoli ipotrofici, aumento del volume delle mammelle e diminuzione/mancanza di peli sulla superficie corporea. L’assetto cromosomico dei soggetti aventi tali caratteristiche fisiche fu identificato negli anni Cinquanta; negli anni Settanta, l’istituto statunitense National Institute of Child Health and Human Development avviò uno screening su larga scala per determinare il tipo di cromosomi sessuali presenti in 40.000 neonati, e la frequenza della condizione XXY. Attualmente, sembra che l’incidenza di XXY sia relativamente alta (circa uno su 1000 neonati maschi); in realtà, solo una bassa percentuale di questi individui sviluppano una vera e propria sindrome, cioè un insieme di disturbi correlati al loro particolare assetto cromosomico. Per questo motivo, molti autori hanno preferito abbandonare la vecchia denominazione di sindrome di Klinefelter, e indicano i soggetti in questione semplicemente come “maschi-XXY”.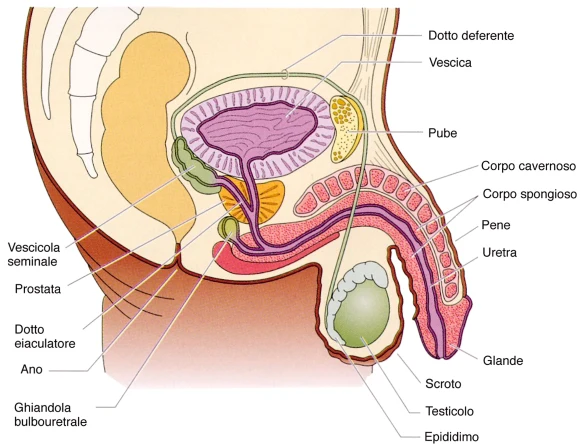 Cos’è il liquido seminale?
Cos’è il liquido seminale?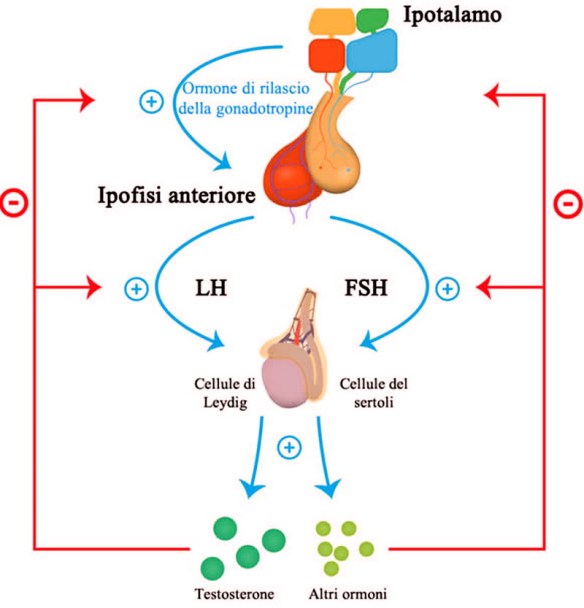 L’ipotalamo rilascia il GnRh, ormone rilasciante le gonadotropine Lh ed FSH rilasciate dall’ipofisi. Le due gonadotropine a livello del testicolo si indirizzano verso (LH) le cellule del Leydig e (FSH) tubulo seminifero, quindi l’LH controlla la steroidogenesi che avviene nelle cellule del Leydig mentre l’FSH controlla la spermatogenesi nel tubulo seminifero con il mantenimento dell’ABP che lega il testosterone.
L’ipotalamo rilascia il GnRh, ormone rilasciante le gonadotropine Lh ed FSH rilasciate dall’ipofisi. Le due gonadotropine a livello del testicolo si indirizzano verso (LH) le cellule del Leydig e (FSH) tubulo seminifero, quindi l’LH controlla la steroidogenesi che avviene nelle cellule del Leydig mentre l’FSH controlla la spermatogenesi nel tubulo seminifero con il mantenimento dell’ABP che lega il testosterone.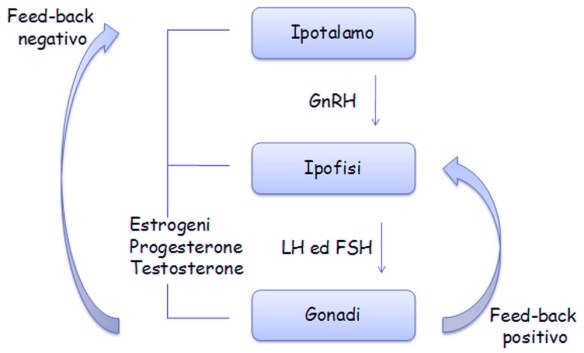 L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.
L’ipotalamo secerne il GnRH che va a stimolare l’adenoipofisi per la secrezione di due gonadotropine, LH ed FSH. Quest’asse neuroendocrino è silente fino al periodo della pubertà e viene sollecitato durante il periodo puberale e grazie all’inizio dell’attività secretoria da parte dell’ipotalamo inizia ad essere sollecitata l’ipofisi che sollecita così l’attività delle gonadi che iniziano la sintesi degli steroidi e la maturazione dei gameti. Ancora non si sa qual è il primo evento che scatena l’attivazione di quest’asse durante la pubertà, le gonadotropine LH ed FSH prima della nascita, dopo la nascita e nell’età matura.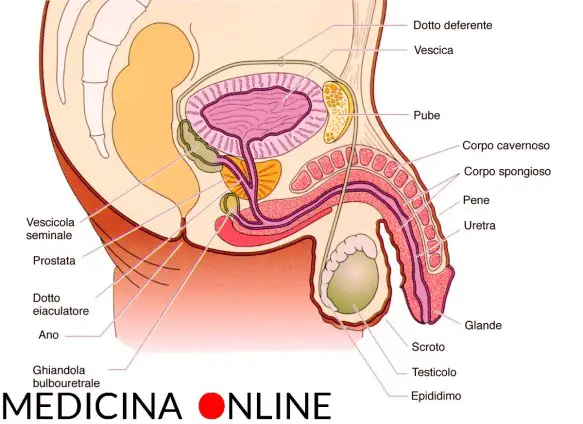 Prima di iniziare la lettura dell’articolo, vi consiglio di leggere:
Prima di iniziare la lettura dell’articolo, vi consiglio di leggere:  Chemioterapia e radioterapia utilizzato nel trattamento dei tumori possono causare, a livello delle gonadi, tossicità temporanea, a lungo termine, o permanente negli uomini. Questi trattamenti citotossici hanno un impatto significativo sulla capacità riproduttiva per i malati di cancro in età fertile. In molti casi, la capacità di raggiungere una gravidanza può essere temporaneamente diminuita, costringendo il paziente a ritardare paternità. In alcuni casi la sterilità può essere permanente.
Chemioterapia e radioterapia utilizzato nel trattamento dei tumori possono causare, a livello delle gonadi, tossicità temporanea, a lungo termine, o permanente negli uomini. Questi trattamenti citotossici hanno un impatto significativo sulla capacità riproduttiva per i malati di cancro in età fertile. In molti casi, la capacità di raggiungere una gravidanza può essere temporaneamente diminuita, costringendo il paziente a ritardare paternità. In alcuni casi la sterilità può essere permanente.