 Con “arresto cardiaco” (anche chiamato “arresto cardiocircolatorio”) si intende un gravissimo ed improvviso deficit delle funzionalità del cuore, che cessa improvvisamente di battere in modo efficace e di conseguenza interrompe la sua azione di pompaggio del sangue in tutto il corpo, mettendo a rischio la vita stessa del paziente. L’arresto cardiaco si può verificare in caso di traumi, ad esempio un forte trauma toracico in un incidente stradale, o in caso di svariate patologie.
Con “arresto cardiaco” (anche chiamato “arresto cardiocircolatorio”) si intende un gravissimo ed improvviso deficit delle funzionalità del cuore, che cessa improvvisamente di battere in modo efficace e di conseguenza interrompe la sua azione di pompaggio del sangue in tutto il corpo, mettendo a rischio la vita stessa del paziente. L’arresto cardiaco si può verificare in caso di traumi, ad esempio un forte trauma toracico in un incidente stradale, o in caso di svariate patologie.
Quando si verifica un arresto cardiaco?
Un arresto cardiaco si verifica in caso di importanti alterazioni del ritmo cardiaco:
- asistolia;
- fibrillazione ventricolare;
- tachicardia ventricolare senza polso;
- attività elettrica senza polso o pulseless electrical activity (PEA).
Quali sono le cause di un arresto cardiaco?
Le cause di arresto cardiaco possono essere:
- cardiache (le più frequenti, spesso determinate da cardiopatia ischemica causata da ostruzione delle arterie coronarie)
- non cardiache.
Le cause non cardiache sono meno frequenti rispetto alle cardiache. Le non cardiache possono essere di due tipi:
- non cardiache meccaniche (tamponamento cardiaco, embolia polmonare, pneumotorace iperteso…);
- non cardiache anossiche (struzione delle vie aeree, eventi neurologici…).
A cosa porta un arresto cardiaco?
I tessuti corporei e cerebrali, durante un arresto cardiaco, non sono più perfusi da sangue ed ossigeno: questo comporta una veloce perdita di coscienza e delle capacità respiratorie. Un arresto cardiaco è così grave che, se non si interviene immediatamente con la rianimazione cardiopolmonare e con un defibrillatore, nel giro di pochissimi minuti provoca dei danni permanenti al cervello e la morte della persona colpita.
Sintomi e sintomi premonitori di un arresto cardiaco
L’insorgenza dell’arresto cardiaco è spesso istantanea, senza segni clinici o sintomi premonitori. In alcuni casi il paziente può avvertire una sintomatologia riferibile alla condizione clinica che è causa dell’arresto: palpitazioni, vertigini, dispnea, dolore toracico. L’obiettività in corso di arresto cardiaco è caratterizzata dall’assenza del polso centrale (carotideo), dalla perdita di coscienza, e da una serie di segni clinici che compaiono dopo un lasso di tempo variabile:
- midriasi,
- pallore,
- cianosi cutanea,
- respiro agonico,
- incontinenza sfinterica,
- rilassamento della muscolatura scheletrica.
L’evoluzione dell’arresto cardiaco verso il coma e la morte biologica irreversibile dipende in maniera critica dal tempo che intercorre tra l’evento primario e la messa in atto delle manovre assistenziali. Il cervello è molto sensibile all’anossia derivante dall’arresto di circolo: in pochi secondi si ha perdita di coscienza, mentre dopo circa 4 minuti si hanno danni irreversibili. Il cuore è meno sensibile, ma anche l’attività cardiaca va deteriorandosi nel giro di qualche minuto; la tachicardia ventricolare senza polso (TV-senza polso) e la fibrillazione ventricolare (FV), che sono in genere i ritmi di esordio dell’arresto cardiaco da ischemia miocardica, decadono in qualche minuto a FV a basso voltaggio, e infine ad asistolia: se la rianimazione cardiopolmonare non portasse alla ripresa dell’attività elettrica cardiaca, in pochi minuti si giungerebbe alla morte biologica.
Terapia: cosa fare in caso di arresto cardiaco?
Il successo delle manovre mediche applicate a un paziente in arresto cardiaco è correlato in maniera significativa al tipo di ritmo inizialmente rilevato dal defibrillatore (il cosiddetto ritmo di presentazione). I ritmi di presentazione si possono schematicamente classificare in due categorie:
- ritmi defibrillabili (tachicardia ventricolare-senza polso e fibrillazione ventricolare);
- ritmi non defibrillabili (asistolia e pulseless electrical activity, o PEA).
Se il soccorritore si trova di fronte ad un ritmo TV-senza polso/FV, ha discrete probabilità che le manovre di rianimazione abbiano successo; se rileva un’asistolia, le probabilità di successo si abbassano. Oltre al massaggio cardiaco si sono recentemente sviluppate delle tecniche rianimatorie con sistemi meccanici (speciali corpetti da apporre sul torace del paziente), che permettono un prolungamento della rianimazione sino all’arrivo in pronto soccorso.
La defibrillazione permette la cardioversione, cioè un ritorno ad un ritmo cardiaco sinusale (normale) e può essere effettuata con un defibrillatore esterno (se il soggetto non possiede un defibrillatore interno ICD) o – in casi limitati – con pugno precordiale.
La defibrillazione, se attuabile, deve avvenire nel minor tempo possibile dall’arresto cardiaco; si ritiene che per ogni minuto trascorso le probabilità di successo decadano del 7-10%. Inoltre, alcuni fattori possono intervenire riducendo le probabilità di successo, ad esempio l’ipotermia, l’ipossia, l’acidosi e l’elevata impedenza toracica.
I tempi di intervento sono importanti
Il tempo massimo per intervenire in modo efficace su un arresto cardiaco è al massimo 10 minuti; ogni minuto perso equivale a una riduzione della sopravvivenza del 7-10%. Il tempo per cardiovertire un arresto cardiaco e “resuscitare” il paziente, prima che i danni al cervello siano irreversibili, è correlato all’efficacia della rianimazione cardiopolmonare.
IMPORTANTE: In caso vi ritroviate di fronte ad un probabile arresto cardiaco e non avete né nozioni di rianimazione, né defibrillatori esterni semiautomatici/automatici, non perdete neanche un secondo e chiedete IMMADIATAMENTE soccorso medico. Un minuto in più od in meno fanno letteralmente la differenza tra la vita e la morte del paziente.
Leggi anche:
- Sapresti riconoscere un infarto del miocardio? Impara ad identificarlo e salverai una vita (anche la tua)
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Differenza tra tachicardia, aritmia, bradicardia e alloritmia
- Cos’è un infarto e quanti tipi di infarto conosci?
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Medicina d’emergenza-urgenza: obiettivi, esami, tecniche, concetti importanti
- Primo soccorso: definizione, significato, simboli, obiettivi, protocolli
- Pronto Soccorso, Dipartimento d’Emergenza e Accettazione, Sala Rossa
- Triage in Pronto soccorso: codice rosso, giallo, verde, bianco, nero, blu, arancione, azzurro
- Come svolgere il triage al Pronto Soccorso? Metodi START e CESIRA
- Codice nero al Pronto Soccorso: cosa significa in Italia e all’estero?
- Blocco barelle al Pronto Soccorso: cosa significa?
- Sala Rossa del Pronto soccorso: cos’è, a cosa serve, quando è necessaria?
- Regola ABC, ABCD e ABCDE in medicina d’urgenza: cosa deve fare il soccorritore
- Scala AVPU: significato e corrispondenza con Glasgow Coma Scale
- Supporto vitale di base (BTLS) e avanzato (ALS) al paziente traumatizzato
- Soccorso psicologico di base (BPS) negli attacchi di panico e nell’ansia acuta
- Dispositivo di estricazione KED per l’estrazione di traumatizzati
- Collarino cervicale nel traumatizzato in medicina d’urgenza
- Manovra GAS (Guardare Ascoltare Sentire) in medicina d’urgenza
- Manovra OPACS in medicina d’urgenza: significato, esecuzione e vantaggi
- AMPIA e SAMPLE in medicina d’urgenza: significato, esecuzione e vantaggi
- Medicina delle grandi emergenze e delle catastrofi: strategie, logistica, strumenti, triage
- Psicologia dell’emergenza: significato, ambiti, applicazioni, formazione
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Differenza tra cardioversione spontanea, elettrica e farmacologica
- Il defibrillatore non funziona: muore a 51 anni per un infarto
- Ritmo sinusale ECG: normofrequente, tachicardico, valori, ai limiti della norma
- Pugno precordiale sul petto: significato, quando farlo, linee guida
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Il massaggio cardiaco si esegue in assenza di…
- Aritmia cardiaca: cause e fattori di rischio, sintomi, diagnosi e cura
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- Differenza tra pacemaker e defibrillatore ICD
- I dubbi su pacemaker e ICD: carica, impulsi, cellulare, banca ed aereo
- Com’è fatto il cuore, a che serve e come funziona?
- ECG: cosa indicano le onde P, T, U, il complesso QRS ed il segmento ST
- Come si muove l’impulso elettrico cardiaco nel cuore?
- Perché il cuore si trova a sinistra e non a destra nel torace?
- Malattie cardiovascolari: i 10 comandamenti del cuore in salute
- Quanto pesa e quanto sangue contiene un cuore?
- Differenza tra pressione arteriosa e venosa
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Differenza tra sintomo e segno con esempi
- Pressione arteriosa: valori normali e patologici
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
- Ecocolordoppler: cos’è, a che serve e come funziona?
- Ecocolordoppler arterioso e venoso degli arti inferiori e superiori
- Effetto Doppler: cos’è e come viene usato in campo medico?
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Endocardite batterica: profilassi in bambini ed adulti
- Riduzione della riserva coronarica: cos’è e come si studia
- Ecocolordoppler dei tronchi sovraortici: come si effettua e quali patologie studia
- Doppler transcranico: a che serve, è pericoloso o doloroso?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Come si muove il sangue all’interno del cuore?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!

 La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti.
La Sindrome di Wolff Parkinson White (WPW, in lingua inglese “Wolff–Parkinson–White Syndrome”) è una patologia caratterizzata da anomala conduzione dell’impulso elettrico cardiaco e determinata dalla presenza di uno o più fasci atrio-ventricolari accessori, che possono dare origine ad episodi di tachicardia sporadica. La malattia, ad eziologia ancora non del tutto chiara, colpisce una persona su 450; nel 70% dei casi interessa i maschi, specie in giovane età, e può presentarsi sia in forma sporadica che famigliare ed essere silente dal punto di vista sintomatico. I neonati da genitori con la sindrome di WPW possono essere a maggior rischio di sviluppare la malattia come pure i neonati con altri difetti cardiaci congeniti.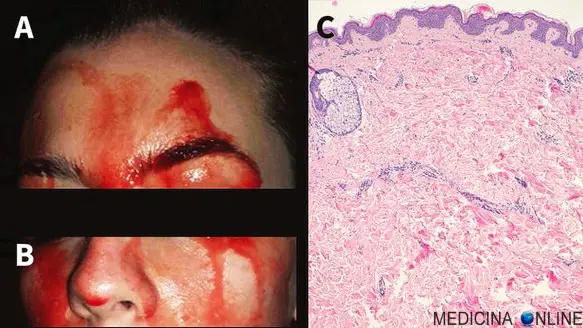 E’ una patologia molto rara tanto che è diventato famoso il caso di una donna di 21 anni di Firenze affetta da ematidrosi, una condizione rarissima che porta appunto a sudare sangue, soprattutto in caso di stress molto forti. La paziente fiorentina, la cui vicenda è descritta dai medici dell’Università di Firenze sul
E’ una patologia molto rara tanto che è diventato famoso il caso di una donna di 21 anni di Firenze affetta da ematidrosi, una condizione rarissima che porta appunto a sudare sangue, soprattutto in caso di stress molto forti. La paziente fiorentina, la cui vicenda è descritta dai medici dell’Università di Firenze sul 
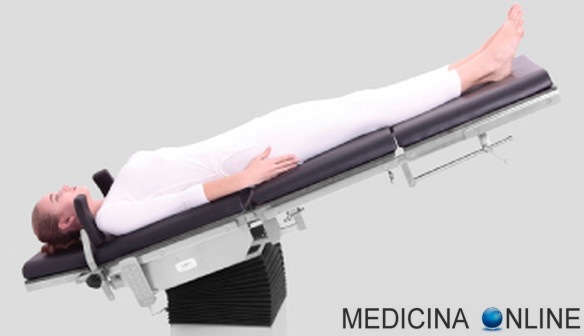 La posizione di Trendelenburg, o posizione anti-shock, è la posizione in cui è posto il paziente in caso di shock o durante l’esecuzione di particolari indagini radiologiche, nonché durante operazioni di chirurgia ginecologica e addominale. Il soggetto è supino, sdraiato in modo che il capo sia situato inferiormente a ginocchia e bacino. Questa posizione prende nome dal chirurgo tedesco Friedrich Trendelenburg, figlio dell’omonimo filosofo.
La posizione di Trendelenburg, o posizione anti-shock, è la posizione in cui è posto il paziente in caso di shock o durante l’esecuzione di particolari indagini radiologiche, nonché durante operazioni di chirurgia ginecologica e addominale. Il soggetto è supino, sdraiato in modo che il capo sia situato inferiormente a ginocchia e bacino. Questa posizione prende nome dal chirurgo tedesco Friedrich Trendelenburg, figlio dell’omonimo filosofo. I tono
I tono L’AIDS, cioè Acquired Immune Deficiency Syndrome la Sindrome da Immunodeficienza Acquisita, è una malattia del sistema immunitario umano causata dal virus dell’immunodeficienza umana (HIV). L’HIV danneggia il sistema immunitario delle persone che lo hanno contratto, rendendole vulnerabili a degli agenti patogeni normalmente innocui, che si trovano nell’ambiente o che, addirittura, sono ospiti abituali dell’organismo umano, cioè microrganismi generalmente inoffensivi che però diventano pericolosi nel paziente con sistema immunitario compromesso.
L’AIDS, cioè Acquired Immune Deficiency Syndrome la Sindrome da Immunodeficienza Acquisita, è una malattia del sistema immunitario umano causata dal virus dell’immunodeficienza umana (HIV). L’HIV danneggia il sistema immunitario delle persone che lo hanno contratto, rendendole vulnerabili a degli agenti patogeni normalmente innocui, che si trovano nell’ambiente o che, addirittura, sono ospiti abituali dell’organismo umano, cioè microrganismi generalmente inoffensivi che però diventano pericolosi nel paziente con sistema immunitario compromesso. La valvola mitrale (anche chiamata valvola bicuspide) è una delle quattro valvole cardiache che mettono in comunicazione, tra loro e con l’esterno, atri e ventricoli del cuore. La valvola mitrale ha un diametro di oltre 30 mm ed unisce l’atrio sinistro al ventricolo sinistro ed ha un orifizio di 4–6 cm2. Insufficienza mitralica e prolasso mitralico, indicano due patologie che interessano questa valvola.
La valvola mitrale (anche chiamata valvola bicuspide) è una delle quattro valvole cardiache che mettono in comunicazione, tra loro e con l’esterno, atri e ventricoli del cuore. La valvola mitrale ha un diametro di oltre 30 mm ed unisce l’atrio sinistro al ventricolo sinistro ed ha un orifizio di 4–6 cm2. Insufficienza mitralica e prolasso mitralico, indicano due patologie che interessano questa valvola.