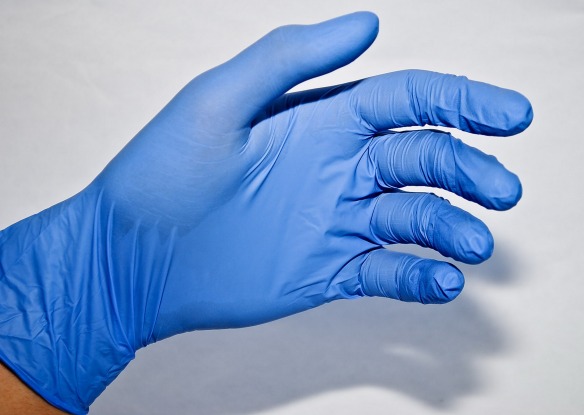
 Quando si parla di guanti monouso, le varietà disponibili sul mercato possono creare confusione, considerati i diversi modelli realizzati per ogni genere di settore professionale e industriale.
Quando si parla di guanti monouso, le varietà disponibili sul mercato possono creare confusione, considerati i diversi modelli realizzati per ogni genere di settore professionale e industriale.
A fare la differenza, di solito, è il materiale utilizzato, il quale determina l’impiego specifico di ciascuna tipologia di guanti usa e getta esistenti in commercio.
Tutti i prodotti disponibili sul nostro eshop sono a marchio Reflexx, leader nel settore dei guanti monouso. Potrete acquistare guanti con o senza polvere, a seconda delle vostre necessità d’uso.
La polvere è costituita da amido di mais biassorbibile dal derma OGM free, difatti, non contenendo glutine, i guanti monouso con polvere possono essere utilizzati anche nella lavorazione di pasti per celiaci.
La sua presenza di talco o polvere agisce da lubrificante per facilitare la calzata.
Guanti monouso in vinile
I guanti in vinile vengono realizzati con materie prime sintetiche, in primis PVC (Poli Vinyl Cloruro – cloruro di polivinile) e ftalati (DINP). L’aggiunta dei plasticizzanti consente di godere di malleabilità, modellabilità, morbidezza ed elasticità.
La loro diffusione è alquanto ampia negli ospedali per ragioni economiche, ma il loro impiego si limita solitamente alle esplorazioni. Questa tipologia di guanti ha una sensibilità e una resistenza minore rispetto a quella in nitrile, difatti può rompersi con facilità (es. pressione delle dita). Il materiale in questione è privo di acceleratori e proteine naturali però, un dettaglio che diminuisce la possibilità di allergie da contatto o Reazioni di Ipersensibilità di tipo IV e che permette l’uso dei guanti dai soggetti allergici alle proteine del lattice.
A seconda dello spessore, questi guanti possono offrire anche sicurezza. E’ indispensabile smaltirli nel modo corretto affinché il PVC non generi diossina.
Un ottimo guanto in vinile è questo: http://amzn.to/2BzZOTR
Guanti monouso in nitrile
Se ricercate elasticità, resistenza meccanica e chimica, sensibilità ed ergonomia, i guanti in nitrile sono la scelta migliore. Queste proprietà, nonostante si tratti di prodotti monouso, sono garantite proprio dall’impiego del nitrile (AcriloNitrile e Butadine), materiale ideale per chi manipola alimenti (tranne quelli alcolici) o necessità di massima protezione lavorando a contatto con sostanze chimiche e/o fluidi corporei. La superficie microruvida, la sensibilità tattile, la perfetta adesione alle mani e l’assenza di talco consentono di utilizzarli come dispositivo medico (per uso ambulatoriale e per medicazione) e riducono il rischio di dermatiti. Inoltre, i soggetti allergici alle proteine del lattice naturale possono trovare una valida alternativa in questa tipologia di guanti usa e getta, più costosa e resistente (a trazione e perforazione) rispetto a quella realizzata in vinile ma in grado di proteggere da agenti chimici, microrganismi e sostanze chimiche aggressive.
Un ottimo guanto in nitrile è questo: http://amzn.to/2BzI1vS
Guanti monouso in lattice
Un prodotto biodegradabile che assicura un elevato livello di sensibilità, elasticità ed impermeabilità, nonostante abbia un costo inferiore rispetto ad altri articoli realizzati con materiali differenti. Tali proprietà non sono le uniche: i guanti monouso prodotti con lattice naturale (proveniente dall’albero della Gomma) vantano una maggiore resistenza a perforazioni e strappi.
Chi lavora a contatto con materiale biologico li predilige per il controllo del livello dei microfori che garantisce un livello di impermeabilità superiore ai molteplici guanti monouso presenti sul mercato. I guanti in lattice vengono spesso utilizzati da dentisti e medici per la propria elasticità (anche a basse temperatura), dato che non esiste attualmente materiale più elastico (la gomma isolata dal lattice assume istantaneamente la forma della mano inserita ma nonostante la pressione o allungamento, riassume la forma originale).
Il loro impiego è comunque favorito anche da chi lavora nel settore dell’estetica o della preparazione di farmaci e cosmetici, data la moderata resistenza chimica (es. soluzioni acquose, detergenti e detersivi diluiti ecc).
Un ottimo guanto in lattice è questo: http://amzn.to/2BRhtn1
Guanti monouso in polietilene
Solitamente idonei al contatto con gli alimenti e conformi a tutti i requisiti di conformità alle normative della Comunità Europea in materia di sicurezza alimentare, i guanti in polietilene sono particolarmente diffusi presso supermercati, banconi per prodotti alimentari, distributori di benzina ecc.
Non sono molto resistenti, ma il loro scopo è principalmente quello di proteggere le mani e gli oggetti manipolati dallo sporco. Oltre che per il rifornimento di carburante o per il contatto con frutta, verdura e altri alimenti, i guanti monouso in polietilene si rivelano utili anche in ambito medicale(aspirazioni, inserimento/svuotamento di cateteri, pulizie ecc) per uso ospedaliero e ambulatoriale, poiché sono in grado di proteggere pur mantenendo la massima sensibilità durante l’uso. I guanti in polietilene sono talmente pratici da essere perfetti anche per un uso casalingo e non solo professionale. Sono un’opzione ideale per chi opta per un prodotto monouso prediligendo la massima igiene, difatti trovano ampio uso anche fra i veterinari e nel settore zootecnico, ma sono adatti anche per trattamenti professionali estetici.
Un ottimo guanto in polietilene è questo: http://amzn.to/2Bp3PGk
Leggi anche:
- Differenza tra eclissi solare e lunare (spiegazione semplice)
- Differenza tra eclissi totale, parziale, anulare e penombrale
- Com’è fatta la tuta degli astronauti?
- Cos’è una galassia? Di cosa è fatta?
- Cos’è e dove si trova la Stella Polare? Come individuarla?
- Cos’è una eclissi lunare? Come e quando si verifica?
- Perché la notte di San Lorenzo cadono le stelle? Cos’è una stella cadente?
- Quante volte l’uomo è stato sulla Luna?
- Perché si verificano le maree?
- Perché la luna ci rivolge sempre la stessa faccia? Com’è il lato oscuro?
- Cos’è un anno luce ed a quanti km corrisponde?
- Le distanze dell’universo, ovvero: bagliori di luce da una stella ormai scomparsa
- Andremo tutti a vivere su Kepler, il pianeta simile alla terra
- Differenza tra raggi infrarossi, ultravioletti e visibili
- Entro dieci anni scopriremo forme di vita extraterrestri
- Cos’è la radiazione solare? Cosa sono i raggi ultravioletti? Che danni possono
- Pale Blue Dot: la Terra vista dallo spazio è un granello nell’universo
- Quando inizia e finisce la primavera?
- Quando inizia e finisce l’estate?
- Quando inizia e finisce l’autunno?
- Quando inizia e finisce l’inverno?
- Differenza tra equinozio e solstizio con date
- Differenza tra massa e peso in fisica ed in medicina
- Teoria del Tempo Fantasma: 297 anni di storia non sono mai esistiti, ora siamo nel 1717
- L’uomo più grasso del mondo pesa 368 kg
- La persona più intelligente al mondo mai esistita nella storia dell’uomo
- Jon Brower Minnoch: quanto è arrivato a pesare l’uomo più grasso del mondo?
- Le 20 droghe più potenti e pericolose al mondo
- Lo scivolo trasparente più alto e pauroso del mondo
- Valeria Levitina pesa 25 kg: è la ragazza più anoressica del mondo [VIDEO]
- Quanto pesa tutta la popolazione mondiale messa assieme?
- Lina Medina è la mamma più giovane al mondo: ha partorito il suo primo figlio a 5 anni
- Bambini scoprono per prima volta la loro ombra
- Arinia: la mancanza congenita del naso
- Il cardiochirurgo stremato dopo un trapianto cardiaco durato 23 ore
- Emette gas intestinali durante l’intervento chirurgico: i risultati sono disastrosi
- Trapianto di faccia: i casi più famosi al mondo
- Ipertimesia: la donna che ricorda tutto da quando è nata
- Ollie, il “bambino Pinocchio” nato con il cervello nel naso
- Sindrome del bambino scosso: i gravissimi danni della violenza sul neonato
- Quanto pesa un litro di acqua liquida o di ghiacciata?
- Differenza tra massa e peso in fisica ed in medicina
- Vi spiego come far entrare sette miliardi di persone nello spazio di una palla da tennis
- La donna più fertile del mondo: 69 figli
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

 Robert Liston (1794-1847) fu un chirurgo scozzese, noto per le sue tecniche pionieristiche. Egli era noto per la sua abilità di chirurgo e per la rapidità di azione, qualità quest’ultima molto importante in un’epoca in cui la velocità delle operazioni era questione di vita o di morte a causa della mancanza di anestesia. Liston divenne primo docente di chirurgia clinica al college di Londra, nel 1835. Egli era in grado di amputare una gamba in 2 minuti e 30 secondi, aumentando le probabilità di sopravvivenza del paziente. Alcune fonti riportano un’amputazione della durata di soli 28 secondi. Robert Liston è stato per questo soprannominato “il coltello più Veloce del West End”.
Robert Liston (1794-1847) fu un chirurgo scozzese, noto per le sue tecniche pionieristiche. Egli era noto per la sua abilità di chirurgo e per la rapidità di azione, qualità quest’ultima molto importante in un’epoca in cui la velocità delle operazioni era questione di vita o di morte a causa della mancanza di anestesia. Liston divenne primo docente di chirurgia clinica al college di Londra, nel 1835. Egli era in grado di amputare una gamba in 2 minuti e 30 secondi, aumentando le probabilità di sopravvivenza del paziente. Alcune fonti riportano un’amputazione della durata di soli 28 secondi. Robert Liston è stato per questo soprannominato “il coltello più Veloce del West End”.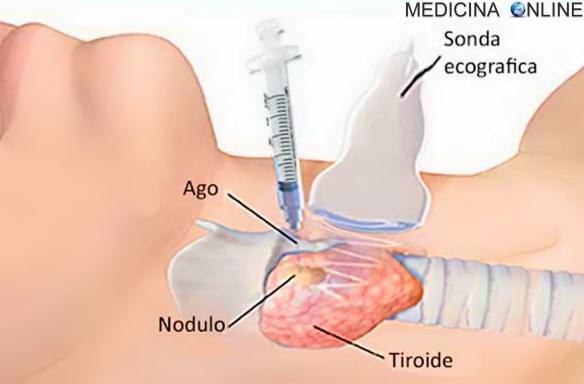
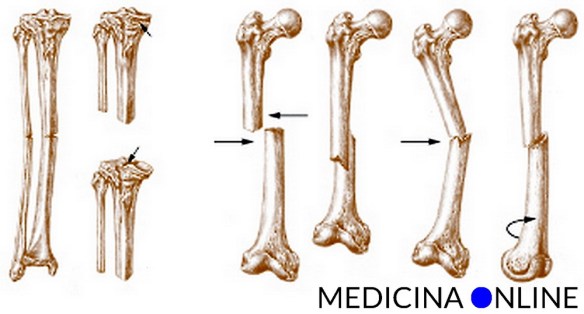 Con frattura si indica, in medicina, l’interruzione parziale o totale della continuità di un osso del corpo, causata da traumi (incidenti stradali, cadute), da patologie (tumore) o da stress (da microtraumi reiterati in un osso con normale resistenza meccanica).
Con frattura si indica, in medicina, l’interruzione parziale o totale della continuità di un osso del corpo, causata da traumi (incidenti stradali, cadute), da patologie (tumore) o da stress (da microtraumi reiterati in un osso con normale resistenza meccanica).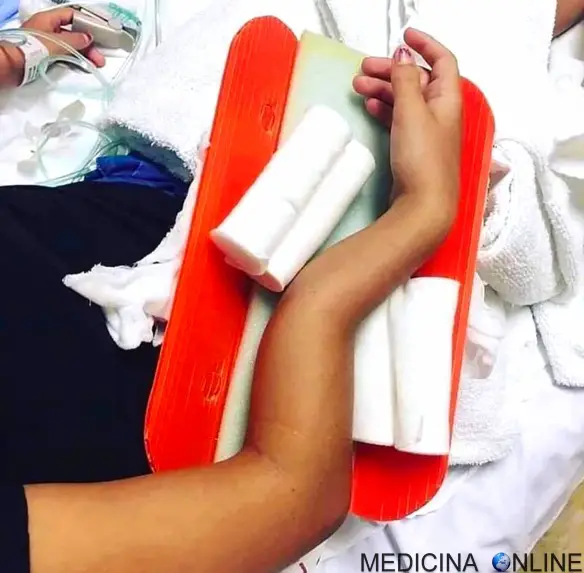
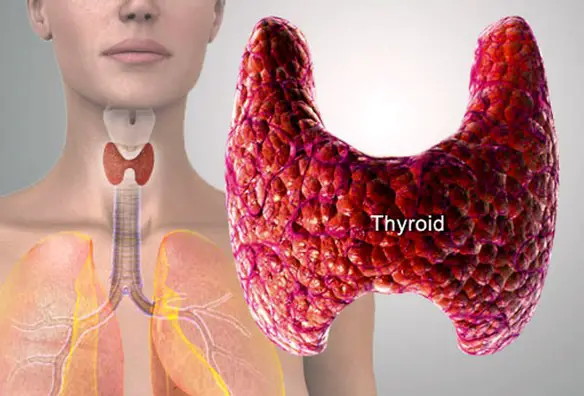 Indicazioni – Perché si usa Eutirox? A cosa serve?
Indicazioni – Perché si usa Eutirox? A cosa serve? L’ipoparatiroidismo è una malattia in cui le paratiroidi non producono quantità sufficienti di ormone paratiroideo (PTH) comportando principalmente l’insorgenza di ipocalcemia; tale deficit di produzione è legato soprattutto a cause iatrogene (lesioni durante interventi chirurgici al collo, ad esempio durante una tiroidectomia totale o parziale) o a cause autoimmunitarie. Una diagnosi precoce permette di limitare gli effetti collaterali dell’ipoparatiroidismo, come problemi ai denti, cataratta e calcificazioni cerebrali. L’ipoparatiroidismo si caratterizza:
L’ipoparatiroidismo è una malattia in cui le paratiroidi non producono quantità sufficienti di ormone paratiroideo (PTH) comportando principalmente l’insorgenza di ipocalcemia; tale deficit di produzione è legato soprattutto a cause iatrogene (lesioni durante interventi chirurgici al collo, ad esempio durante una tiroidectomia totale o parziale) o a cause autoimmunitarie. Una diagnosi precoce permette di limitare gli effetti collaterali dell’ipoparatiroidismo, come problemi ai denti, cataratta e calcificazioni cerebrali. L’ipoparatiroidismo si caratterizza: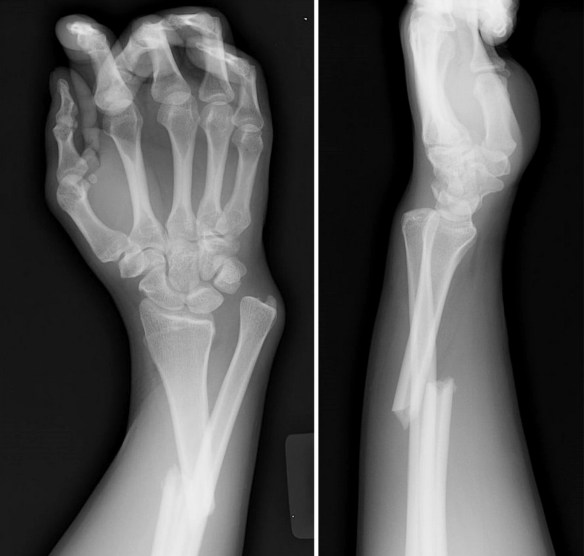 Quando un osso subisce una frattura, in condizioni fisiologiche inizia un processo biologico di riparazione che con il tempo porta alla formazione del “callo osseo”. Il callo osseo è un tessuto di riparazione che viene creato grazie al processo di callogenesi che solitamente si manifesta dopo tre settimane dall’evento traumatico che ha portato alla frattura. Il callo osseo salda i frammenti dell’osso fratturato e si modifica progressivamente modulandosi in risposta alle forze meccaniche esercitate su di esso, diventando sempre più resistente. Nelle settimane o nei mesi seguenti, il callo osseo ricostituisce l’integrità e le normali caratteristiche biomeccaniche del segmento scheletrico lesionato, tuttavia – se il processo di calcificazione subisce un condizionamento o un’interruzione tale da non consentire un consolidamento – è possibile che la frattura non guarisca correttamente. In tale evenienza si ha la formazione di un callo di tipo fibroso che comporta dolore e limitazione funzionale (pseudoartrosi) e, spesso, rende necessario intervenire chirurgicamente. In alcuni casi si può parlare di “ritardo di consolidazione” quando l’osso inizia a formare callo ma impiega più tempo del normale per ultimare la guarigione. La guarigione dell’osso può essere ostacolata da alcuni fattori di rischio preesistenti come ad esempio patologie metaboliche o fumo di sigaretta.
Quando un osso subisce una frattura, in condizioni fisiologiche inizia un processo biologico di riparazione che con il tempo porta alla formazione del “callo osseo”. Il callo osseo è un tessuto di riparazione che viene creato grazie al processo di callogenesi che solitamente si manifesta dopo tre settimane dall’evento traumatico che ha portato alla frattura. Il callo osseo salda i frammenti dell’osso fratturato e si modifica progressivamente modulandosi in risposta alle forze meccaniche esercitate su di esso, diventando sempre più resistente. Nelle settimane o nei mesi seguenti, il callo osseo ricostituisce l’integrità e le normali caratteristiche biomeccaniche del segmento scheletrico lesionato, tuttavia – se il processo di calcificazione subisce un condizionamento o un’interruzione tale da non consentire un consolidamento – è possibile che la frattura non guarisca correttamente. In tale evenienza si ha la formazione di un callo di tipo fibroso che comporta dolore e limitazione funzionale (pseudoartrosi) e, spesso, rende necessario intervenire chirurgicamente. In alcuni casi si può parlare di “ritardo di consolidazione” quando l’osso inizia a formare callo ma impiega più tempo del normale per ultimare la guarigione. La guarigione dell’osso può essere ostacolata da alcuni fattori di rischio preesistenti come ad esempio patologie metaboliche o fumo di sigaretta. I reni possono essere interessati da vari processo morbosi, di interesse sia nefrologico che urologico. Questa distinzione è fondamentale perché in questo modo si distinguono due specialità: il nefrologo e l’urologo. Entrambi sono medici, ma l’urologo è specializzato in urologia mentre il nefrologo può essere specializzato in urologia ma non è raro trovare specialisti in medicina interna o geriatria che si occupano di nefrologia, generalmente grazie a corsi di ultra-specializzazione o master appositi.
I reni possono essere interessati da vari processo morbosi, di interesse sia nefrologico che urologico. Questa distinzione è fondamentale perché in questo modo si distinguono due specialità: il nefrologo e l’urologo. Entrambi sono medici, ma l’urologo è specializzato in urologia mentre il nefrologo può essere specializzato in urologia ma non è raro trovare specialisti in medicina interna o geriatria che si occupano di nefrologia, generalmente grazie a corsi di ultra-specializzazione o master appositi.