 I microrganismi eterotrofi possono essere invece classificati in:
I microrganismi eterotrofi possono essere invece classificati in:
- prototrofi: sono quei microrganismi eterotrofi che sono in grado di sintetizzare tutti i composti organici di cui necessitano;
- auxotrofi: sono quei microrganismi eterotrofi che, in aggiunta ai nutrienti energetici forniti dall’alimentazione, devono necessariamente nutrirsi di uno o più particolari composti organici necessari per la propria crescita in quanto incapaci di sintetizzarli.
I microrganismi eterotrofi possono nutrirsi per:
- ingestione: essi fanne penetrare il cibo all’interno del loro corpo per poi procedere alla sua demolizione enzimatica e al successivo assorbimento delle sostanze ottenute dal processo di demolizione.
- assorbimento: essi demoliscono il cibo al loro esterno per poi assumere le sostanze ottenute dal processo di demolizione facendole passare attraverso la membrana cellulare.
Leggi anche:
- Differenza tra organismi autotrofi ed eterotrofi
- Differenza tra organico inorganico
- Differenza tra virus e batteri: chi è più pericoloso? Diagnosi, sintomi e terapia
- Invasività microbica: la capacità di invadere l’organismo ospite
- Differenza tra invasività clinica e microbica
- Il virus più pericoloso del mondo è più vicino a te di quanto pensi
- Qual è il virus che ha ucciso più persone in assoluto?
- Qual è il virus più letale al mondo?
- Quante persone uccide ogni anno il virus HIV che causa l’AIDS?
- L’insospettabile influenza ogni anno uccide più persone dell’Ebola
- Il virus che uccide mezzo milione di bambini ogni anno
- Febbre gialla, dengue ed altre malattie trasmesse dalle zanzare
- Febbre dengue: sintomi, trasmissione, diagnosi, terapia e prevenzione
- Virus mortali: ecco gli 11 più pericolosi al mondo
- Sierotipo in microbiologia: significato ed importanza per i vaccini
- Differenza tra DNA ed RNA
- I 12 batteri più pericolosi per l’uomo
- Differenza tra microrganismi, batteri, virus, microbi e germi
- Differenza tra funghi, muffe e lieviti
- Differenza tra capside a simmetria icosaedrica, elicoidale e complessa
- Differenza tra unicellulare e pluricellulare con esempi
- Tubercolosi: trasmissione, sintomi, diagnosi e cure in sintesi
- Tubercolosi: cause e patogenesi della malattia
- Mycobacterium tuberculosis: il batterio che causa la tubercolosi
- Sintomi della tubercolosi polmonare ed extrapolmonare
- Come si trasmette la tubercolosi?
- Tubercolosi: diagnosi e progressione della malattia
- Test cutaneo della tubercolina: Test di Mantoux per la tubercolosi
- Trattamento farmacologico per la tubercolosi
- Trattamento della tubercolosi resistente ai farmaci
- Tubercolosi: prognosi, vaccino e strategie di prevenzione
- Virus e virioni: cosa sono, come sono fatti, come funzionano e come si riproducono
- Differenza tra cellula aploide e diploide con esempi
- Riproduzione cellulare e ciclo cellulare
- Mitosi: spiegazione delle quattro fasi
- Meiosi: spiegazione di tutte tappe
- Differenza tra gene e allele
- Differenza tra allele dominante e recessivo
- Differenza tra omozigote ed eterozigote
- Differenza tra genotipo e fenotipo
- Quanti cromosomi hanno esseri umani, scimmie, cani, gatti e topi?
- Quanti cromosomi ha chi è affetto da Sindrome di Down?
- Cos’è un cromosoma ed a che serve?
- Cos’è un gene ed a che serve?
- Cosa sono gli alleli ed a che servono?
- Differenza tra cellule eucariote e procariote
- Differenza tra coronarografia ed angioplastica
- Differenza tra tumore benigno, maligno, neoplasia, cancro e metastasi
- HIV: sintomi iniziali in donne e uomini
- Differenza tra HIV e AIDS: sono uguali?
- Shock settico e sepsi: sintomi, terapia, conseguenze, si può guarire
- Differenza tra sepsi e Sindrome da risposta infiammatoria sistemica (SIRS)
- Meningite: contagio, sintomi, vaccino, gravità e profilassi
- Endocardite: cause, sintomi, diagnosi e terapie
- Differenza tra batteri Gram negativi e Gram positivi
- Differenza tra batteri bacilli, cocchi, streptococchi e spirilli
- Coprocoltura feci per salmonella: perché e come si fa
- Batteriemia: cura, segni, sintomi, diagnosi ed antibiotici
- I cinque segni cardinali dell’infiammazione
- Differenza tra infezione ed infiammazione: sono la stessa cosa?
- Differenza tra infiammazione cronica granulomatosa e non granulomatosa
- Differenza tra granulomi asettici (da corpo estraneo) e settici
- Si muore di AIDS? Qual è l’aspettativa di vita?
- Sistema immunitario, immunità innata e specifica: riassunto, schema e spiegazione
- Immunodeficienza primaria e secondaria: sintomi, cause e terapie
- Immunità innata (aspecifica): barriere, infiammazione e complemento
- Immunità innata (aspecifica): neutrofili, macrofagi e linfociti natural killer
- Immunità specifica (acquisita): linfociti, T killer, T helper, T γδ, B ed anticorpi
- Immunità specifica (acquisita): memoria passiva, attiva ed immunizzazione
- Immunità specifica (acquisita) umorale e cellulare
- Patologie del sistema immunitario: immunodeficienze, autoimmunità ed ipersensibilità
- Anticorpi: (immunoglobuline): tipi, caratteristiche e funzioni
- Dolore: cos’è, da cosa è causato, quanti tipi di dolore esistono?
- Differenza tra sintomo e segno con esempi
- Differenza tra malattia, sindrome e disturbo con esempi
- Differenza tra organismi aerobi obbligati e facoltativi con esempi
- Differenza tra organismi anaerobi obbligati, facoltativi, microaerofili ed aerotolleranti
- Com’è fatto il cuore, a che serve e come funziona?
- La mammografia: un esame rapido che può salvarti la vita
- Ecografia della tiroide: a cosa serve, come si svolge e come ci si prepara all’esame
- Differenza tra prevenzione primaria, secondaria e terziaria con esempi
- Capire se si ha un tumore: come viene diagnosticato un cancro
- La colonscopia: cos’è, quando si fa, che rischi comporta, come ci si prepara ad affrontarla
- L’ecografia transvaginale esplora gli organi genitali interni femminili
- Mineralometria Ossea Computerizzata (MOC), a cosa serve, come si interpretano i risultati?
- Differenza tra pressione arteriosa e venosa
- Differenza tra atri e ventricoli
- Valvole cardiache: cosa sono, quali sono ed a che
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Pressione arteriosa: valori normali e patologici
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure
- Perché la pressione arteriosa alta (ipertensione) è pericolosa?
- Ipertensione: cibi consigliati e da evitare per abbassare la pressione sanguigna
- Qual è la differenza tra arteria e vena?
- Che significa malattia terminale?
- Capire se si ha un tumore: come viene diagnosticato un cancro
- Quanto tempo mi rimane da vivere?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Cure palliative: cosa sono ed a che servono?
- Eccesso di colesterolo (ipercolesterolemia): perché è pericoloso?;
- Pressione alta (ipertensione arteriosa): sintomi, cause, valori e cure;
- Emoglobina glicata alta, valori normali, IFCC e diabete;
- L’obesità è una malattia;
- Differenza tra malattia acuta e cronica con esempi
- Che significa malattia cronica? Esempi di malattia cronica
- Differenza tra adenocarcinoma e carcinoma con esempi
- Differenza tra cancro e carcinoma con esempi
- Stomie: cosa sono, a che servono, quanti tipi esistono?
- Differenza tra ipertrofia muscolare sarcolplasmatica e miofibrillare
- Ipertrofia muscolare: cosa significa e come si raggiunge
- Cosa sono le metastasi? Tutti i tumori danno metastasi?
- Come nasce un cancro? Cosa sono i cancerogeni e come avviene la cancerogenesi?
- Come prevenire i tumori ed il cancro? I 10 cambiamenti consigliati
- Differenza tra ipertrofia ed iperplasia con esempi
- Differenza tra iperplasia e neoplasia
- Un oggetto che tocchi 150 volte al giorno ha più batteri della tavoletta del wc. Di cosa si tratta e come difendersi
- Differenze tra ileostomia, colostomia e urostomia
- Differenza tra atrofia, distrofia ed aplasia con esempi
- Differenza tra organismi aerobi ed anaerobi con esempi
- Ciclo di Krebs e respirazione cellulare: spiegazione facile e schema
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

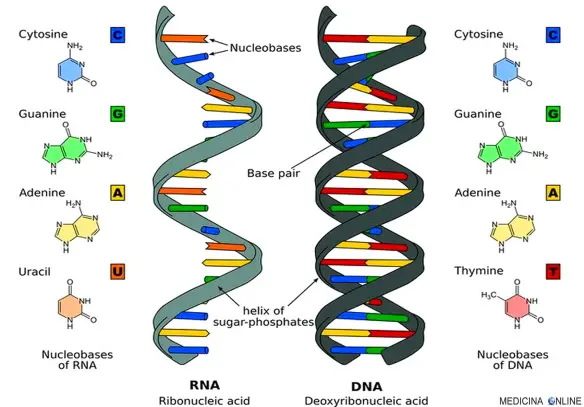 Cos’è il DNA
Cos’è il DNA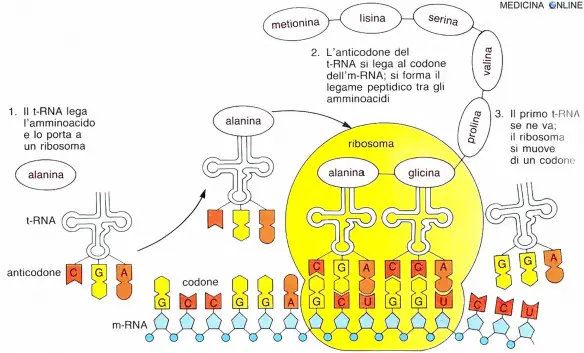
 La proteinuria è la presenza di proteine all’interno dell’urina, il che indica un alterato funzionamento dell’apparato di filtrazione dei reni causato da svariate patologie. La proteinuria può essere di tipo transitorio, persistente od ortostatico.
La proteinuria è la presenza di proteine all’interno dell’urina, il che indica un alterato funzionamento dell’apparato di filtrazione dei reni causato da svariate patologie. La proteinuria può essere di tipo transitorio, persistente od ortostatico. Chimica e fisica sono rami della scienza che studiano la materia. La differenza tra le due risiede nel loro ambito e nel loro approccio. Chimici e fisici ricevono una formazione diversa e hanno diversi ruoli professionali, anche quando operano in squadra. La divisione tra chimica e fisica diventa diffusa nell’interfaccia dei due rami, in particolare in campi come la chimica fisica, la meccanica quantistica, la fisica/chimica nucleare, la scienza dei materiali, la spettroscopia, la fisica dello stato solido, la cristallografia e la nanotecnologia.
Chimica e fisica sono rami della scienza che studiano la materia. La differenza tra le due risiede nel loro ambito e nel loro approccio. Chimici e fisici ricevono una formazione diversa e hanno diversi ruoli professionali, anche quando operano in squadra. La divisione tra chimica e fisica diventa diffusa nell’interfaccia dei due rami, in particolare in campi come la chimica fisica, la meccanica quantistica, la fisica/chimica nucleare, la scienza dei materiali, la spettroscopia, la fisica dello stato solido, la cristallografia e la nanotecnologia. Sono molti i virus letali al mondo. Alcuni esperti hanno stilato una classifica degli 11 più letali:
Sono molti i virus letali al mondo. Alcuni esperti hanno stilato una classifica degli 11 più letali: L’influenza può non suonare molto spaventosa, ma in realtà uccide molte più persone ogni anno dell’Ebola, sebbene il numero esatto di decessi annuali sia oggetto di molte discussioni. La grande variabilità dei decessi annuali nasce dal fatto che molte morti di influenza non sono segnalati come tali.
L’influenza può non suonare molto spaventosa, ma in realtà uccide molte più persone ogni anno dell’Ebola, sebbene il numero esatto di decessi annuali sia oggetto di molte discussioni. La grande variabilità dei decessi annuali nasce dal fatto che molte morti di influenza non sono segnalati come tali. Il fibrinogeno è il nome con il quale si indica una proteina che fa parte del plasma. È conosciuta anche come Fattore I, fibrinogeno attivo e antigene del fibrinogeno. Il nome significa letteralmente “produttore di fibrina”. Infatti, per permettere la coagulazione del sangue, la trombina si trasforma il fibrinogeno in fibrina, dando inizio al processo di coagulazione.
Il fibrinogeno è il nome con il quale si indica una proteina che fa parte del plasma. È conosciuta anche come Fattore I, fibrinogeno attivo e antigene del fibrinogeno. Il nome significa letteralmente “produttore di fibrina”. Infatti, per permettere la coagulazione del sangue, la trombina si trasforma il fibrinogeno in fibrina, dando inizio al processo di coagulazione.