 Lo shock settico, o shock setticemico, è una sindrome da shock dovuta ad una grave infezione con sepsi; la sindrome è sistemica, cioè coinvolge l’intero organismo, anche se l’agente infettante può essere presente solo in un particolare sito corporeo.
Lo shock settico, o shock setticemico, è una sindrome da shock dovuta ad una grave infezione con sepsi; la sindrome è sistemica, cioè coinvolge l’intero organismo, anche se l’agente infettante può essere presente solo in un particolare sito corporeo.
Può causare sindrome da insufficienza multiorgano (MODS) (precedentemente nota come multiple organ failure, MOF) e morte; il tasso di mortalità è circa il 25–50%. Lo shock settico è una situazione di emergenza medica. Per la gravità e la complessità della patologia i pazienti affetti da shock settico necessitano di essere curati in ambiente intensivo.
I sintomi
Lo shock settico provoca un arresto delle funzioni vitali primarie – ovvero, un indebolimento degli organi interni, come polmoni e cuore – e, nei casi più gravi, la morte. I sintomi, nello specifico, includono febbre molto alta che non si abbassa, blocco della diuresi, stato confusionale, diminuzione della pressione sanguigna, difficoltà respiratorie, palpitazioni, ipotermia, tachicardia – che può avere anche altre cause – irrequietezza, fiato corto, brividi, tachipnea, leucocitosi o leucopenia e perdita di coscienza. In alcuni casi, potrebbero essere presenti insufficienza epatica, insufficienza renale e ipotensione grave.
I fattori di rischio
Tra i fattori di rischio, ci sono l’età – anziani e bambini sono a maggior rischio – e il ricovero in ospedale: spesso, infatti, sono proprio coloro che sono già ricoverati in ospedale a contrarre infezioni. Anche malattie che indeboliscono il sistema immunitario possono essere considerate dei fattori di rischio: AIDS, diabete, linfomi, patologie del sistema genito-urinario e intestinale, neoplasie del sangue – come, ad esempio, la leucemia – polmoniti, appendiciti, diverticolite, meningiti, pancreatiti, fascite necrotizzante e pielonefrite.
Leggi anche:
- Differenza tra sepsi e Sindrome da risposta infiammatoria sistemica (SIRS)
- Meningite: contagio, sintomi, vaccino, gravità e profilassi
- Endocardite: cause, sintomi, diagnosi e terapie
- Differenza tra batteri Gram negativi e Gram positivi
Patogenesi
La scoperta, relativamente recente, dei mediatori endogeni della risposta infiammatoria dell’ospite, ha fatto comprendere come clinicamente la sepsi rappresenti il risultato di un eccesso di attivazione dei meccanismi di difesa dell’ospite, piuttosto che l’effetto diretto dei microrganismi. La sepsi e le sue conseguenze sono l’espressione di un continuum evolutivo legate ad un effetto amplificante e moltiplicativo dei vari meccanismi che sottendono la manifestazione clinica e la sua fisiopatologia.
In altri termini le infezioni con o senza batteriemia comportano cambiamenti fisiologici dell’organismo, con risposte del sistema immunitario finalizzate alla soppressione dell’agente infettante. Questi cambiamenti però sono causa di shock (settico), che si manifesta quando un’adeguata somministrazione endovenosa di fluidi non riesce ad aumentare la pressione sanguigna a livelli accettabili, e l’evidenza clinica mostra una ipoperfusione tissutale sistemica; si determina così un cedimento progressivo delle funzioni dei vari organi e successivamente di tutto l’organismo, cioè la sindrome da insufficienza multiorgano, che rappresenta l’estremo del continuum prima citato.
Esiste una cascata di eventi che porta dalla semplice infezione allo shock settico.
- In seguito all’infezione c’è una risposta generalizzata dell’organismo di tipo neuroumorale, pro- e antinfiammatoria;
- Attivazione di monociti, macrofagi e neutrofili che interagiscono con l’endotelio (le cellule della parete dei vasi sanguigni) tramite numerosi recettori attivati dai microrganismi;
- L’attivazione di queste cellule ed il danno endoteliale porta alla mobilizzazione di sostanze plasmatiche come citochine, TNF, interleuchine, caspasi, proteasi, leucotrieni, chinine, radicali liberi dell’Ossigeno, NO, acido arachidonico, PAF (fattore attivante le piastrine) ed eicosanoidi. Questa cascata viene amplificata dall’attivazione del complemento e dalla cascata coagulativa;
- Tale amplificazione porta in definitiva ad un danno endoteliale con gravi problemi del microcircolo, dove si verifica trombosi e perdita dell’integrità capillare;
- Nelle falle a livello capillare si perde una buona parte dei liquidi dell’organismo, per cui esiste sempre un’ipovolemia, cioè una carenza di fluidi corporei. È per questo che è necessaria, almeno all’inizio, la somministrazione di grandi quantità di liquidi;
- La produzione di NO crea vasodilatazione, che aggrava ulteriormente l’ipotensione
Gli eventi finali della combinazione di danno e insufficiente circolazione del microcircolo sono l’ipossiemia e l’ischemia degli organi, che è l’evento finale dello shock settico.
Clinica
Lo shock settico esiste in due forme.
- Ipercinetica precoce, caratterizzata da:
- caduta delle resistenze vascolari periferiche
- differenza arterovenosa in ossigeno diminuita
- cute calda e secca, rosea
- pressione normale o leggermente abbassata
- Ipocinetica, che si distingue per:
- resistenze vascolari periferiche aumentate
- differenza arterovenosa in ossigeno aumentata
- ipotensione arteriosa e venosa
- tachicardia
- oliguria
- cute pallida e sudata.
Una forma particolare di shock settico è la sindrome da shock tossico, nelle sue eziologie:
- da enterotossina F, TSCT-1, tossina prodotta da un ceppo di Stafilococco aureo
- da enterotossina SGA, prodotta dallo Streptococco di gruppo A, spesso complicazione di una fascite o miosite necrotizzante.
Leggi anche:
- Differenza tra batteri bacilli, cocchi, streptococchi e spirilli
- Triade di Virchow: i tre fattori di rischio per la trombosi
- Chetosi: cos’è, da cosa è causata, sintomi e terapia in adulti e bambini
- Coagulazione intravascolare disseminata: cause e trattamenti
- Sepsi: cause, sintomi, diagnosi e terapie
- Differenza tra sepsi e setticemia
- Sindrome da disfunzione multiorgano: cause, sintomi, stadi e cure
- Coprocoltura feci per salmonella: perché e come si fa
Diagnosi differenziale
Nell’uomo, per definizione, la diagnosi di shock settico richiede la presenza contemporanea di diverse condizioni:
- deve essere diagnosticata la presenza di SIRS (systemic inflammatory response syndrome) con almeno due di queste condizioni:
- Tachipnea > 20 respiri per minuto o, all’emogasanalisi, una PCO2 inferiore a 32 mmHg, segno di iperventilazione.
- Conta dei globuli bianchi significativamente bassa (< 4000 cellule/mm³) o elevata (> 12000 cellule/mm³).
- Frequenza cardiaca > 90 battiti al minuto
- Temperatura: febbre > 38.5 °C (101.3 °F) o ipotermia < 35.0 °C (95.0 °F)
- Deve essere presente sepsi, e non una forma alternativa di SIRS; pertanto deve esserci infezione, cioè almeno uno fra:
- emocolture positive
- Segni di polmonite alla Rx del torace
- altri segni radiologici o laboratoristici di infezione
- Deve essere presente almeno un segno di insufficienza d’organo, fra:
- Insufficienza renale
- Insufficienza cardiaca
- Acute lung injury, una forma meno grave di ARDS
- Trombocitopenia
- Coagulopatie
- Disfunzione epatica
- Alterazioni dello stato mentale
- Lattato sierico aumentato.
- Infine, lo shock settico viene diagnosticato quando esiste ipotensione refrattaria al riempimento volemico, vale a dire che la sola somministrazione di liquidi non è sufficiente ad evitare l’ipotensione.
-
- L’ipotensione è definita come una pressione arteriosa sistolica sotto i 90 mmHg, una pressione arteriosa media al di sotto dei 60 mmHg, oppure una riduzione della pressione arteriosa sistolica maggiore di 40 mmHg rispetto ai valori di base, persistente nonostante adeguata somministrazione di liquidi.
Lo shock settico si differenzia quindi da
- batteriemia, caratterizzata dal semplice rilievo, mediante emocoltura, della presenza di batteri nel sangue;
- setticemia, malattia sistemica causata dal batterio o tossina in causa;
- SIRS, sindrome reattiva infiammatoria sistemica;
- sepsi, cioè la copresenza di infezione e SIRS;
- MODS, sindrome da insufficienza multiorgano.
Cure
- Trattamento della malattia sottostante.
- Antibioticoterapia a largo spettro: l’avvio è da farsi dopo prelievo ematico per emocoltura.
- Apporto di liquidi (colloidi, cristalloidi) e, in casi selezionati, glucocorticoidi.
- Normalizzazione della pressione, che spesso richiede l’utilizzo di amine vasoattive.
- Correzione di un’eventuale acidosi metabolica.
- Prevenzione delle complicanze e loro trattamento.
Leggi anche:
- Batteriemia: cura, segni, sintomi, diagnosi ed antibiotici
- I cinque segni cardinali dell’infiammazione
- Differenza tra infezione ed infiammazione: sono la stessa cosa?
- Infiammazione: le alterazioni dei vasi sanguigni, permeabilità vascolare e migrazione leucocitaria
- Differenza tra infezione acuta e cronica
- Morte cellulare: differenza tra necrosi, apoptosi ed autofagia
La prevenzione
La cura migliore è sempre la prevenzione: occorre, infatti, evitare le infezioni – soprattutto, se ci si trova in ospedale – adottando le normali e necessarie norme igieniche nella vita di tutti i giorni. È, inoltre, opportuno evitare il pericolo di antibiotico-resistenza e, dunque, non abusare di medicinali, quando non strettamente necessario.
La prognosi
La prognosi dello shock settico non è molto buona: questa dipende, infatti, da molte varianti, come la malattia scatenante, la tempestività di intervento, la gravità dei sintomi, la cura intrapresa, lo stato di salute del paziente e la sua età. Infine, è bene specificare che non sempre i trattamenti sono sufficienti – in special modo, quando l’organismo è molto indebolito – e la mortalità è abbastanza elevata: in generale, si va dal 30% al 60% dei casi di morte.
Leggi anche:
- Differenza tra virus e batteri: chi è più pericoloso? Diagnosi, sintomi e terapia
- Shock ipovolemico, emorragico, allergico, anafilattico, cardiogeno, ostruttivo, distributivo, settico
- Shock cardiogeno: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock ipovolemico emorragico: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock ipovolemico non emorragico: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock ostruttivo: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock settico e tossico: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock neurogeno: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Shock spinale: cause, sintomi, rischi, diagnosi, terapie, prognosi, morte
- Infestazione: cos’è, da cosa è causata, come si cura
- Differenza tra infezione ed infestazione
- Differenza tra infestazione interna ed esterna
- Differenza tra infiammazione cronica granulomatosa e non granulomatosa
- Differenza tra granulomi asettici (da corpo estraneo) e settici
- Linfonodi: cosa sono, come riconoscerli, quando sono pericolosi
- Linfonodo sentinella: cos’è e perché è importante in caso di cancro
- Biopsia del linfonodo sentinella: a che serve, perché è importante
- Sistema linfatico e linfonodi: anatomia e funzioni in sintesi
- Differenza tra cisti e linfonodo
- Differenza tra cisti, pseudocisti, ascesso ed empiema
- Differenza infiammabile, combustibile, comburente e facilmente infiammabile
- Differenza tra acidosi ed alcalosi, metabolica e respiratoria
- Peritonite: tipi, cause, sintomi, diagnosi e terapie
- Virus e virioni: cosa sono, come sono fatti, come funzionano e come si riproducono
- HIV: dopo quanto si manifestano i sintomi? I 4 stadi dell’infezione
- HIV: sintomi iniziali in donne e uomini
- Differenza tra HIV e AIDS: sono uguali?
- Si muore di AIDS? Qual è l’aspettativa di vita?
- Sistema immunitario, immunità innata e specifica: riassunto, schema e spiegazione
- Immunodeficienza primaria e secondaria: sintomi, cause e terapie
- Immunità innata (aspecifica): barriere, infiammazione e complemento
- Immunità innata (aspecifica): neutrofili, macrofagi e linfociti natural killer
- Immunità specifica (acquisita): linfociti, T killer, T helper, T γδ, B ed anticorpi
- Immunità specifica (acquisita): memoria passiva, attiva ed immunizzazione
- Immunità specifica (acquisita) umorale e cellulare
- Appendicite acuta e cronica: cause, sintomi e terapie
- Differenza tra empiema ed ascesso
- Differenza tra aterosclerosi e arteriosclerosi
- Differenza tra trombo, embolo, coagulo, embolia e trombosi
- Differenza tra arterie, vene, capillari, arteriole e venule
- Differenza tra arteriola afferente ed efferente: struttura e funzioni
- Differenza tra edema infiammatorio, non infiammatorio, essudato, trasudato, idropisìa e idrope
- Cos’è l’Idropisìa?
- Idrope: cause, tipi e terapia
- Cos’è l’edema, come e perché si forma?
- Differenza tra edema localizzato, generalizzato e sistemico
- Differenza tra insufficienza renale acuta, cronica e dialisi
- Crisi respiratoria acuta e rischio di morte: cosa fare?
- Apparato respiratorio: anatomia in sintesi, struttura e funzioni
- Asma bronchiale: spirometria e diagnosi differenzialeAsma bronchiale: spirometria e diagnosi differenziale
- Esofago e trachea: zona, anatomia, rapporti e differenze
- Spirometria diretta ed indiretta: come si esegue ed a cosa serve
- Differenza tra BPCO ed asma: terapia e sintomi comuni e diversi
- Broncopneumopatia cronica ostruttiva (BPCO): sintomi, diagnosi e cura
- Asma bronchiale in bambini e adulti: cause, sintomi e cura
- Differenza tra inspirazione e espirazione: l’atto respiratorio
- Tumore al polmone in chi non fuma: da cosa viene causato?
- Differenza tra ventilazione polmonare e alveolare: spazio morto anatomico e fisiologico
- Broncoscopia polmonare con biopsia: a cosa serve, fa male, è pericolosa?
- Tutti gli articoli sullo smettere di fumare
- Enfisema polmonare: sintomi, tipi, cause, diagnosi e terapia
- Alveoli polmonari: cosa sono e che funzioni svolgono?
- Enfisema polmonare: cure, complicazioni, quando chiamare il medico
- Spirometria diretta ed indiretta: come si esegue ed a cosa serve
- Che significa malattia autoimmune? Spiegazione ed esempi
- Parametri della spirometria: capacità, volumi, rapporti e flussi
- Polmoni: anatomia e funzioni in sintesi
- Differenza tra laringe, faringe e trachea
- Pneumotorace spontaneo primario, secondario ed iperteso: cause, sintomi, terapie
- Sangue dal naso (epistassi) in bambini e adulti: cause, rimedi naturali, cosa fare e cosa NON fare
- Differenza tra dispnea, apnea e tachipnea
- Differenza apnea statica, dinamica e profonda
- Differenza tra ipossiemia, ipossia ed anossia
- Differenza tra ipossiemia e ipercapnia
- Differenza tra insufficienza respiratoria di tipo 1 e 2
- Differenza tra costola incrinata e rotta
- Cos’è una costa? Differenza tra costole e coste
- Gabbia toracica: dove si trova, a che serve e da cosa è composta
- Costola rotta (frattura costale): sintomi, diagnosi e terapia
- Costola incrinata: sintomi, terapia e tempi di recupero
- Differenza tra costole e vertebre
- Muscoli respiratori volontari ed involontari
- Frattura costale multipla, volet costale e pneumotorace
- Invasività microbica: la capacità di invadere l’organismo ospite
- Differenza tra invasività clinica e microbica
- Il virus più pericoloso del mondo è più vicino a te di quanto pensi
- Qual è il virus che ha ucciso più persone in assoluto?
- Qual è il virus più letale al mondo?
- Quante persone uccide ogni anno il virus HIV che causa l’AIDS?
- L’insospettabile influenza ogni anno uccide più persone dell’Ebola
- Il virus che uccide mezzo milione di bambini ogni anno
- Febbre gialla, dengue ed altre malattie trasmesse dalle zanzare
- Febbre dengue: sintomi, trasmissione, diagnosi, terapia e prevenzione
- Virus mortali: ecco gli 11 più pericolosi al mondo
- Sierotipo in microbiologia: significato ed importanza per i vaccini
- Differenza tra DNA ed RNA
- Differenza tra organismi autotrofi ed eterotrofi
- Differenza tra organismi prototrofi ed auxotrofi
- Differenza tra organico inorganico
- I 12 batteri più pericolosi per l’uomo
- Differenza tra microrganismi, batteri, virus, microbi e germi
- Differenza tra funghi, muffe e lieviti
- Differenza tra capside a simmetria icosaedrica, elicoidale e complessa
- Differenza tra unicellulare e pluricellulare con esempi
- Tubercolosi: trasmissione, sintomi, diagnosi e cure in sintesi
- Tubercolosi: cause e patogenesi della malattia
- Mycobacterium tuberculosis: il batterio che causa la tubercolosi
- Sintomi della tubercolosi polmonare ed extrapolmonare
- Come si trasmette la tubercolosi?
- Tubercolosi: diagnosi e progressione della malattia
- Test cutaneo della tubercolina: Test di Mantoux per la tubercolosi
- Trattamento farmacologico per la tubercolosi
- Trattamento della tubercolosi resistente ai farmaci
- Tubercolosi: prognosi, vaccino e strategie di prevenzione
- Papilloma vescicale: virus, sintomi, vaccino e cure
- Virus del papilloma (HPV): tipi più pericolosi ed a basso rischio
- Come si contrae il Virus del papilloma (HPV)?
- Infezione da Virus del papilloma, gravidanza e problemi al feto
- Trattamento del Virus del papilloma (HPV)
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

 La chetosi o acetonemia (termine più conosciuto nella manifestazione infantile) è il sintomo di un alterato metabolismo degli acidi grassi. La chetosi fisiologica o alimentare si manifesta durante il digiuno prolungato (dopo 2-3 giorni) e durante una privazione di carboidrati alimentari a lungo termine. La chetosi patologica o diabetica si manifesta prevalentemente nei pazienti diabetici.
La chetosi o acetonemia (termine più conosciuto nella manifestazione infantile) è il sintomo di un alterato metabolismo degli acidi grassi. La chetosi fisiologica o alimentare si manifesta durante il digiuno prolungato (dopo 2-3 giorni) e durante una privazione di carboidrati alimentari a lungo termine. La chetosi patologica o diabetica si manifesta prevalentemente nei pazienti diabetici.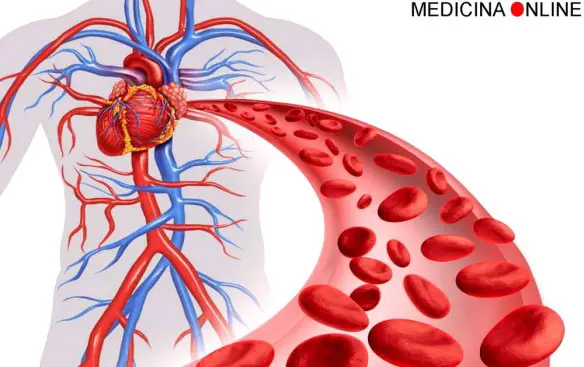 La volemia (volume totale del sangue, quindi sia del plasma sia degli elementi figurati) normale degli esseri umani corrisponde a 77 ml/Kg di peso corporeo (può essere lievemente inferiore in anziani ed obesi) e si può calcolare partendo dall’ematocrito e dal volume del plasma.
La volemia (volume totale del sangue, quindi sia del plasma sia degli elementi figurati) normale degli esseri umani corrisponde a 77 ml/Kg di peso corporeo (può essere lievemente inferiore in anziani ed obesi) e si può calcolare partendo dall’ematocrito e dal volume del plasma. Eziologia della tubercolosi
Eziologia della tubercolosi Gli indici corpuscolari sono rappresentati dal volume cellulare medio (
Gli indici corpuscolari sono rappresentati dal volume cellulare medio (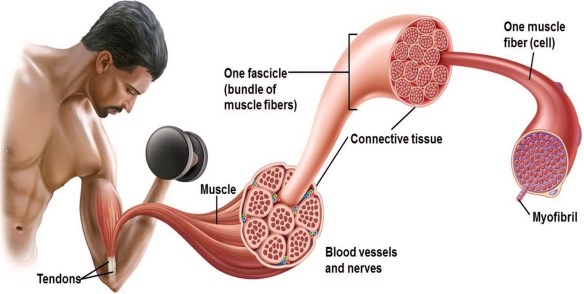 La creatinina è una sostanza che deriva dalla degradazione della creatina (1-Methylhydantoin-2-Imide). La creatina è una proteina che si trova nei muscoli scheletrici ed è fondamentale per i processi che portano al movimento e alla contrazione muscolare dal momento che ha la funzione principale di immagazzinare energia nel muscolo (ad uno dei suoi gruppi azoto gli si può attaccare l’ATP, trasformandola in fosfocreatina o creatin-fosfato). Nel corso delle reazioni energetiche che avvengono durante la contrazione muscolare, una parte della creatina stessa viene trasformata in creatinina che passa nel sangue e viene poi eliminata tramite i reni.
La creatinina è una sostanza che deriva dalla degradazione della creatina (1-Methylhydantoin-2-Imide). La creatina è una proteina che si trova nei muscoli scheletrici ed è fondamentale per i processi che portano al movimento e alla contrazione muscolare dal momento che ha la funzione principale di immagazzinare energia nel muscolo (ad uno dei suoi gruppi azoto gli si può attaccare l’ATP, trasformandola in fosfocreatina o creatin-fosfato). Nel corso delle reazioni energetiche che avvengono durante la contrazione muscolare, una parte della creatina stessa viene trasformata in creatinina che passa nel sangue e viene poi eliminata tramite i reni. Le anemie sono un gruppo di patologie caratterizzate dalla diminuzione di livelli di emoglobina. Un tipo di anemia è quella emolitica, che trova la sua origine in una emolisi (distruzione di massa dei globuli rossi) che si ripete a intervalli talmente ravvicinati da non essere controbilanciata dalla produzione di nuovi globuli rossi, da parte del midollo osseo. L’attacco agli eritrociti spesso è compiuto da anticorpi, prodotti dallo stesso organismo, che pongono fine in modo precoce alla vita degli eritrociti. Oltre a malattie autoimmuni e ad alcune patologie ematologiche, le anemie emolitiche possono essere provocate da certe sostanze aggressive, come quelle contenute in determinati preparati deputati alla cura di infezioni. Tra le principali anemie emolitiche, ricordiamo l’anemia falciforme e le talassemie: in quest’ultimo gruppo trova posto l’anemia mediterranea.
Le anemie sono un gruppo di patologie caratterizzate dalla diminuzione di livelli di emoglobina. Un tipo di anemia è quella emolitica, che trova la sua origine in una emolisi (distruzione di massa dei globuli rossi) che si ripete a intervalli talmente ravvicinati da non essere controbilanciata dalla produzione di nuovi globuli rossi, da parte del midollo osseo. L’attacco agli eritrociti spesso è compiuto da anticorpi, prodotti dallo stesso organismo, che pongono fine in modo precoce alla vita degli eritrociti. Oltre a malattie autoimmuni e ad alcune patologie ematologiche, le anemie emolitiche possono essere provocate da certe sostanze aggressive, come quelle contenute in determinati preparati deputati alla cura di infezioni. Tra le principali anemie emolitiche, ricordiamo l’anemia falciforme e le talassemie: in quest’ultimo gruppo trova posto l’anemia mediterranea. L’emoglobina una proteina solubile di colore rosso che troviamo nei globuli rossi del sangue; la sua funzione è quella di trasporto dell’ossigeno in tutti i tessuti dell’organismo.
L’emoglobina una proteina solubile di colore rosso che troviamo nei globuli rossi del sangue; la sua funzione è quella di trasporto dell’ossigeno in tutti i tessuti dell’organismo.