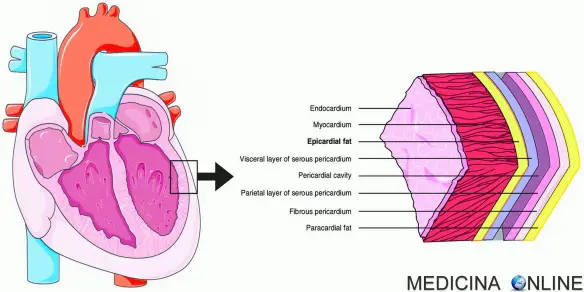
 Per endocardite si intende uno stato infiammatorio dell’endocardio, il tessuto che riveste le cavità interne e le valvole del cuore; in particolare i tessuti endocardici maggiormente coinvolti nella malattia infettiva risultano essere le valvole cardiache.
Per endocardite si intende uno stato infiammatorio dell’endocardio, il tessuto che riveste le cavità interne e le valvole del cuore; in particolare i tessuti endocardici maggiormente coinvolti nella malattia infettiva risultano essere le valvole cardiache.
Epidemiologia
L’incidenza rimane costante negli ultimi anni attestandosi a 3 casi su 100.000 persone, mentre in passato (si parla degli anni intorno al 1950) era leggermente più alta (si arrivava a 4,2). Risulta più colpito il sesso maschile e, nella maggioranza dei casi, l’età con maggiori manifestazioni è quella che parte dalla quinta decade.
Infanzia
L’incidenza della malattia risulta in continua crescita per quanto riguarda i neonati e i bambini (1 su 4.500, mentre è molto più bassa nei Paesi Bassi). Quando sono coinvolti i nascituri il rischio di mortalità è molto elevato.
Leggi anche:
- Differenza tra virus e batteri: chi è più pericoloso? Diagnosi, sintomi e terapia
- Shock settico e sepsi: sintomi, terapia, conseguenze, si può guarire
Fattori di rischio
Costituiscono fattori di rischio molte malattie cardiache e altre condizioni fra cui:
- Prolasso valvolare mitralico, soprattutto se associato a insufficienza della valvola (rigurgito di sangue dal ventricolo sinistro all’atrio sinistro)
- Nell’anziano esiti di cardiopatia reumatica (7-18%), valvola aortica bicuspide, stenosi e calcificazioni valvolari degenerative.
- Cardiopatie congenite, trilogia e tetralogia di Fallot, pervietà di setto atriale o ventricolare, stenosi della polmonare isolata, valvola aortica bicuspide.
- Sindrome di Marfan, per predisposizione a prolasso e insufficienza mitralica
- Esiti di infarto del miocardio
- Nutrizione parenterale continua, catetere venoso centrale
- Tossicodipendenza, con maggiore manifestazione del cuore destro.
- Pazienti portatori di protesi valvolari, soprattutto se diabetici e/o immunodepressi.
Cause
Si distinguono due macrocategorie eziologiche: cause infettive e cause non infettive. Queste ultime, più rare, si caratterizzano per emocoltura negativa e per la presenza di vegetazioni endocardiche sterili; tra queste, la più importante è sindrome di Libman-Sacks, estrinsecazione endocardica del lupus eritematoso sistemico. Nei soggetti anziani, affetti da carcinomi metastatici può presentarsi una “endocardite marantica”, soprattutto in presenza di adenocarcinoma mucinoso o di sindrome di Trousseau. L’eziologia della endocarditi infettive varia in base all’età e alle condizioni predisponenti. I due generi batterici più frequenti sono lo Staphylococcus e lo Streptococcus. Tra i primi è di particolare importanza lo Staphylococcus aureus, molto spesso correlato a procedure invasive e in grado di infettare valvole native. Gli stafilococchi coagulasi negativi (come Staphylococcus epidermidis, Staphylococcus lugdunensis, Staphylococcus hominis) insorgono invece più frequentemente su valvole protesiche. Tra gli streptococchi assumono particolare importanza gli streptococchi di gruppo D (come Streptococcus bovis, Streptococcus galloliticus, presenti nel tratto gastrointestinale) e gli streptococchi viridanti (come Streptococcus mutans, Streptococcus oralis, Streptococcus salivarius, presenti nel cavo orale), entrambi genere in grado di infettare valvole native o protesiche. Occorre inoltre ricordare che un ampio gruppo di batteri possono provocare endocardite, tra questi:
- Enterococcus faecalis
- Pseudomonas aeruginosa, soprattutto nei tossicodipendenti
- Enterobacteriaceae
- Neisseria
- Brucella
- Yersinia
- Listeria
- Coxiella
- Bacterioides
- Acinetobacter
- Corynebacterium
Deve essere altresì ricordato che un’endocardite infettiva può essere sostenuta da Candida albicans, soprattutto in soggetti immunocompromessi, sottoposti a intervento cardiochirurgico o in terapia endovenosa attraverso catetere venoso centrale.
Leggi anche:
- Differenza tra sepsi e Sindrome da risposta infiammatoria sistemica (SIRS)
- Meningite: contagio, sintomi, vaccino, gravità e profilassi
Sintomi e segni
Molti sono i sintomi e i segni clinici che si riscontrano nelle persone affette da questa patologia.
- Manifestazioni maggiori: febbre, anemia (talora piastrinopenia), sudorazione, sensazione di brivido;
- Manifestazioni minori: snoressia, astenia, artralgie (40% dei casi), splenomegalia (30% dei casi), emboli settici (30% dei casi) in cute, palato e congiuntive, con segni caratteristici come noduli periungueali di Osler, macchie cutanee a fiamma di Janeway, lesioni retiniche di Roth, leucocitosi. Possono inoltre manifestarsi infarti embolici renali, glomerulonefrite focale o diffusa e altre patologie da immunocomplessi
Diagnosi
La diagnosi si pone con almeno due su tre dei criteri maggiori:
- Ecocardiogramma – che presenta vegetazioni valvolari
- Coltura positiva per stafilococchi o streptococchi
- Presenze di un soffio cardiaco generato da valvulopatia endocarditica.
La diagnosi si può porre anche con uno solo dei criteri maggiori (ECOcardio, coltura positiva, nuovo soffio cardiaco) e almeno tre tra le varie manifestazioni minori.
Terapia
Il trattamento da seguire per tale malattia è molto studiato in letteratura ma rimane ancora controverso, preferendo un intervento chirurgico di resezione e sostituzione valvolare.
Leggi anche:
- Sepsi: cause, sintomi, diagnosi e terapie
- Differenza tra sepsi e setticemia
- Sindrome da disfunzione multiorgano: cause, sintomi, stadi e cure
- Coprocoltura feci per salmonella: perché e come si fa
- Batteriemia: cura, segni, sintomi, diagnosi ed antibiotici
- Differenza tra batteri Gram negativi e Gram positivi
- Differenza tra batteri bacilli, cocchi, streptococchi e spirilli
- Triade di Virchow: i tre fattori di rischio per la trombosi
- Chetosi: cos’è, da cosa è causata, sintomi e terapia in adulti e bambini
- Coagulazione intravascolare disseminata: cause e trattamenti
- I cinque segni cardinali dell’infiammazione
- Differenza tra infezione ed infiammazione: sono la stessa cosa?
- Infiammazione: le alterazioni dei vasi sanguigni, permeabilità vascolare e migrazione leucocitaria
- Differenza tra infezione acuta e cronica
- Morte cellulare: differenza tra necrosi, apoptosi ed autofagia
- Infestazione: cos’è, da cosa è causata, come si cura
- Differenza tra infezione ed infestazione
- Differenza tra infestazione interna ed esterna
- Differenza tra infiammazione cronica granulomatosa e non granulomatosa
- Differenza tra granulomi asettici (da corpo estraneo) e settici
- Linfonodi: cosa sono, come riconoscerli, quando sono pericolosi
- Linfonodo sentinella: cos’è e perché è importante in caso di cancro
- Biopsia del linfonodo sentinella: a che serve, perché è importante
- Sistema linfatico e linfonodi: anatomia e funzioni in sintesi
- Differenza tra cisti e linfonodo
- Differenza tra cisti, pseudocisti, ascesso ed empiema
- Differenza infiammabile, combustibile, comburente e facilmente infiammabile
- Differenza tra acidosi ed alcalosi, metabolica e respiratoria
- Peritonite: tipi, cause, sintomi, diagnosi e terapie
- Appendicite acuta e cronica: cause, sintomi e terapie
- Differenza tra empiema ed ascesso
- Virus e virioni: cosa sono, come sono fatti, come funzionano e come si riproducono
- HIV: dopo quanto si manifestano i sintomi? I 4 stadi dell’infezione
- HIV: sintomi iniziali in donne e uomini
- Differenza tra HIV e AIDS: sono uguali?
- Si muore di AIDS? Qual è l’aspettativa di vita?
- Sistema immunitario, immunità innata e specifica: riassunto, schema e spiegazione
- Immunodeficienza primaria e secondaria: sintomi, cause e terapie
- Immunità innata (aspecifica): barriere, infiammazione e complemento
- Immunità innata (aspecifica): neutrofili, macrofagi e linfociti natural killer
- Immunità specifica (acquisita): linfociti, T killer, T helper, T γδ, B ed anticorpi
- Immunità specifica (acquisita): memoria passiva, attiva ed immunizzazione
- Immunità specifica (acquisita) umorale e cellulare
- Differenza tra aterosclerosi e arteriosclerosi
- Differenza tra trombo, embolo, coagulo, embolia e trombosi
- Differenza tra arterie, vene, capillari, arteriole e venule
- Differenza tra arteriola afferente ed efferente: struttura e funzioni
- Differenza tra edema infiammatorio, non infiammatorio, essudato, trasudato, idropisìa e idrope
- Cos’è l’Idropisìa?
- Idrope: cause, tipi e terapia
- Cos’è l’edema, come e perché si forma?
- Differenza tra edema localizzato, generalizzato e sistemico
- Differenza tra insufficienza renale acuta, cronica e dialisi
- Crisi respiratoria acuta e rischio di morte: cosa fare?
- Apparato respiratorio: anatomia in sintesi, struttura e funzioni
- Asma bronchiale: spirometria e diagnosi differenzialeAsma bronchiale: spirometria e diagnosi differenziale
- Esofago e trachea: zona, anatomia, rapporti e differenze
- Spirometria diretta ed indiretta: come si esegue ed a cosa serve
- Differenza tra BPCO ed asma: terapia e sintomi comuni e diversi
- Broncopneumopatia cronica ostruttiva (BPCO): sintomi, diagnosi e cura
- Asma bronchiale in bambini e adulti: cause, sintomi e cura
- Differenza tra inspirazione e espirazione: l’atto respiratorio
- Tumore al polmone in chi non fuma: da cosa viene causato?
- Differenza tra ventilazione polmonare e alveolare: spazio morto anatomico e fisiologico
- Broncoscopia polmonare con biopsia: a cosa serve, fa male, è pericolosa?
- Tutti gli articoli sullo smettere di fumare
- Enfisema polmonare: sintomi, tipi, cause, diagnosi e terapia
- Alveoli polmonari: cosa sono e che funzioni svolgono?
- Enfisema polmonare: cure, complicazioni, quando chiamare il medico
- Spirometria diretta ed indiretta: come si esegue ed a cosa serve
- Che significa malattia autoimmune? Spiegazione ed esempi
- Parametri della spirometria: capacità, volumi, rapporti e flussi
- Polmoni: anatomia e funzioni in sintesi
- Differenza tra laringe, faringe e trachea
- Pneumotorace spontaneo primario, secondario ed iperteso: cause, sintomi, terapie
- Sangue dal naso (epistassi) in bambini e adulti: cause, rimedi naturali, cosa fare e cosa NON fare
- Differenza tra dispnea, apnea e tachipnea
- Differenza apnea statica, dinamica e profonda
- Differenza tra ipossiemia, ipossia ed anossia
- Differenza tra ipossiemia e ipercapnia
- Differenza tra insufficienza respiratoria di tipo 1 e 2
- Differenza tra costola incrinata e rotta
- Cos’è una costa? Differenza tra costole e coste
- Gabbia toracica: dove si trova, a che serve e da cosa è composta
- Costola rotta (frattura costale): sintomi, diagnosi e terapia
- Costola incrinata: sintomi, terapia e tempi di recupero
- Differenza tra costole e vertebre
- Muscoli respiratori volontari ed involontari
- Frattura costale multipla, volet costale e pneumotorace
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn e su Pinterest, grazie!

 La microcitemia è un particolare tipo di anemia congenita (ossia l’individuo nasce già con questa malattia), dovuta ad una alterazione genetica per cui l’emoglobina (i “mattoni” con cui sono costruiti i globuli rossi) è alterata.
La microcitemia è un particolare tipo di anemia congenita (ossia l’individuo nasce già con questa malattia), dovuta ad una alterazione genetica per cui l’emoglobina (i “mattoni” con cui sono costruiti i globuli rossi) è alterata. Il pandoro contiene mediamente 410 calorie per 100 grammi; per quanto riguarda i carboidrati tutte tre le versioni del dolce si aggirano intorno ai 45-50 grammi, mentre i grassi corrispondono a circa 19-20 grammi.
Il pandoro contiene mediamente 410 calorie per 100 grammi; per quanto riguarda i carboidrati tutte tre le versioni del dolce si aggirano intorno ai 45-50 grammi, mentre i grassi corrispondono a circa 19-20 grammi.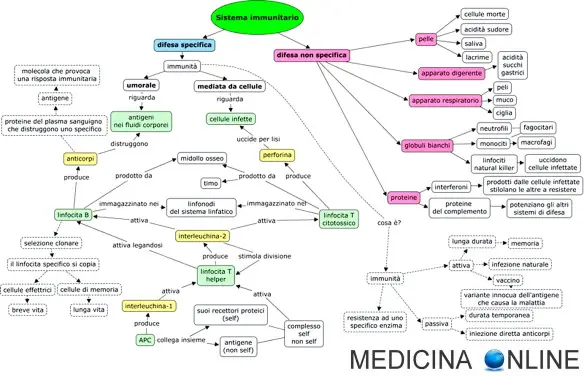 I microrganismi o le tossine che entrano con successo nell’organismo, incontrano le cellule e dei processi del sistema immunitario innato. Solitamente, la risposta innata si attiva quando i microbi vengono identificati dai Pattern Recognition Receptors (PRR), in grado di riconoscere i componenti dei grandi gruppi di microrganismi, le eventuali cellule danneggiate o stressati, inviando segnali di allarme. Le difese immunitarie innate sono dunque “non-specifiche”, il che significa questi sistemi rispondono agli agenti patogeni in modo generico. Questo sistema non conferisce immunità duratura contro un patogeno. Nella maggior parte degli organismi viventi, il sistema immunitario innato è il sistema dominante della difesa.
I microrganismi o le tossine che entrano con successo nell’organismo, incontrano le cellule e dei processi del sistema immunitario innato. Solitamente, la risposta innata si attiva quando i microbi vengono identificati dai Pattern Recognition Receptors (PRR), in grado di riconoscere i componenti dei grandi gruppi di microrganismi, le eventuali cellule danneggiate o stressati, inviando segnali di allarme. Le difese immunitarie innate sono dunque “non-specifiche”, il che significa questi sistemi rispondono agli agenti patogeni in modo generico. Questo sistema non conferisce immunità duratura contro un patogeno. Nella maggior parte degli organismi viventi, il sistema immunitario innato è il sistema dominante della difesa. I microrganismi o le tossine che entrano con successo nell’organismo, incontrano le cellule e dei processi del sistema immunitario innato. Solitamente, la risposta innata si attiva quando i microbi vengono identificati dai Pattern Recognition Receptors (PRR), in grado di riconoscere i componenti dei grandi gruppi di microrganismi, le eventuali cellule danneggiate o stressati, inviando segnali di allarme. Le difese immunitarie innate sono dunque “non-specifiche”, il che significa questi sistemi rispondono agli agenti patogeni in modo generico. Questo sistema non conferisce immunità duratura contro un patogeno. Nella maggior parte degli organismi viventi, il sistema immunitario innato è il sistema dominante della difesa.
I microrganismi o le tossine che entrano con successo nell’organismo, incontrano le cellule e dei processi del sistema immunitario innato. Solitamente, la risposta innata si attiva quando i microbi vengono identificati dai Pattern Recognition Receptors (PRR), in grado di riconoscere i componenti dei grandi gruppi di microrganismi, le eventuali cellule danneggiate o stressati, inviando segnali di allarme. Le difese immunitarie innate sono dunque “non-specifiche”, il che significa questi sistemi rispondono agli agenti patogeni in modo generico. Questo sistema non conferisce immunità duratura contro un patogeno. Nella maggior parte degli organismi viventi, il sistema immunitario innato è il sistema dominante della difesa.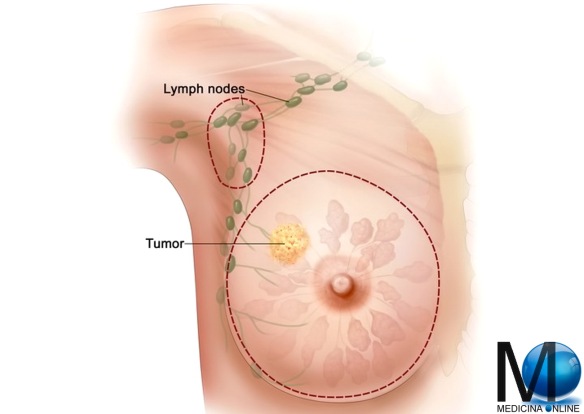 La biopsia del linfonodo sentinella è un metodo efficace per scoprire se il tumore si è propagato fino ai linfonodi vicini, indicando quindi una prognosi peggiore. Può essere eseguito durante l’intervento chirurgico principale o, in alcuni casi, prima di quest’ultimo. La biopsia del linfonodo sentinella consiste nell’iniettare, alcune ore prima, una piccola quantità di liquido radioattivo o di colorante vitale nella zona del seno vicino al tumore. Il liquido iniettato raggiunge il linfonodo sentinella che è il 1° filtro ad essere eventualmente raggiunto dalle cellule tumorali. Il linfonodo sentinella viene identificato al momento della biopsia mediante una sonda radioguidata. Essa viene passata lentamente in corrispondenza dei linfonodi dell’ascella (in caso di tumore alla mammella), e individua la zona ascellare di maggiore emissione del segnale radioattivo. Il linfonodo (o linfonodi) così identificati sono rimossi ed esaminati.
La biopsia del linfonodo sentinella è un metodo efficace per scoprire se il tumore si è propagato fino ai linfonodi vicini, indicando quindi una prognosi peggiore. Può essere eseguito durante l’intervento chirurgico principale o, in alcuni casi, prima di quest’ultimo. La biopsia del linfonodo sentinella consiste nell’iniettare, alcune ore prima, una piccola quantità di liquido radioattivo o di colorante vitale nella zona del seno vicino al tumore. Il liquido iniettato raggiunge il linfonodo sentinella che è il 1° filtro ad essere eventualmente raggiunto dalle cellule tumorali. Il linfonodo sentinella viene identificato al momento della biopsia mediante una sonda radioguidata. Essa viene passata lentamente in corrispondenza dei linfonodi dell’ascella (in caso di tumore alla mammella), e individua la zona ascellare di maggiore emissione del segnale radioattivo. Il linfonodo (o linfonodi) così identificati sono rimossi ed esaminati. Il glutammato monosodico o, più semplicmente “gluttamato”, è il sale di sodio dell’acido glutammico, uno dei 23 amminoacidi naturali che costituiscono le proteine. E’ il responsabile di uno dei cinque gusti principali delle papille gustative della lingua, il gusto “umami”, che corrisponde grossolanamente a “saporito”.
Il glutammato monosodico o, più semplicmente “gluttamato”, è il sale di sodio dell’acido glutammico, uno dei 23 amminoacidi naturali che costituiscono le proteine. E’ il responsabile di uno dei cinque gusti principali delle papille gustative della lingua, il gusto “umami”, che corrisponde grossolanamente a “saporito”.