 Quella nella foto qui sopra sono io: Stella. Sono più vicina ai 40 che ai 30, sono fidanzata, di lavoro faccio la stylist e sono una transessuale. Mi sono rifatta il naso, ho eliminato barba e peli con la luce pulsata, prendo ormoni femminili, e poche settimane fa ho fatto la mastoplastica additiva, una quarta coppa D. Ma mi fermerò qui. Come la maggior parte delle transessuali, non interverrò chirurgicamente sui miei organi genitali. Mi vanno benissimo così. Ho un ottimo rapporto con il mio pene. E finalmente adesso sono quello che ho sempre voluto essere. Non un uomo. Non una donna. Ma una transessuale. Ci ho messo più di vent’anni ad arrivare dove sono ora. A capirmi, a prendere coraggio delle mie azioni, a sbagliare, a ricominciare. Sono stati anni duri. Anni disperati, di depressione, e intensi, di serate ed eccessi. Ma anche anni belli. A volte guardo le ragazze transessuali più giovani, persone che hanno 15 anni meno di me, e che hanno già fatto tutto (ormoni, epilazione, seno), e mi sento una stupida per aver sprecato tutto questo tempo. Perché non l’ho fatto prima? Non lo so. Non lo so proprio. Ognuno ha il suo cammino da fare, immagino. Quello che leggi qui è il mio.
Quella nella foto qui sopra sono io: Stella. Sono più vicina ai 40 che ai 30, sono fidanzata, di lavoro faccio la stylist e sono una transessuale. Mi sono rifatta il naso, ho eliminato barba e peli con la luce pulsata, prendo ormoni femminili, e poche settimane fa ho fatto la mastoplastica additiva, una quarta coppa D. Ma mi fermerò qui. Come la maggior parte delle transessuali, non interverrò chirurgicamente sui miei organi genitali. Mi vanno benissimo così. Ho un ottimo rapporto con il mio pene. E finalmente adesso sono quello che ho sempre voluto essere. Non un uomo. Non una donna. Ma una transessuale. Ci ho messo più di vent’anni ad arrivare dove sono ora. A capirmi, a prendere coraggio delle mie azioni, a sbagliare, a ricominciare. Sono stati anni duri. Anni disperati, di depressione, e intensi, di serate ed eccessi. Ma anche anni belli. A volte guardo le ragazze transessuali più giovani, persone che hanno 15 anni meno di me, e che hanno già fatto tutto (ormoni, epilazione, seno), e mi sento una stupida per aver sprecato tutto questo tempo. Perché non l’ho fatto prima? Non lo so. Non lo so proprio. Ognuno ha il suo cammino da fare, immagino. Quello che leggi qui è il mio.
CHE LE DONNE NON MI PIACESSERO, MI È STATO CHIARO FIN DALL’INIZIO
Ero in quarta, quinta elementare e già prendevo le mie cottarelle per i compagni maschi. Ma per il resto (sono uomo o donna?), buio totale. Non sapevo neppure che esistessero i transessuali. Sapevo solo che avevo delle fantasie: avevo 12 anni, guardavo Madonna nel video di Material Girl e pensavo: «Che figa. Io voglio essere così». Guardavo Guesch Patti che cantava Étienne, con il suo look Anni 40 (longuette, camicia bianca. Sotto: un corpetto, un body, giarrettiere) e mi dicevo: «Magari essere lei, una donna di potere, bella, determinata. Una femme fatale. Supersexy». Da adolescente, andavo a cena con i miei amici, alle serate, ai pranzi di famiglia, mi mettevo in un angolo e mi annullavo. Immaginavo di fare il mio ingresso come Guesch Patti, di attirare gli sguardi di tutti i maschi, di sedurli, di piacere. Nessuno sapeva delle mie fantasie, e io diventavo sempre più cupo. Ai miei avevo detto che ero gay, ma nulla di più. Non è stato un dramma, erano di mentalità aperta, ma da allora non mi hanno chiesto più niente. La mia adolescenza è stata lunga, solitaria, incerta. Brutta.
Leggi anche:
TUTTO È CAMBIATO QUANDO MI SONO TRASFERITO A MILANO DALLA SARDEGNA
Milano mi ha aiutato a fiorire: qui ho fatto le mie prime esperienze omosessuali, ho cominciato a uscire, a divertirmi. Una sera, avrò avuto 22, 23 anni, in un locale gay mi sono avvicinato a una transessuale: ero un bel ragazzo sardo, abbronzato, col pizzetto. Mi avvicino e le dico: «Ciao ti posso conoscere?». E lei: «Ma certo». Io: «Non l’ho mai detto a nessuno: voglio diventare una transessuale». Risposta sua: «Ma vai a quel paese. Credevo volessi provarci con me!». Non mi ricordo neppure come si chiamava, ma quella trans lì, quella sera, fu la prima ad accogliere le mie prime confidenze e a spiegarmi le cose. Nel nostro ambiente c’è una tradizione: le più adulte aiutano le più giovani. È una specie di regola non scritta, come in una tribù, in cui la conoscenza passa di generazione in generazione. Perché quando hai 20 anni, sei un uomo e scopri che vuoi vestirti da donna, tutto è complicatissimo. Non sai come nascondere la barba, come truccarti, che parrucca usare, dove comprare gli abiti. Da solo non ce la faresti mai. Anch’io, ora che sono (ehm…) grandicella, sto aiutando alcune transessuali giovani. Mi piace. Le guido, do loro consigli, le ascolto, lo scorso weekend le ho portate a ballare… Ma sto divagando. Torniamo alla mia storia.
LA SERA CHE HO FATTO LA MIA PRIMA USCITA DA DRAG QUEEN
(odio il termine travestito, mi sembra dispregiativo), il mio amico Riccardo, che era un truccatore, mi ha aiutato a prepararmi. A diventare Stella. Ho ancora una polaroid di quella sera lì: caschetto biondo platino (chissà perché è la prima parrucca che usiamo tutte), abito nero, zeppe altissime. Ho rischiato di rompermi una caviglia a ogni passo. È stato bellissimo: eravamo al Tunnel di Milano, una serata gay, e io finalmente interpretavo la parte che avevo sempre desiderato fare. Da quel giorno ho cominciato a lavorare nei locali: adoravo fare la door selector, soprattutto dei privé. Ero una femme fatale potentissima che decideva chi poteva entrare o rimanere fuori. Feci il primo passo: mi sbarazzai della barba. Per una trans i peli in faccia sono un incubo: se fai una serata in discoteca, quando arrivi alle sei del mattino, il mostro comincia a spuntare. Terribile. Dio benedica chi ha scoperto la luce pulsata. La prima seduta è stata dolorosissima, tornai a casa con il viso tutto rosso. Poi dopo qualche giorno, mentre mi lavavo la faccia al mattino, mi resi conto che i peli mi rimanevano in mano.
PER ANNI LA MIA VITA FU COSÌ: ALLA SERA ERO STELLA, LA DRAG, DI GIORNO ERO FULVIO, IL GAY
Con chi stavo? Alla luce del sole avevo storie con ragazzi omosessuali, da uomo. Di sera, con gli etero, vestita da donna. Ero condannata a essere spaccata in due. Col tempo, mi accorsi che i ragazzi gay non mi piacevano più. Io stavo bene solo con gli eterosessuali. Mi completavano. Ero diventata brava a sedurli con gli sguardi, le parole, il cervello. Il problema era che Stella, con le sue tette finte troppo grosse, i suoi eccessi, le parrucche, il trucco pesante, esisteva solo alla sera. Mica potevo andare in giro di giorno conciata così. Dopo una serata con qualcuno, aspettavo sempre una chiamata al mattino che non arrivava mai. In quegli anni ho sofferto molte volte di attacchi di depressione. Mi curavo, ma poi abbandonavo i farmaci e dopo un po’ era tutto daccapo. Ripensandoci ora, la depressione era causata dal rapporto con il mio corpo: volevo essere una transessuale, invece ero una drag queen. Era tutto finto. Alcune mattine mi svegliavo senza forze, annichilita. Non riuscivo ad alzarmi dal letto. Gli uomini con cui stavo io erano tutti fidanzati o sposati. Che cosa trovavano in me? Non saprei. Ma non pensare che fosse, banalmente, il desiderio della trasgressione. Non c’è solo quello, e comunque con una transessuale le “combinazioni” sono tante.
Leggi anche:
POI, UN BRUTTO GIORNO, È ARRIVATA LA CRISI ECONOMICA
Persi il lavoro. Fu come diventare adulta all’improvviso. Altri mesi bui. Di incoscienza e sofferenza. Pian piano però facevo dei cambiamenti: un trucco meno forte, un look meno eccessivo, qualche iniezione a zigomi e labbra. Il mio viso diventava sempre più effemminato. Ripresi a lavorare, le cose cominciavano ad andare meglio. Ma non riuscivo a trovare il coraggio per fare il passo. Il passo degli ormoni, il vero spartiacque. Gli ormoni ti cambiano il viso, ti addolciscono i lineamenti, ti modificano l’umore: diventi molto emotiva, vulnerabile. E poi, se fai una cura forte, hai problemi di erezione. È un prezzo da pagare altissimo. Ma faresti qualsiasi cosa pur di non prolungare l’agonia. Io ci ho messo anni prima di decidere. Un giorno una mia amica trans mi disse: «Sei ridicolo. Sei una testa di donna messa sopra un corpo da ragazzo. Ti vedi?». Eravamo in centro, mi sono guardata riflessa in una vetrina: era vero. Presi appuntamento dall’endocrinologo, ma rimandai per un anno ancora. Finalmente arriviamo alla primavera del 2014. Vado da un endocrinologo, questa volta decisa davvero, e mi faccio dare una cura ormonale.
COMINCIO CON GLI ORMONI, E MI FACCIO CHIAMARE DA TUTTI STELLA
Mi metto pure le ciglia finte, quelle permanenti. Di colpo, gli etero cominciano a guardarmi sempre di più, anche di giorno. Anche se sono Fulvio. E io sono felice.Sto meglio. Dopo qualche mese faccio la mia prima uscita al mattino con un trucco leggero, al bar sotto casa. Sorpresa: nessuno sguardo di disapprovazione. A ottobre 2014 vado in centro con un paio di jeans e i tacchi. Altra sorpresa: nessuno episodio spiacevole. Certo, ci sono gli sguardi, soprattutto delle donne, a quelli ti devi abituare. Ma saranno occhiate di curiosità o di disapprovazione? Nel frattempo incontro un ragazzo che ha 25 anni, eterosessuale, e cominciamo a uscire. Ci fidanziamo. Andiamo al cinema assieme, usciamo con le mie amiche trans e i loro fidanzati. Una vita quasi normale. Prendo coraggio, e decido di fare quello che ho sempre sognato: le tette. Il primo luglio 2015 mi sottopongo all’intervento. Quando mi sveglio sono così dolorante che non riesco neppure a essere felice.
LA FELICITÀ ARRIVA DOPO, A CASA, COME UN FIUME
Un fiume di lacrime che ogni due per tre mi viene su agli occhi. Sono spossata, svuotata, come dopo aver fatto una gran fatica. Anni di fatiche. Mi guardo le tette, e mi commuovo. Io che non ho mai fatto il bagno o la doccia con nessuno (nessuno!) ora a casa giro sempre nuda. Mi guardo allo specchio e vedo che sono quello che ho sempre voluto essere. Una trans che si chiama Stella. Di giorno e di notte.
Leggi anche:
- Intersessualità: cause, tipi, sintomi, terapia
- Ermafrodita, ermafroditismo, pseudoermafroditismo maschile e femminile, cosa significa?
- Androgino e androginia: etimologia, sessualità, genitali, mito di Platone
- Differenza tra ermafrodita e androgino
- Sindrome di Reifenstein (parziale insensibilità agli androgeni): cause, sintomi, diagnosi, terapia, complicanze
- Sindrome di Swyer (disgenesia gonadica pura) e gonadi a striscia
- Sindrome di Perrault: cause, sintomi, diagnosi, terapia, prognosi
- Sindrome dell’ovaio resistente (sindrome di Savage)
- Vivian Wheeler è la donna con la barba più lunga del mondo
- Cisessualità, cisgender, cisnormatività, cissessismo: che significa essere uomo cis e donna cis?
- Sapiosessualità: cosa significa essere un uomo o una donna sapiosessuale?
- Differenze tra orientamento sessuale, preferenza sessuale, sesso biologico, identità di genere e ruolo di genere
- Identità non binarie (genderqueer) cosa significa essere una persona non binaria?
- Disforia di genere (incongruenza di genere): denominazioni e diffusione
- Disforia di genere (incongruenza di genere): cause e sintomi in bambini, adolescenti e adulti
- Disforia di genere (incongruenza di genere): diagnosi e criteri diagnostici nel DSM-5 e nell’ICD-11
- Disforia di genere (incongruenza di genere): legge italiana e iter legale
- Disforia di genere (incongruenza di genere): trattamento, psicoterapia, terapia ormonale e chirurgica
- Cisnormatività, eteronormatività, etero-cis-normatività, transfobia, omofobia e omotransfobia
- Cissessismo, eterosessismo, eterocissessismo, disforia di genere, terzo sesso, transfobia interiorizzata
- Donna rimane incinta dopo sesso anale, ecco la spiegazione scientifica
- L’incredibile storia delle fotografie ritrovate di Vivian Maier
- La “donna vampiro” e la sua trasformazione [FOTO]
- Donna spende 100 mila euro per assomigliare a Jessica Rabbit
- Tutti i vantaggi di avere una barba folta
- Ragazza si fa tatuare il nome del fidanzato sull’ano [VIDEO]
- In un rapporto anale dove va a finire e cosa accade allo sperma? Può dare problemi alla salute? Posso rimanere incinta?
- Lubrificanti, clisteri e lavande anali: 6 consigli per il sesso anale
- Guida completa al sesso anale piacevole e sicuro
- Le 4 fantasie sessuali più diffuse tra le donne
- I 6 motivi per preferire un pene più piccolo ad uno grande
- Le 9 cose che nessuno ti dice sul sesso quando si invecchia
- Squirting: quello che c’è da sapere sull’eiaculazione femminile
- Perché alcuni uomini sono feticisti dei piedi?
- Quanto sesso deve fare una coppia sposata per essere felice?
- Vivere senza fare sesso: le 5 conseguenze di cui potresti soffrire
- Sex toy rimane incastrato nell’ano durante il sesso anale
- Camel Toe: le mutandine a “zampa di cammello” che spopolano in Giappone
- Barba e baffi: una moda che alla lunga può avere effetti negativi
- Norrie May Welby è la prima persona al mondo dichiarata ufficialmente né uomo né donna: non ha sesso
- Donna spende 100 mila euro per assomigliare a Jessica Rabbit
- Quali sono le differenze tra orgasmo vaginale e clitorideo?
- In un rapporto orale dove va a finire e cosa accade allo sperma ingoiato? Può dare problemi alla salute? Posso rimanere incinta?
- Donna rimane incinta dopo sesso anale, ecco la spiegazione scientifica
- Quali sono le differenze tra orgasmo vaginale e clitorideo?
- Andrew Wardle: “Sono nato senza pene ma sono stato con oltre cento donne”
- Fino a che età un uomo può avere figli?
- Mappa mondiale della lunghezza del pene: gli italiani quale posizione occupano?
- Diphallia: l’uomo nato con due peni [FOTO]
- Mappa delle zone erogene femminili: scopri i punti che la fanno impazzire
- La ragazza con due vagine [VIDEO]
- L’uomo con il pene più grande del mondo:”Faccio sesso orale da solo e da morto donerò il mio pene a…
- La ragazza con tre seni
- Il bambino con tre peni
- Come avere un’eiaculazione più abbondante e migliorare sapore, odore, colore e densità dello sperma?
- Come avere la più potente erezione della tua vita senza farmaci
- Come capire se una donna ha avuto davvero un orgasmo? Ecco i segnali del piacere femminile
- Non ho mai raggiunto l’orgasmo: è un problema? Quali soluzioni?
- Il sesso è davvero importante in una coppia?
- Amore senza sesso o sesso senza amore?
- Come distinguere un vero orgasmo femminile da uno “finto”
- L’orgasmo femminile è tutta questione di ritmo
- Lui ha il pene piccolo? I 6 trucchi per raggiungere lo stesso l’orgasmo
- Le 6 cose che gli uomini con il pene piccolo vogliono che la donna sappia
- Micropene: intervista a due uomini che hanno il pene piccolo
- Le donne rivelano le 16 piccole cose che rendono un uomo irresistibile
- Orgasmo femminile: dieci consigli per raggiungerlo più facilmente
- Differenza tra orgasmo maschile e femminile
- L’orgasmo e le altre fasi del ciclo di risposta sessuale
- Orgasmo maschile e femminile: nuovo studio sulle differenze fisiologiche
- Qual è la lunghezza media del pene?
- Come raggiungere un orgasmo femminile lungo ed intenso
- Orgasmo femminile: una donna su 5 non lo ha mai provato in vita sua
- Dare un nome al proprio pene ed altre cose che fanno gli uomini di nascosto
- Come avere un orgasmo vaginale
- Orgasmo femminile: le posizioni migliori per raggiungerlo
- Sintomi di eccitazione sessuale femminile e maschile
- Cos’è il liquido emesso da una donna durante l’orgasmo?
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su Tumblr e su Pinterest, grazie!
Condividi questo articolo:
 Vivian Maier è il nome di una donna che probabilmente non avete mai sentito nominare in vita vostra, tuttavia la sua storia è molto interessante a partire da uno strano fatto: scattò migliaia di foto senza svilupparne nessuna. Per quale motivo? Per difficoltà economiche? Scelta? Non si sa con esattezza. Dopo la sua morte furono trovati i negativi e divenne famosa per foto che quindi lei stessa non aveva mai visto. C’è un bellissimo documentario di Maloof e Siskel che la raccontano.
Vivian Maier è il nome di una donna che probabilmente non avete mai sentito nominare in vita vostra, tuttavia la sua storia è molto interessante a partire da uno strano fatto: scattò migliaia di foto senza svilupparne nessuna. Per quale motivo? Per difficoltà economiche? Scelta? Non si sa con esattezza. Dopo la sua morte furono trovati i negativi e divenne famosa per foto che quindi lei stessa non aveva mai visto. C’è un bellissimo documentario di Maloof e Siskel che la raccontano.
 La cura e la salute della pelle sono molto importanti, specie quella del viso. Esistono centinaia di trattamenti adatte a questo scopo, dalle maschere allo yogurt, a quelle al fango, ma la 28enne inglese
La cura e la salute della pelle sono molto importanti, specie quella del viso. Esistono centinaia di trattamenti adatte a questo scopo, dalle maschere allo yogurt, a quelle al fango, ma la 28enne inglese  Quella nella foto qui sopra sono io: Stella. Sono più vicina ai 40 che ai 30, sono fidanzata, di lavoro faccio la stylist e sono una transessuale. Mi sono rifatta il naso, ho eliminato barba e peli con la luce pulsata, prendo ormoni femminili, e poche settimane fa ho fatto la mastoplastica additiva, una quarta coppa D. Ma mi fermerò qui. Come la maggior parte delle transessuali, non interverrò chirurgicamente sui miei organi genitali. Mi vanno benissimo così. Ho un ottimo rapporto con il mio pene. E finalmente adesso sono quello che ho sempre voluto essere. Non un uomo. Non una donna. Ma una transessuale. Ci ho messo più di vent’anni ad arrivare dove sono ora. A capirmi, a prendere coraggio delle mie azioni, a sbagliare, a ricominciare. Sono stati anni duri. Anni disperati, di depressione, e intensi, di serate ed eccessi. Ma anche anni belli. A volte guardo le ragazze transessuali più giovani, persone che hanno 15 anni meno di me, e che hanno già fatto tutto (ormoni, epilazione, seno), e mi sento una stupida per aver sprecato tutto questo tempo. Perché non l’ho fatto prima? Non lo so. Non lo so proprio. Ognuno ha il suo cammino da fare, immagino. Quello che leggi qui è il mio.
Quella nella foto qui sopra sono io: Stella. Sono più vicina ai 40 che ai 30, sono fidanzata, di lavoro faccio la stylist e sono una transessuale. Mi sono rifatta il naso, ho eliminato barba e peli con la luce pulsata, prendo ormoni femminili, e poche settimane fa ho fatto la mastoplastica additiva, una quarta coppa D. Ma mi fermerò qui. Come la maggior parte delle transessuali, non interverrò chirurgicamente sui miei organi genitali. Mi vanno benissimo così. Ho un ottimo rapporto con il mio pene. E finalmente adesso sono quello che ho sempre voluto essere. Non un uomo. Non una donna. Ma una transessuale. Ci ho messo più di vent’anni ad arrivare dove sono ora. A capirmi, a prendere coraggio delle mie azioni, a sbagliare, a ricominciare. Sono stati anni duri. Anni disperati, di depressione, e intensi, di serate ed eccessi. Ma anche anni belli. A volte guardo le ragazze transessuali più giovani, persone che hanno 15 anni meno di me, e che hanno già fatto tutto (ormoni, epilazione, seno), e mi sento una stupida per aver sprecato tutto questo tempo. Perché non l’ho fatto prima? Non lo so. Non lo so proprio. Ognuno ha il suo cammino da fare, immagino. Quello che leggi qui è il mio. La stragrande maggioranza dei maschi italici ama il calcio. E la stragrande maggioranza delle mogli, delle compagne o delle fidanzate di questi maschi, invece, del calcio se ne infischia. E’ storia vecchia e ben nota ormai da decenni. Volendo approfondire l’argomento, però, ci si rende conto che molte liti e, di conseguenza, alcune delle crisi che vengono a svilupparsi tra lui e lei prendono origine proprio dal calcio o, in generale, dall’eccessivo attaccamento degli uomini alle loro passioni sportive.
La stragrande maggioranza dei maschi italici ama il calcio. E la stragrande maggioranza delle mogli, delle compagne o delle fidanzate di questi maschi, invece, del calcio se ne infischia. E’ storia vecchia e ben nota ormai da decenni. Volendo approfondire l’argomento, però, ci si rende conto che molte liti e, di conseguenza, alcune delle crisi che vengono a svilupparsi tra lui e lei prendono origine proprio dal calcio o, in generale, dall’eccessivo attaccamento degli uomini alle loro passioni sportive. Il giorno in cui è morto, David Kirby aveva 32 anni. Giaceva sul letto, il suo volto sofferente e il corpo consumato dall’Aids, circondato dalla sua famiglia. Quell’istante in cui l’uomo è spirato, è stato impresso dalla macchina fotografica di Therese Frare, all’epoca una giovane studentessa di foto-giornalismo in un’università dell’Ohio. Frare riuscì a catturare quel momento straziante con freddezza e professionalità, dando un volto umano a quella malattia fino ad allora socialmente stigmatizzata. Nel novembre del 1990, la rivista Life decise di pubblicare quella foto che divenne rapidamente l’immagine simbolo per tutte le persone affette dal virus dell’Hiv.
Il giorno in cui è morto, David Kirby aveva 32 anni. Giaceva sul letto, il suo volto sofferente e il corpo consumato dall’Aids, circondato dalla sua famiglia. Quell’istante in cui l’uomo è spirato, è stato impresso dalla macchina fotografica di Therese Frare, all’epoca una giovane studentessa di foto-giornalismo in un’università dell’Ohio. Frare riuscì a catturare quel momento straziante con freddezza e professionalità, dando un volto umano a quella malattia fino ad allora socialmente stigmatizzata. Nel novembre del 1990, la rivista Life decise di pubblicare quella foto che divenne rapidamente l’immagine simbolo per tutte le persone affette dal virus dell’Hiv. Dieta ipoproteica ed aproteica: cosa mangiare e chi la deve seguire?
Dieta ipoproteica ed aproteica: cosa mangiare e chi la deve seguire? Le persone in sovrappeso hanno solitamente una sensibilità molto particolare e tutti i giorni sono sottoposti a sguardi (per lo più di disapprovazione) e commenti ritenuti spiritosi sulle loro dimensioni o sul loro appetito. Un inferno che almeno per le feste hanno diritto di dimenticare. E siccome è il pensiero quello che conta, possiamo assicurarvi per esperienza diretta che ci sono alcuni regali da evitare assolutamente, in quanto sottointendono un giudizio più o meno negativo sulle loro forme.
Le persone in sovrappeso hanno solitamente una sensibilità molto particolare e tutti i giorni sono sottoposti a sguardi (per lo più di disapprovazione) e commenti ritenuti spiritosi sulle loro dimensioni o sul loro appetito. Un inferno che almeno per le feste hanno diritto di dimenticare. E siccome è il pensiero quello che conta, possiamo assicurarvi per esperienza diretta che ci sono alcuni regali da evitare assolutamente, in quanto sottointendono un giudizio più o meno negativo sulle loro forme.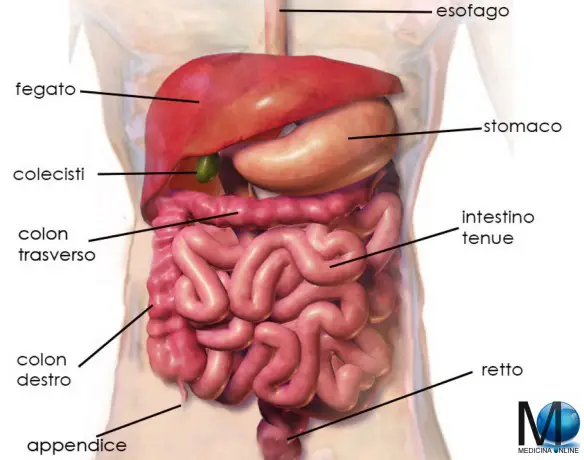 L’intestino è l’ultima parte dell’apparato digerente ed è un tubo di diametro variabile con pareti flessibili, ripiegato più volte su se stesso e lungo circa 8 metri in tutto.
L’intestino è l’ultima parte dell’apparato digerente ed è un tubo di diametro variabile con pareti flessibili, ripiegato più volte su se stesso e lungo circa 8 metri in tutto.