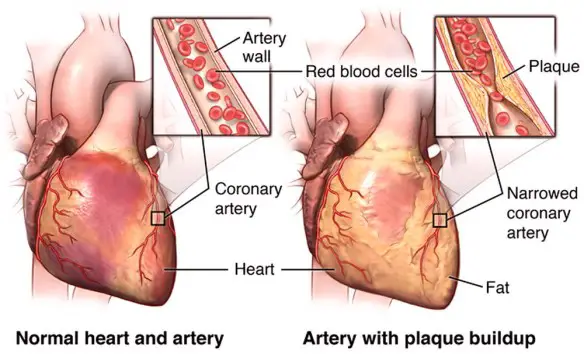
 Con “angina pectoris” si intende un dolore al torace retrosternale (posteriore allo sterno, l’osso piatto e centrale del torace). L’angina pectoris non è quindi una vera e propria patologia, bensì un sintomo.
Con “angina pectoris” si intende un dolore al torace retrosternale (posteriore allo sterno, l’osso piatto e centrale del torace). L’angina pectoris non è quindi una vera e propria patologia, bensì un sintomo.
Da cosa è causato il dolore anginoso al petto?
È causato da un temporaneo scarso afflusso di sangue al cuore attraverso le arterie coronariche che determina mancanza di ossigeno al tessuto cardiaco. Il fenomeno prende anche il nome di ischemia; nell’angina pectoris l’ischemia è reversibile e non arriva al punto di provocare danno cardiaco permanente come invece avviene nell’infarto del miocardio. La malattia si manifesta abitualmente con dolore toracico improvviso, acuto e transitorio; sono stati descritti anche: pesantezza a torace e arti superiori, formicolìo o indolenzimento nella stessa sede, affaticamento, sudorazione, nausea. I sintomi possono essere molto diversi da individuo a individuo per intensità e durata.
Leggi anche:
Classificazione dell’angina pectoris
L’angina pectoris si distingue in diverse forme:
- Angina stabile o da sforzo: è innescata da uno sforzo fisico, dal freddo o dall’emozione. In questo caso il sintomo della malattia si manifesta quando si sta svolgendo l’attività fisica, soprattutto se esposti alle basse temperature, o all’apice di uno stress emotivo. È la forma più diffusa e anche quella maggiormente controllabile.
- Angina instabile: in questo caso il dolore si presenta in maniera imprevista, anche a riposo, o per sforzi fisici modesti. La causa può essere l’ostruzione temporanea di una coronaria da parte di un coagulo, detto anche trombo, che si forma su una malattia aterosclerotica delle pareti vasali. Per questo rappresenta la forma più pericolosa, da trattare tempestivamente, in quanto fortemente associata al rischio di progressione verso un infarto acuto del miocardio. Si può considerare una forma di angina instabile anche l’angina variante o di Prinzmetal. L’angina variante è causata da uno spasmo in una delle coronarie, con restringimento importante, anche se temporaneo, del vaso fino a compromettere in modo significativo il flusso di sangue e causare ischemia associata a dolore toracico. L’angina di Prinzmetal è una malattia abbastanza rara che non è generalmente associata ad aterosclerosi del vaso coronarico interessato dallo spasmo.
- Angina secondaria: vi rientrano tutte quelle forme di “ischemia” cardiaca che non sono provocate da restringimenti o ostruzioni coronariche, ma da altre patologie quali l’insufficienza aortica, la stenosi mitralica, l’anemia grave, l’ipertiroidismo e le aritmie.
Leggi anche:
Quali sono le cause dell’angina pectoris?
L’angina è causata dalla riduzione, temporanea, dell’afflusso di sangue al cuore. Il sangue trasporta l’ossigeno necessario ai tessuti del muscolo cardiaco per vivere. Se il flusso di sangue è inadeguato si creano le condizioni per un’ischemia. La riduzione del flusso può essere prodotta da un restringimento critico delle coronarie (stenosi), tale per cui, in presenza di aumentate richieste di ossigeno da parte del tessuto cardiaco (durante attività fisica, freddo o stress emotivo), non vi è di fatto un apporto sufficiente. Questo avviene più spesso in presenza di aterosclerosi coronarica, malattia che coinvolge le pareti dei vasi sanguigni attraverso la formazione di placche a contenuto lipidico o fibroso, che evolvono verso la progressiva riduzione del lume o verso l’ulcerazione e la formazione brusca di un coagulo sovrastante il punto di lesione. L’ostruzione/restringimento della coronaria può avvenire più raramente anche per spasmo della stessa, solitamente senza alterazioni aterosclerotiche delle pareti vasali. Condizioni che favoriscono lo sviluppo di aterosclerosi sono il fumo, il diabete, l’ipertensione e l’obesità.
Quali sono i sintomi dell’angina pectoris?
I sintomi dell’angina includono:
- Dolore acuto, pesantezza, formicolio o indolenzimento al torace, che talvolta si può irradiare verso spalle, braccia, gomiti, polsi, schiena, collo, gola e mandibola
- Dolore prolungato nella parte superiore dell’addome
- Mancanza di respiro (dispnea)
- Sudorazione
- Svenimento
- Nausea e vomito
Come prevenire l’angina pectoris?
La prevenzione dell’angina pectoris si attua in primo luogo attraverso la prevenzione dell’aterosclerosi coronarica, mettendo in atto tutte le misure volte a controllare i principali fattori di rischio cardiovascolare. È necessario evitare la sedentarietà, effettuare un’attività fisica moderata e regolare; evitare, se si sono avuti episodi di dolore anginoso, sforzi eccessivi e fonti di stress psicofisico; evitare sovrappeso e obesità, seguire una dieta sana, povera di grassi e ricca di frutta e verdura; evitare pasti abbondanti e l’assunzione di alcolici; non fumare o smettere di fumare.
Chi soffre di diabete deve attuare tutte le misure per un controllo adeguato della glicemia. È necessario, inoltre, controllare periodicamente la pressione sanguigna.
Diagnosi ed interpretazione diagnostica
Chi ha un episodio di angina, anche sospetto, dovrebbe riferirlo tempestivamente al medico per gli esami del caso, che includono:
- Elettrocardiogramma (ECG): registra l’attività elettrica del cuore e consente di individuare la presenza di anomalie suggestive per ischemia miocardica. L’Holter è il monitoraggio prolungato nelle 24 ore dell’ECG: nel caso di sospetta angina consente di registrare l’elettrocardiogramma nella vita di tutti i giorni e soprattutto in quei contesti in cui il paziente riferisce di avere la sintomatologia.
- Il test da sforzo: l’esame consiste nella registrazione di un elettrocardiogramma mentre il paziente compie un esercizio fisico, generalmente camminando su un tapis roulant o pedalando su una cyclette. Il test viene condotto secondo protocolli predefiniti, volti a valutare al meglio la riserva funzionale del circolo coronarico. Viene interrotto alla comparsa di sintomi, alterazioni ECG o pressione elevata o una volta raggiunta l’attività massimale per quel paziente in assenza di segni e sintomi indicativi di ischemia.
- Scintigrafia miocardica: è una metodica utilizzata per valutare l’ischemia da sforzo in pazienti il cui solo elettrocardiogramma non sarebbe adeguatamente interpretabile. Anche in questo caso Il paziente può eseguire l’esame con cyclette o tapis roulant. Al monitoraggio elettrocardiografico viene affiancata la somministrazione endovenosa di un tracciante radioattivo che si localizza nel tessuto cardiaco se l’afflusso di sangue al cuore è regolare. Il tracciante radioattivo emana un segnale che può essere rilevato da un’apposita apparecchiatura, la Gamma-camera. Somministrando il radiotracciante in condizioni di riposo e all’apice dell’attività si valuta l’eventuale comparsa di mancanza di segnale in quest’ultima condizione, segno che il paziente manifesta un’ischemia da sforzo. L’esame consente non solo di diagnosticare la presenza di ischemia ma anche di fornire un’informazione più accurata sulla sua sede e sull’estensione. Lo stesso esame può essere effettuato producendo l’ipotetica ischemia con un farmaco ad hoc e non con l’esercizio fisico vero e proprio.
- Ecocardiogramma: è un test di immagine che visualizza le strutture del cuore e il funzionamento delle sue parti mobili. L’apparecchio dispensa un fascio di ultrasuoni al torace, attraverso una sonda appoggiata sulla sua superficie, e rielabora gli ultrasuoni riflessi che tornano alla stessa sonda dopo aver interagito in modo diverso con le varie componenti della struttura cardiaca (miocardio, valvole, cavità). Le immagini in tempo reale possono essere raccolte anche durante l’esecuzione di un test da sforzo, fornendo in quel caso informazioni preziose sulla capacità del cuore di contrarsi correttamente in corso di attività fisica. Analogamente alla scintigrafia anche l’ecocardiogramma può essere registrato dopo aver somministrato al paziente un farmaco che può scatenare un’eventuale ischemia (ECO-stress), permettendone la diagnosi e la valutazione di estensione e sede.
- Coronografia o angiografia coronarica: è l’esame che consente di visualizzare le coronarie attraverso l’iniezione di mezzo di contrasto radiopaco al loro interno. L’esame viene effettuato in un’apposita sala radiologica, nella quale sono rispettate tutte le misure di sterilità necessarie. L’iniezione del contrasto nelle coronarie presuppone il cateterismo selettivo di un’arteria e l’avanzamento di un catetere fino all’origine dei vasi esplorati.
- TC cuore o tomografia computerizzata (TC): è un esame diagnostico per immagini per valutare la presenza di calcificazioni dovute a placche aterosclerotiche nei vasi coronarici, indicatore indiretto di un rischio elevato di patologia coronarica maggiore. Con gli apparecchi attuali, somministrando anche mezzo di contrasto per via endovenosa, è possibile ricostruire il lume coronarico e ottenere informazioni su eventuali restringimenti critici.
- Risonanza magnetica nucleare (RMN): produce immagini dettagliate della struttura del cuore e dei vasi sanguigni attraverso la registrazione di un segnale emesso dalle cellule sottoposte a un intenso campo magnetico. Permette di valutare la morfologia delle strutture del cuore, la funzione cardiaca ed eventuali alterazioni del movimento di parete secondarie a ischemia indotta farmacologicamente (RMN cardiaca da stress).
Trattamenti
Il trattamento dell’angina è diretto a migliorare la perfusione delle coronarie e a evitare il rischio di infarto e trombosi. La terapia include diverse opzioni, farmacologiche o interventistiche, che vengono valutate dal cardiologo in relazione al quadro clinico:
- Nitrati (nitroglicerina): è una categoria di farmaci adoperata per favorire la vasodilatazione delle coronarie, permettendo così un aumento del flusso di sangue verso il cuore.
- Aspirina: studi scientifici hanno appurato che l’aspirina riduce la probabilità di infarto. L’azione antiaggregante di questo farmaco previene infatti la formazione di trombi. La stessa azione viene svolta anche da altri farmaci antipiastrinici (ticlopidina, clopidogrel, prasugrel e ticagrelor), che possono essere somministrati in alternativa o in associazione all’aspirina stessa, secondo le diverse condizioni cliniche.
- Beta-bloccanti: rallentano il battito cardiaco e abbassano la pressione sanguigna contribuendo in questo modo a ridurre il lavoro del cuore e quindi anche del suo fabbisogno di ossigeno.
- Statine: farmaci per il controllo del colesterolo che ne limitano la produzione e l’accumulo sulle pareti delle arterie, rallentando lo sviluppo o la progressione dell’aterosclerosi.
- Calcio-antagonisti: hanno un’azione di vasodilazione sulle coronarie che consente di aumentare il flusso di sangue verso il cuore.
L’opzione interventistica include:
- L’angioplastica coronarica percutanea, un intervento che prevede l’inserimento nel lume della coronaria, in corso di angiografia, di un piccolo pallone solitamente associato a una struttura metallica a maglie (stent), che viene gonfiato ed espanso in corrispondenza del restringimento dell’arteria. Questa procedura migliora il flusso di sangue a valle, riducendo o eliminando l’angina.
- Bypass coronarico, un intervento chirurgico che prevede il confezionamento di condotti vascolari (di origine venosa o arteriosa) in grado di “bypassare” il punto di restringimento delle coronarie, facendo pertanto comunicare direttamente la porzione a monte con quella a valle della stenosi. L’intervento viene effettuato a torace aperto, con il paziente in anestesia generale e quasi sempre con il supporto della circolazione extra-corporea.
Leggi anche:
- Angina pectoris walk-through, mista, notturna, postprandiale, vasospastica e sindrome X
- Cardiopatia ischemica: cronica, definizione, sintomi, conseguenze
- Infarto, ischemia, necrosi, aterosclerosi, trombo, embolo, ictus, miocardio… Facciamo chiarezza
- Differenza tra sindrome coronarica acuta ed infarto
- Differenza tra infarto ed angina
- Differenza tra angina stabile, instabile e secondaria
- Differenza tra infarto cardiaco, infarto miocardico e attacco di cuore
- Differenza tra attacco di cuore (infarto del miocardio) ed arresto cardiaco
- Insufficienza della valvola mitralica lieve, moderata, severa: sintomi, diagnosi e terapia
- Sindrome del QT lungo: valorie, cause, cura, farmaci, sportivi
- Morte cardiaca improvvisa: cause, sintomi premonitori e cure
- Enzimi cardiaci: alti, bassi, tempi, risultati, ogni quante ore
- Come, dove e quando si misura la frequenza cardiaca?
- Cos’è un infarto e quanti tipi di infarto conosci?
- Ecocolordoppler cardiaco (ecocardio): funzioni, preparazione, gravidanza
- Ecocardiogramma per via transesofagea: preparazione, è doloroso?
- Differenza tra ecocardiografia ed elettrocardiogramma
- Ecocardiogramma da stress (ecostress) fisico e farmacologico: come si svolge, è pericoloso?
- Valvole cardiache: cosa sono, quali sono ed a che servono
- Defibrillatore: cos’è, come funziona, prezzo, voltaggio, manuale ed esterno
- Bradicardia: sintomi, conseguenze, rimedi, notturna e grave
- Fibrillazione atriale: terapia, rischi, cosa fare, ECG, quando preoccuparsi
- Fibrillazione atriale: parossistica, persistente e cronica
- Differenza tra fibrillazione ventricolare ed arresto cardiaco
- Arresto cardiaco: conseguenze, cause, coma, terapia, cosa fare
- Fibrillazione ventricolare: cos’è, terapia, cause scatenanti, frequenza
- Tachicardia improvvisa: cosa fare, ansia, rimedi, valori, dopo i pasti
- Extrasistole: a riposo, ansia, sono pericolose, cure e gravidanza
- Fibrillazione atriale: farmaci e terapia dell’aritmia cardiaca
- Farmaci antiaritmici: meccanismo d’azione ed effetti collaterali
- Primo soccorso e BLS (Basic Life Support): cos’è e come si fa
- Respirazione artificiale bocca a bocca: quando farla e come farla
- Massaggio cardiaco: quando farlo e come farlo [LINEE GUIDA]
- Massaggio cardiaco: quante compressioni al minuto?
- Differenza tra pressione massima (sistolica), minima (diastolica) e differenziale
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Trombo: cause, classificazione, trombosi venose, arteriose e sistemiche
- Pressione arteriosa: valori normali e patologici
- Qual è la differenza tra arteria e vena?
- Fattori di rischio cardiovascolare modificabili e non modificabili
- Come si muove il sangue all’interno del cuore?
- La Sindrome del cuore infranto: il falso infarto di chi ha il “cuore spezzato”
- Sistole e diastole nel ciclo cardiaco: fasi durata e spiegazione
- Che differenza c’è tra sistole e diastole?
- Ipertensione: quali farmaci usare per abbassare la pressione arteriosa?
- Sarò iperteso per tutta la vita? Dovrò continuare ad assumere il farmaco per sempre?
- Elettrocardiogramma (ECG) a riposo e sotto sforzo: cos’è ed a che serve?
- VES alta o bassa: cause, sintomi e valori normali della velocità di eritrosedimentazione
- Glicemia alta o bassa: valori normali, che patologie indica e come si controlla nei diabetici
- Transaminasi alte, basse, cosa sono, cosa indicano e come si curano
- Bilirubina diretta e indiretta: ittero, significato, patologie collegate
- Epatiti croniche: cosa sono, sintomi, diagnosi e cura
- Ittero emolitico, colestatico, ostruttivo, neonatale: significato, occhi, cura
- Funzionalità epatica; cos’è, cosa indica e come si misura
- Malattie del fegato: sintomi, prurito, alcol, tipi, autoimmuni
- Insufficienza epatica lieve, acuta e cronica: dieta e rischio di morte
- Azotemia (Urea) alta o bassa: valori, cause, sintomi e cosa fare
- Creatinina alta o bassa: cos’è, cosa indica e come si corregge
- Clearance della creatinina: alta o bassa, valori, calcolo e sintomi
- Albumina ed albuminemia alta o bassa: cause, valori e terapie
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Condividi questo articolo:

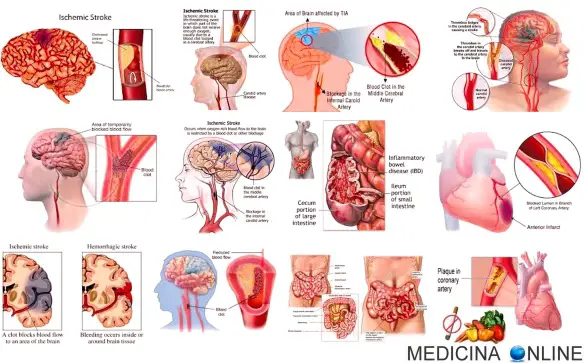 Facciamo oggi chiarezza su molti termini che si sentono spesso in campo medico, ma che spesso vengono confusi tra loro dai “non addetti ai lavori”.
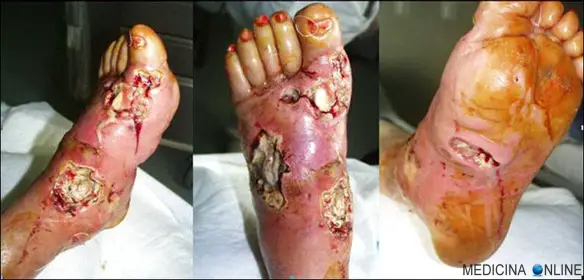
Facciamo oggi chiarezza su molti termini che si sentono spesso in campo medico, ma che spesso vengono confusi tra loro dai “non addetti ai lavori”. La peritonite è un’infiammazione della sierosa (chiamata appunto “peritoneo”) che riveste i visceri e la cavità addominale, dovuta, in genere, ad una contaminazione batterica.
La peritonite è un’infiammazione della sierosa (chiamata appunto “peritoneo”) che riveste i visceri e la cavità addominale, dovuta, in genere, ad una contaminazione batterica. La morte cellulare si può attuare in vari modi e per diverse cause (fisiologiche o patologiche).
La morte cellulare si può attuare in vari modi e per diverse cause (fisiologiche o patologiche). Con il termine “ipossia” (in inglese “hypoxia”) si intende una condizione patologica determinata da una carenza di ossigeno nei tessuti. La carenza di ossigeno può essere:
Con il termine “ipossia” (in inglese “hypoxia”) si intende una condizione patologica determinata da una carenza di ossigeno nei tessuti. La carenza di ossigeno può essere: Con “angina pectoris” si intende un dolore al torace retrosternale (posteriore allo sterno, l’osso piatto e centrale del torace). L’angina pectoris non è quindi una vera e propria patologia, bensì un sintomo.
Con “angina pectoris” si intende un dolore al torace retrosternale (posteriore allo sterno, l’osso piatto e centrale del torace). L’angina pectoris non è quindi una vera e propria patologia, bensì un sintomo.