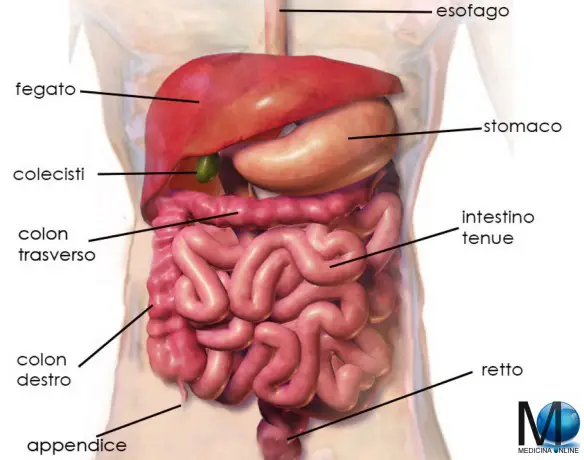
 Il sangue occulto nelle feci è uno scenario nel quale gli escrementi presentano delle tracce di sangue non tali da essere visibili a occhio nudo, ma comunque sufficienti da poter essere apprezzate attraverso delle analisi di laboratorio. Si tratta dunque di un test molto importante per lo screening per il tumore del colon-retto, che i medici consigliano di ripetere almeno una volta ogni due anni, superata la cinquantina. Naturalmente, come spesso avviene attraverso tali test di screening, anche questa analisi non ha valenza diagnostica, ma serve unicamente per identificare le persone a rischio per tale tipologia di patologia, e per i polipi intestinali.
Il sangue occulto nelle feci è uno scenario nel quale gli escrementi presentano delle tracce di sangue non tali da essere visibili a occhio nudo, ma comunque sufficienti da poter essere apprezzate attraverso delle analisi di laboratorio. Si tratta dunque di un test molto importante per lo screening per il tumore del colon-retto, che i medici consigliano di ripetere almeno una volta ogni due anni, superata la cinquantina. Naturalmente, come spesso avviene attraverso tali test di screening, anche questa analisi non ha valenza diagnostica, ma serve unicamente per identificare le persone a rischio per tale tipologia di patologia, e per i polipi intestinali.
Da cosa può dipendere il sangue occulto nelle feci
Sancito quanto precede, è altrettanto ovvio che per poter diagnosticare quali siano le motivazioni sottostanti al sangue occulto nelle feci è necessario indirizzare il paziente verso altri specifici esami, come la colonscopia. Il sangue occulto nelle feci può infatti dipendere da un lungo elenco di diverse condizioni come, tra i principali, l’ulcera duodenale o gastrica, le varici esofagee, la colite ulcerosa, il morbo di Crohn, la diverticolite, le fistole anali, o ancora la possibile contaminazione del campione con sangue mestruale o delle urine, emorroidi, ragadi, dieta inadeguata e così via. Nonostante non sia utile per poter diagnosticare correttamente la patologia alla base del sangue occulto nelle feci, effettuare regolarmente questo esame risulta essere molto utile per una prognosi tempestiva di qualche problema. Stando ai risultati di alcuni studi recenti, ad esempio, la ricerca di sangue occulto nelle feci ha mostrato una riduzione del 33% se il test veniva effettuato ogni anno, e del 21% se effettuato ogni due anni.
Leggi anche:
- Colonscopia: cos’è, quando si fa, preparazione e rischi
- Colonscopia tradizionale o colonscopia virtuale?
- Colonscopia: rischi, effetti collaterali e complicanze
Come prepararsi al test
La preparazione al test per il sangue nelle feci può essere effettuata secondo le indicazioni specifiche del medico, considerando che dipenderà dalla tecnica di diagnostica scelta. In linea di massima, le tecniche tradizionali si basano sull’uso del guaiaco, sfruttando delle striscette di carta che sviluppano un colore definito in presenza di sangue. Per evitare dei falsi risultati positivi, è comunque consigliabile, nei giorni precedenti l’esame, astenersi dal consumo di carni rosse crude o semicrude, salumi, fonti ricchi di vitamine C, alcolici, medicinali antinfiammatori. È ancora consigliato pulire i denti con delicatezza al fine di evitare emorragie gengivali, e seguire un’alimentazione ricca di fibre.
Esistono ad ogni modo delle nuove tecniche di diagnostica molto più avanzate di queste tradizionali, in seguito alle quali non è più necessario rispettare tali norme. I test sono tuttavia in grado di evidenziare solamente la presenza di sangue occulto che proviene dal colon e dal retto, poiché la globina (la porzione proteica che viene impattata da anticorpi diretti attraverso tali test) non supera “indenne” il tratto gastrointestinale superiore, essendo sostanzialmente digerita.
Di norma, questi test più innovativi vengono riservati dunque per i soli test di screening per il cancro al colon / retto, anche per il plus determinato dall’indipendenza dei risultati da possibili emorragie dei tratti iniziali del tubo digerente.
Leggi anche:
- Esame e raccolta delle feci: come si fa nel modo corretto ed a che serve
- Il mio alito odora di feci: cause, quando è pericoloso e rimedi
- Quanto peso perdiamo ogni volta che andiamo in bagno?
- Coprocoltura e antibiogramma: procedura e perché si eseguono
Qualche ulteriore consiglio
Si ricorda infine che per poter incrementare l’utilità dei test, è importante – durante la raccolta delle feci – campione – cercare di rispettare le indicazioni che il centro di analisi fornirà a tutti i pazienti. Di solito, queste indicazioni sono abbastanza basilari, e fanno riferimento alla necessità di usare un apposito recipiente sterile, ed emettere le feci in un recipiente, evitando di mescolarle con altre sostanze come urine, acqua del wc, detergenti. Quindi, occorre procedere a raccogliere il campione con un’apposita spatolina in almeno tre punti diversi delle feci, fino a riempire metà del recipiente (ottenendo così un campione quanto più omogeneo possibile). Si dovrà infine procedere a scrivere il nome sull’etichetta del sistema per la raccolta delle feci, condurre il campione in laboratorio entro alcune ore o, nella necessità di raccogliere più campioni, conservare le stesse all’interno del frigorifero. Per i motivi e le intuizioni che dovrebbero essere ben chiare a questo punto, evitare di eseguire il test di ricerca del sangue occulto nelle feci durante le mestruazioni, in presenza di emorroidi sanguinanti o quando si perde del sangue con le urine: in tutte queste ipotesi, infatti, i test potrebbero essere inficiati e contaminati da altre sostanza che potrebbero fornire falsi risultati.
Quale contenitore sterile usare?
Per raccogliere e conservare correttamente il campione di feci da inviare in laboratorio, è necessario usare un contenitore sterile apposito, dotato di spatolina. Il prodotto di maggior qualità, che ci sentiamo di consigliare per raccogliere e conservare le feci, è il seguente: http://amzn.to/2C5kKig
Leggi anche:
- Apparato digerente: cos’è, com’è fatto, a che serve e come funziona?
- Frequenza defecazione: quante volte al giorno è normale andare di corpo?
- Fa male trattenere l’urina troppo a lungo? Per quale motivo?
- Quante volte al giorno è normale urinare? Vescica iperattiva e ansia
- Idratazione corretta: quanta acqua bere al giorno e perché è così importante
- Differenza tra ulcera gastrica, duodenale, peptica ed esofagea
- Ulcera peptica: complicanze, cura, dieta, quando è pericolosa
- Fare un clistere evacuativo: procedura semplice con peretta
- Differenze tra clistere, peretta, enteroclisma, microclisma
- Quando è utile fare un clistere evacuativo?
- Differenze tra clistere ed enteroclisma
- Clistere: quanto tempo va trattenuto affinché agisca?
- Fecaloma: tappo di feci durissime, cause, sintomi e rimedi
- Feci dure, stitichezza e dolore defecazione: cause e cure
- Come ammorbidire le feci dure in modo naturale e con i farmaci
- L’esofagogastroduodenoscopia: cos’è, preparazione, è dolorosa o pericolosa?
- Colangiopancreatografia retrograda (ERCP): cos’è, preparazione, è dolorosa o pericolosa?
- Legatura/sclerosi delle varici esofagee: perché si esegue, quali sono i rischi?
- Cirrosi epatica e fegato: sintomi, dieta, diagnosi, terapia e prevenzione
- Fegato ed epatociti: anatomia, funzioni e patologie in sintesi
- Epatiti croniche: cosa sono, sintomi, diagnosi e cura
- Polipi intestinali e polipectomia: come si esegue, biopsia e pericoli
- Differenza tra polipi e diverticoli: sintomi comuni e diversi
- Differenza tra diverticolite e diverticolosi
- Diverticolite e diverticolosi: sintomi, diagnosi e trattamento
- Sangue occulto nelle feci: come interpretare il risultato dell’esame
- Vomitare sangue ed ematemesi: cos’è, cosa fare, cause e terapie
- Da cosa viene causata l’ulcera allo stomaco?
- Acido cloridrico e succo gastrico dello stomaco: di cosa è fatto ed a che serve
- Meccanismi e controllo della secrezione acida dello stomaco
- Dispepsia: com’è, sintomi, come si fa la diagnosi e terapia
- Gastrite cronica, quando il bruciore di stomaco non dà tregua
- Incontinenza fecale primitiva e secondaria: cos’è e come si cura
- Infezione da Helicobacter Pylori: cosa causa, come si riconosce e cura
- Le 5 cose da fare a stomaco vuoto, secondo la scienza
- Stomaco: come fa a digerire il cibo che mangi ed a dirti che sei “pieno”
- Come vincere l’ansia per evitare di mangiare fuori pasto
- Eliminare la tensione nervosa allo stomaco con i rimedi naturali
- Stomaco: anatomia e funzioni in sintesi
- Acidità di stomaco in gravidanza: farmaci, cibi e rimedi naturali
- Reflusso gastroesofageo: sintomi, diagnosi e cura
- Perché viene la diarrea in gravidanza? Fa male al bambino? Cure e rimedi
- Reflusso gastroesofageo: terapia farmacologica e chirurgica
- La dieta per prevenire l’ernia iatale ed evitare il reflusso gastroesofageo
- Cosa succede al tuo corpo quando smetti di mangiare pasta e pane
- Lesioni da decubito: prevenzione, stadi, classificazione e trattamento
- Dieta e reflusso gastroesofageo
- Acidità di stomaco e bruciore: tutti i farmaci antiacidi
- Bruciore di stomaco: cosa mangiare, come dormire e rimedi naturali
- Quanto peso perdiamo ogni volta che andiamo in bagno?
- Ritirato in tutta Italia il famoso farmaco anti reflusso: ecco i lotti interessati
- Ma perché non riesco a dimagrire? I nove errori tipici di chi è a dieta
- Dimagrire riducendo le dimensioni dello stomaco senza chirurgia e bendaggio gastrico
- Zucchero: il killer del terzo millennio. Ecco i cibi insospettabili dove si nasconde
- Glucomannano per dimagrire: nel tuo stomaco aumenta di 100 volte il proprio volume, ti sazia e ti impedisce di mangiare troppo
- Capacità massima dello stomaco: si può “mangiare fino a scoppiare”?
- Esofago: anatomia e funzioni in sintesi
- Esofago e trachea: zona, anatomia, rapporti e differenze
- Cosa succede al cibo nello stomaco dopo averlo ingerito?
- Esofago di Barrett: sintomi iniziali, diagnosi, terapia, dieta e chirurgia
- Differenza tra metaplasia, displasia e neoplasia con esempi
- Differenza tra disfagia ed odinofagia: cause comuni e diverse
- Differenza tra disfagia orofaringea ed esofagea: sintomi comuni e diversi
- Differenza tra disfagia di tipo ostruttivo e di tipo motorio
- Differenza tra disfagia ostruttiva ed occlusione intestinale
- Differenze tra ileo meccanico ed ileo paralitico
- Differenza tra disfagia ai liquidi e ai solidi
- Cistifellea: cos’è, a cosa serve e dove si trova
- Bile: dove si trova, a che serve e da cosa è composta?
- Dotto epatico comune, cistico e coledoco: anatomia del sistema biliare
- Pancreas: anatomia e funzioni in sintesi
- Differenza tra laringe, faringe e trachea
- Trachea: anatomia e funzioni in sintesi
- Quanto è lungo l’intestino in adulto e neonato (tenue e crasso)
- Stitichezza acuta e cronica: tipi, cause, trattamenti medici e rimedi
- Differenza tra stipsi, stitichezza e costipazione
- Stitichezza o stipsi acuta e cronica: terapie farmacologiche
- Sistema nervoso: com’è fatto, a che serve e come funziona
- Differenza tra occlusione e subocclusione
- Si può vivere senza bere acqua? Per quanto tempo?
- Si può vivere senza mangiare cibo? Per quanto tempo?
- Si può vivere senza respirare aria? Quanto può durare una apnea?
- Differenza tra emorroidi e ragadi
- Differenza tra emorroidi interne ed esterne
- Differenza tra emorroidi e fistole
- Differenza tra emorroidi e tumore
- Gli alimenti più lassativi: addio stitichezza!
- Feci dalla bocca: il vomito fecaloide
- Riconoscere i differenti tipi di vomito a seconda del colore
- Vomito: le cause più frequenti
- Vomito: rimedi naturali e cure farmacologiche (farmaci anti-emetici)
- Differenza tra vomito e rigurgito nel neonato
- Cibi che macchiano i denti: quali evitare ed i consigli per mantenerli bianchi
- Feci nere e melena: cause e cure in adulti e neonati
- Differenze tra morbo di Crohn e colite ulcerosa: sintomi comuni e diversi
- Sindrome dell’intestino irritabile: sintomi, dieta e cibi da evitare
- Mal di pancia e di stomaco: da cosa può dipendere e quali sono le cure
- Mal di pancia forte: quando chiamare il medico?
- Feci del neonato verdi, gialle, con muco, schiumose: cosa fare?
- Meconio, transizione e svezzamento: feci diverse nel neonato
- Differenza tra feci del neonato allattato al seno o con latte artificiale
- È normale che il mio bambino non emetta feci ogni giorno?
- Quante volte al giorno va cambiato il pannolino in neonati e bimbi?
- Feci galleggianti e maleodoranti: cause e quando chiamare il medico
- Colore delle feci: normale e patologico
- Feci pastose e maleodoranti: malassorbimento e cattiva digestione
- Carboidrati, proteine e grassi: come vengono assorbiti nell’intestino?
- Differenza tra colite ulcerosa, muco-membranosa, da fermentazione e da putrefazione
- Alimentazione e disfagia nel paziente con morbo di Parkinson
- Differenza tra tumore benigno, maligno, neoplasia, cancro e metastasi
- Cosa sono le metastasi? Tutti i tumori danno metastasi?
- Differenza tra metaplasia, displasia e neoplasia con esempi
- Differenza tra adenocarcinoma e carcinoma con esempi
- Differenza tra cancro e carcinoma con esempi
- Stomie: cosa sono, a che servono, quanti tipi esistono?
- Acalasia esofagea: cause, sintomi, cure e prevenzione
- Tumore del colon retto: sintomi iniziali, tardivi e ritardo nella diagnosi
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

 In condizioni normali lo stomaco e l’intestino perdono una quantità di sangue minima durante la digestione, quindi la presenza nelle feci è trascurabile e non è rilevabile dall’esame del sangue occulto.
In condizioni normali lo stomaco e l’intestino perdono una quantità di sangue minima durante la digestione, quindi la presenza nelle feci è trascurabile e non è rilevabile dall’esame del sangue occulto. Diagnosi
Diagnosi
 In chimica, l’orbita è la traiettoria che, secondo la vecchia teoria dell’atomo di Bohr, un elettrone segue nella rotazione attorno al nucleo, attraversando una linea.
In chimica, l’orbita è la traiettoria che, secondo la vecchia teoria dell’atomo di Bohr, un elettrone segue nella rotazione attorno al nucleo, attraversando una linea.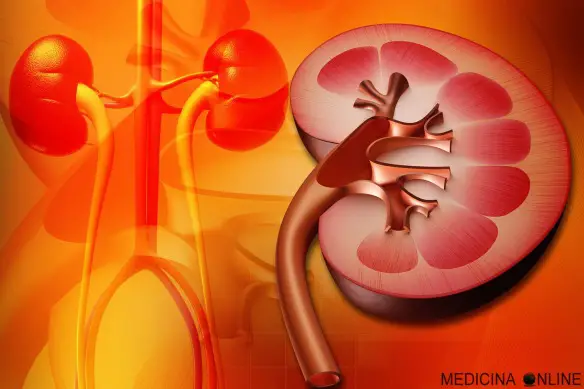 La sindrome nefritica è un complesso di segni e sintomi che può manifestarsi in molte nefropatie. Si presenta con ematuria, edema e ipertensione. In alcuni casi è associata ad insufficienza renale acuta. La proteinuria è spesso presente in quantità modesta, comunque inferiore ai 3 grammi nelle 24 ore. Per approfondire:
La sindrome nefritica è un complesso di segni e sintomi che può manifestarsi in molte nefropatie. Si presenta con ematuria, edema e ipertensione. In alcuni casi è associata ad insufficienza renale acuta. La proteinuria è spesso presente in quantità modesta, comunque inferiore ai 3 grammi nelle 24 ore. Per approfondire: 