 Cancro e tumore sono usati spesso come sinonimi, ma non sono due parole necessariamente equivalenti. Il discorso si complica con l’aggiunta di una Continua a leggere
Cancro e tumore sono usati spesso come sinonimi, ma non sono due parole necessariamente equivalenti. Il discorso si complica con l’aggiunta di una Continua a leggere
Archivi categoria: Medicina di laboratorio, chimica, fisica, biologia, genetica e statistica
Cos’è un tumore? Perché viene il cancro? Quali sono le cause?
 Le parole “cancro” e “tumore” sono conosciute da ognuno di noi come patologie spesso molto insidiose, tuttavia non tutti sanno esattamente cosa siano: cerchiamo di capirlo oggi, in generale e senza entrare nello specifico di un singolo tipo di tumore.
Le parole “cancro” e “tumore” sono conosciute da ognuno di noi come patologie spesso molto insidiose, tuttavia non tutti sanno esattamente cosa siano: cerchiamo di capirlo oggi, in generale e senza entrare nello specifico di un singolo tipo di tumore.
Cos’è un tumore?
Un tumore (dal latino tumor, “rigonfiamento”), anche chiamato neoplasia (dal greco νέος nèos, “nuovo”, e πλάσις plásis, “formazione”), è una massa di tessuto anormale che cresce in eccesso ed in modo scoordinato rispetto ai tessuti normali, e che persiste in questo stato dopo la cessazione degli stimoli che hanno indotto il processo.
Semplificando: il tumore è un insieme di cellule che si moltiplicano senza fermarsi, al contrario dei tessuti sani che invece sono composti da cellule che hanno una proliferazione controllata e limitata.
Leggi anche: Che differenza c’è tra tumore benigno o maligno, neoplasia, cancro?
Quali sono i medici che si occupano di tumori?
La branca della medicina che si occupa di studiare i tumori sotto l’aspetto eziopatogenetico, diagnostico e terapeutico è chiamata oncologia, tuttavia, potendosi i tumori formare in qualsiasi tessuto, qualsiasi medico può occuparsene. Ad esempio un tumore della pelle sarà probabilmente diagnosticato da un dermatologo, un tumore delle ossa da un ortopedico, un tumore del sangue da un ematologo, un tumore al seno da un senologo o da un chirurgo generale, un tumore del cervello da un neurologo o da un neurochirurgo, un tumore al rene da un urologo, un tumore ai polmoni da uno pneumologo o da un chirurgo toracico, un tumore al colon da un gastroenterologo o da un chirurgo generale. Tutti questi specialisti si servono anche dell’aiuto di professionisti che lavorano nella medicina di laboratorio, nella diagnostica per immagini (ad esempio radiologi) e di patologi, figure necessarie per la diagnosi di certezza di un tumore. La cura di un tumore si serve spesso di un equipe di medici che coinvolge oncologi e chirurghi.
Da cosa origina un tumore?
Può sembrare incredibile, eppure qualsiasi tumore, anche il più pericoloso, origina da una sola cellula iniziale mutata. Nei tessuti normali le cellule si riproducono dividendosi, per far crescere l’organismo o rimpiazzare le cellule morte: tale processo è finemente controllato da messaggi chimici inviati da una cellula all’altra e dai geni che si trovano nel loro DNA. Nei tumori, tale processo di controllo è alterato e la cellula iniziale, mutata per varie cause, continua a riprodursi senza freni e vengono meno anche i processi con cui le cellule danneggiate vanno incontro all’apoptosi, cioè alla morte programmata.
Leggi anche: Come nasce un cancro? Cosa sono i cancerogeni e come avviene la cancerogenesi?
In cosa consiste il danno della cellula iniziale?
La singola cellula iniziale che dà il via al tumore, ha una o più mutazioni geniche che fanno saltare i meccanismi di controllo della replicazione cellulare. La cellula mutata ha vari sistemi di riparazione genica, tuttavia, quando tali sistemi non sono sufficienti e più errori si accumulano, la cellula può iniziare a replicarsi senza controllo e dare avvio al tumore. Alcune di queste mutazioni geniche sono ereditarie (nell’uomo la trasmissione di un tumore da un individuo ad un altro è un evento rarissimo, ma non impossibile), mentre altre – più frequenti – sono provocate da fattori esterni, come sostanze chimiche o radiazioni, che vengono dette “cangerogene”, in quanto sono capaci di generare un cancro.
Quali sono i cancerogeni più diffusi?
Il fumo di sigaretta contiene più di 50 sostanze riconosciute come cancerogene, tra cui nitrosammine e di idrocarburi policiclici aromatici, ed infatti il fumo è responsabile di circa un terzo di tutte le morti per cancro nei paesi sviluppati e circa uno su cinque in tutto il mondo. Decenni di ricerche hanno dimostrato il legame tra il fumo e le neoplasie del polmone, della laringe, della testa, del collo, dello stomaco, della vescica, dei reni, dell’esofago e del pancreas. Per approfondire, leggi: Quali sostanze nocive e cancerogene contiene il fumo di una sigaretta?
L’esposizione prolungata all’amianto è una delle principali cause di mesotelioma, un tipo di tumore maligno del polmone. Altre sostanze catalogabili in questa categoria sono la wollastonite, l’attapulgite, la lana di vetro e la lana di roccia. Si ritiene che queste possano avere un effetto simile all’amianto e tipicamente l’essere umano è esposto ad esse per cause professionali. Materiali particellari non fibrosi che causano il cancro sono: la polvere di cobalto, il nichel metallico e la silice cristallina (quarzo, cristobalite e tridimite). Di solito, gli agenti fisici cancerogeni devono penetrare all’interno del corpo (ad esempio tramite inalazione di piccole parti) e richiedono anni di esposizione prima di sviluppare un tumore. Anche le bevande alcoliche aumentano il rischio di contrarre molti tipi di cancro, fra cui quello al seno, all’esofago, al colon, al pancreas, al cervello e alla gola. Anche l’inquinamento ambientale è cancerogeno.
Fino al 10% delle neoplasie maligne sono legate all’esposizione alle radiazioni ionizzanti (quelle a cui si sottopone il corpo durante una radiografia o una TAC). Le radiazioni ionizzanti possono provocare il cancro in molte parti del corpo ed a qualsiasi età. Ovviamente l’esposizione necessaria a sviluppare un cancro deve – nella maggioranza dei casi – essere prolungata: non basta ad esempio sottoporsi ad una singola radiografia per sviluppare un tumore.
L’esposizione prolungata ai raggi ultravioletti provenienti dal sole può portare allo sviluppo di melanoma e tumori maligni della pelle. Prove evidenti stabiliscono che le radiazioni ultraviolette siano la causa della maggior parte dei tumori della pelle non-melanomi, che sono le forme più comuni di cancro in tutto il mondo. Altre radiazioni non ionizzanti, come le frequenze radio utilizzate dagli smartphone, la trasmissione di energia elettrica, e altre fonti simili sono ritenute come possibili agenti cancerogeni dalla Agenzia Internazionale per la Ricerca sul Cancro dell’Organizzazione Mondiale della Sanità.
Alcuni ormoni sono correlati allo sviluppo di neoplasie, promuovendo la proliferazione cellulare. I tumori la cui nascita è maggiormente influenzata dagli ormoni sono quelli legati al sesso come il cancro della mammella, dell’endometrio, della prostata, dell’ovaio e del testicolo, oltre ai tumori della tiroide e delle ossa.
Anche traumi fisici, specie se ripetuti, possono dare origine ad un tumore, anche se molto più raramente rispetto a sostanze chimiche e radiazioni. Una causa accettata dalla comunità scientifica è l’applicazione a lungo termine di oggetti caldi sul corpo. Ripetute bruciature sulla stessa parte del corpo, come quelle prodotte dagli scaldamani a carbone, possono condurre allo sviluppo di neoplasie della pelle, specialmente se sono presenti anche cancerogeni chimici. L’assunzione di bevande calde può creare delle scottature che favoriscono neoplasie esofagee.
Leggi anche: È vero che i campi elettromagnetici causano tumore e cancro?
Il ruolo dei geni
Alla base della patogenesi del tumore c’è la mutazione di determinati geni:
- i proto-oncogeni,
- i geni oncosoppressori,
- i geni coinvolti nella riparazione del DNA.
Questi ultimi sono quelli che garantiscono la stabilità genetica perché se altri geni sono mutati per azione per esempio di agenti cancerogeni, questi riparano il DNA prima che vada incontro alla replicazione, prima cioè che queste mutazioni diventino stabili. Il cancro può colpire persone di ogni età, ma le persone anziane sono colpite con maggiore frequenza, perché i danni genetici tendono ad accumularsi con il tempo. Le mutazioni necessarie che una data cellula deve accumulare per dare origine a un cancro sono le seguenti, e sono comuni a tutti i tipi di cancro:
- acquisizione dell’autonomia moltiplicativa per sopravvenuta incapacità a sottostare ai meccanismi regolatori della proliferazione cellulare;
- assenza di inibizione dipendente dalla densità (le cellule normali si moltiplicano fino a una definita densità cellulare, raggiunta la quale diventano quiescenti);
- ridotta capacità di adesione con altre cellule o componenti tissutali;
- assenza di matrice extracellulare (spesso digerita da proteasi) che favorisce l’invasione di tessuti normali adiacenti;
- angiogenesi: formazione di nuovi vasi sanguigni per fornire ossigeno e fattori nutritivi alle cellule tumorali;
- riduzione o perdita della capacità differenziativa;
- acquisizione della capacità di replicazione illimitata per effetto dell’espressione della telomerasi o con sistemi alternativi chiamati “ALT” (Alternative Lengthening of Telomeres);
- riduzione o perdita della possibilità di andare incontro a morte cellulare programmata (apoptosi).
- perdita della cosiddetta inibizione da contatto.
Oltre a queste possono verificarsi (e di solito si verificano) anche altre mutazioni, dipendenti dal particolare tipo di cellula originaria e dalla esatta sequenza dei danni genetici.
Leggi anche: Cosa sono le metastasi? Tutti i tumori danno metastasi?
Angiogenesi
Come qualsiasi altro tessuto, per svilupparsi il tumore ha bisogno di ossigeno e sostanze nutritive: per questo produce sostanze capaci di stimolare l’angiogenesi, cioè la formazione di nuovi vasi sanguigni, che vadano a irrorare il nuovo tessuto in crescita.
I fattori di rischio per il tumore
Molto raramente un tumore ha una unica causa. Molto più spesso un tumore è causato da vari fattori di rischio che agiscono in modo sinergico. Alcuni fattori di rischio non modificabili, sono:
- età avanzata (alcuni tipi di tumore);
- giovane età (alcuni tipi di tumore);
- sesso (ad esempio il tumore al seno è molto più diffuso nel sesso femminile che in quello maschile);
- familiarità (parenti con tumori);
Alcuni fattori di rischio modificabili, sono:
- vita sedentaria;
- sovrappeso e obesità;
- alimenti ricchi di grassi e calorie;
- fumo di sigaretta;
- inquinamento atmosferico;
- agenti infettivi (virus e batteri);
- esposizione a sostanze chimiche;
- esposizione prolungata al sole;
- esposizione ripetuta a radiografie e tac.
Leggi anche: Come prevenire i tumori ed il cancro? I 10 cambiamenti consigliati
Stadiazione
L’estensione della maggior parte dei tumori maligni nell’organismo (espressa dalla “stadiazione”) viene classificata, in genere, attraverso la Classificazione TNM, proposta e mantenuta aggiornata dalla Union for International Cancer Control. Per approfondire, leggi: Stadiazione e classificazione TNM: cancro curabile o terminale?
Tumore benigno o maligno
In base al comportamento biologico i tumori si classificano in:
- tumori benigni: sono costituiti da cellule che mantengono in parte le loro caratteristiche morfologiche e funzionali, pur esibendo autonomia moltiplicativa. Essi sono caratterizzati da un tipo di sviluppo detto espansivo, perché comprime i tessuti vicini senza distruggerli: i tumori benigni che originano dall’epitelio ghiandolare (adenomi) sono spesso avviluppati da una capsula di tessuto connettivo fibroso che li delimita nettamente dai tessuti confinanti, coi quali assumono un rapporto di contiguità. Sono meno gravi dei tumori maligni.
- tumori maligni o cancro: sono costituiti da cellule che appaiono morfologicamente e funzionalmente diverse dalle corrispondenti normali. L’atipia morfologica, che è tanto maggiore quanto più indifferenziato è il tumore, si manifesta con mancanza di uniformità nella forma e nelle dimensioni delle cellule (polimorfismo) e degli organi cellulari, in particolare del nucleo, che è frequentemente ipercromico ed in fase mitotica. I tessuti vicini al tumore maligno vengono invariabilmente infiltrati e distrutti dalle cellule tumorali che si sostituiscono a quelle normali, fenomeno questo caratteristico della malignità e noto col termine “invasività neoplastica”. L’invasività si verifica anche a distanza, poiché un tumore maligno – al contrario del benigno – può dare origine a metastasi. Sono più gravi dei tumori benigni. In caso di tumore maligno, è importante intervenire al più presto con la terapia adeguata allo stato di diffusione della malattia, ad esempio con chirurgia, chemioterapia o radioterapia. In caso di tumore benigno, invece, la tempestività è molto meno importante ed anzi spesso il medico, anziché decidere per la sua asportazione, opta per una osservazione attenta e periodica e solo se il tumore benigno dovesse mutare caratteristiche (ad esempio: lipoma che aumenta in dimensioni) allora sceglierà di asportarlo chirurgicamente.
- borderline: in alcuni casi i tumori presentano un comportamento intermedio fra la malignità e la benignità (tumori “borderline”) o risultano inclassificabili (tumori a comportamento biologico incerto). In questi casi, generalmente la frequenza delle metastasi è molto bassa e il decorso è lento. Un esempio è il tumore stromale gastrointestinale.
La pericolosità di un tumore non dipende solo dalla sua natura, ma da molte altre caratteristiche come grandezza, tessuto di origine ed invasione o meno dei linfonodi.
Leggi anche:
- Che differenza c’è tra tumore benigno o maligno, neoplasia, cancro?
- Capire se si ha un tumore: come viene diagnosticato un cancro
- Che significa malattia terminale?
- Chemioterapia: durata, in pastiglie, come funziona, fa male, perché farla?
- Radioterapia: cos’è, come si fa, come funziona e durata del trattamento
- Chemioterapia: gli effetti collaterali più e meno comuni
- Radioterapia: rischi, dolore, fastidio ed effetti collaterali
- Differenza tra radioterapia e chemioterapia
- E’ più “pesante” la chemioterapia o la radioterapia?
- Tumore del polmone: epidemiologia, cause, fattori di rischio
- Tumore del polmone: classificazione, anatomia patologica
- Tumore del polmone: fisiopatologia
- Tumore del polmone: sintomi e segni della presenza del tumore primario
- Tumore del polmone: sintomi e segni della presenza di metastasi
- Tumore del polmone: diagnosi, anamnesi, esame obiettivo, esami
- Tumore del polmone: stadiazione TNM, operabilità, resecabilità
- Tumore del polmone: terapia chirurgica, procedure, mortalità intraoperatoria
- Tumore del polmone: radioterapia, chemioterapia, radiologia interventistica
- Tumore del polmone: prognosi, mortalità, sopravvivenza
- Quando si fa la radioterapia e quando la chemioterapia?
- Radioterapia stereotassica (Gamma Knife): cos’è e quando si usa?
- Chemio e radioterapia: i bambini possono visitare i parenti durante i trattamenti?
- Gravidanza e radioterapia di un parente: effetti su terzi e cosa fare
- La chemioterapia può provocare un secondo tumore?
- La chemioterapia uccide? Il lato oscuro della terapia antitumorale
- Chemioterapia in gravidanza: può far male al bambino?
- Radioterapia in gravidanza: può far male al bambino?
- Differenza tra remissione parziale, totale e guarigione
- Differenza tra esame istologico, biopsia, agoaspirato ed agobiopsia
- Quando si fa l’esame istologico e perché?
- Tumore del colon retto: diagnosi, metastasi, prognosi e stadiazione
- Tumore del colon retto: sintomi iniziali, tardivi e ritardo nella diagnosi
- Tumore del colon retto: trattamento chirurgico, radioterapia e chemioterapia
- Tumore del colon retto con metastasi: chirurgia, chemioterapia e terapie biologiche
- Tumore del colon retto: terapia personalizzata col test RAS
- Anticorpi monoclonali contro il tumore del colon retto metastatico
- Differenza tra ipertrofia muscolare sarcolplasmatica e miofibrillare
- Ipertrofia muscolare: cosa significa e come si raggiunge
- Differenza tra ipertrofia ed iperplasia con esempi
- Differenza tra iperplasia e neoplasia
- Differenza tra atrofia, distrofia ed aplasia con esempi
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Glicemia alta o bassa: valori normali, che patologie indica e come si controlla nei diabetici
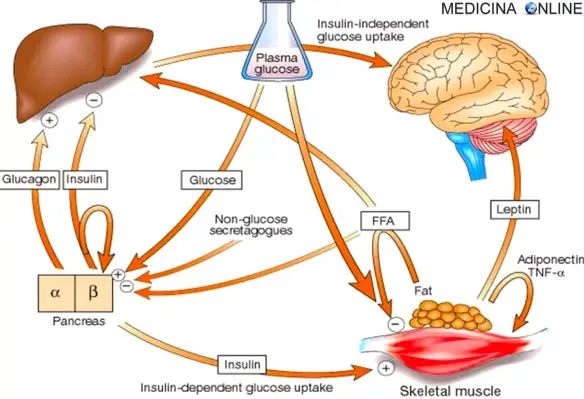 Il glucosio è il principale zucchero contenuto nel sangue, origina dal cibo ingerito ed è la principale fonte di energia dell’organismo. Il sangue trasporta il glucosio a Continua a leggere
Il glucosio è il principale zucchero contenuto nel sangue, origina dal cibo ingerito ed è la principale fonte di energia dell’organismo. Il sangue trasporta il glucosio a Continua a leggere
Creatinina alta o bassa: cos’è, cosa indica e come si corregge
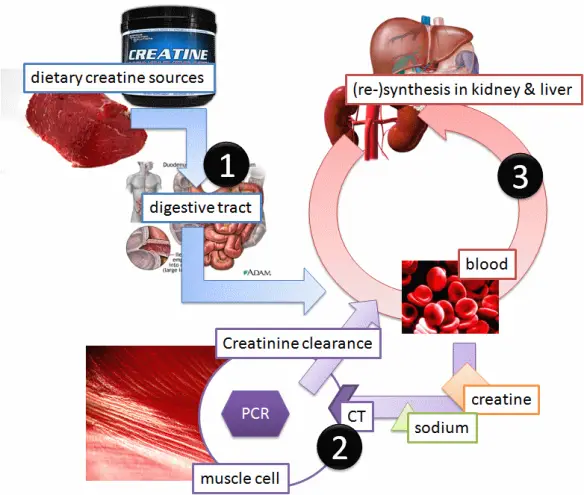 Cos’è la creatinina e cos’è la creatina?
Cos’è la creatinina e cos’è la creatina?
La creatinina è una sostanza che deriva dalla degradazione della creatina (1-Methylhydantoin-2-Imide). La creatina è una proteina che si trova nei muscoli scheletrici ed è fondamentale per i processi che portano al movimento e alla contrazione muscolare dal momento che ha la funzione principale di immagazzinare energia nel muscolo. Nel corso delle reazioni energetiche che avvengono durante la contrazione muscolare una parte della creatina stessa viene trasformata in creatinina che passa nel sangue e viene poi eliminata tramite i reni. Nell’organismo la creatina svolge anche alcune funzioni biologiche correlate con la crescita e lo sviluppo cellulare. La creatina è frequentemente utilizzata come integratore alimentare per sportivi, sotto forma di polvere bianca cristallina, solubile in acqua, utile specialmente nella sua versione micronizzata, più facilmente assorbita dall’organismo. La creatina è in grado di inibire l’attività dell’enzima tirosinasi nei melanociti, bloccando il processo di melanogenesi e contribuendo in tal modo a contrastare i disturbi da iperpigmentazione.
Leggi anche:
- Clearance della creatinina: alta o bassa, valori, calcolo e sintomi
- Differenze tra apparato urinario maschile e femminile
Cos’è la creatininemia?
Abbiamo visto che la creatina, durante il lavoro muscolare, viene degradata a creatinina. La creatininemia è un valore che va ad indicare quanta creatinina è presente nel sangue (per essere più corretti: la concentrazione di creatinina nel sangue). La creatininemia può essere dosata e viene espressa in mg di creatinina per dL di sangue.
Leggi anche: Glicemia alta o bassa: valori normali, che patologie indica e come si controlla nei diabetici
Quali sono i valori normali di creatinina nel sangue nell’uomo, nella donna e nei bambini?
Valori standard di creatinina si attestano tra 0 e 1,5 mg/dl, tuttavia questi valori possono variare in base al sesso, all’età, alla struttura muscolare (motivo per cui nell’uomo è mediamente più alta, specie se muscoloso) ed allo sforzo muscolare.
1) Sesso maschile
Adulti: 0.8-1.3 mg/dl
14-15 anni: 0.5-0.9 mg/dl
12-13 anni: 0.4-0.8 mg/dl
10-11 anni: 0.3-0.7 mg/dl
5-9 anni: 0.2-0.6 mg/dl
3-4 anni: 0.1-0.5 mg/dl
1-2 anni: 0.1-0.4 mg/dl
2) Sesso femminile
Adulti: 0.6-1.1 mg/dl
9-15 anni: 0.4-0.7 mg/dl
6-8 anni: 0.3-0.6 mg/dl
4-5 anni: 0.2-0.5 mg/dl
1-3 anni: 0.1-0.4 mg/dl
Quali sono i valori normali della clearance della creatinina?
Il valore normale della clearance di creatinina è compreso tra 95 e 140 ml/minuto nell’uomo e tra 85 e 130 ml/minuto nella donna.
Come si misura la creatinina?
Comunemente la creatinina viene misurata tramite una analisi del sangue e completato con una analisi delle urine delle 24 ore. L’esame ematico deve avvenire con il paziente a digiuno da almeno otto ore. Tramite la raccolta di urine si analizza la creatinina clearance (dosaggio della clearance della creatinina nelle 24 ore, cioè la velocità di eliminazione della creatinina ad opera dei reni).
Leggi anche:
- Zucchero o aspartame: quali sono le differenze?
- Tiroide: anatomia, funzioni e patologie in sintesi
- Paratiroidi: anatomia e funzioni in sintesi
- Differenza tra tiroide e paratiroide
- Paratiroidectomia: intervento, convalescenza e conseguenze
In base a quali fattori varia la creatinina nel sangue?
La concentrazione di creatinina nel sangue varia principalmente in base a tre fattori:
1) lavoro muscolare: aumenta fisiologicamente all’aumentare dello sforzo muscolare;
2) massa muscolare: aumenta fisiologicamente all’aumentare della massa muscolare;
3) funzionalità renale: aumenta patologicamente al diminuire della funzionalità dei reni.
Perché ho la creatinina alta?
1) Insufficienza renale. Qualsiasi patologia o agente che è in condizione di compromettere la funzionalità renale può essere la causa di un’anomala creatinina alta. In questo caso una creatinina alta è un campanello d’allarme che spinge noi medici a indagare su quali siano i motivi di questa disfunzione renale. Un elemento importante è accertare se questa insufficienza renale permane da molto tempo o se è recente. Spesso una pressione alta o il diabete mellito cronico possono provocare disfunzioni renali tali da far innalzare il valore di concentrazione ematica della creatinina.
2) Farmaci. Tra i farmaci la cui assunzione può provocare questo innalzamento ricordiamo: farmaci chemioterapici, alcuni antibiotici (Amfotericina B, Gentamicina, ecc.), i farmaci inibitori dell’Enzima di conversione dell’Angiotensina (ACE), alcuni diuretici (come il Lasix) ed alcuni analgesici (come l’Ibuprofene, l’Aspirina, etc.).
3) Grande consumo di carne o comunque di proteine con la dieta.
4) Uso smodato di integratori usati nel campo del fitness e del body building. La maggior parte degli studi concordano che l’uso corretto, anche se ad alte dosi, di integratori alimentari tipici delle palestre (creatina, aminoacidi, proteine…) non determinano un reale danno renale, tuttavia, l’uso in maniera smodata e del tutto impropria di alcuni integratori possono cronicamente alterare la funzionalità renale e determinare quindi indirettamente un aumento della creatininemia.
5) Esagerato allenamento muscolare o sforzo eccessivo eseguito prima del prelievo ematico.
6) Molte patologie: oltre a insufficienza renale, ipertensione arteriosa e diabete, la creatinina alta può essere spia di artrite reumatoide, disidratazione, endocardite, glomerulonefrite, gotta, insufficienza cardiaca congestizia, ipertiroidismo, lupus eritematoso sistemico, mieloma multiplo, nefriti, ostruzione delle vie urinarie, pielonefrite, shock, uremia.
Quali sono i sintomi che spesso si legano a creatinina alta?
Possono essere molti ed estremamente vari: disidratazione, affaticamento, stanchezza frequente e cronica, gonfiore ai piedi o alle caviglie, scarso appetito, gonfiore intorno agli occhi, prurito e pelle secca, crampi muscolari, minzione frequente e/o dolorosa, dispnea, confusione mentale.
Leggi anche: Azotemia (Urea) alta o bassa: valori, cause, sintomi e cosa fare
Creatinina bassa in gravidanza
La creatinina bassa nel sangue può verificarsi in diverse situazioni, anche se spesso è un valore che desta meno preoccupazioni di una creatinina alta. Comunemente si registra creatinina bassa in gravidanza. La gravidanza è una delle cause più comuni della creatinina bassa: una volta che il feto inizia a svilupparsi nel grembo materno, i nutrienti vengono trasportati dalla madre al bambino tramite il cordone ombelicale. Le donne incinte possono quindi avere meno creatina a disposizione e di conseguenza meno creatinina nel sangue.
Leggi anche: Azotemia alta e reni: cibi da evitare per abbassarla
Il paradosso negli anziani
Come abbiamo visto, in caso di riduzione della funzionalità renale la creatinina, e quindi la creatininemia, aumenta e nella pratica clinica il suo dosaggio viene utilizzato come indice di funzionalità renale. Tuttavia nei soggetti in cui, parallelamente alla riduzione della funzione renale, si ha anche una riduzione della massa muscolare (come accade per esempio negli anziani), la creatininemia può rimanere paradossalmente nella norma. Questo deve ancor di più farci capire che valori alterati di creatinina non sono necessariamente indice di patologia e valori normali di creatinina non ci mettono al sicuro da una patologia.
Cosa fare se ho la creatinina alta o bassa?
Per rispondere a questa domanda, leggi questo articolo: Creatinina alta o bassa: cure e terapie per correggere i valori
Leggi anche:
- Perché la cistite è più frequente nelle donne che negli uomini?
- Cistite: i cibi consigliati e quelli da evitare per guarire rapidamente
- Insufficienza renale acuta: sintomi, terapia, linea guida, morte
- Insufficienza renale cronica: stadi, dieta, sintomi, diagnosi e terapia
- Differenza tra insufficienza renale acuta e cronica
- Esami per valutare funzionalità renale ed insufficienza renale
- Emodialisi: come funziona, effetti collaterali e complicanze
- Differenza tra dialisi, emodialisi e dialisi peritoneale
- Dove si trovano i reni ed a che servono?
- Quali sono i sintomi di malattia o cattivo funzionamento dei reni?
- Cistite: ne soffro spesso, come diminuire le recidive?
- Differenza tra poliuria e pollachiuria
- Differenza tra poliuria e polidipsia
- Emocromo: guida completa a tutti i valori del sangue normali e patologici
- Emocromo: valori di riferimento e significato clinico [SCHEMA]
- Ematocrito (HCT): basso, alto, in gravidanza, valori normali e interpretazione
- Indici corpuscolari MCV, MCH, MCHC, RDW: cosa sono ed a che servono
- Volume corpuscolare medio (MCV): alto, basso, valori normali e significato
- MCH alto, basso, valori normali ed interpretazione
- MCHC alto, basso, valori normali ed interpretazione
- RDW alto, basso, valori normali ed interpretazione
- Ormoni tiroidei: differenza T3 e T4, valori normali e patologici
- TSH alto, basso e valori normali: qual è il significato clinico?
- Tireoglobulina alta, bassa, valori normali ed interpretazione
- Globuli rossi (eritrociti) alti, bassi, valori normali e interpretazione
- Globuli bianchi (leucociti) alti, bassi, valori normali ed interpretazione
- Eosinofili alti, bassi, valori normali ed interpretazione
- Neutrofili alti, bassi, valori normali ed interpretazione
- Basofili alti, bassi, valori normali ed interpretazione
- Emoglobina bassa, alta, cause e valori normali
- Emoglobina nelle urine (emoglobinuria): cause, sintomi e terapia
- Differenza tra anemia ed anemia mediterranea (talassemia)
- Differenza tra anemia e leucemia
- Perché la mononucleosi è chiamata anche “malattia del bacio”?
- Leucemia: sintomi, cause, cure e le diverse forme
- Leucemia mieloide acuta: cause, sintomi, diagnosi e cura
- Mieloma multiplo: cause, sintomi, diagnosi e cura
- Microcitemia (talassemia) : cause, sintomi, diagnosi e cura
- Differenza tra anemia e microcitemia
- Differenza tra anemia megaloblastica e perniciosa
- Differenza tra anemia mediterranea e falciforme
- Differenza tra emoglobina e mioglobina
- Differenza tra emoglobina fetale ed adulta
- Differenza tra emoglobina, ferro, ferritina e transferrina
- Differenza tra emoglobina e globuli rossi
- Differenza tra emocromo ed ematocrito
- Testosterone basso, alto, valori normali ed interpretazione
- Ormone follicolo stimolante (FSH) alto, basso, valori normali e significato
- Quanto peso perdiamo ogni volta che andiamo in bagno?
- Cistite in estate: come diminuire le recidive nei mesi caldi?
- Bruciore e stimoli frequenti di urinare: cistite, sintomi e cure
- Perché viene la cistite e come curarla?
- Quando la donna ha troppi peli: irsutismo, cause e trattamenti
- Uomo nel DNA, donna all’esterno: la Sindrome da insensibilità agli androgeni (Sindrome di Morris)
- Surrene: anatomia, funzioni e patologie in sintesi
- Differenza tra renella e calcoli renali
- Rene: anatomia, funzioni e patologie in sintesi
- Differenza tra surrene e rene
- Differenza tra rene policistico e multicistico
- Differenza tra rene destro e sinistro
- Differenza tra nefrologo ed urologo: patologie e competenze specifiche e comuni
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!
Aceruloplasminemia: sintomi, diagnosi e terapia
 L’aceruloplasminemia è una rarissima patologia neurodegenerativa genetica contraddistinta da accumulo di ferro nel cervello causato dalla completa assenza dell’attività della ceruloplasmina ferrossidasi dovuta a mutazioni omozigoti del gene della ceruloplasmina. E’ caratterizzata da anemia associata a degenerazione della retina, diabete mellito e vari sintomi neurologici.
L’aceruloplasminemia è una rarissima patologia neurodegenerativa genetica contraddistinta da accumulo di ferro nel cervello causato dalla completa assenza dell’attività della ceruloplasmina ferrossidasi dovuta a mutazioni omozigoti del gene della ceruloplasmina. E’ caratterizzata da anemia associata a degenerazione della retina, diabete mellito e vari sintomi neurologici.
Epidemiologia
Colpisce una persona su un milione, esordisce in età adulta. Essendo una malattia estremamente rara, in letteratura scientifica sono stati descritti meno di 60 casi.
Cause
La aceruloplasminemia è una malattia genetica causata da mutazioni nel gene della ceruloplasmina, una proteina coinvolta nel metabolismo del ferro. Viene ereditata dai genitori e si trasmette con modalità autosomica recessiva.
Trasmissione autosomica recessiva
Una malattia è detta a trasmissione autosomica recessiva quando l’allele alterato deve essere presente in coppia (omozigosi), cioè sono necessarie due copie dell’allele difettoso per far sì che la malattia si esprima, a prescindere dal sesso. Non basta un solo genitore portatore sano o malato, bensì entrambi i genitori devono essere portatori sani o malati. Il fenotipo quindi si esprime quando nel genotipo dell’individuo sono presenti entrambi gli alleli responsabili, fatto che spiega l’alta probabilità di sviluppare malattie genetiche in caso di incesto. Quindi:
- un individuo che possegga entrambi gli alleli alterati: è portatore ed è malato;
- un individuo che possegga solo un allele alterato: è portatore ma è sano;
- un individuo che non possegga nessun allele alterato: NON è portatore ed è sano.
Essere portatore sano vuol dire quindi NON avere la patologia ma possedere nel proprio genotipo un allele mutato, che può essere trasmesso alle generazioni successive.
Dalla combinazione delle possibili condizioni di genitori sani, malati e portatori sani, deriva la distribuzione probabilità che la malattia sia trasmessa ai figli:
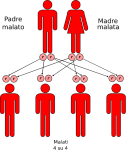
- genitori malato-malato: la probabilità che il figlio/a nasca malato è del 100%;
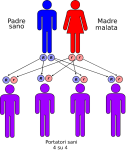
- genitori sano-malato: la probabilità che il figlio/a nasca portatore sano è del 100%;
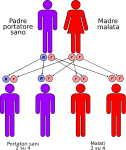
- genitori malato-portatore sano: la probabilità che il figlio/a nasca malato è del 50% e del 50% che nasca portatore sano;
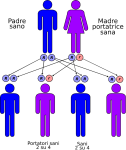
- genitori sano-portatore sano: la probabilità che il figlio/a nasca sano è del 50% e del 50% che nasca portatore sano;
- genitori portatore-portatore: la probabilità che il figlio/a nasca portatore sano è del 50% mentre è del 25% che nasca sano o malato.
Se nessuno dei genitori ha un allele mutato, non c’è ovviamente alcuna trasmissione autosomica recessiva ed i figli saranno tutti sani e NON portatori dell’allele mutato.
Nell’immagine che segue, è raffigurata la tipica situazione in cui entrambi i genitori sono sani ma portatori dell’allele mutato:
- un figlio su quattro avrà entrambi gli alleli alterati e sarà malato ed ovviamente portatore;
- due figli su quattro avranno un allele normale ed uno alterato e saranno sani ma anche portatori;
- un figlio su quattro avrà entrambi gli alleli normali e sarà sano e NON portatore.

Le altre quattro situazioni possibili sono raffigurate nelle seguenti immagini:
Sintomi e segni
Come già in parte prima accennato, l’aceruloplasminemia si manifesta nell’adulto con degenerazione retinica, diabete mellito e anemia. L’anemia nella aceruloplasminemia è refrattaria al trattamento con il ferro. Altri sintomi sono di tipo neurologico:
- atassia cioè mancanza di coordinazione muscolare che rende difficoltoso eseguire i movimenti volontari (mancanza di coordinazione fra tronco e braccia, tronco e capo, incoordinazione dei movimenti dell’occhio, incontinenza, difficoltà di deglutizione);
- movimenti involontari (blefarospasmo, contrazioni del viso, distonia della faccia e del collo, tremori e corea);
- parkinsonismo (tremore tremore a riposo che diminuisce con i movimenti volontari e scompare durante il sonno);
- depressione;
- deficit cognitivo.
Diagnosi
La diagnosi di laboratorio si basa su:
- assenza della ceruloplasmina sierica;
- bassa concentrazione sierica di rame e di ferro;
- alta concentrazione sierica di ferritina.
La diagnosi è suggerita inoltre dal riscontro alla risonanza magnetica cerebrale di una caratteristica anomala bassa intensità di segnale, che riflette l’accumulo di ferro nel cervello (striato, talamo, nucleo dentato) e nel fegato, nelle immagini T1, T2 pesate. L’analisi genetica può confermare la diagnosi. La diagnosi differenziale si pone con le altre forme di NBIA a esordio tardivo, lentamente progressive, compresa la neurodegenerazione atipica associata al difetto di pantotenato-chinasi (PKAN), la neuroferritinopatia, l’emocromatosi ereditaria, la malattia di Wilson, la malattia di Huntington, l’atrofia dentato-rubro-pallido-luisiana (DRPLA), la malattia di Parkinson giovanile, le atassie spinocerebellari ereditarie (si vedano questi termini) e gli effetti o la tossicità da farmaci.
Diagnosi prenatale
La diagnosi prenatale per le gravidanze ad aumentato rischio può essere disponibile presso laboratori specializzati, nei casi in cui la mutazione responsabile della malattia sia stata preventivamente identificata in un soggetto affetto della famiglia.
Trattamento
Il trattamento si basa sulla somministrazione orale o endovenosa di chelanti del ferro (deferiprone o deferasirox), che producono un miglioramento del diabete e dei sintomi neurologici. La combinazione di desferoxamina e plasma umano fresco congelato (FFP) contribuisce a ridurre il contenuto epatico di ferro. Gli antiossidanti, come la vitamina E, e la somministrazione orale di zinco possono prevenire il danno tissutale.
Prognosi
La prognosi è legata all’insufficienza cardiaca da accumulo di ferro nell’organo. Sono noti 5 pazienti con aceruloplasminemia deceduti per insufficienza cardiaca, probabilmente secondaria all’accumulo intracardiaco di ferro in un arco di 60 anni. In assenza di insufficienza cardiaca e con un adeguato trattamento del diabete, la prognosi è buona.
Leggi anche:
- Sovraccarico di ferro: emosiderosi ed emocromatosi
- Emocromatosi ereditaria e secondaria: sintomi, dieta, diagnosi, cure
- Anemia da carenza di ferro: cause, sintomi e cure
- Ferro: alimenti ricchi di ferro, fabbisogno giornaliero, integratore
- Sali minerali: definizione, funzioni, alimenti, integratori [GUIDA COMPLETA]
- Carenza, sovraccarico e tossicità da ferro: anemia ed emocromatosi
- Iodio: fabbisogno giornaliero, funzioni, dieta, carenza, tossicità
- Fluoro: carenza, tossicità, fabbisogno, dieta e funzioni
- Zinco: carenza, tossicità, fabbisogno, dieta, integratore e funzioni
- Cromo: benefici, funzioni, fabbisogno, dieta, integratore, carenza, tossicità
- Iodio: benefici, funzioni, fabbisogno, dieta, integratore, carenza, tossicità
- Selenio: benefici, funzioni, fabbisogno, dieta, integratore, carenza, tossicità
- Manganese: benefici, funzioni, fabbisogno, dieta, integratore, carenza, tossicità
- Molibdeno: benefici, funzioni, fabbisogno, dieta, integratore, carenza, tossicità
- Rame: benefici, funzioni, fabbisogno, dieta, integratore, carenza, tossicità
- Malattia di Wilson: dieta, sintomi, mortalità, aspettativa di vita
- Ipovitaminosi (carenza di vitamine): sintomi, lingua, unghie, cura
- Ipervitaminosi (eccesso di vitamine): sintomi ed esempi
- Malnutrizione per difetto o eccesso: definizione, sintomi, significato
- Ecco come il nostro corpo ci segnala la carenza di vitamine
- Hai voglia di un cibo in particolare? E’ il tuo corpo che ti rivela le carenze nutrizionali che hai
- Classifiche di calorie e di tutti i valori nutrizionali dei cibi
- Celiachia: cos’è il glutine, in quali alimenti è contenuto ed in quali no?
- Morbo di Crohn: cos’è, cause scatenanti, sintomi, cure e dieta
- Sindrome di Korsakoff e alcol: cause, sintomi, amnesia e cura
- Perdita di appetito: cause, ansia, stanchezza, tumore, cure
- Malassorbimento intestinale: esami, carboidrati, vitamine, dimagrimento
- Pellagra: significato, cause, subclinica, rischi, terapia, dieta consigliata
- Scorbuto: significato, pelle, sintomi, diagnosi, cura, immagini
- Carenza di vitamina A (retinolo): sintomi, dieta e integratori consigliati
- Carenza di vitamina D, rachitismo, osteomalacia: cause, sintomi, terapie, dieta, integratori
- Carenza di vitamina K: sintomi, fabbisogno, dieta e integratori consigliati
- Carenza di niacina e triptofano: pellagra, cause, terapie e dieta
- Carenza e dipendenza da vitamina B6: cause, sintomi, terapie, dieta, integratori
- Carenza di biotina: cause, sintomi, fabbisogno, dieta, integratori
- Carenza di vitamina C e scorbuto: cause, sintomi, cura, dieta, integratori
- Carenza di acido pantotenico (vitamina B5): cause, sintomi, cure, dieta, integratore
- Vitamina A (retinolo): a cosa serve, cosa provoca la sua carenza e quali alimenti ne sono ricchi?
- Una vostra amica è troppo magra? Vi insegno a capire se soffre di anoressia
- Alcolismo: test, cause, sintomi, definizione, effetti, danni, quando preoccuparsi
- Cachessia: oncologica, terminale, senile, significato e rimedi
- Gastrectomia parziale e totale: rischi, sopravvivenza, dieta
- Assumi abbastanza vitamina D? I sintomi che indicano la sua carenza e i cibi che ne contengono in abbondanza
- Beta carotene: cos’è, a cosa serve e in quali cibi lo trovo?
- Quali sono i cibi con più vitamina C, vitamina E, magnesio e beta carotene?
- Acido folico (vitamina B9): a cosa serve, in quali alimenti trovarlo e perché è importante prima e durante la gravidanza
- A che serve la vitamina B12? L’importanza in gravidanza e allattamento
- Perché cadono i capelli? Quanti capelli al giorno è normale perdere? E’ vero che i calvi hanno più testosterone?
- I tuoi capelli rivelano la tua salute: ecco come leggere i segnali che ti inviano
- Antiossidanti: alimenti ed integratori migliori contro i radicali liberi
- Radicali liberi: cosa sono, significato, invecchiamento, combatterli
- Radicali liberi: come combatterli e rimanere giovani
- Tutto sul Coenzima Q10: dove si trova, a cosa serve e dosaggi
- Astaxantina: benefici, integratore, controindicazioni, dosaggio
- Carnosina: benefici, integratore, controindicazioni, cibi, dose
- Bromelina: integratore, compresse, benefici, controindicazioni
- Polifenoli: integratori, significato, dove si trovano, benefici
- Flavonoidi: integratori, benefici, alimenti, controindicazioni
- Isoflavoni: integratori, alimenti, dove si trovano, controindicazioni
- Resveratrolo: benefici, integratori, dosaggio, alimenti
- Catechine: integratori, alimenti, dove si trovano, effetti collaterali
- Quercetina: integratore, alimenti, cibi, benefici, effetti collaterali
- Ginkgo biloba: a cosa serve, indicazioni, dosaggio, effetti collaterali
- Melatonina 1 e 2mg per insonnia: quando assumerla e controindicazioni
Lo Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram o su Pinterest, grazie!
Rosolia: come si trasmette, quali sono i sintomi e perché è pericolosa in gravidanza?
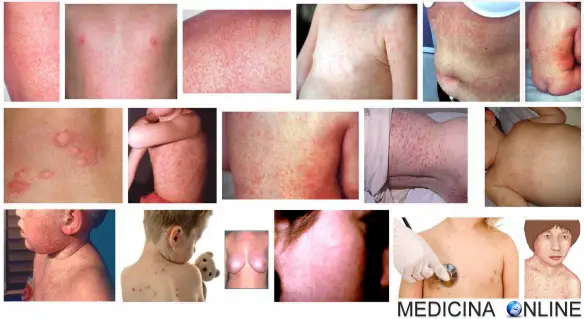 Oggi parliamo di una malattia infettiva, estremamente contagiosa, di origine virale. E’ una malattia che molti di noi hanno avuto da bambini e che non desta particolari problemi a meno che non sia contratta durante la gravidanza, specialmente nel primo trimestre. Sto parlando della rosolia.
Oggi parliamo di una malattia infettiva, estremamente contagiosa, di origine virale. E’ una malattia che molti di noi hanno avuto da bambini e che non desta particolari problemi a meno che non sia contratta durante la gravidanza, specialmente nel primo trimestre. Sto parlando della rosolia.
Cos’è la rosolia?
La rosolia, come anche il morbillo e la varicella, è una malattia esantematica, cioè un tipo di malattia che causa appunto l’esantema (termine derivante dal greco εξανθέω che significa “sbocciare”) noto anche come rash (dal francese antico rasche, che significa “grattare”), che si manifesta come una eruzione cutanea di pustole, vescicole e bolle; molto spesso – però – la rosolia non si presenta con segni clinici evidenti e con una sintomatologia ben definita, per cui le infezioni possono passare del tutto inosservate; questo può essere particolarmente rischioso nel caso di un’infezione contratta durante la gravidanza. La rosolia è causata da un virus appartenente al genere Rubivirus, famiglia Togaviridae, che si localizza in vari organi e tessuti. Precedentemente alla introduzione dei vaccini antirosolia, almeno l’80% delle persone venivano infettate dal virus della rosolia prima dei 20 anni.
La rosolia è, come il morbillo, una malattia endemo-epidemica: essa è cioè sempre presente nelle collettività con picchi epidemici ogni 7 anni e più.
La rosolia, sia in forma clinicamente evidente che di infezione inapparente, lascia un’immunità (protezione nei confronti di successive infezioni) che dura per tutta la vita. Anche l’immunità indotta dal vaccino è di lunga durata.
Leggi anche: Vaccini: servono davvero? Tutte le verità scientifiche
Come si trasmette la rosolia?
La rosolia è una malattia molto contagiosa, anche se non raggiunge i livelli di diffusività del morbillo. Il virus della rosolia viene trasmesso per via aerea, attraverso le goccioline di saliva emesse con la tosse, gli starnuti o anche semplicemente parlando. Il virus della rosolia passa attraverso la placenta e, per questa via, infetta il prodotto del concepimento.
Per quanto tempo si è contagiosi?
Il periodo di contagiosità, in cui la malattia può essere trasmessa dalle persone infette (con o senza sintomi manifesti) a quelle suscettibili, va da una settimana prima a 4 giorni dopo la comparsa dell’esantema, che però a volte può mancare del tutto.
I bambini affetti da sindrome da rosolia congenita possono eliminare il virus e quindi, rimanere infettanti per molti mesi dopo la nascita.
Chi è a rischio?
Praticamente tutti, tranne i vaccinati o coloro che sono immuni per avere già contratto la malattia.
Nel caso delle donne in gravidanza, il rischio si estende, con conseguenze che possono essere drammatiche, al prodotto del concepimento (come vedremo in seguito).
Quanto dura l’incubazione?
Il periodo di incubazione può variare da un minimo di 12 ad un massimo di 23 giorni (solitamente però è di 16-18 giorni). Durante l’incubazione il soggetto è asintomatico (non ha sintomi della malattia) ma è comunque in grado di contagiare altre persone.
Leggi anche: Che significa incubazione? Cos’è il periodo di incubazione di virus e batteri?
Quali sono i sintomi della rosolia?
Dopo il periodo di incubazione si ha comparsa di febbre, mal di testa, dolori alle articolazioni, raffreddore e gonfiore dei linfonodi posti ai lati delle orecchie e dietro la nuca.
Sul viso e sul collo compaiono macchioline leggermente sollevate, di colore roseo o rosso pallido, molto meno fitte di quelle del morbillo e senza alcuna tendenza a confluire tra loro.
Tale eruzione cutanea, sotto forma di esantema, si estende successivamente al resto del corpo e scompare nel giro di due o tre giorni.
Un bagno o una doccia caldi rendono più evidente l’esantema, che non compare affatto in circa il 40% dei casi, mentre nel 20-25% dei casi compaiono soltanto la febbre e la tumefazione dei linfonodi. La rosolia, quindi, si manifesta in modo conclamato soltanto nel 50% circa dei casi. Ricapitolando:
- eruzione cutanea consistente in piccole macchie rosa che compaiono prima dietro le orecchie, poi sulla fronte e su tutto il corpo e durano 2-3 giorni;
- febbre lieve e mal di testa;
- leggeri gonfiori dei linfonodi alla base della nuca, sul retro del collo e dietro le orecchie;
- dolori articolari;
- diminuzione del numero di globuli bianchi nel sangue;
- occhi arrossati e lacrimosi.
Le complicanze
La rosolia è considerata una malattia ad evoluzione benigna, tuttavia complicazioni come artriti acute e artralgie sono frequenti, soprattutto nel caso di rosolia contratta in età adulta.
Complicazioni meno frequenti della rosolia sono la trombocitopenia (anche detta “piastrinopenia“, cioè la diminuzione del numero delle piastrine, elementi del sangue fondamentali per il processo della coagulazione) e l’encefalite, che si manifesta in circa un caso su 6.000. L’encefalite da rosolia può essere mortale. Le complicanze sono più gravi se ad essere colpito è un adulto.
Leggi anche: Piastrinopenia lieve e grave: valori, cura, farmaci, autoimmune, cosa fare
Quali sono le complicanze in gravidanza?
Se la rosolia viene contratta da una donna durante la gravidanza, tutti gli organi ed i tessuti fetali sono coinvolti e gli effetti sul prodotto del concepimento possono essere molto gravi: aborto spontaneo; morte intrauterina del feto; malformazioni e lesioni di tipo infiammatorio, principalmente a carico del sistema nervoso, dell’apparato cardiocircolatorio, degli organi di senso, con ritardato sviluppo fisico e psichico (Sindrome da rosolia congenita). Il rischio di avere gravi malformazioni nel feto quando la rosolia viene contratta in gravidanza è massimo nel primo trimestre (85% nelle prime 8 settimane, 52% dalla nona alla dodicesima settimana di gestazione), mentre le infezioni contratte dopo la ventesima settimana raramente provocano malformazioni congenite.
Le donne che intendano intraprendere una gravidanza, non vaccinate o non immuni in seguito alla malattia, dovrebbero sottoporsi, prima del concepimento, ad una ricerca degli anticorpi antirosolia ed eventualmente alla vaccinazione (il test è offerto gratuitamente secondo il Decreto ministeriale 10 settembre 1998 per la tutela della maternità).
Come si cura la rosolia?
Al momento non esiste una terapia specifica della rosolia, a parte l’uso di paracetamolo per abbassare la febbre. Il riposo a letto, insieme con una dieta leggera ma ricca di zuccheri e liquidi, costituiscono la base per il trattamento della rosolia. Per alleviare i sintomi dell’artrite il medico curante potrà prescrivere la terapia sintomatica più adatta. In caso di dolore possono essere usati FANS (farmaci antinfiammatori non steroidei, come l’ibuprofene).
Leggi anche: Il paracetamolo (Tachipirina) è un antinfiammatorio non steroideo (FANS)?
Come funziona la vaccinazione?
L’arma migliore contro la malattia è la vaccinazione preventiva con il vaccino vivo attenuato, con un’efficacia > 95% e che garantisce immunità a vita. Non si tratta di una vaccinazione obbligatoria, ma altamente consigliata, e gratuita, sia per tutti i bambini che per le ragazze non immunizzate dopo la pubertà e per tutti gli operatori che svolgono mansioni a contatto con bambini e/o con donne in età riproduttiva. Per i nuovi nati, si consiglia una prima dose verso i 12-15 mesi di età, e un richiamo verso i 5-6 anni. Fino al 1999, in Italia veniva eseguita solo la vaccinazione sulle bambine in età pre-puberale, verso i 12-13 anni. Analogamente a quanto osservato in altre nazioni, questa strategia si è però rivelata insufficiente, in quanto l’elevata circolazione del virus in tutti i soggetti non vaccinati ha comportato una persistenza del rischio di infezione. La strategia attuale, in linea con quella attuata in altri paesi, è dunque quella di vaccinare tutti i bambini nel secondo anno di vita con il vaccino trivalente, contro morbillo, parotite e rosolia, di somministrarne una seconda dose entro i 5-6 anni di età. Contemporaneamente, è indispensabile vaccinare tutte le ragazze e le donne che non sono state vaccinate da bambine.
Come per tutti vaccini vivi attenuati, la vaccinazione non viene praticata negli individui con deficit immunitario o sotto terapia immunosoppressiva (corticoidi, antineoplastici, antirigetto), nelle donne gravide o che desiderano esserlo nel mese successivo (per sicurezza, anche se non si sono mai verificati problemi correlati). Il vaccino è invece consigliato alle persone infette da Hiv che non hanno sviluppato Aids.
Come comportarsi nel sospetto che una donna in gravidanza possa avere contratto la rosolia?
Nel caso che si sospetti che una donna in gravidanza possa avere contratto l’infezione, è opportuno eseguire immediatamente la ricerca degli anticorpi antirosolia su un campione di sangue conservando una parte del campione utilizzato per l‘esame, in modo da poterlo confrontare con campioni prelevati successivamente. La presenza di anticorpi della classe IgG nel campioni è segno di un’infezione avvenuta nel passato e, quindi, di immunità nei confronti di infezioni successive, mentre la presenza di anticorpi della classe IgM indica infezioni in atto. Se nel campione non si riscontrano anticorpi, è necessario ripetere l’esame a distanza di circa un mese. La positività nel secondo campione è segno di infezione recente o in atto; se anche il secondo campione risulta negativo, il test deve essere nuovamente ripetuto dopo 6 settimane dall’esposizione al contagio. La persistenza della negatività indica che l’infezione non è avvenuta.
Leggi anche:
- Vaccini anti meningite: quanti sono, quando farli, quali sono indispensabili, effetti collaterali
- Febbre dopo vaccino: come curarla e quanto dura?
- Il calendario delle vaccinazioni obbligatorie per i vostri figli
- Cos’è il vaccino esavalente? Quando, come e perché farlo?
- Differenza tra vaccino e profilassi con esempi
- Differenza tra vaccino Salk e Sabin
- Differenza tra vaccino ed immunoglobuline
- Differenza tra vaccino trivalente, quadrivalente ed esavalente
- Differenza tra profilassi e prevenzione
- Differenza tra profilassi diretta e indiretta con esempi
- Differenza tra immunizzazione attiva e passiva
- Differenza tra profilassi attiva e passiva con esempi
- Cos’è la poliomielite? Importanza del vaccino e controindicazioni
- Differenza tra virus e batteri: chi è più pericoloso? Diagnosi, sintomi e terapia
- Meningite batterica e virale: sintomi, profilassi, cura e vaccini
- Differenza tra allele dominante e recessivo
- Sistema immunitario, immunità innata e specifica: riassunto, schema e spiegazione
- Immunodeficienza primaria e secondaria: sintomi, cause e terapie
- Immunità innata (aspecifica): barriere, infiammazione e complemento
- Immunità innata (aspecifica): neutrofili, macrofagi e linfociti natural killer
- Immunità specifica (acquisita): linfociti, T killer, T helper, T γδ, B ed anticorpi
- Immunità specifica (acquisita): memoria passiva, attiva ed immunizzazione
- Immunità specifica (acquisita) umorale e cellulare
- Patologie del sistema immunitario: immunodeficienze, autoimmunità ed ipersensibilità
- Anticorpi: (immunoglobuline): tipi, caratteristiche e funzioni
- Differenza tra antigene, aptene allergene ed epitopo
- Aptene: cos’è e perché è importante per il sistema immunitario
- Antigene: cos’è e perché è importante per il sistema immunitario
- Differenza tra antigeni esogeni, endogeni, tumorali, nativi ed autoantigeni
- Epitopi sequenziali e conformazionali: cosa sono e come funzionano
- HIV: dopo quanto si manifestano i sintomi? I 4 stadi dell’infezione
- Differenza tra HIV e AIDS: sono uguali?
- Si muore di AIDS? Qual è l’aspettativa di vita?
- HIV: sintomi iniziali in donne e uomini
- Differenza tra malattia, sindrome e disturbo con esempi
- Differenza tra virus HIV1 e HIV2
- Sesso e AIDS: l’HIV si trasmette anche tramite il rapporto orale
- Il liquido pre-eiaculatorio può indurre gravidanza e trasmettere l’HIV?
- HIV e AIDS: come, dove e quando si eseguono i test per la diagnosi?
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su Mastodon, su Tumblr e su Pinterest, grazie!
Indossi sempre lo stesso pigiama? Ecco quali sono i rischi per la tua salute
 Vi siete mai chiesti per quanto tempo potete indossare mediamente un pigiama prima di doverlo lavare? Secondo un sondaggio condotto in Gran Bretagna da una società che produce materassi, gli uomini fanno passare circa due settimane prima di cambiarlo, le donne addirittura 17 giorni. Facendo passare così tanto tempo tra un lavaggio e l’altro, si rischiano infezioni alla pelle e cistite.
Vi siete mai chiesti per quanto tempo potete indossare mediamente un pigiama prima di doverlo lavare? Secondo un sondaggio condotto in Gran Bretagna da una società che produce materassi, gli uomini fanno passare circa due settimane prima di cambiarlo, le donne addirittura 17 giorni. Facendo passare così tanto tempo tra un lavaggio e l’altro, si rischiano infezioni alla pelle e cistite.
Escherichia coli e colleghi
“Tutti noi ospitiamo sulla pelle e nell’intestino microrganismi vari – spiega al Daily Mail online Sally Bloomfield, della London School of Hygiene and Tropical Medicine – che generalmente non sono dannosi, ma possono diventarlo se finiscono nel posto sbagliato, entrando in contatto con altre parti del nostro corpo”. Fra questi c’è l’Escherichia coli, che può causare la cistite, oppure vari Stafilococchi e anche lo Staphylococcus aureus resistente alla meticillina (o MRSA acronimo di Methicillin-Resistant Staphylococcus Aureus) cioè uno Stafilococco che si è evoluto sviluppando una resistenza agli antibiotici beta-lattamici, che comprendono le penicilline e le cefalosporine. In alcuni casi l’E.coli può essere l’agente eziologico di malattie intestinali ed extra-intestinali come meningite, peritonite, setticemia e polmonite, oltre alla già citata cistite. Alcuni ceppi di E.coli sono inoltre tossigenici, producono cioè tossine che possono essere causa di diarrea.
Leggi anche: Un oggetto che tocchi 150 volte al giorno ha più batteri della tavoletta del wc. Di cosa si tratta e come difendersi
Pochi pigiami di ricambio?
Ignaro di tutto questo, il 54% delle donne sostiene di avere solo un paio di pigiami da alternare, così dimentica da quanto tempo non li cambia. La scusa addotta dal 51%, invece, è che indossa il pigiama per non più di un paio d’ore per notte e dunque non lo lava spesso. Gli uomini scaricano la responsabilità sulle partner, dicendo che sono loro a occuparsi di fare la lavatrice. La maggior parte ammette di non avere tanti pigiami da cambiare. E così quello indossato per due settimane o più diventa un covo di batteri che possono poi finire sugli altri indumenti con cui entra in contatto, per esempio in lavatrice. Quindi lavate ogni settimana la biancheria con cui si dormite e, visto che siamo ancora in periodi di saldi, fate una bella scorta di pigiami di ricambio!
Leggi anche:
- Bruciore e stimoli frequenti di urinare: cistite, sintomi e cure
- Piattole: cosa sono, si vedono, quanto durano, come eliminarle?
- Dimmi come dormi e ti dirò chi sei
- Dieci domande sull’allergia agli acari ed i consigli per contrastarli
- Scabbia su pelle e cuoio capelluto: sintomi, cause e cure
- Pelle arrossata ed irritata a causa del sudore: come curare l’irritazione cutanea?
- Irritazione cutanea in neonati, bambini e gravidanza: i soggetti più a rischio
- Rossore ed irritazione della pelle sotto e tra il seno: cause e rimedi
- Pelle arrossata ed irritata: cause patologiche e non patologiche
- Pelle arrossata ed irritata a causa del sudore: i rimedi naturali
- Pelle arrossata ed irritata: ecco quali farmaci usare
- Peli incarniti: cause, creme, infezione, depilazione e rimedi
- Peli incarniti: rimedi naturali per eliminarli in modo rapido e sicuro
- Follicolite da depilazione inguinale ed alle gambe: rimedi naturali
- Depilazione inguine: i metodi più efficaci, indolori e sicuri
- Differenza tra ceretta brasiliana e classica: pro, contro e consigli per farla bene
- Pelle screpolata: cause e rimedi naturali per viso e corpo
- Ceretta: quale scegliere? Tecniche a confronto con pro e contro
- La differenza tra epilazione e depilazione e le rispettive tecniche
- Eliminare i peletti dal viso con rimedi casalinghi e con il laser
- Cosa fare quando la pelle è sensibile e si irrita facilmente?
- Impieghi terapeutici dell’Aloe Vera nella dieta, nella cosmesi, nelle terapie antitumorali e contro gastrite e colesterolo
- Secca, grassa, mista o sensibile: tu che tipo di pelle hai?
- Prurito alla pelle: cos’è e come fare per alleviarlo?
- Cos’è la radiazione solare? Cosa sono i raggi ultravioletti? Che danni possono provocare alla nostra pelle?
- I dieci fantastici usi del bicarbonato che ancora non conosci
- Cosa significa avere la “pelle grassa”?
- Eczema: sintomi, cause e cure
- I deodoranti non sono tutti uguali
- Perché la nostra pelle è acida?
- Dermatite atopica: cause, sintomi e terapie di una patologia della pelle molto diffusa
- Primo sole: i consigli per proteggere la nostra pelle dalle scottature (anche a tavola)
- I vari tipi di ghiandole e di sudore che influenzano l’odore del nostro corpo
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!
Presenza di sangue nello sperma: cause e terapie dell’ematospermia
 Con ematospermia (anche detta “emospermia“, i due termini sono sinonimi) in medicina si indica la presenza di sangue nello sperma. La maggior parte dei pazienti affetti descrive il problema lamentando evidenti chiazze o striature di sangue color rosso acceso all’interno del liquido seminale; alcuni soggetti affermano che le macchie si presentano addirittura con un colore nero, paragonandole alle tonalità del caffè. Pur rappresentando un segno clinico fortemente allarmante per il paziente affetto, nella stragrande maggioranza dei casi, il sangue nello sperma, clinicamente, non desta preoccupazioni particolari: l’ematospermia viene infatti considerata una condizione benigna ed autolimitata nella maggior parte dei casi. Ad ogni modo, visto che in alcuni casi può essere spia di patologie anche molto gravi, il parere del medico risulta fondamentale, al fine di escludere eventuali patologie nascoste e chiarire ogni dubbio.
Con ematospermia (anche detta “emospermia“, i due termini sono sinonimi) in medicina si indica la presenza di sangue nello sperma. La maggior parte dei pazienti affetti descrive il problema lamentando evidenti chiazze o striature di sangue color rosso acceso all’interno del liquido seminale; alcuni soggetti affermano che le macchie si presentano addirittura con un colore nero, paragonandole alle tonalità del caffè. Pur rappresentando un segno clinico fortemente allarmante per il paziente affetto, nella stragrande maggioranza dei casi, il sangue nello sperma, clinicamente, non desta preoccupazioni particolari: l’ematospermia viene infatti considerata una condizione benigna ed autolimitata nella maggior parte dei casi. Ad ogni modo, visto che in alcuni casi può essere spia di patologie anche molto gravi, il parere del medico risulta fondamentale, al fine di escludere eventuali patologie nascoste e chiarire ogni dubbio.
Leggi anche: Cancro del testicolo: prevenzione, diagnosi, stadiazione, cure
Incidenza dell’ematospermia
Molti sono i pazienti che, almeno una volta nel corso della vita, hanno osservato tracce di sangue nello sperma: il più delle volte, il target della condizione apparentemente patologica sono i giovani, in particolare quelli con una vita sessualmente attiva e promiscua. Per contro, altre fonti riportano che anche l’astinenza sessuale prolungata potrebbe rappresentare un fattore di rischio per l’ematospermia.
Solo di rado, gli adulti e gli anziani lamentano episodi di ematospermia legata ad un’intensità e ad una certa frequenza dei rapporti sessuali: in simili frangenti, spesso, la causa del sangue nello sperma risiede in problematiche più gravi, che saranno esaminate nel prossimo paragrafo. Chiaramente, l’occasionalità della condizione non deve preoccupare esageratamente; quando invece l’ematospermia diviene un fenomeno frequente è assolutamente inevitabile la visita medica. Si osserva che l’ematospermia è una situazione ricorrente all’incirca nel 2% delle problematiche di tipo urologico.
Cosa causa l’ematospermia?
Sono molte le possibili cause di ematospermia. A tal proposito è doveroso distinguere due grandi classi di ematospermia:
- sangue nello sperma da cause non patologiche;
- sangue nello sperma secondario a patologie.
Per approfondire le cause che possono determinare ematospermia, argomento importante perché vi permetterà di comprendere appieno le sue possibile cure, vi consiglio di leggere questo articolo: Cause patologiche e non patologiche dell’ematospermia
Leggi anche: Ipoposia: quando lo sperma è troppo poco. Cause e terapie per aumentare la quantità di eiaculato
Classificazione delle ematospermie
Sulla base della caratteristiche cliniche del sangue nello sperma, è opportuno effettuare una precisa classificazione: a tal proposito, si distingue il sangue prettamente rosso vivo, dal sangue più scuro (marrone o nero) all’interno del liquido seminale.
Nella maggior parte del soggetti diagnosticati, il sangue nello sperma si presenta di un colore rosso acceso: quando la condizione si manifesta frequentemente, è assai probabile che sia in atto una flogosi a carico dell’uretra, della prostata o delle vescicole seminali. Ciò è spiegato dalla rottura – o comunque da microlesioni dei vasi ematici – verificatasi durante l’eiaculazione: infatti, le inevitabili contrazioni della muscolatura liscia generate dall’atto eiaculatorio sottopongono le pareti dei capillari, già lese precedentemente, ad una sforzo eccessivo, che si traduce nella fuoriuscita di sangue mescolato allo sperma. Quando l’ematospermia diviene una problematica particolarmente ricorrente, il sangue emesso insieme allo sperma, durante l’eiaculazione, tende a divenire più scuro, variando tonalità dal marrone al nero. Nella quasi totalità dei casi, i pazienti che lamentano episodi di sangue marrone nello sperma hanno assistito precedentemente anche ad emissioni di sangue rosso vivo nel liquido seminale. Il sangue marrone o nero è la conseguenza di residui di sangue accumulato in precedenza nella prostata o nella vescica seminale: a causa di processi ossidativi, il colore del sangue varia dal rosso acceso al bordeaux – marrone.
Diagnosi delle ematospermie
Lo spermiogramma rappresenta sicuramente l’esame diagnostico più indicato per il riconoscimento di eventuali patogeni nello sperma. La spermiocoltura, invece, completa lo spermiogramma e dà un’idea sulla tipologia e sulla quantità di microorganismi presenti all’interno del liquido seminale.
Quando il paziente, dopo i 50 anni, lamenta episodi di sangue nello sperma sarebbe opportuno un approfondito test della prostata: i rigonfiamenti anomali ed eventuali ascessi potrebbero essere i responsabili del sanguinamento in esame. Quando la palpazione medica ano-rettale non risulta sufficiente, il paziente dovrà sottoporsi ad un’ecografia trans-rettale, sicuramente più precisa rispetto al controllo manuale: quest’ultima evidenzia altre ipotizzabili patologie, quali calcolosi, cisti della prostata, dei dotti eiaculatori o calcificazioni prostatiche.
L’esame PSA (Antigene Prostatico Specifico) è un test diagnostico di screening utile ad escludere la possibile eventualità di carcinoma prostatico. A tale proposito, leggi anche: PSA totale e free alto: capire i risultati dell’esame e rischio di tumore alla prostata
È opportuno il monitoraggio periodico della pressione arteriosa, soprattutto in quei pazienti avanti con l’età: abbiamo visto, infatti, che l’ipertensione potrebbe rappresentare un fattore di rischio per l’ematospermia.
Ancora, al fine di accertare se il sanguinamento nello sperma deriva da una condizione morbosa prostatica od uretrale, sono consigliate, rispettivamente, la cistoscopia e l’uretroscopia.
In caso di sospetta infezione sessualmente trasmessa, sono opportuni i relativi test diagnostici.
Terapie: cura dell’ematospermia
La terapia dell’ematospermia varia notevolmente in base alla causa che l’ha determinata, a tale proposito leggi: Cure dell’ematospermia: dilatatori uretrali, farmaci e chirurgia
Leggi anche:
- L’uomo con il pene più grande del mondo:”Faccio sesso orale da solo e da morto donerò il mio pene a…”
- Si può essere allergici allo sperma?
- Quante calorie contiene lo sperma?
- Ragazza di 15 anni rimane incinta dopo sesso orale
- Lo sperma ingoiato fa bene alla salute?
- L’uomo nato con due peni [FOTO]
- L’autopalpazione del testicolo ti salva dal cancro testicolare
- Torsione del testicolo: sintomi, cure, conseguenze, neonati. E’ doloroso?
- Cosa contiene lo sperma?
- La Sindrome da spogliatoio o Dismorfofobia peniena: quando il pene sembra deforme o più piccolo o più grande di quanto realmente sia. Diagnosi e cure
- Com’è fatto il pene al suo interno?
- Prostata ingrossata ed infiammata: ecco cosa fare per mantenerla in salute
- Micropene: quanto misura, complicazioni, c’è una cura?
- Testicolo ritenuto (criptorchidismo): terapia e complicazioni
- Ipospadia nel bambino e nell’adulto: sintomi, diagnosi e cure
- Ipospadia nel bambino e nell’adulto: terapia chirurgica e post-operatorio
- Le dimensioni del pene contano o no? Le confessioni senza censura delle mie pazienti ed i loro consigli per avere un pene più bello
- Cosa accade e cosa si prova quando si frattura il pene?
Dott. Emilio Alessio Loiacono
Medico Chirurgo
Direttore dello Staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o unisciti al nostro gruppo Facebook o ancora seguici su Twitter, su Instagram, su YouTube, su LinkedIn, su Tumblr e su Pinterest, grazie!