 Le ciglia ed i flagelli
Le ciglia ed i flagelli
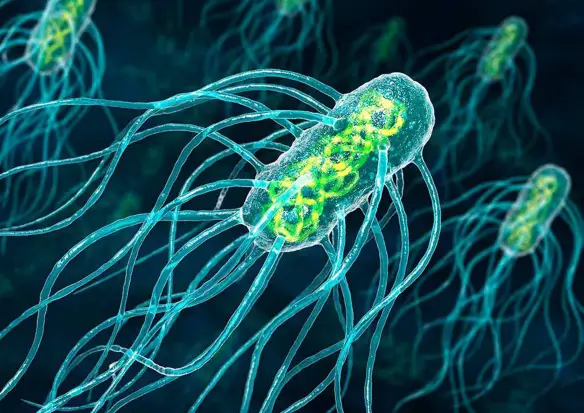
Le ciglia e i flagelli sono appendici locomotorie che sporgono da alcune cellule. Le piccole e numerose appendici che permettono il movimento di protisti come Paramecium sono dette ciglia; altri protisti possiedono, invece, i flagelli, appendici più lunghe delle ciglia e generalmente meno numerose (solo uno o pochi per cellula). I flagelli sono presenti anche nelle cellule spermatiche di molti animali pluricellulari e di alcune piante. Le cellule dotate di flagelli si spostano spinte dal movimento ondulatorio di questi ultimi, simile a quello di una frusta, mentre le ciglia agiscono più come remi azionati contemporaneamente da un equipaggio di canottieri. Oltre a essere utili per la locomozione, ciglia e flagelli possono svolgere funzioni particolari all’interno di organi specializzati. Le cellule della trachea umana, per esempio, hanno ciglia che si muovono per allontanare dai polmoni il muco contenente particelle estranee.
La struttura ed il movimento di ciglia e flagelli
Le ciglia e i flagelli hanno una struttura e un meccanismo di movimento molto simili. Entrambi sono costituiti da microtubuli avvolti da una estroflessione della membrana plasmatica; nove coppie di microtubuli sono disposte ad anello intorno a una coppia centrale in una configurazione, chiamata 9 + 2, comune a quasi tutti i flagelli e alle ciglia degli eucarioti. Nel citoplasma, il complesso di microtubuli si prolunga in una struttura di ancoraggio chiamata corpo basale, con una configurazione caratteristica comprendente nove triplette di microtubuli disposte ad anello. Quando un ciglio o un flagello incomincia a crescere, il corpo basale agisce da punto di partenza per l’assemblaggio dei microtubuli mediante la progressiva aggiunta di unità di tubulina. I corpi basali hanno una struttura molto simile a quella dei centrioli del centrosoma delle cellule animali. Il movimento di ciglia e flagelli dipende dall’azione di una proteina motrice, la dineina, che forma strutture dette braccia attaccate a ciascuna coppia di microtubuli esterni. Utilizzando l’energia proveniente dall’ATP, le braccia di dineina di una coppia di microtubuli si agganciano a quelle di una coppia adiacente ed esercitano una forza di trazione. Le coppie di microtubuli sono tenute insieme da ponti trasversali di natura proteica e da raggi diretti verso i microtubuli centrali. Se le coppie non fossero tenute saldamente in posizione, l’azione delle braccia di dineina le farebbe scivolare l’una sull’altra. Tale azione, invece, fa flettere i microtubuli, determinando in questo modo il movimento di ciglia e flagelli.
Leggi anche:
- Differenza tra riproduzione sessuata e asessuata
- Differenza tra vaccini vivi ed attenuati: vantaggi e svantaggi
- Differenza tra immunità specifica ed immunità aspecifica
- Differenza tra linfociti B e T
- Differenza tra immunità umorale e cellulare
- Differenza tra self non self in immunologia
- Differenza tra ciglia e stereociglia: movimento, struttura e funzioni
- Differenza tra ciglia e microvilli: struttura, movimento e funzioni
- Differenza tra cellule eucariote e procariote
- Differenza tra cellula aploide e diploide con esempi
- Riproduzione cellulare e ciclo cellulare
- Organelli (organuli) citoplasmatici della cellula animale: cosa sono ed a che servono?
- Mitosi: spiegazione delle quattro fasi
- Meiosi: spiegazione di tutte tappe
- Differenza tra allele dominante e recessivo
- Virus e virioni: cosa sono, come sono fatti, come funzionano e come si riproducono
- Differenza tra omozigote ed eterozigote
- Differenza tra gene e allele
- Differenza tra genotipo e fenotipo
- Quanti cromosomi hanno esseri umani, scimmie, cani, gatti e topi?
- Quanti cromosomi ha chi è affetto da Sindrome di Down?
- Cos’è un cromosoma ed a che serve?
- Cos’è un gene ed a che serve?
- Cosa sono gli alleli ed a che servono?
- Differenza tra mitocondri e cloroplasti
- Differenza tra citosol e citoplasma
- Mitocondri: definizione, dimensioni e funzioni
- Citoscheletro: funzioni e struttura
- Ribosomi e reticolo endoplasmatico: cosa sono e che funzioni svolgono?
- Nucleo cellulare: funzioni, dimensioni e membrane nucleari
- Lisosomi: cosa sono? Significato e dimensioni
- Perossisomi: definizione e funzioni
- Membrana plasmatica: definizione e funzioni
- Apparato del Golgi: spiegazione semplice e funzioni
- Citosol: definizione e funzioni
Lo staff di Medicina OnLine
Se ti è piaciuto questo articolo e vuoi essere aggiornato sui nostri nuovi post, metti like alla nostra pagina Facebook o seguici su Twitter, su Instagram o su Pinterest, grazie!

 La maggior parte delle persone conosce la donazione di sangue intero, una procedura indolore che dura solo una decina di minuti (oltre al tempo necessario alla preparazione e al recupero). Ma è anche possibile donare solo il plasma tramite una procedura chiamata plasmaferesi. Durante la plasmaferesi, il sangue viene prelevato, il plasma viene separato, mentre i globuli rossi e le e le piastrine vengono re-infusi al donatore. Solitamente il processo richiede circa 45 minuti e il plasma si rigenera rapidamente. La frequenza delle donazioni e il loro volume, in genere tra i 650 ml e gli 880 ml, sono regolate normativamente da ciascun Paese.
La maggior parte delle persone conosce la donazione di sangue intero, una procedura indolore che dura solo una decina di minuti (oltre al tempo necessario alla preparazione e al recupero). Ma è anche possibile donare solo il plasma tramite una procedura chiamata plasmaferesi. Durante la plasmaferesi, il sangue viene prelevato, il plasma viene separato, mentre i globuli rossi e le e le piastrine vengono re-infusi al donatore. Solitamente il processo richiede circa 45 minuti e il plasma si rigenera rapidamente. La frequenza delle donazioni e il loro volume, in genere tra i 650 ml e gli 880 ml, sono regolate normativamente da ciascun Paese.





 Ad oggi esistono sette diverse release di Blade Runner, le cui differenze spaziano da mere imprecisioni tecniche a “dettagli” che suggeriscono una completa re-interpretazione del protagonista.
Ad oggi esistono sette diverse release di Blade Runner, le cui differenze spaziano da mere imprecisioni tecniche a “dettagli” che suggeriscono una completa re-interpretazione del protagonista.
 Cosa studia l’ecocolordoppler?
Cosa studia l’ecocolordoppler? Il palato è la parete superiore della cavità orale. È costituito nei 2/3 anteriori dal palato duro e nel terzo posteriore dal palato molle. Queste due porzioni normalmente sono scarsamente distinguibili alla vista, anche se il palato molle è più vascolarizzato e quindi può apparire di colore rosso più intenso, sono invece ben distinguibili al tatto.
Il palato è la parete superiore della cavità orale. È costituito nei 2/3 anteriori dal palato duro e nel terzo posteriore dal palato molle. Queste due porzioni normalmente sono scarsamente distinguibili alla vista, anche se il palato molle è più vascolarizzato e quindi può apparire di colore rosso più intenso, sono invece ben distinguibili al tatto. “Se fai la pipì in piscina l’acqua diventa rossa e ti scoprono subito“: chi non ha mai creduto, almeno per un giorno, almeno per un’ora, al mito degli anni Ottanta secondo il quale nelle piscine pubbliche mettevano dei reagenti coloranti all’acido urico? Be’, leggenda o meno, di fatto molti sono rimasti segnati da questa storia e in vasca non urinano. Questione di educazione, e questione di igiene. Ma ci sono invece molte persone che invece la pipì in piscina la fanno eccome. Il vostro vicino di corsia? Probabilmente, ma non solo, visto che Micheal Phelps (
“Se fai la pipì in piscina l’acqua diventa rossa e ti scoprono subito“: chi non ha mai creduto, almeno per un giorno, almeno per un’ora, al mito degli anni Ottanta secondo il quale nelle piscine pubbliche mettevano dei reagenti coloranti all’acido urico? Be’, leggenda o meno, di fatto molti sono rimasti segnati da questa storia e in vasca non urinano. Questione di educazione, e questione di igiene. Ma ci sono invece molte persone che invece la pipì in piscina la fanno eccome. Il vostro vicino di corsia? Probabilmente, ma non solo, visto che Micheal Phelps (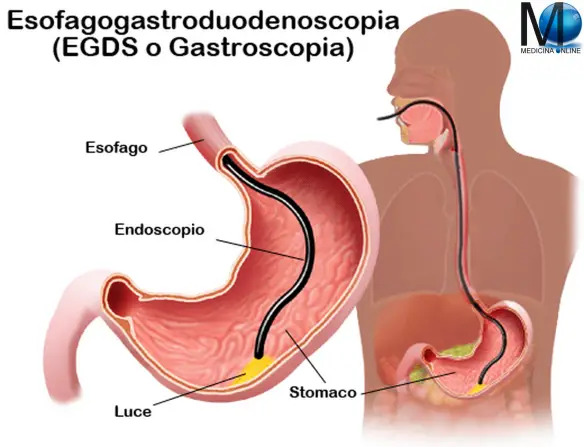 È un’infezione cronica della mucosa gastrica, a opera dell’Helicobacter Pylori (HP). Questo batterio riesce a sopravvivere nell’ambiente acido dello stomaco e ne danneggia le cellule, innescando una reazione infiammatoria che determina una malattia cronica, la gastrite cronica superficiale o atrofica. L’infezione è anche il principale fattore eziologico dell’ulcera peptica (sia duodenale che gastrica).
È un’infezione cronica della mucosa gastrica, a opera dell’Helicobacter Pylori (HP). Questo batterio riesce a sopravvivere nell’ambiente acido dello stomaco e ne danneggia le cellule, innescando una reazione infiammatoria che determina una malattia cronica, la gastrite cronica superficiale o atrofica. L’infezione è anche il principale fattore eziologico dell’ulcera peptica (sia duodenale che gastrica).